Abstract
Type 1 diabetes requires lifelong insulin therapy because insulin-secretion capability is diminished. Glycemic control and glucose monitoring are important to prevent type 1 diabetes complications. Diabetes technologies have developed rapidly; continuous glucose monitoring (CGM) and continuous subcutaneous insulin infusion (CSII) are now common and greatly aid glycemic control, especially in children and adolescents. The National Health Insurance Service has provided partial reimbursements for both CGM and CSII devices since 2019 and 2020, respectively; the devices are thus expected to become more popular. CGM reduces the frequency of hypoglycemia and the level of glycated hemoglobin. CSII affords more precise glycemic control than multi-dose insulin therapy. CSII showed reduced frequency of hypoglycemia and improved metabolic outcome without an increase in the body mass index z-score. Technological advancement of combined CGM and CSII will eventually serve as an artificial pancreas. The National Health Insurance Service should fund not only the devices but also education of patients and caregivers. In addition, healthcare providers must be continuously updated on new diabetes technologies.
Go to : 
1형 당뇨병은 췌장의 베타세포가 자가면역 기전에 의해 점진적으로 파괴되어 발생하는 질환으로 결국에는 인슐린 결핍에 의한 증상이 나타나게 된다[1-3]. 따라서, 1형 당뇨병 환자들에게 적절한 혈당조절과 만성합병증의 예방을 위해 평생 동안 인슐린 치료가 필요하다[4,5]. 최근의 보고에 의하면 전 세계적으로나 우리나라에서 모두 1형 당뇨병의 발생률이 증가하고 있어, 질병 부담률을 높일 것으로 예상되고 있다[6,7].
1형 당뇨병에서 혈당조절을 잘하기 위해서는 혈당측정 및 인슐린투여가 필수적이다. 혈당측정은 최근까지는 손가락 끝에서 직접 채혈침을 찔러 검사하는 자가혈당측정법과 혈액에서 당화혈색소를 측정하는 방법이 주로 사용되었다. 자가혈당측정법은 하루 6–10회 정도로 자주 측정을 하여 혈당조절을 하는 경우 당화혈색소를 감소시키는 것으로 알려졌다[8-10]. 자가혈당측정법은 측정 당시의 혈당은 알 수 있으나, 측정 사이의 혈당 변화와 추세를 알 수 없다는 단점이 있다. 당화혈색소는 약 3개월 정도의 평균혈당을 반영하는 것으로 공복과 무관하게 측정할 수 있고, 혈당조절과 합병증 발생을 예측하는 좋은 지표라는 장점이 있으나[11,12], 혈당의 일중, 일간 변동을 반영하지 못하며 혈색소의 농도에 따른 변화가 있다는 단점이 존재한다[13,14]. 가장 최근의 가이드라인에 따르면 소아청소년 연령에서의 목표 당화혈색소는 <7.0%이다[10,15].
연속혈당측정기(continuous glucose monitoring)는 피하에 삽입된 센서가 간질액의 당 수치를 1–5분 간격으로 측정하는 의료기기로 자가혈당측정법과 당화혈색소의 한계를 보완할 수 있다[16,17]. 여러 연구에서 연속혈당측정기를 사용하는 경우 혈당조절이 잘되고 저혈당의 빈도가 감소함을 보고하였다[17-22]. 최근 가이드라인에서는 1형 당뇨병 소아청소년에서 연속혈당측정기를 사용하는 것을 추천하고 있다[18,23,24].
1형 당뇨병에서 인슐린 투여는 1990년대 미국의 Diabetes Control and Complication Trial 연구 이후, 생리적인 인슐린 분비에 가깝게 인슐린을 공급하는 인슐린 집중치료법이 표준치료로 자리잡았다[5]. 인슐린 집중치료법에서의 인슐린투여는 기저인슐린과 탄수화물 계산법을 바탕으로[25] 식사인슐린을 공급하여 주는 방법에 따라 인슐린 다회주사요법과 인슐린펌프(continuous subcutaneous insulin infusion)를 사용하는 방법으로 나눌 수 있다. 인슐린펌프는 초속효성 인슐린의 주입 시기와 속도에 따라 기초주입과 추가주입의 두 가지 방법으로 인슐린을 공급한다. 캐뉼라를 피하에 거치하여 인슐린을 투여할 때마다 주사하지 않아도 되며, 저혈당 및 고혈당에 대하여 좀 더 유연하게 대처할 수 있다. 최근에는 인슐린펌프에 연속혈당측정기의 혈당 데이터가 전송되도록 하여 저혈당을 예방할 수 있는 센서 연동형 인슐린펌프(sensor augmented pump)와 기저 인슐린 용량이 정해진 혈당으로 자동으로 조절되는 하이브리드 폐회로 인슐린펌프(hybrid closed-loop pump)도 사용 중이다.
우리나라에서는 2019년 1월부터 1형 당뇨병 환자를 대상으로 연속혈당측정기의 전극에 대해서 부분적으로 급여화가 되었고, 2020년 1월부터는 연속혈당측정기의 송신기와 인슐린펌프에 대해서도 일부 급여화 되었다. 이를 계기로 특히 소아청소년 연령에서 1형 당뇨병 환자들의 연속혈당측정기와 인슐린펌프 사용이 증가하고 있는 추세이다. 이에 본 논문에서는 미국당뇨병협회(American Diabetes Association) 및 국제소아청소년당뇨병협회(International Society for Pediatric and Adolescent Diabetes)의 가이드라인[18,24]을 바탕으로 소아청소년 연령에서의 연속혈당측정기와 인슐린펌프의 사용에 대하여 정리해보고자 한다.
Go to : 
1) 연속혈당측정기의 구성 및 종류
연속혈당측정기는 후향적(전문적) 연속혈당측정기와 실시간(개인용) 연속혈당측정기, 간헐적 연속혈당측정기의 세 가지로 분류할 수 있다. 후향적 연속혈당측정기는 환자가 혈당을 알지 못하는 상태로 연속혈당을 10–14일 동안 시행하고, 의료진이 자료를 분석하게 된다. 실시간 연속혈당측정기는 측정되는 당이 실시간으로 환자의 수신기로 전송되며, 혈당의 추세나 예측, 미리 설정된 값에 대한 알람을 제공한다. 최근의 연속혈당측정기에서 측정된 당수치는 각 회사의 클라우드 저장소에 저장이 되며, 이 자료를 환자의 보호자나 의료진이 공유할 수 있다. 간헐적 연속혈당측정기는 간질액의 당을 연속적으로 측정은 하지만 기기를 센서에 스캔할 때만 당 수치를 확인할 수 있다.
연속혈당측정기는 센서, 송신기, 수신기의 세 부분으로 구성되어 있다. 센서는 피하조직으로 삽입되어 당수치를 측정하며, 종류에 따라 6일에서 14일까지 사용할 수 있다. 센서의 종류에 따라 혈당 보정이 하루 0–2회 필요하다. 송신기는 센서에서 측정된 당수치를 수신기로 전송하는 역할을 하며 기기에 따라 3개월부터 1년까지 사용할 수 있다. 하지만, 간헐적 연속혈당측정기의 경우 송신기가 필요 없으며 스마트폰과 같은 연동된 기기로 스캔을 하면 당수치가 전송된다.
2) 연속혈당측정기의 주요 지표
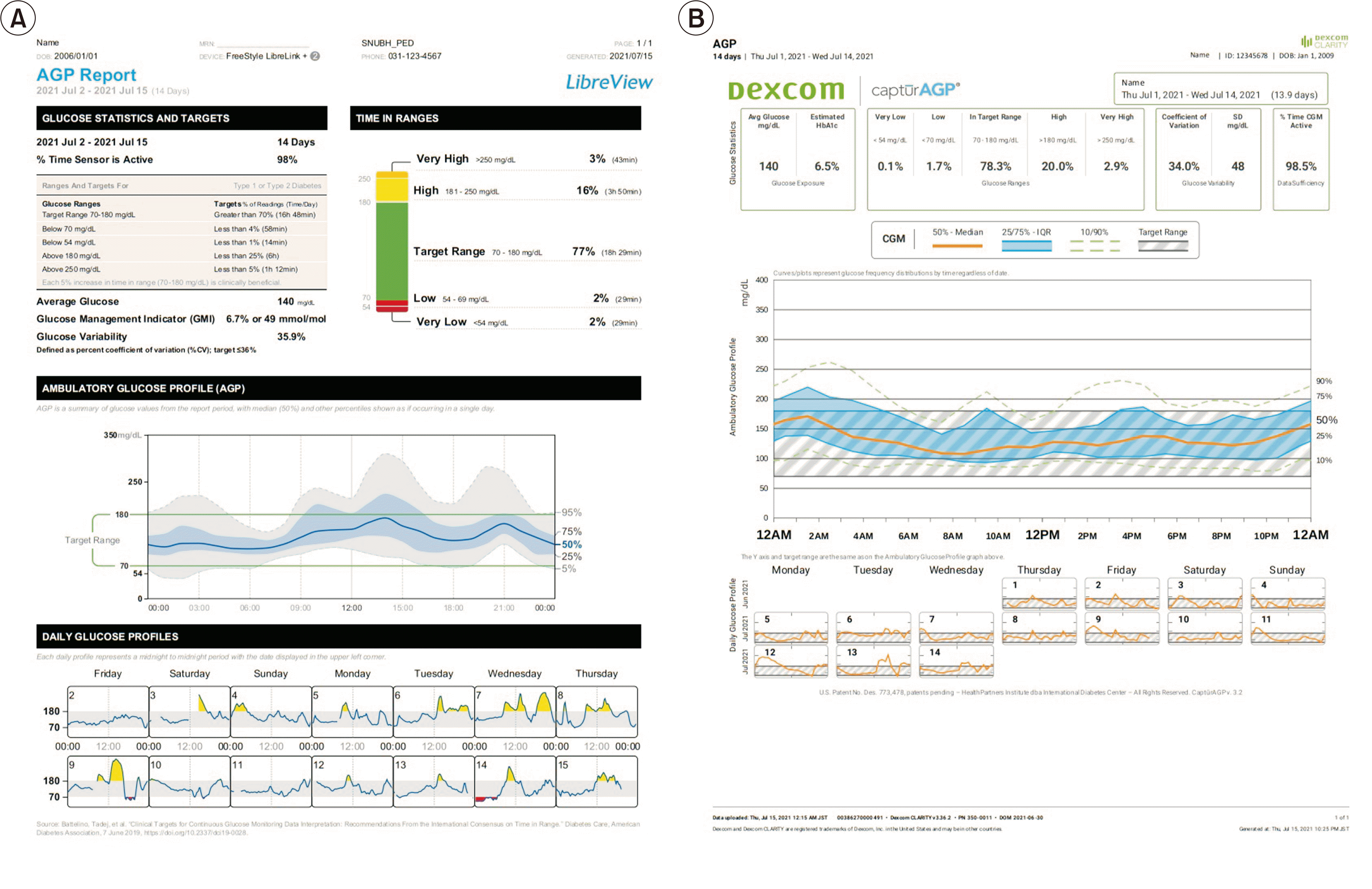
2017년에 제안되고, 2019년에 개정된 Advanced Technologies & Treatments for Diabetes의 권고사항에 의한 연속혈당측정기의 중요한 지표들은 다음과 같다[23,26]. 총 10개의 지표가 제안되었으며, (1) 연속혈당측정기의 사용일수(최소 14일) [27]; (2) 연속혈당측정기 착용 비율(14일 중 최소 70%); (3) 평균 당 수치; (4) 당 관리 지표(glucose management indicator, 이전의 estimated HbA1c) [28]; (5) 혈당변동성 지표(% of coefficient of variation ≤36%); (6) 당수치 >250 mg/dL인 시간의 비율(<5%); (7) 당 수치 181–250 mg/dL인 시간의 비율(<25%); (8) 당 수치 70–180 mg/dL인 시간의 비율(>70%); (9) 당 수치 54–69 mg/dL인 시간의 비율(<4%); (10) 당 수치 <54 mg/dL인 시간의 비율(<1%)과 연속혈당측정기의 보고서로서 외래 혈당 프로필(ambulatory glucose profile)의 사용이다.
외래 혈당 프로필 보고서는 표준화된 한 페이지로 구성된 양식이다[29]. 가장 최신인 버전 4.0에서는 위에서 언급한 10개의 주요 지표가 ‘혈당 통계와 목표(glucose statistics and targets)’와 ‘범위 내 혈당(time in rage)’ 부분에 표시되어 있다. 또한, 설정한 기간의 일중 혈당 변동을 중위값과 5, 25, 75, 95 백분위수 라인, 목표혈당 수치인 70–180 mg/dL와 함께 그래프로 제시한다. 각 연속혈당측정기 제조사마다 각각의 프로그램을 제공하여 위의 주요 지표들을 볼 수 있다(Fig. 1).
3) 연속혈당측정기의 효용
여러 연구에서 연속혈당측정기를 사용하는 경우 혈당조절에 도움이 된다고 보고하였다. Juvenile Diabetes Research Foundation의 연구에 의하면 연속혈당측정기를 사용할 때 성인에서 당화혈색소는 0.5% 감소하였으나, 소아에서는 유의미한 차이가 없었다[22]. 하지만, 2차 분석에서는 주당 6일 이상 부착하고 있는 소아청소년에서는 혈당개선의 효과가 있었다[30]. 또한, 연속혈당측정기는 혈당을 잘 유지하고 당화혈색소가 <7.0%인 경우에도 저혈당이 감소하는 효과가 있었고[21], 당화혈색소를 감소시키고 혈당 변동성을 감소시키는데 효과적이었다[31,32]. 4세 이하의 1형 당뇨병 환자에서 시행된 연구에서는 연속혈당측정기를 사용하는 보호자들은 저혈당과 인슐린 용량을 조절하는 부분에 있어서 만족도가 높았다[33].
성인 1형 당뇨병 환자에서 연속혈당측정기는 고위험군에서 저혈당의 빈도를 감소시켰다[34-36]. 소아청소년 1형 당뇨병 환자에서는 저혈당 시간과 빈도를 감소시키는 효과가 있다는 보고도 있었으나[19,21], 그렇지 않은 경우도 있었다[22,37]. 연속혈당측정기를 사용할 때 부착부위의 피부 문제가 있는 경우가 있으므로 주의 깊게 관찰해야 한다.
4) 국내 연속혈당측정기의 현황
현재 우리나라에서 사용 가능한 연속혈당측정기는 Table 1에 정리되어 있다. 2019년부터 급여화 된 연속혈당측정기는 2019년 12월까지 7.3%만 처방을 받았지만, 20세 미만 1형 당뇨병 환자 중에서는 18.7%가 처방을 받은 것으로 조사되었다[17]. 미국의 경우 18세 미만의 당뇨병 환자에서 2011년에는 4%, 2016년에는 19%만이 연속혈당측정기를 사용하고 있었고, 독일과 오스트리아에서는 2011년에는 3%, 2016년에는 22%만이 연속혈당측정기를 사용하였다[20,38].
Characteristics of available continuous glucose monitoring system in Korea
1) 인슐린펌프의 구성 및 종류
인슐린펌프는 일반적으로 인슐린펌프 기기 본체(pump)와 인슐린펌프용 주사바늘을 포함한 주입세트(infusion set), 인슐린펌프용 주사기(reservoir)로 구성되어 있다. 이런 구성을 일체화 시키고 인슐린주입속도의 조절은 별도의 휴대용 리모컨으로 조절하는 패치형 인슐린펌프도 있으며, 최근 우리나라에서도 개발되어 허가되었고, 임상에서 사용 중이다.
인슐린펌프는 피하에 위치한 캐뉼라를 통하여 초속효성 인슐린을 주입하는데, 사전에 프로그램된 대로 기초주입(기저인슐린, basal insulin)과 추가주입(식사인슐린 또는 추가인슐린, bolus insulin)의 방식으로 작용한다. 피하에 위치한 캐뉼라는 약 3일 동안 사용할 수 있어 다회주사요법에 비하여 몸에 직접 인슐린을 주사하지 않아도 되는 장점이 있으며, 기저인슐린을 여러 시간 구간으로 나누어 설정할 수 있고, 아픈 날의 고혈당과 같은 특별한 상황에서는 임시 기저인슐린 주입속도를 설정하여 상황에 따라 좀더 세밀하고 유연하게 혈당조절을 할 수 있는 장점이 있다. 또한, 센서 연동형 인슐린펌프에는 저혈당 및 저혈당이 예측되는 경우에 인슐린의 주입이 일시적으로 중지되도록 하는 기능이 있다. 청소년들의 사춘기 호르몬 분비에 따른 혈당의 변화에 맞추어 인슐린 주입을 세밀하게 조절하여 혈당조절을 더 잘 할 수 있다.
2) 인슐린펌프의 적용 대상자
소아청소년 1형 당뇨병 환자에서, 인슐린펌프는 연령이나 유병 기간에 상관없이 누구에게나 사용을 고려할 수 있다. 인슐린펌프가 좀 더 유용할 것이라고 생각되는 경우는 신생아나 영아와 같이 매우 어린 나이일 경우, 새벽현상이 두드러지는 소아청소년, 주사공포증이 있는 경우, 운동선수 등의 경우가 있고, 인슐린펌프의 사용을 적극적으로 고려해야 하는 경우는 심한 저혈당이 자주 반복되는 경우, 당화혈색소 수치와 관련없이 혈당의 변동폭이 매우 큰 경우, 혈당조절이 잘 되지만 인슐린 다회주사요법으로 일상생활의 제약을 받아 삶의 질이 저하되는 경우 등이 있다[24,41]. 이전과 달리 최신가이드라인에서는 1형 당뇨병이 진단되는 시점부터 인슐린펌프를 사용하는 것이 성공적인 혈당조절에 도움이 되며, 지속적으로 혈당조절을 잘 하는데도 도움이 되고, 심한 저혈당이나 당뇨병성 케톤산증과 같은 급성합병증의 빈도도 줄일 수 있다고 하였다[24].
3) 인슐린펌프의 임상적 효과
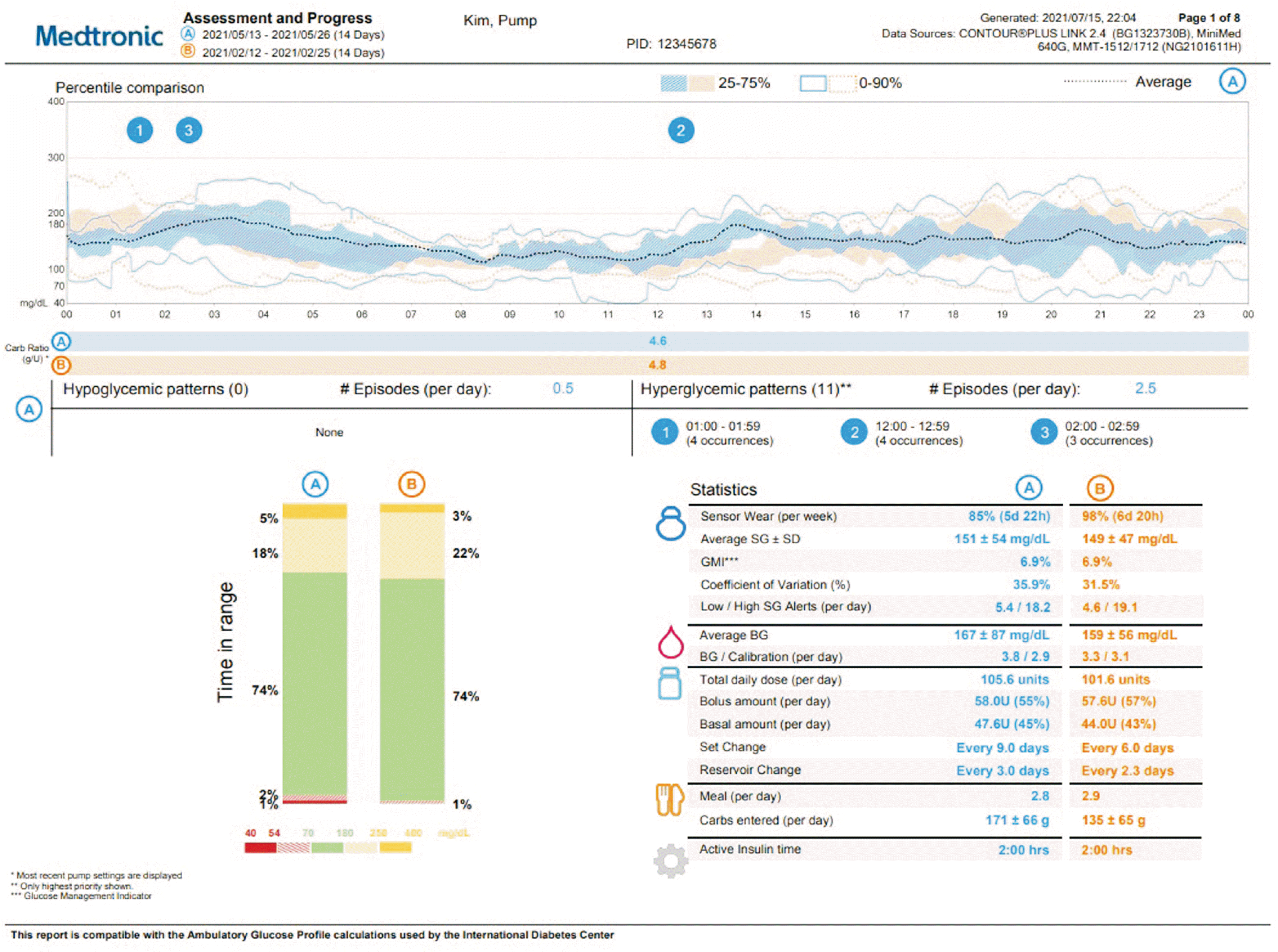
인슐린펌프의 사용은 다회주사요법에 비해 심한 저혈당 및 당뇨병성 케톤산증의 발생 위험을 낮추고 혈당조절에 도움을 준다. 특히 연속혈당조절기와 함께 사용하는 센서 연동형 인슐린펌프는 다회주사요법과 비교하여 저혈당의 위험을 증가시키지 않으면서도 당화혈색소 수치를 크게 개선시켰다[42,43]. 인슐린의 투여 용량은 같더라도 인슐린펌프를 사용하게 되면 통계적으로 유의미한 당화혈색소의 감소를 보이고 따라서 체질량지수 표준편차점수(body mass index z-score)가 증가하지 않는 효과를 보였다. 같은 당화혈색소 수치에서도 연속혈당측정기로 확인하였을 때 혈당의 변동폭이 감소하며, 이는 심한 저혈당 및 당뇨병성 케톤산증과 같은 급성 합병증이 감소하는 효과를 보이고, 장기적으로는 미세혈관 및 대혈관 합병증의 발병을 감소시킬 수 있을 것이다[44-46]. 실제로 같은 당화혈색소 수치에서도 인슐린 다회주사요법을 사용했을 때 보다 인슐린펌프를 사용하였을 때 당뇨병성 망막증이나 당뇨병성 말초신경병증의 합병증이 적게 나타났다고 보고되었다[47]. 인슐린펌프의 효과적인 사용을 위해서는 정기적으로 데이터를 다운로드 받아 분석하고 평가하는 것이 중요하다(Fig. 2).
인슐린펌프 사용을 중단하는 원인은 환자에 따라 여러 가지 이유가 있다. 주로 청소년기, 여자 환자에서 중단하는 경우가 많다고 알려져 있다[48,49]. 우리나라의 연구[45]에서는 인슐린펌프 사용을 중단하는 환자들의 성별이나 연령의 특징은 크게 보이지 않았으나, 인슐린펌프를 사용하는 환자의 숫자가 외국에 비해 상대적으로 매우 적기 때문에 추가적인 연구가 필요하다. 인슐린펌프를 중단하는 이유로는 착용 불편감 및 스포츠활동 장애 등의 일상생활 방해 요인, 주입세트 부착부위의 피부 관련 부작용, 고비용, 특히 센서 연동형 인슐린펌프 환자에서는 센서 정확도에 대한 만족도가 낮은 경우, 그리고 알람 피로도와 같은 여러 가지가 있다[50].
인슐린펌프의 부작용은 주로 주입세트의 문제로 발생하게 된다. 주입세트의 막힘으로 인슐린이 주입되지 않아 발생하는 당뇨병성 케톤산증의 위험성이 있고, 주입세트를 3일간 사용하게 되어 같은 부위를 통해 인슐린이 주입되어 지방이상증이 생기기 쉽고, 주입세트 부착 부위의 피부 발진, 감염, 흉터 등이 생기기 쉽다[24,50]. 따라서 주입세트 변경 시 이전 부위로부터 약 5 cm 이상 떨어진 부위에 삽입하도록 해야 한다.
4) 우리나라에서의 인슐린펌프 사용
인슐린펌프는 1970년대 후반 처음 사용되기 시작한 이후 현재 미국 및 유럽에서는 소아청소년 1형 당뇨병 환자의 약 절반가량이 인슐린펌프를 사용하고 있다[46]. 그러나 우리나라에서는 고가로 인한 경제적 부담과 적절한 교육 및 관리 시스템의 부재로 인해 널리 사용되지 못하다가[50], 2020년 1월부터 인슐린펌프에 대해 건강보험 적용이 확대 시행되면서 인슐린펌프를 사용하는 환자들이 점차 증가하고 있다.
2000년 이후 연속혈당측정기와 인슐린펌프 및 인공췌장 기술이 급격하게 발전하고 있다. 이와 같은 기술의 발전으로 인슐린펌프를 연속혈당측정기와 연결하여 사용하거나 인슐린펌프에 연속혈당측정기 데이터가 전송되어 저혈당 한계치에 도달하기 전에 기저인슐린 주입을 자동으로 멈추어 저혈당을 예방해주는 센서 연동형 인슐린펌프가 사용되고 있으며, 더 나아가 하이브리드 인공췌장 형태의 인슐린펌프도 개발되었고, 곧 국내에도 도입될 예정이다.
그러나 아직 우리나라에서는 소아청소년 1형 당뇨병 환자들의 인슐린펌프 사용에 대한 연구가 거의 없다. 2016년부터 2019년까지 3년간 54명의 환자들을 대상으로 한 연구에서 인슐린펌프를 사용하였을 때, 이전보다 당화혈색소가 통계적으로 유의하게 감소하였으며, 이는 인슐린 용량의 변화나 체질량지수 표준편차점수의 변화 없이 혈당조절이 잘 되었음을 보여주었다[45].
현재 우리나라에서는 다양한 국내 제품을 포함한 여러 종류의 인슐린펌프가 사용 가능 하며, 최근에는 패치형 펌프도 국내에서 개발되어 시판되고 있다. 현재 우리나라에서 사용 가능한 인슐린펌프는 Fig. 3에 정리하였다.
Go to : 
최근 당뇨병 관련 기술의 발전으로 연속혈당측정기와 인슐린펌프의 사용이 증가하고 있다. 연속혈당측정기와 인슐린펌프는 당화혈색소를 감소시키고 저혈당을 감소시키며, 소아청소년 연령에서도 안전하게 사용될 수 있기 때문에 1형 당뇨병 환자의 혈당관리를 위한 중요한 도구로 주목 받고 있다. 우리나라에서는 혈당 관리 기기들의 부분적인 급여화로 연속혈당측정기와 인슐린펌프의 사용이 증가하고 있는 것으로 보인다. 이러한 의료기기의 성공적인 사용을 위해서는 기기에 대한 경제적인 접근성이 좋아져야 하며, 효과적인 데이터 활용을 위한 적절한 교육과 이를 뒷받침할 충분한 수가가 마련되어야 한다. 또한, 1형 당뇨병 환자를 진료하는 의료진은 최선의 임상진료를 위해 새로운 의료기기에 대한 지식을 지속적으로 습득하는 것이 필요하다.
Go to : 
Notes
Conflict of Interest Statement
Jae Hyun Kim received honorarium from Medtronic. No other potential conflicts of interest relevant to this article was reported.
Go to : 
REFERENCES
1. Atkinson MA, Eisenbarth GS, Michels AW. 2014; Type 1 diabetes. Lancet. 383:69–82. DOI: 10.1016/S0140-6736(13)60591-7. PMID: 29916386. PMCID: PMC6661119.

2. Ilonen J, Lempainen J, Veijola R. 2019; The heterogeneous pathogenesis of type 1 diabetes mellitus. Nat Rev Endocrinol. 15:635–650. DOI: 10.1038/s41574-019-0254-y. PMID: 31534209.

3. Lee HS, Hwang JS. 2019; Genetic aspects of type 1 diabetes. Ann Pediatr Endocrinol Metab. 24:143–148. DOI: 10.6065/apem.2019.24.3.143. PMID: 31607106. PMCID: PMC6790877.

4. Lee J. 2021; Diagnosis and management of pediatric type 1 diabetes mellitus. J Korean Med Assoc. 64:425–431. DOI: 10.5124/jkma.2021.64.6.425.

5. Nathan DM. DCCT/EDIC Research Group. 2014; The diabetes control and complications trial/epidemiology of diabetes interventions and complications study at 30 years: overview. Diabetes Care. 37:9–16. DOI: 10.2337/dc13-2112. PMID: 24356592. PMCID: PMC3867999.

6. Kim JH, Lee CG, Lee YA, Yang SW, Shin CH. 2016; Increasing incidence of type 1 diabetes among Korean children and adolescents: analysis of data from a nationwide registry in Korea. Pediatr Diabetes. 17:519–524. DOI: 10.1111/pedi.12324. PMID: 26420382.

7. Patterson CC, Karuranga S, Salpea P, Saeedi P, Dahlquist G, Soltesz G, et al. 2019; Worldwide estimates of incidence, prevalence and mortality of type 1 diabetes in children and adolescents: results from the International Diabetes Federation Diabetes Atlas, 9th edition. Diabetes Res Clin Pract. 157:107842. DOI: 10.1016/j.diabres.2019.107842. PMID: 31518658.

8. Chiang JL, Kirkman MS, Laffel LM, Peters AL. Type 1 Diabetes Sourcebook Authors. 2014; Type 1 diabetes through the life span: a position statement of the American Diabetes Association. Diabetes Care. 37:2034–2054. DOI: 10.2337/dc14-1140. PMID: 24935775. PMCID: PMC5865481.

9. Ziegler R, Heidtmann B, Hilgard D, Hofer S, Rosenbauer J, Holl R, et al. 2011; Frequency of SMBG correlates with HbA1c and acute complications in children and adolescents with type 1 diabetes. Pediatr Diabetes. 12:11–17. DOI: 10.1111/j.1399-5448.2010.00650.x. PMID: 20337978.

10. DiMeglio LA, Acerini CL, Codner E, Craig ME, Hofer SE, Pillay K, et al. 2018; ISPAD Clinical Practice Consensus Guidelines 2018: glycemic control targets and glucose monitoring for children, adolescents, and young adults with diabetes. Pediatr Diabetes. 19 Suppl 27:105–114. DOI: 10.1111/pedi.12737. PMID: 30058221.

11. Holman RR, Paul SK, Bethel MA, Matthews DR, Neil HA. 2008; 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med. 359:1577–1589. DOI: 10.1056/NEJMoa0806470. PMID: 18784090.

12. Orchard TJ, Nathan DM, Zinman B, Cleary P, Brillon D, et al. Writing Group for the DCCT/EDIC Research Group. 2015; Association between 7 years of intensive treatment of type 1 diabetes and long-term mortality. JAMA. 313:45–53. DOI: 10.1001/jama.2014.16107. PMID: 25562265. PMCID: PMC4306335.

13. Bry L, Chen PC, Sacks DB. 2001; Effects of hemoglobin variants and chemically modified derivatives on assays for glycohemoglobin. Clin Chem. 47:153–163. DOI: 10.1093/clinchem/47.2.153. PMID: 11159762.

14. Ford ES, Cowie CC, Li C, Handelsman Y, Bloomgarden ZT. 2011; Iron-deficiency anemia, non-iron-deficiency anemia and HbA1c among adults in the US. J Diabetes. 3:67–73. DOI: 10.1111/j.1753-0407.2010.00100.x. PMID: 20942846.

15. American Diabetes Association. 2021; 13. Children and adolescents: standards of medical care in diabetes: 2021. Diabetes Care. 44(Suppl 1):S180–S199. DOI: 10.2337/dc21-S013. PMID: 33298424.
16. Cappon G, Vettoretti M, Sparacino G, Facchinetti A. 2019; Continuous glucose monitoring sensors for diabetes management: a review of technologies and applications. Diabetes Metab J. 43:383–397. DOI: 10.4093/dmj.2019.0121. PMID: 31441246. PMCID: PMC6712232.

17. Kim JH. 2020; Current status of continuous glucose monitoring among Korean children and adolescents with type 1 diabetes mellitus. Ann Pediatr Endocrinol Metab. 25:145–151. DOI: 10.6065/apem.2040038.019. PMID: 32871645. PMCID: PMC7538300.

18. American Diabetes Association. 2021; 7. Diabetes technology: standards of medical care in diabetes: 2021. Diabetes Care. 44(Suppl 1):S85–S99. DOI: 10.2337/dc21-S007. PMID: 33298418.
19. Battelino T, Phillip M, Bratina N, Nimri R, Oskarsson P, Bolinder J. 2011; Effect of continuous glucose monitoring on hypoglycemia in type 1 diabetes. Diabetes Care. 34:795–800. DOI: 10.2337/dc10-1989.

20. DeSalvo DJ, Miller KM, Hermann JM, Maahs DM, Hofer SE, Clements MA, et al. 2018; Continuous glucose monitoring and glycemic control among youth with type 1 diabetes: International comparison from the T1D Exchange and DPV Initiative. Pediatr Diabetes. 19:1271–1275. DOI: 10.1111/pedi.12711. PMID: 29923262. PMCID: PMC6175652.

21. Beck RW, Hirsch IB, Laffel L, Tamborlane WV, Bode BW, et al. Juvenile Diabetes Research Foundation Continuous Glucose Monitoring Study Group. 2009; The effect of continuous glucose monitoring in well-controlled type 1 diabetes. Diabetes Care. 32:1378–1383. DOI: 10.2337/dc09-0108. PMID: 19429875. PMCID: PMC2713649.

22. Tamborlane WV, Beck RW, Bode BW, Buckingham B, Chase HP, et al. Juvenile Diabetes Research Foundation Continuous Glucose Monitoring Study Group. 2008; Continuous glucose monitoring and intensive treatment of type 1 diabetes. N Engl J Med. 359:1464–1476. DOI: 10.1056/NEJMoa0805017. PMID: 18779236.

23. Danne T, Nimri R, Battelino T, Bergenstal RM, Close KL, DeVries JH, et al. 2017; International consensus on use of continuous glucose monitoring. Diabetes Care. 40:1631–1640. DOI: 10.2337/dc17-1600. PMID: 29162583. PMCID: PMC6467165.

24. Sherr JL, Tauschmann M, Battelino T, de Bock M, Forlenza G, Roman R, et al. 2018; ISPAD Clinical Practice Consensus Guidelines 2018: diabetes technologies. Pediatr Diabetes. 19 Suppl 27:302–325. DOI: 10.1111/pedi.12731. PMID: 30039513.

25. Bayram S, Kızıltan G, Akın O. 2020; Effect of adherence to carbohydrate counting on metabolic control in children and adolescents with type 1 diabetes mellitus. Ann Pediatr Endocrinol Metab. 25:156–162. DOI: 10.6065/apem.1938192.096. PMID: 32871653. PMCID: PMC7538303.

26. Battelino T, Danne T, Bergenstal RM, Amiel SA, Beck R, Biester T, et al. 2019; Clinical targets for continuous glucose monitoring data interpretation: recommendations from the International Consensus on Time in Range. Diabetes Care. 42:1593–1603. DOI: 10.2337/dci19-0028. PMID: 31177185. PMCID: PMC6973648.
27. Riddlesworth TD, Beck RW, Gal RL, Connor CG, Bergenstal RM, Lee S, et al. 2018; Optimal sampling duration for continuous glucose monitoring to determine long-term glycemic control. Diabetes Technol Ther. 20:314–316. DOI: 10.1089/dia.2017.0455. PMID: 29565197.

28. Bergenstal RM, Beck RW, Close KL, Grunberger G, Sacks DB, Kowalski A, et al. 2018; Glucose Management Indicator (GMI): a new term for estimating A1C from continuous glucose monitoring. Diabetes Care. 41:2275–2280. DOI: 10.2337/dc18-1581. PMID: 30224348. PMCID: PMC6196826.

29. International Diabetes Center. 2020. AGP Reports: Ambulatory Glucose Profile [Internet]. International Diabetes Center;St. Louis Park (MN): Available from: http://www.agpreport.org/agp/agpreports. cited 2021 Jul 16.
30. Beck RW, Buckingham B, Miller K, Wolpert H, Xing D, et al. Juvenile Diabetes Research Foundation Continuous Glucose Monitoring Study Group. 2009; Factors predictive of use and of benefit from continuous glucose monitoring in type 1 diabetes. Diabetes Care. 32:1947–1953. DOI: 10.2337/dc09-0889. PMID: 19675206. PMCID: PMC2768196.

31. Juvenile Diabetes Research Foundation Continuous Glucose Monitoring Study Group. 2010; Effectiveness of continuous glucose monitoring in a clinical care environment: evidence from the Juvenile Diabetes Research Foundation continuous glucose monitoring (JDRF-CGM) trial. Diabetes Care. 33:17–22. DOI: 10.2337/dc09-1502. PMID: 19837791. PMCID: PMC2797966.
32. Pickup JC, Freeman SC, Sutton AJ. 2011; Glycaemic control in type 1 diabetes during real time continuous glucose monitoring compared with self monitoring of blood glucose: meta-analysis of randomised controlled trials using individual patient data. BMJ. 343:d3805. DOI: 10.1136/bmj.d3805. PMID: 21737469. PMCID: PMC3131116.

33. Tsalikian E, Fox L, Weinzimer S, Buckingham B, White NH, Beck R, et al. 2012; Feasibility of prolonged continuous glucose monitoring in toddlers with type 1 diabetes. Pediatr Diabetes. 13:301–307. DOI: 10.1111/j.1399-5448.2011.00837.x. PMID: 22151826. PMCID: PMC3665108.

34. Bolinder J, Antuna R, Geelhoed-Duijvestijn P, Kroger J, Weitgasser R. 2016; Novel glucose-sensing technology and hypoglycaemia in type 1 diabetes: a multicentre, non-masked, randomised controlled trial. Lancet. 388:2254–2263. DOI: 10.1016/S0140-6736(16)31535-5. PMID: 27634581.

35. Hermanns N, Schumann B, Kulzer B, Haak T. 2014; The impact of continuous glucose monitoring on low interstitial glucose values and low blood glucose values assessed by point-of-care blood glucose meters: results of a crossover trial. J Diabetes Sci Technol. 8:516–522. DOI: 10.1177/1932296814524105. PMID: 24876615. PMCID: PMC4455434.
36. van Beers CA, DeVries JH, Kleijer SJ, Smits MM, Geelhoed-Duijvestijn PH, Kramer MH, et al. 2016; Continuous glucose monitoring for patients with type 1 diabetes and impaired awareness of hypoglycaemia (IN CONTROL): a randomised, open-label, crossover trial. Lancet Diabetes Endocrinol. 4:893–902. DOI: 10.1016/S2213-8587(16)30193-0. PMID: 27641781.

37. Mauras N, Beck R, Xing D, Ruedy K, Buckingham B, Tansey M, et al. 2012; A randomized clinical trial to assess the efficacy and safety of real-time continuous glucose monitoring in the management of type 1 diabetes in young children aged 4 to <10 years. Diabetes Care. 35:204–210. DOI: 10.2337/dc11-1746.

38. Foster NC, Beck RW, Miller KM, Clements MA, Rickels MR, DiMeglio LA, et al. 2019; State of type 1 diabetes management and outcomes from the T1D exchange in 2016-2018. Diabetes Technol Ther. 21:66–72. DOI: 10.1089/dia.2018.0384. PMID: 30657336. PMCID: PMC7061293.

39. Laffel LM, Aleppo G, Buckingham BA, Forlenza GP, Rasbach LE, Tsalikian E, et al. 2017; A practical approach to using trend arrows on the Dexcom G5 CGM system to manage children and adolescents with diabetes. J Endocr Soc. 1:1461–1476. DOI: 10.1210/js.2017-00389. PMID: 29344578. PMCID: PMC5760209.

40. Messer L, Ruedy K, Xing D, Coffey J, Englert K, Caswell K, et al. 2009; Educating families on real time continuous glucose monitoring: the DirecNet navigator pilot study experience. Diabetes Educ. 35:124–135. DOI: 10.1177/0145721708325157. PMID: 19244568. PMCID: PMC3756565.
41. Phillip M, Battelino T, Rodriguez H, Danne T, Kaufman F, et al. European Society for Paediatric Endocrinology. 2007; Use of insulin pump therapy in the pediatric age-group: consensus statement from the European Society for Paediatric Endocrinology, the Lawson Wilkins Pediatric Endocrine Society, and the International Society for Pediatric and Adolescent Diabetes, endorsed by the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care. 30:1653–1662. DOI: 10.2337/dc07-9922. PMID: 17372151.

42. Bergenstal RM, Tamborlane WV, Ahmann A, Buse JB, Dailey G, Davis SN, et al. 2010; Effectiveness of sensor-augmented insulin-pump therapy in type 1 diabetes. N Engl J Med. 363:311–320. DOI: 10.1056/NEJMoa1002853. PMID: 20587585.

43. Zimmerman C, Albanese-O'Neill A, Haller MJ. 2019; Advances in type 1 diabetes technology over the last decade. Eur Endocrinol. 15:70–76. DOI: 10.17925/EE.2019.15.2.70. PMID: 31616496. PMCID: PMC6785958.

44. Karges B, Schwandt A, Heidtmann B, Kordonouri O, Binder E, Schierloh U, et al. 2017; Association of insulin pump therapy vs insulin injection therapy with severe hypoglycemia, ketoacidosis, and glycemic control among children, adolescents, and young adults with type 1 diabetes. JAMA. 318:1358–1366. DOI: 10.1001/jama.2017.13994. PMID: 29049584. PMCID: PMC5818842.

45. Lee YJ, Lee YA, Kim JH, Chung HR, Gu MJ, Kim JY, et al. 2020; The durability and effectiveness of sensor-augmented insulin pump therapy in pediatric and young adult patients with type 1 diabetes. Ann Pediatr Endocrinol Metab. 25:248–255. DOI: 10.6065/apem.2040048.024. PMID: 33401881. PMCID: PMC7788343.

46. Sherr JL, Hermann JM, Campbell F, Foster NC, Hofer SE, Allgrove J, et al. 2016; Use of insulin pump therapy in children and adolescents with type 1 diabetes and its impact on metabolic control: comparison of results from three large, transatlantic paediatric registries. Diabetologia. 59:87–91. DOI: 10.1007/s00125-015-3790-6. PMID: 26546085.

47. Zabeen B, Craig ME, Virk SA, Pryke A, Chan AK, Cho YH, et al. 2016; Insulin pump therapy is associated with lower rates of retinopathy and peripheral nerve abnormality. PLoS One. 11:e0153033. DOI: 10.1371/journal.pone.0153033. PMID: 27050468. PMCID: PMC4822832.

48. Hofer SE, Heidtmann B, Raile K, Frohlich-Reiterer E, Lilienthal E, Berghaeuser MA, et al. 2010; Discontinuation of insulin pump treatment in children, adolescents, and young adults. A multicenter analysis based on the DPV database in Germany and Austria. Pediatr Diabetes. 11:116–121. DOI: 10.1111/j.1399-5448.2009.00546.x. PMID: 19566740.

49. Wong JC, Boyle C, DiMeglio LA, Mastrandrea LD, Abel KL, Cengiz E, et al. 2017; Evaluation of pump discontinuation and associated factors in the T1D Exchange clinic registry. J Diabetes Sci Technol. 11:224–232. DOI: 10.1177/1932296816663963. PMID: 27595711. PMCID: PMC5478021.

50. Gu M. 2020; Effective use of insulin pump in patients with type 1 diabetes. J Korean Diabetes. 21:36–40. DOI: 10.4093/jkd.2020.21.1.36.

Go to : 




 PDF
PDF Citation
Citation Print
Print




 XML Download
XML Download