Abstract
Eosinophilic otitis media is characterized by highly viscous middle ear effusion and associated with bronchial asthma and chronic rhinosinusitis with nasal polyps. It is difficult to treat with conventional therapy such as corticosteroid and ventilation tube insertion. We have encountered a 58-year-old patient with refractory eosinophilic otitis media who was successfully treated with dupilumab.
호산구성 중이염은 점성이 높은 중이의 호산구성 삼출액을 특징적으로 하는 난치성의 중이염으로, 기관지천식과 비용종을 동반한 만성부비동염의 원인으로 생각되는 호흡기의 제2형 알레르기 염증반응에 의해 발생한다고 알려져 있다[1]. 50-60세의 여성에서 잘 생기며 양측 중이를 침범하는 경우가 81%로 높게 보고되고 있다[2]. 이 질환은 치료하지 않을 경우 중증의 혼합성 난청 또는 청각장애로 악화될 수 있기 때문에 적절한 치료가 필요하다[1].
호산구성 중이염의 치료는 국소 또는 전신 스테로이드로 시행되며, 유양돌기절제술이나 고실성형술과 같은 수술적 치료는 감각신경성 난청을 악화시킬 수 있어 권고되지 않는다[2]. 하지만 기존의 치료법은 재발이 많아 새로운 치료법에 대한 필요성이 대두되고 있다[3].
항 면역글로불린 E, 항 인터루킨-5 단일클론성 항체와 같은 생물학적 제제는 근래에 제2형 알레르기 염증반응에 의한 천식과 비용종을 동반한 만성부비동염에 널리 사용되고 있다[3]. 호산구성 중이염의 삼출액에는 호산구와 제2형 알레르기 염증반응과 연관된 면역글로불린 E, 인터루킨-5와 같은 물질이 다수 존재한다는 점을 통해 최근 들어 호산구성 중이염에도 이러한 생물학적 제제를 이용한 사례가 국외에서 일부 보고되고 있다[4,5]. 하지만 국내에서의 보고는 극히 드문 것으로 확인된다.
저자들은 기저질환으로 천식 및 비용종을 동반한 만성부비동염이 있으며 양측 호산구성 중이염으로 경구 스테로이드 및 환기관 삽입술을 시행하였으나 지속적으로 재발하는 환자에서 생물학적 제제인 dupilumab을 사용한 뒤 안정적으로 치료된 증례를 경험하였고, 이를 문헌 고찰과 함께 보고하는 바이다.
58세 남자 환자로 2달 전부터 시작된 양측 청력저하 및 이통을 주소로 내원하였다. 환자는 기저질환으로 천식이 있으며 세 차례 천식 발작으로 입원하여 치료받은 적이 있고 현재는 스테로이드 흡입제로 치료 유지 중이나 간헐적으로 숨 차는 증상이 있었다. 이외 양측 비용종을 동반한 만성부비동염에 대해 두 차례 양측 내시경하 부비동 수술을 받은 적이 있으며 간헐적으로 재발하는 양측 농성 비루에 대해 경구 스테로이드 및 항생제 치료 중이었다.
내시경에서 양측 고막에 천공은 없었으나 우측 고막의 팽륜과 양측 고막 안쪽으로 점액성의 삼출액이 관찰되었다(Fig. 1). 비인강에는 아데노이드의 비대 소견은 관찰되지 않았다. 순음청력검사상 우측 귀의 기도청력역치 51 dB, 골도청력역치 16 dB이며 좌측 귀의 기도청력역치 48 dB, 골도청력역치 14 dB로 양측의 전음성 난청 소견이 보였다. 고막 운동성 검사에서는 양측 B형이 확인되었다.
양측 삼출성 중이염 의심하에 경구 항생제 및 삼출액 흡인 치료를 시행하였다. 하지만 치료 직후에는 증상의 호전이 있었으나 1개월도 되지 않아 증상이 재발하였다. 세 차례의 경구 항생제 및 삼출액 흡인 치료에도 불구하고 지속되는 재발 소견에 대해 국소마취하 양측 환기관 삽입술을 시행하였다. 고막에 절개를 가한 후 중이를 관찰하였으며, 삼출액보다는 육아조직에 가까운 점성이 높은 물질이 확인되었고 흡인이 잘 되지 않는 양상이었다(Fig. 2). 이에 대해 조직검사를 시행하였다.
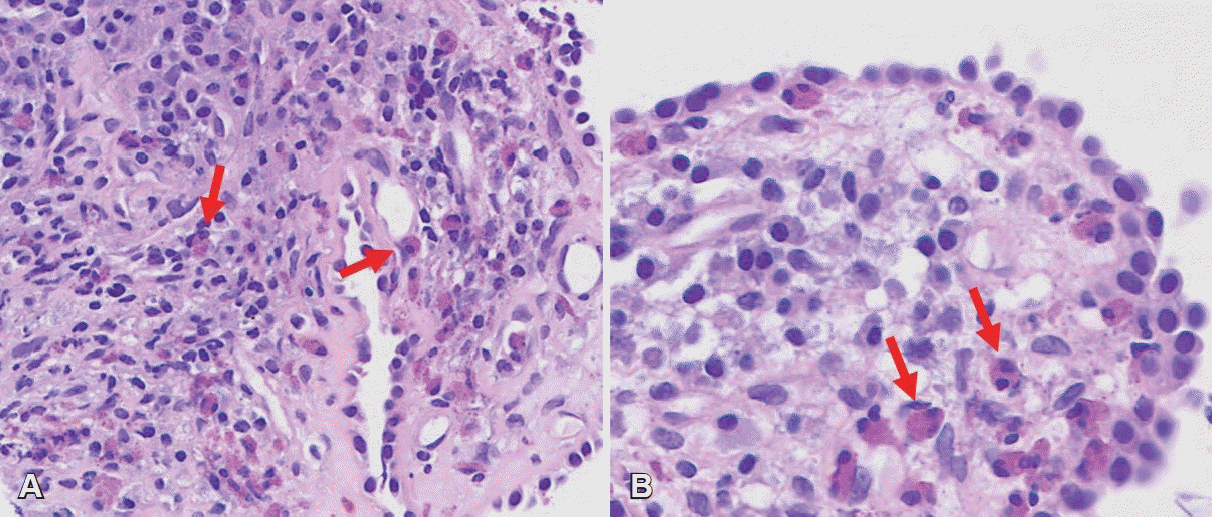
조직검사에서 광학 현미경 고배율(×400)상 림프구와 호중구가 관찰되는 염증성 배경에 다수의 호산구가 침윤된 소견이 관찰되었다(Fig. 3).
2011년도 Iino 등[6]이 제시한 진단기준에 따라 호산구가 다수 침범한 중이염의 조직검사 소견과 더불어 중이의 점성 높은 삼출액, 기존의 치료에 잘 반응하지 않는 점, 그리고 천식과 비용종을 동반한 만성부비동염의 과거력을 종합해 봤을 때 양측 호산구성 중이염으로 진단할 수 있었다. 또한 발열, 피부발진, 신경통 및 관절통 등의 전신증상이 없어 척-스트라우스 증후군도 배제할 수 있었다.
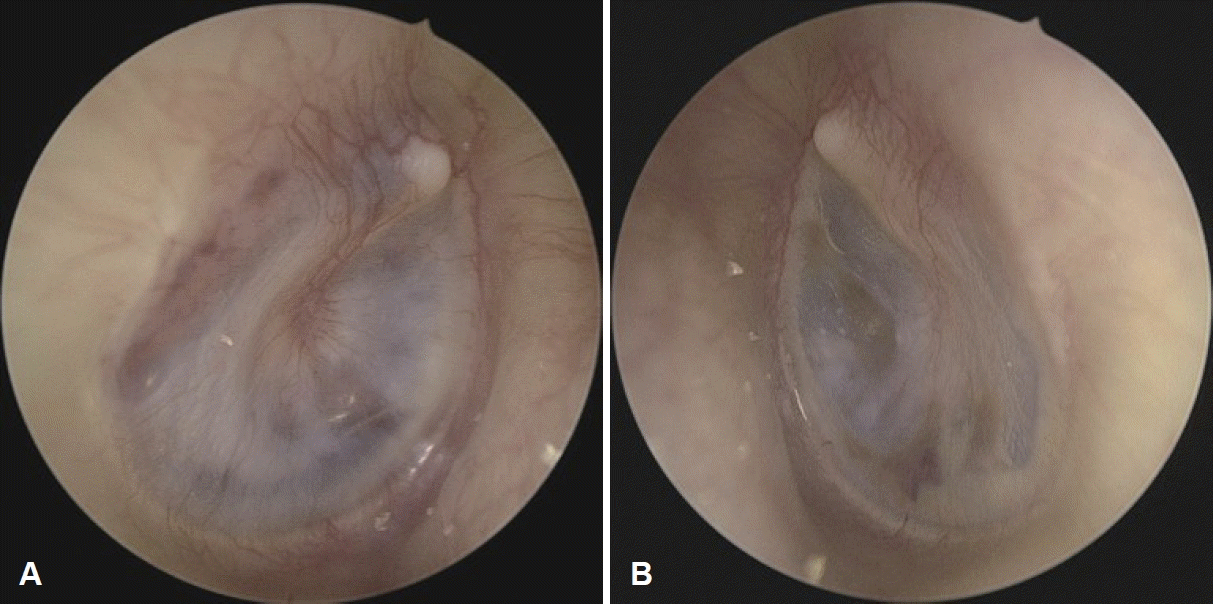
이에 대해 경구 스테로이드 치료를 병행하였으나 효과가 1개월 내외로 오래 지속되지 않고 네 차례 재발하였으며, 고막 내측의 고점도성 삼출액에 의해 환기관이 지속적으로 밀려나와 탈출하였다. 난치성의 호산구성 중이염 소견에 대해 호흡기내과와 상의하에 동반된 천식과 함께 치료하기 위한 목적으로 생물학적 제제인 dupilumab (인터루킨-4 수용체 알파 길항제)을 투여하기로 하였으며, 피하주사로 1년 동안월 2회, 총 24회 투여를 계획하였다. 환자분은 6개월 뒤, 12회 투여 이후 외래 내원하였으며 증상의 재발 없이 청력저하와 이통 모두 호전되었다고 하였다. 순음청력검사상 우측 귀의 기도청력역치 23 dB, 골도청력역치 18 dB이며 좌측 귀의 기도청력역치 21 dB, 골도청력역치 13 dB로 양측의 기도-골도차가 상당히 호전된 소견이 확인되었으며 고막 운동성 검사에서 양측 A형이 확인되었다. 내시경에서도 양측 고막 안쪽의 점액성 삼출액이 감소하였다(Fig. 4). 더불어 동반된 비용종성 만성부비동염에 의한 양측 농성 비루가 호전되었으며 폐기능검사상 1초간 노력성 호기량의 증가 소견이 확인되었고 간헐적으로 숨이 찬 증상도 없어졌다고 하였다. 이외 약물에 의한 부작용은 없었다. 환자는 추후 외래에서 지속 추적관찰 할 예정이다.
제2형 알레르기 염증반응은 천식, 만성폐쇄성폐질환, 비용종을 동반한 만성부비동염, 알레르기비염과 같은 만성 상기도 및 하기도 질병의 원인으로 알려져 있다[7]. 이 반응은 2형 조력 T세포와 2형 선천성 림프 세포에 의해 분비되는 인터루킨-4, 인터루킨-5, 인터루킨-13과 같은 2형 사이토카인에 의해 호산구가 조직으로 침투하여 일어난다[7]. 호산구성 중이염의 삼출액을 검사하였을 때 높은 농도의 호산구 양이온 단백질과 인터루킨-5, 에오탁신(eotaxin)과 같은 화학유인물질이 확인되어 이 또한 제2형 알레르기 염증반응에 의해 생기는 것으로 생각되고 있다[3]. 이전 연구에 따르면 호산구성 중이염의 환자들 중 75%에서 기관지천식과 비용종성 부비동염을 앓았던 것으로 보고되었다[2].
호산구성 중이염에 대한 기존의 치료법은 이러한 제2형 알레르기 염증반응을 줄이기 위해 고실내 스테로이드 주사 또는 전신적 스테로이드를 투여하거나 환기관 삽입술로 시행되었다[1]. 이러한 방법들은 효과적이지만 장기적으로 그 효과가 유지되지는 않는다고 보고된다[8]. 최근에는 제2형 알레르기 염증반응을 일으키는 인터루킨-4, 인터루킨-5, 인터루킨-13과 같은 사이토카인을 표적으로 하는 생물학적 제제가 천식 및 만성부비동염에 사용되고 있으며 같은 기전에 의한 호산구성 중이염에도 유용하다는 보고가 일부 이뤄지고 있다[3-5]. 생물학적 제제는 표적으로 하는 사이토카인에 따라 종류가 다양하며 항 인터루킨-4인 dupilumab, 항 인터루킨-5인 mepolizumab, 항 인터루킨-13인 lebricizumab, 항 면역글로불린 E인 omalizumab 등이 있다[2]. Benralizumab, mepolizumab, reslizumab을 사용한 후향적 연구에서는 생물학적 제제를 사용한 경우에 내시경 및 주관적 소견이 사용하지 않은 경우보다 54%-57% 더 향상되었다고 보고하였다[9]. 한 체계적 문헌고찰에서도 omalizumab, mepolizumab, benralizumab을 사용한 이후 더 높은 증상의 완화율과 스테로이드 사용의 감소를 확인하였다[8]. Dupilumab을 사용하여 효과적으로 치료한 사례 연구가 보고되었으며, 스테로이드 사용과 증상의 악화 빈도 및 중증도를 유의미하게 줄일 수 있었다는 후향적 연구도 확인된다[5,10]. 이 외에도 mepolizumab을 사용하거나 dupilumab과 benralizumab을 교차로 사용하여 효과적으로 치료한 사례 연구도 확인된다[11,12]. 아직까지 호산구성 중이염에 있어 생물학적 제제 사용 후 중단시 재발에 관한 연구가 보고되지는 않았으나, 비용종성 부비동염에서 omalizumab을 사용한 임상시험에서는 치료 중단 이후 6개월째 증상의 악화가 있었으나 치료 전에 비해서는 증상이 경미하며 치료 효과가 유지되는 것이 확인되었다[13]. 본 증례에서는 6개월간의 dupilumab 투여 이후 재발 없이 증상 및 내시경 소견 모두 호전된 것이 확인되었다. 하지만 내시경상 중이의 삼출액이 소량 남아있으며, 청력검사상 기도-골도차가 일부 존재하는 것으로 보아 추후 지속적인 관찰을 통해 완치 여부와 함께 약제 중단시 효과의 지속 및 재발 여부에 대한 확인이 필요할 것으로 생각된다.
호산구성 중이염은 적절한 치료가 되지 않을시 50%에서 골전도 청력이 감소하며 6%에서는 전농까지 일어날 수 있기 때문에 기존 치료에 반응이 없을시 생물학적 제제를 통한 치료의 선택지도 고려가 필요하겠다[2]. 또한 이를 통해 동반된 천식과 비용종성 비부비동염의 호전도 기대해볼 수 있다[7]. 본 증례의 경우 dupilumab을 사용하는 동안 기존 증상의 악화 및 부작용이 관찰되지 않았다. 하지만 이전 연구들에서 dupilumab을 사용한 이후 일부 환자들에서 혈중 호산구 수치의 상승이 확인되었으며 호산구성 폐렴과 척-스트라우스 증후군에 이르는 심각한 부작용까지 관찰되었기 때문에 약제를 사용한 이후 지속적인 혈액검사와 전신증상 발현 여부를 확인하는 것이 필요하겠다[14,15]. 추후 효과 및 부작용에 대한 다수 연구의 확보와 고액의 치료 비용에 대한 보험 문제 해결이 필요할 것으로 생각된다.
본 증례를 통해 호산구성 중이염이 확진된 환자에서 스테로이드와 환기관 삽입술과 같은 기존의 치료법에 잘 반응하지 않는 경우 생물학적 제제를 사용하여 성공적으로 치료할 수 있음을 경험하였기에 이를 공유하고자 보고하는 바이다.
Notes
Author contributions
Conceptualization: Jae Jun Song. Data curation: Hyunseok Choi. Formal analysis: Hyunseok Choi, Sung Won Chae. Investigation: Hyunseok Choi, Dongha Kim. Methodology: Hyunseok Choi. Project administration: Sung Won Chae. Supervision: Jae Jun Song, Sung Won Chae. Validation: Dongha Kim. Visualization: Hyunseok Choi. Writing—original draft: Hyunseok Choi. Writing—review & editing: Hyunseok Choi, Jae Jun Song.
REFERENCES
1. Iino Y. Eosinophilic otitis media; state-of-the-art diagnosis and treatment. Auris Nasus Larynx. 2023; 50(4):479–89.
2. Shevchik E, Svistushkin V, Nikiforova G, Zolotova A. Eosinophilic otitis media: modern aspects of pathogenesis, clinical features, diagnosis and treatment. Indian J Otolaryngol Head Neck Surg. 2022; 74(Suppl 1):132–40.
3. De Corso E, Montuori C, Settimi S, Mele DA, Cantiani A, Corbò M, et al. Efficacy of biologics on refractory eosinophilic otitis media associated with bronchial asthma or severe uncontrolled CRSwNP. J Clin Med. 2022; 11(4):926.
4. Iino Y, Sekine Y, Yoshida S, Kikuchi S. Dupilumab therapy for patients with refractory eosinophilic otitis media associated with bronchial asthma. Auris Nasus Larynx. 2021; 48(3):353–60.
5. van der Lans RJL, van Spronsen E, Fokkens WJ, Reitsma S. Complete remission of severe eosinophilic otitis media with dupilumab: a case report. Laryngoscope. 2021; 131(12):2649–51.
6. Iino Y, Tomioka-Matsutani S, Matsubara A, Nakagawa T, Nonaka M. Diagnostic criteria of eosinophilic otitis media, a newly recognized middle ear disease. Auris Nasus Larynx. 2011; 38(4):456–61.
7. Maspero J, Adir Y, Al-Ahmad M, Celis-Preciado CA, Colodenco FD, Giavina-Bianchi P, et al. Type 2 inflammation in asthma and other airway diseases. ERJ Open Res. 2022; 8(3):00576–2021.
8. Chen T, Ashman PE, Bojrab DI 2nd, Johnson AP, Hong RS, Benson B, et al. Diagnosis and management of eosinophilic otitis media: a systematic review. Acta Otolaryngol. 2021; 141(6):579–87.
9. Ryder CY, Zacharek MA, Welch CM. Improvement of suspected eosinophilic otitis media with targeted biologic therapy. Otol Neurotol. 2023; 44(5):462–8.
10. Nakashima D, Nakayama T, Minagawa S, Adachi T, Mitsuyama C, Shida Y, et al. Dupilumab improves eosinophilic otitis media associated with eosinophilic chronic rhinosinusitis. Allergol Int. 2023; 72(4):557–63.
11. Hamada S, Ogino E, Yasuba H. Cycling therapy with benralizumab and dupilumab for severe eosinophilic asthma with eosinophilic chronic rhinosinusitis and eosinophilic otitis media. Allergol Int. 2021; 70(3):389–91.
12. Suzaki I, Kimura Y, Tanaka A, Hirano K, Ishibashi A, Mizuyoshi T, et al. Successful treatment of eosinophilic otitis media associated with severe bronchial asthma with an anti-IL-5 monoclonal antibody, mepolizumab. Auris Nasus Larynx. 2019; 46(1):141–6.
13. Gevaert P, Saenz R, Corren J, Han JK, Mullol J, Lee SE, et al. Long-term efficacy and safety of omalizumab for nasal polyposis in an open-label extension study. J Allergy Clin Immunol. 2022; 149(3):957–65.e3.
14. Kurihara M, Masaki K, Matsuyama E, Fujioka M, Hayashi R, Tomiyasu S, et al. How can dupilumab cause eosinophilic pneumonia? Biomolecules. 2022; 12(12):1743.
15. Suzaki I, Tanaka A, Yanai R, Maruyama Y, Kamimura S, Hirano K, et al. Eosinophilic granulomatosis with polyangiitis developed after dupilumab administration in patients with eosinophilic chronic rhinosinusitis and asthma: a case report. BMC Pulm Med. 2023; 23(1):130.
Fig. 1.
Endoscopic findings of right ear (A) and left ear (B). Right tympanic membrane shows mild bulging and viscous middle ear effusion is visible inside both eardrums.
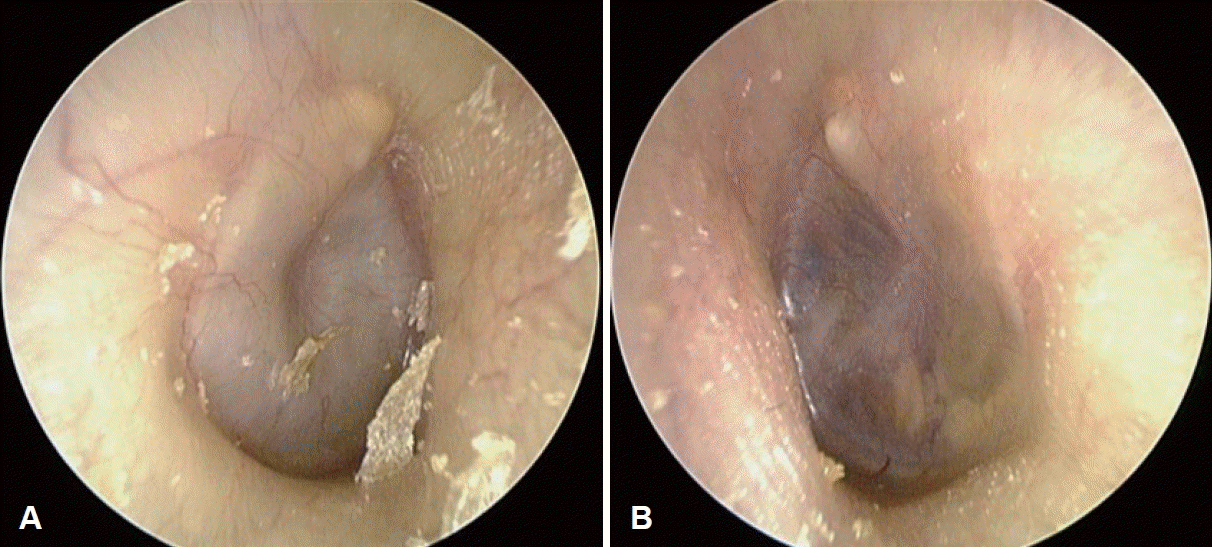
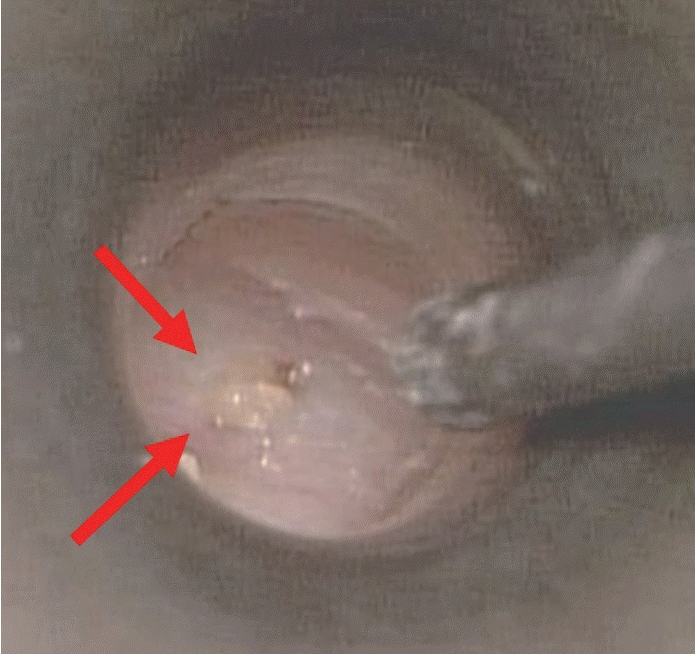
Fig. 2.
Microscopic finding of right ear shows highly viscous granulation tissue inside tympanic membrane after myringotomy (arrows).




 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download