Abstract
The rapid COVID-19 polymerase chain reaction (PCR) test using Xpert Xpress SARS-CoV-2 and the conventional COVID-19 PCR test using Standard M nCoV Detection were compared after matching for sex, age, and hospitalization period. The rapid COVID-19 PCR test group exhibited shorter turnaround time and emergency department stay.
COVID-19는 2019년 12월 중국 우한에서 처음 발생한 이후 중국 전역과 전 세계로 확산된, 새로운 유형의 코로나바이러스(SARS-CoV-2)에 의한 호흡기 감염질환이다[1]. COVID-19 감염의 확산을 막고 적절한 치료를 위해서는 신속하고 정확한 COVID-19 검사가 매우 중요하다. 흔히 검사실에서 표준방법으로 사용되는 것은 유전자 증폭을 이용한 PCR 기반의 분자진단법이다[2]. 이는 진단 정확도가 높지만, 검체 전처리, 바이러스 핵산 추출, COVID-19 특이유전자 부위 증폭, 및 결과 분석에 약 6시간이 소요되며, 일괄검사(batch test)로 개발되어 있다[2]. 이에 비해 COVID-19 PCR 신속 검사는 약 1시간 이내에 검사 결과를 얻을 수 있어 빠른 결과를 확인해야 하는 응급상황의 경우 특히 유용하다[3]. 본 연구의 목적은 COVID-19가 의심되지 않는 응급실 내원환자를 대상으로 COVID-19 PCR 신속 검사가 응급실 체류시간의 감소에 도움이 되는지 알아보는 것이다.
경기도에 위치한 905병상 규모의 종합병원 응급실에 내원한 환자를 대상으로 하였다. 응급실의 병상 수는 33병상이고 연구 기간 중 일평균 환자수는 103명이었다. COVID-19 PCR 통상 검사(conventional test)로는 Standard M nCoV Detection (SD Biosensor Inc., Suwon, Korea)로 하였고, COVID-19 PCR 신속 검사는 Xpert Xpress SARS-CoV-2 (Cepheid, Sunnyvale, CA)로 검사하였다. 본원 COVID-19 PCR 검사의 처방 지침은 다음과 같다. COVID-19 PCR 통상 검사의 경우 COVID-19 감염 의심 환자, 응급실 내원 환자, 입원 예정 환자, 및 응급분만 환자이고, COVID-19 PCR 신속 검사의 경우 응급실 내원 환자 및 응급분만 환자이다.
COVID-19 PCR 신속 검사는 Xpert Xpress SARS-CoV-2 (Cepheid)는 실시간 중합효소법(real-time reverse transcriptase PCR, real-time RT-PCR)으로 비인두 면봉(nasopharyngeal swab) 혹은 비강면봉(nasal swab)같은 상부호흡기 검체에서 사스 코로나바이러스-2 (SARS-CoV-2)의 핵산을 정성적으로 검출한다[4,5]. COVID-19 PCR 신속 검사는 검체가 접수되는 대로 검사를 실시하고 있다(2021년 기준). COVID-19 PCR 통상 검사는 실시간 중합효소법인 Standard M nCoV Detection (SD Biosensor)을 이용하여 6시간 마다 검사를 실시하고 있다(2021년 기준) [6]. 연구 기간 동안 COVID-19 PCR 통상 검사의 양성률은 10.7% (4,169/39,006)이었고, COVID-19 PCR 신속 검사의 양성률은 10.1% (1,013/ 10,048)로 큰 차이가 없었다.
연구 대상은 2021년 1월부터 2022년 5월까지 한 개의 종합병원 응급실에 내원하여 COVID-19 PCR 신속 검사를 시행한 환자와 COVID-19 PCR 통상 검사를 시행한 환자 중 중복없이 총 228명(신속 검사 107명, 통상 검사 121명)을 선정하였다. 선정 시 COVID-19(검사 양성)환자는 제외하였고, 연구 대상 환자들은 COVID-19 관련 증상은 보이지 않았다. 검사소요시간(turnaround time, TAT)은 검체 접수에서 결과 보고까지 소요된 시간으로 진단검사의학과 데이터 베이스에서 확보하였고, 응급실 체류시간은 퇴원결정시각과 응급실 내원시각의 차이로 원무기록을 통해 구하였다. 또한 전자의무기록을 검토를 통해 임상적인 정보(성별, 연령, 진단명, 전체 체류일, 입원 유무, 치료법 및 한국형 응급환자 분류도구에 필요한 임상정보)를 얻었다.
본 연구에서는 응급실 체류시간에 영향을 줄 것으로 예상하는 변수들을 매칭한 후 비교하였을 때 COVID-19 PCR 신속 검사를 받은 군의 응급실 체류시간이 유의하게 짧았다는 것을 제시하고자 하였다. 사용한 교란 변수는 성별, 연령 및 입원기간으로, 이 때 병원입원 기간은 단기(1일 이하), 중기(2-14일) 및 장기(15일 이상)로 구분하였다. 응급실에서 COVID-19 PCR 신속 검사를 시행한 군과 COVID- 19 PCR 통상 검사를 시행한 군 간에 성별, 연령, 및 병원입원기간의 P값은 각각 0.792, 0.378, 및 0.410으로 통계적인 차이가 없었다. 교란 변수에 대해 차이가 없는 것을 확인한 후 검사소요시간(turnaround time, TAT)과 응급실 체류시간을 각각 비교하였다. 또한 두 군 간의 특성을 비교하기 위하여 입원(병동 혹은 중환자실) 유무, 치료법(수술 및 중재술 포함) 및 한국형 응급환자 분류도구의 단계도 검토하였다. 통계적 분석은 SAS program version 9.4 (SAS Institute, Cary, NC, USA)를 사용하여 기술통계량, T-test, 및 카이제곱 검정을 실시하였다. 본 연구는 기관생명윤리위원회의 연구 승인을 받았다(IRB 22-04-002).
COVID-19 PCR 통상 검사를 시행한 환자의 TAT는 평균 281분(표준편차 17분)이었고, COVID-19 PCR 신속 검사를 시행한 환자의 TAT는 평균 55분(표준편차 6분)을 보여 통계적으로 유의한 차이가 있었다(Fig. 1). COVID- 19 PCR 통상 검사를 시행한 환자의 응급실 체류시간은 평균 453분(표준편차 203분)이었고, COVID-19 PCR 신속 검사를 시행한 환자의 응급실 체류시간은 평균 358분(표준편차 294분)을 보여 통계적으로 유의한 차이가 있었다(Fig. 2). 제시한 교란 변수 외 특성을 한국형 응급환자 분류, 치료법(수술/중재/약물치료만), 입원 유무(중환자실/병동/응급실 퇴원) 및 기저질환(주진단명, Supplementary Table 1)으로 비교해 보았는데, 두 군 간에 한국형 응급환자 분류 단계와 치료법은 차이가 있었지만(P값 각각 <0.001과 0.003), 입원 유무는 차이가 없었다(P값 0.263, Table 1).
빠르고 정확한 COVID-19 PCR 검사는 치료 및 관리에 필수적이며, 특히 COVID-19 의심 증상을 보이는 응급 환자를 치료하려면 감염 여부를 확인할 수 있는 것이 필수적이다. COVID-19 PCR 통상 검사는 COVID-19 감염의 진단의 표준검사로 생각되고 있으며, 세계보건기구에서도 확진 검사로 권장하고 있다[7]. 이 진단검사법은 감염된 환자의 검체 안에 있는 아주 적은 양의 바이러스를 확인할 만큼 민감하며, 동시에 감염되지 않은 사람에서는 정확하게 음성 결과가 나올 만큼 특이적인 검사법이다[7]. 환자의 검체에 존재하는 SARS-CoV-2의 특이한 유전자 부위를 두 군데 이상을 real time RT-PCR을 이용해 통해 수 천 배 이상으로 증폭함으로써 민감하게 진단할 수 있다[7]. 하지만 검사 소요시간이 상대적으로 길고, 일괄검사로 개발되어 있어, 대부분 병원에서 운영시간을 정해두고 검사를 실시하고 있으며, 따라서 신속한 진단에는 적절하지 않은 단점이 있다[7].
검사 소요시간이 좀더 짧고 단독 수시 검사가 가능한 검사로는 COVID-19 항원 검사와 COVID-19 PCR 신속 검사가 있다. 이중 항원검사는 특이도는 좋지만 민감도가 낮아[8], COVID-19 PCR 신속 검사의 시약을 충분히 확보하지 못하였거나, 장비와 인력이 없는 기관에서 주로 이용되고 있다. 국내에서 흔히 사용되는 Xpert Xpress SARS-CoV-2 (Cepheid)와 BioFire Respiratory Panel 2.1 (bioMérieux, Marcy-l’étoile, France)은 민감도와 특이도가 우수한 것으로 알려져 있다. Xpert Xpress SARS-CoV-2는 미국 식품의약품국의 응급사용허가를 받은 real time RT-PCR 검사로, 양성 검사 결과를 얻는 데 30분 정도 밖에 소요되지 않고, 검체 하나씩 검사할 수 있는 랜덤 엑세스 방식이며, 핵산 추출부터 증폭 및 판정까지 전 과정이 자동으로 이루어져서 응급검사에 활용이 가능하다[8]. BioFire assay는 FilmArray법으로 종단점 DNA 용융 곡선 분석(endpoint DNA melting curve analysis)으로, Xpert와 동일하게 신속한 COVID-19를 검출이 가능하고, 샘플대 응답 탐지(sample to answer detection)를 갖추고 있다[8].
기존 연구에서 Xpert Xpress SARS-CoV-2 (Cepheid)는 COVID-19 PCR 통상 검사와 비교했을 때, 민감도 100% (95% confidence interval [CI], 88.1-100)와 특이도 97.2% (95% CI, 89.4-99.3)를 보였고, BioFire Respiratory Panel 2.1 (bioMérieux)은 98% 이상의 양성일치도(positive percent agreement)와 100%의 음성일치도(negative percent greement)를 보였다[5]. 국내에서는 COVID-19 PCR 검사가 현장검사로 시행되고 있지 않아 도입은 어렵지만, 15분 내에 검사결과를 얻을 수 있는 현장 검사인 ID NOW COVID-19 system (IDNOW)을 이용한 경우 응급실 체류시간이 COVID-19 PCR 신속 검사인 Xpert Xpress SARS-CoV-2 (Cepheid)나 BioFire Respiratory Panel 2.1 (bioMérieux)을 사용한 시기에 비해 의미있게 감소하였다는 보고가 있다(평균 276분과 208분, P<0.0001) [9]. 이러한 연구는 신속한 COVID-19 결과를 얻을수록 응급실 체류 시간의 감소 효과가 있다는 것을 시사한다.
본 연구 결과에서 COVID-19 PCR 신속 검사를 시행한 환자군에서의 TAT와 응급실 체류시간이 COVID-19 PCR 통상 검사를 받은 환자군에 비해 짧았는데, 아마도 TAT가 짧아 결과를 좀 더 빨리 확인할 수 있었고, 이를 바탕으로 환자에 대한 의사결정이 신속하게 이루어졌을 가능성이 있다. 따라서 응급환자에서 COVID-19 신속 검사가 충분한 시행되도록 노력하는 것이 필요하겠다.
결론적으로 응급실에서 COVID-19 PCR 신속 검사를 적용한 환자군은 TAT와 응급실 체류 시간이 짧아 응급실 내원 환자에서의 임상적 유용성을 확인할 수 있었다.
Supplementary material can be found via https://doi.org/10.14192/kjicp.2024.29.1.59.
REFERENCES
1. Ochani R, Asad A, Yasmin F, Shaikh S, Khalid H, Batra S, et al. 2021; COVID-19 pandemic: from origins to outcomes. A comprehensive review of viral pathogenesis, clinical manifestations, diagnostic evaluation, and management. Infez Med. 29:20–36.
2. Tang YW, Schmitz JE, Persing DH, Stratton CW. 2020; Laboratory diagnosis of COVID-19: current issues and challenges. J Clin Microbiol. 58:e00512–20. DOI: 10.1128/JCM.00512-20. PMID: 32245835. PMCID: PMC7269383.
3. Rödel J, Egerer R, Suleyman A, Sommer-Schmid B, Baier M, Henke A, et al. 2020; Use of the variplexTM SARS-CoV-2 RT-LAMP as a rapid molecular assay to complement RT-PCR for COVID-19 diagnosis. J Clin Virol. 132:104616. DOI: 10.1016/j.jcv.2020.104616. PMID: 32891938. PMCID: PMC7457909.
4. Bruijns B, Folkertsma L, Tiggelaar R. 2022; FDA authorized molecular point-of-care SARS-CoV-2 tests: a critical review on principles, systems and clinical performances. Biosens Bioelectron X. 11:100158. DOI: 10.1016/j.biosx.2022.100158. PMID: 35619623. PMCID: PMC9122839.
5. Kim M, Kim HS, Bae HG, Huh HJ, Sung H. 2021; Laboratory diagnosis and utilization for COVID-19. Korean J healthc assoc Infect Control Prev. 26:47–56. DOI: 10.14192/kjicp.2021.26.2.47.
6. Hur KH, Park K, Lim Y, Jeong YS, Sung H, Kim MN. 2020; Evaluation of four commercial kits for SARS-CoV-2 real-time reverse-transcription polymerase chain reaction approved by emergency-use-authorization in Korea. Front Med (Lausanne). 7:521. DOI: 10.3389/fmed.2020.00521. PMID: 32903503. PMCID: PMC7438443.
7. World Health Organization (WHO). 2020. Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases. WHO;Geneva: p. 1–7.
8. Park J, Kim SY, Lee J, Hong KH. 2023; Clinical evaluation of BioFire COVID-19 test, BioFire respiratory panel 2.1, and Cepheid Xpert Xpress SARS-CoV-2 assays for sample-to-answer detection of SARS-CoV-2. Genes (Basel). 14:233. DOI: 10.3390/genes14010233. PMID: 36672974. PMCID: PMC9859140.
9. Baron A, Peyrony O, Salmona M, Mahjoub N, Ellouze S, Anastassiou M, et al. 2022; Impact of fast SARS-CoV-2 molecular point-of-care testing on patients' length of stay in an emergency department. Microbiol Spectr. 10:e0063622. DOI: 10.1128/spectrum.00636-22. PMID: 35730967. PMCID: PMC9431206.
Fig. 1
Turnaround time of rapid test and confirm test of COVID- 19. The horizontal line refers to mean value.
Abbreviation: min, minute.
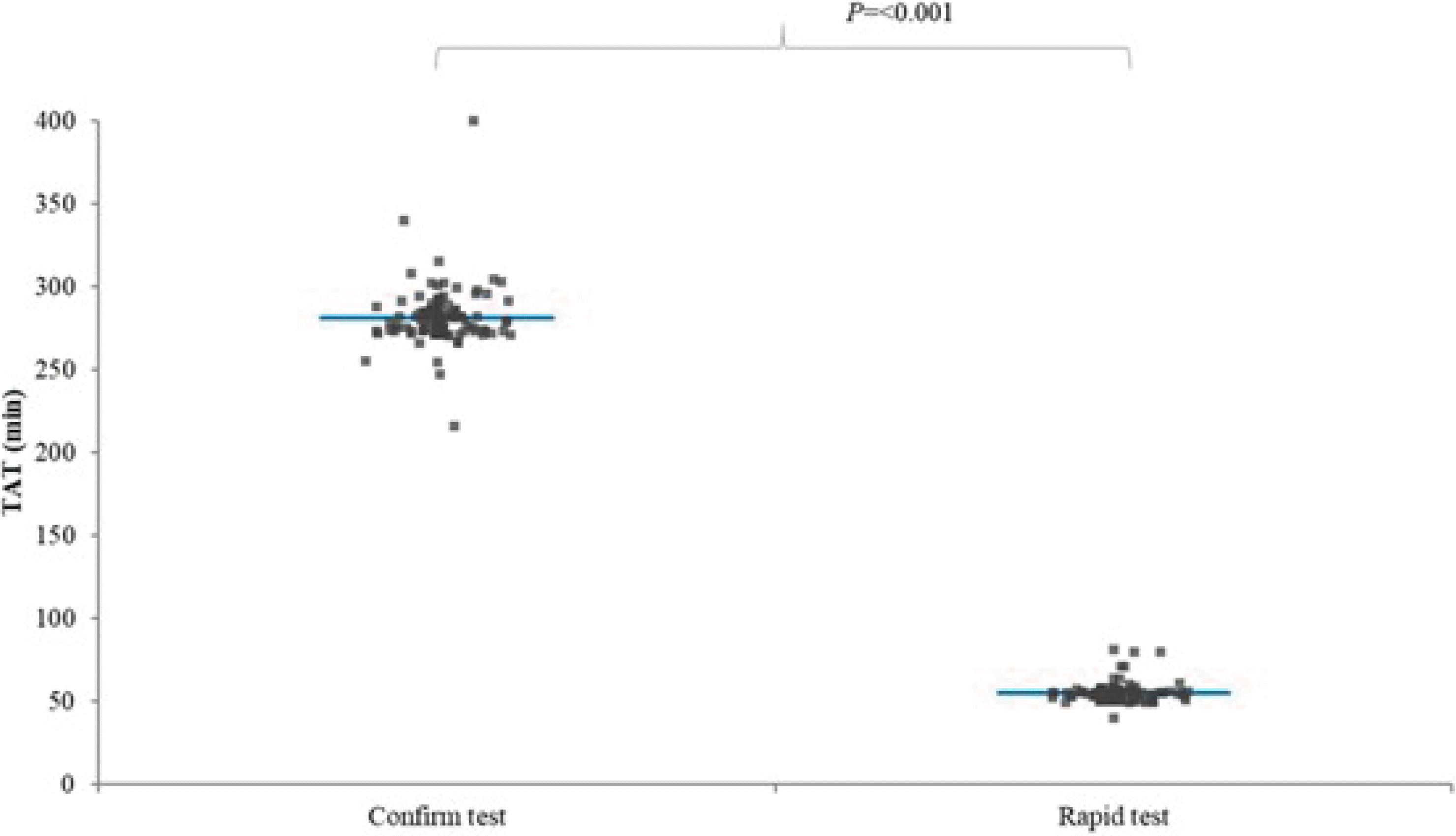
Fig. 2
Emergency department stay time of patients with rapid test and confirm test of COVID-19. The horizontal line refers to mean value.
Abbreviation: min, minute.
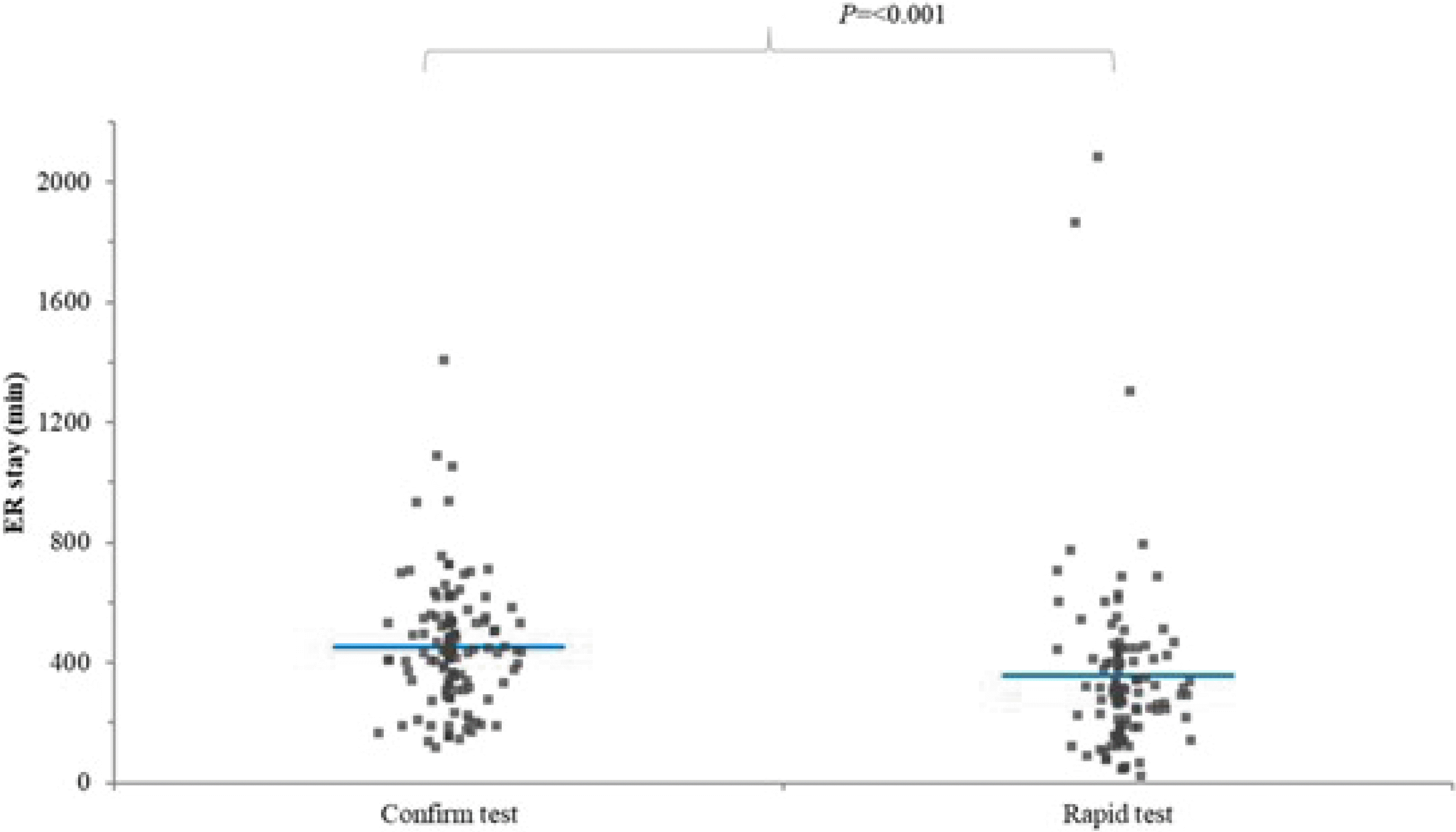
Table 1
Comparisons of patients with rapid test and conventional test of COVID-19




 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download