This article has been
cited by other articles in ScienceCentral.
초록
배경
Elecsys AMH plus (Roche Diagnostics GmbH, Mannheim, Germany)는 항뮬러관 호르몬 검사를 위한 새로운 시약으로 기존 시약 Elecsys AMH (Roche Diagnostics GmbH, Mannheim)의 혈중 비오틴의 간섭 현상을 보완하였다. 본 연구는 Elecsys AMH plus의 수행능과 기존 시약과의 상관성을 평가하고자 하였다.
방법
CLSI 지침에 따라 Elecsys AMH plus의 정밀도, 직선성, 측정한계를 평가하였고 기존 시약과의 상관성 및 비오틴 간섭효과를 비교 분석하였다.
결과
시약의 정밀도는 저농도와 고농도 모두에서 5% 이내였으며 적절한 직선성을 보였다. 제조사에서 제시한 검출한계 값도 검증되었다. 상관성 평가 결과, 저농도에서 백분율 바이어스가 관찰되었으나 상관계수 0.975 이상으로 우수한 상관성을 보였다. Elecsys AMH plus는 기존 시약에 비해 비오틴 간섭영향이 적었으며 500 ng/mL의 비오틴 농도에서도 5% 미만 변화율 보였다.
결론
Elecsys AMH plus의 정밀도, 직선성, 측정한계, 상관성, 그리고 비오틴 간섭효과 평가에서 우수한 결과를 보여 AMH 측정에서 기존 시약의 대체제로 적합할 것으로 판단된다.
Go to :

Abstract
Background
This study aimed to evaluate the performance of Elecsys AMH plus (Roche Diagnostics GmbH, Mannheim, Germany), an improved version of the reagent used for measuring anti-Mullerian hormone, compared to its predecessor, Elecsys AMH (Roche Diagnostics GmbH).
Methods
The precision, linearity, and limit of detection were assessed according to the CLSI (Clinical and Laboratory Standards Institute) guidelines. Method comparison and biotin interference evaluations were also conducted.
Results
Our results demonstrated that Elecsys AMH plus exhibited precision within 5% for both low and high concentrations, maintained linearity within the analytical measuring intervals, was verified for the detection limit established by the manufacturer, and demonstrated excellent correlation with Elecsys AMH (correlation coefficient >0.975). Furthermore, Elecsys AMH plus exhibited enhanced resistance to biotin interference, with a change rate of under 5% even at a biotin concentration of 500 ng/mL.
Conclusions
Elecsys AMH plus demonstrated excellent performance in terms of precision, linearity, detection limit, and biotin interference resistance.
Go to :

Keywords: Anti-Mullerian Hormone, Biotin, Interference, Performance evaluation
서 론
항뮬러관 호르몬(Anti-Mullerian hormone, AMH)은 여성에게서 태령 36주부터 폐경 직전까지 분비되며 가임기 초기에 가장 높게 측정되고 폐경 후에는 검출되지 않기 때문에 난소 기능과 밀접한 연관성을 보인다[
1]. 성선자극호르몬의 영향을 받지 않고, 월경 주기에 따른 변화가 적기 때문에 AMH는 배란유도의 반응이나 폐경기 난소의 기능 예측에 적합한 지표이다[
1]. AMH 측정값을 기준으로 난소 예비능을 평가하고 난임 치료제의 용량을 결정하기 때문에 정확한 측정이 필요하다[
2,
3].
2022년 대한임상검사정도관리협회의 외부정도관리 보고서에 따르면 39개의 임상 검사실 중 28개(71.8%)가 Elecsys AMH (Roche Diagnostics GmbH, Mannheim, Germany), 11개(28.2%)가 Access AMH (Beckman Coulter, Brea, CA, USA) 시약을 사용하고 있었다[
4]. Elecsys AMH는 국내에서 가장 많이 사용되고 있는 방법이지만 streptavidin-based immunoassay를 이용하기 때문에 비오틴에 의해 측정값이 영향을 받는다는 문제가 있다[
5]. 비오틴 간섭 문제를 개선한 새로운 시약인 Elecsys AMH plus가 최근 개발되면서 보다 정확한 AMH 측정이 가능하게 되었다.
본원 검사실에서는 Elecsys AMH plus를 도입하기에 앞서 검사의 성능을 시험하고 기존 시약과 비교 분석하여 임상 검사실에서의 유용성을 평가하였다.
Go to :

재료 및 방법
1. 대상
측정장비로 Cobas8000 e801 (Roche Diagnostics, Basel, Switzerland)를 이용하여 평가시약 Elecsys AMH plus의 정밀도, 직선성, 측정한계, 그리고 기존 시약인 Elecsys AMH와의 상관성을 평가하였다. 두 가지 농도의 정도관리물질과 AMH 검사가 의뢰된 환자들의 잔여 혈청 총 97개의 검체를 평가에 사용하였다. 본 연구는 서울아산병원 기관생명윤리심의위원회의 승인을 취득하였다 (IRB No. S2022-2201-0004).
2. 방법
1) 정밀도 평가
상품화된 고농도와 저농도의 정도관리물질을 20일 동안 오전,오후에 각각 두 번씩 반복 측정하였다. 검사 중 정밀도, 검사 간 정밀도, 검사일 간 정밀도와 총정밀도를 측정하여 Clinical & Laboratory Standards Institute (CLSI) EP5-A3에 따라 평가하였다[
6].
2) 직선성 평가
CLSI EP 6-A2를 따라 시약의 측정가능구간(analytical measuring interval, 0.01–23 ng/mL)에 포함되는 5단계의 농도(0.14, 4.94, 9.75, 14.55, 19.35 ng/mL)를 준비하여 각각 4회 반복 측정한 후 가중최소제곱회귀분석(Weighted least squares regression analysis)을 통해 직선성을 평가했다[
7,
8].
3) 측정한계 평가
Elecsys AMH plus 시약의 공시료측정한계(limit of blank, LoB)와 검출한계(limit of detection, LoD)는 CLSI EP17-A2를 따라서 검증하였다[
9]. LoB 평가용 검체로는 제조사에서 제공하는 희석액을 사용하였고, LoD 평가용 검체로는 고농도 보정물질을 1:6으로 희석하여 사용하였다. 각각 20회씩 반복 측정하여 LoB 평가 검체가 제조사 제시 LoB를 넘는 빈도 및 LoD 평가 검체가 LoB보다 낮은 측정값을 보이는 빈도가 15% 미만이면 적절하다고 판단하였다.
4) 상관성 및 일치도 평가
AMH가 의뢰된 환자의 잔여검체를 측정가능구간 내에 골고루분포하도록 40개를 수집하였다. 각각의 검체를 Cobas8000 e801 장비에서 Elecsys AMH plus와 Elecsys AMH 두 가지 시약으로 각각 2회씩 반복 측정하였다. 두 시약 결과 간에 회귀방정식과 상관계수(coefficient of correlation, r)를 산출하였다. CLSI EP09c를 따라 상관계수 0.975 이상이면 상관성이 우수하다고 판단하였으며,일치도는 평균 바이어스 백분율(%)이 제조사에서 제시한 기준인12% 이하면 적절하다고 판단하였다[
8,
10].
5) 비오틴 간섭효과 평가
낮은 값, 중간 값, 높은 값의 AMH 잔여검체에 비오틴(Sigma-Aldrich, St. Louis, MO, USA)을 혼합하여 각각 7가지(0, 13.75, 27.5, 55, 125, 250, 500 ng/mL) 비오틴 농도가 되도록 총 21개의 검체를 만들었다. 새로운 시약과 기존 시약으로 두 번씩 반복 측정하고, 두 가지 시약 각각에 대해서 비오틴 농도 증가에 따른 AMH 측정값의 변화율을 계산하였다.
3. 통계분석 프로그램
통계프로그램은 Microsoft Excel (Microsoft, Redmond, WA, USA), EP evaluator 8 software package (Data Innovations, VT, USA), SPSS version 19.0 (SPSS Inc., IL, USA)을 사용하였다.
Go to :

결 과
1. 정밀도
Level 1의 평균은 1.05 ng/mL, level 2는 5.64 ng/mL였으며 각각의 검사 중 정밀도, 검사 간 정밀도, 검사일 간 정밀도와 총정밀도는 모두 5% 이내였다(
Table 1).
Table 1
Precision of the Elecsys AMH plus
|
QC level |
Mean |
SD |
CV |
|
Within-run |
Between-run |
Between-day |
Total |
Within-run |
Between-run |
Between-day |
Total |
|
Level 1 |
1.05 |
0.0141 |
0.0129 |
0.0096 |
0.0214 |
1.3 |
1.2 |
0.9 |
2.0 |
|
Level 2 |
5.64 |
0.045 |
0.072 |
0.080 |
0.117 |
0.8 |
1.3 |
1.4 |
2.1 |

2. 직선성
기대치, 잔차와 직선성 확인 결과 허용범위 내로 확인되어 직선성이 유효했다(
Fig. 1).
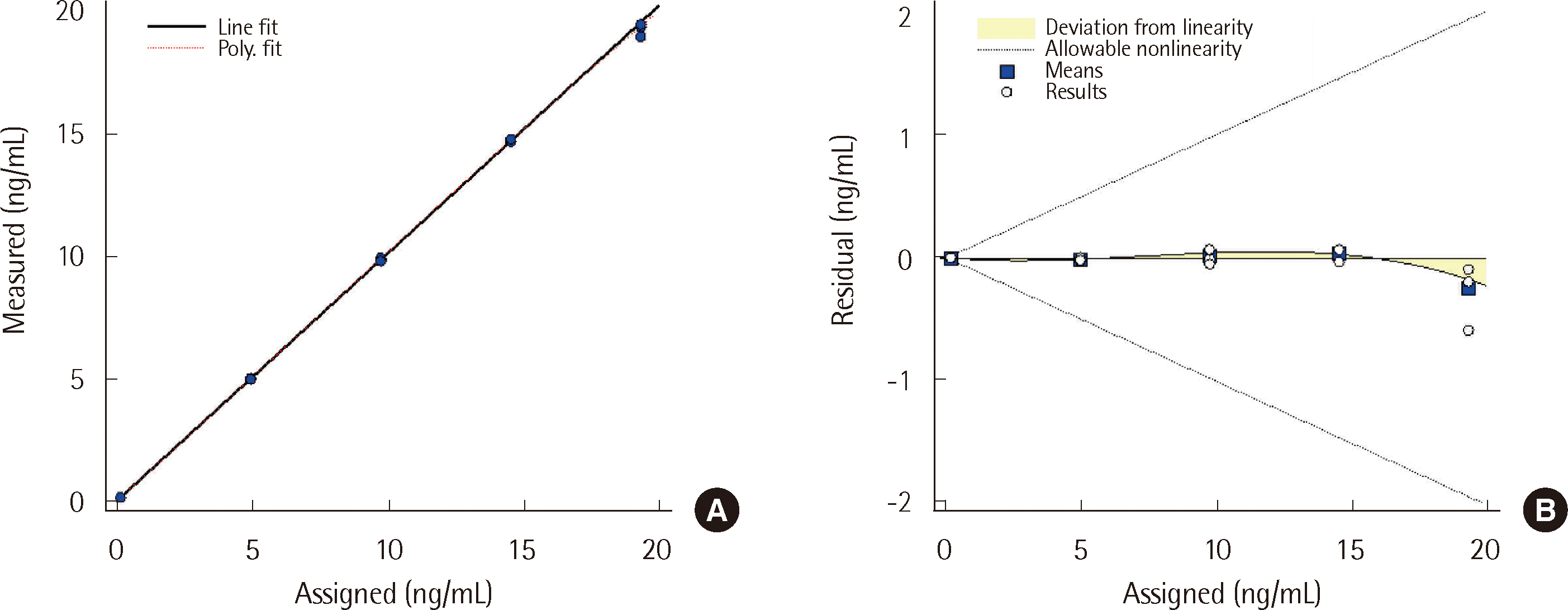 | Fig. 1Linear regression of the Elecsys AMH plus. (A) Regression line of the reagent, depicted by the solid line. The dotted line represents polynomial regression. (B) Residual plot; the dotted lines represent allowable nonlinearity of 10%. 
|
3. 측정한계
Blank 검체를 20번 반복 측정한 결과 평균 0.0038 ng/mL (SD 0.0005)의 결과를 보였고, 제조사가 제시한 LoB (0.007 ng/mL)를 초과한 값은 없었다. LoD 평가물질은 평균 0.0125 ng/mL (SD 0.0004)의 결과를 보였고, LoB 미만의 결과는 없었다. 따라서, 제조사에서 제시한 LoB와 LoD는 적절한 것으로 검증하였다(
Table 2).
Table 2
Measurements for evaluating LoB and LoD
|
Runs |
LoB (ng/mL) |
LoD (ng/mL) |
|
1 |
0.0038 |
0.0122 |
|
2 |
0.0046 |
0.0128 |
|
3 |
0.0049 |
0.0129 |
|
4 |
0.0041 |
0.0126 |
|
5 |
0.0032 |
0.0126 |
|
6 |
0.0033 |
0.0128 |
|
7 |
0.0042 |
0.0131 |
|
8 |
0.0040 |
0.0129 |
|
9 |
0.0036 |
0.0125 |
|
10 |
0.0037 |
0.0130 |
|
11 |
0.0035 |
0.0123 |
|
12 |
0.0037 |
0.0116 |
|
13 |
0.0040 |
0.0124 |
|
14 |
0.0034 |
0.0129 |
|
15 |
0.0032 |
0.0123 |
|
16 |
0.0047 |
0.0122 |
|
17 |
0.0027 |
0.0121 |
|
18 |
0.0035 |
0.0133 |
|
19 |
0.0036 |
0.0117 |
|
20 |
0.0036 |
0.0124 |

4. 상관성 및 일치도 평가
Passing-Bablok regression에서 상관계수 r은 0.9994, 평균 바이어스는 0.097 ng/mL, 평균 바이어스 백분율(%)은 -5.89%로 두 검사 간 상관성 및 일치도가 우수하였다(
Fig. 2).
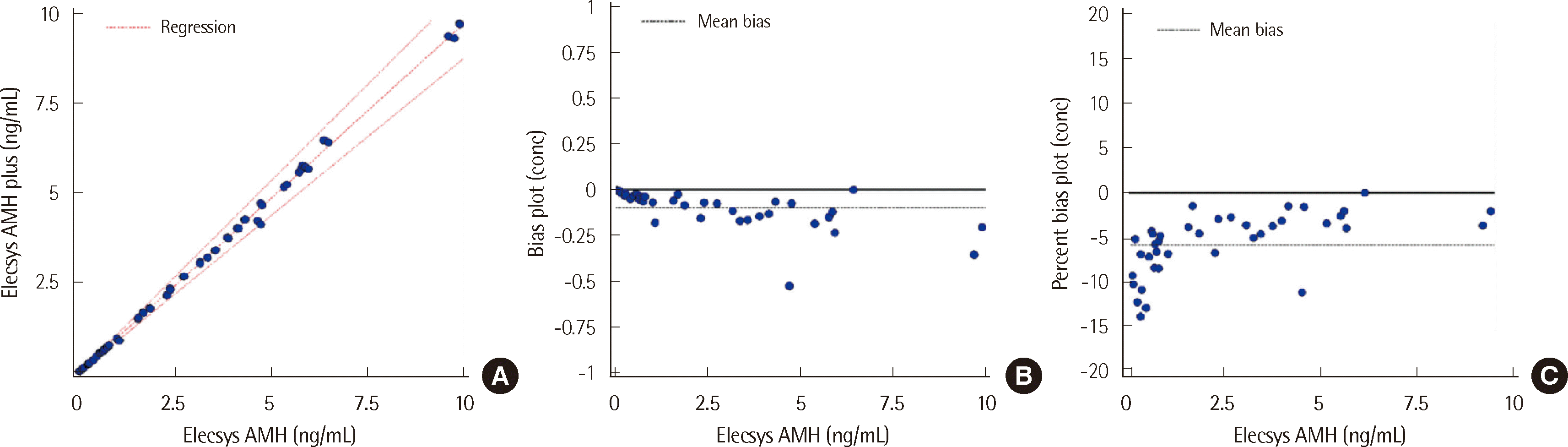 | Fig. 2
Method comparison. (A) Passing-Bablok regression; the dashed line represents the regression line and the dotted lines indicate 10% bias claim plot. (B) Bias plot; the black horizontal dashed line represents mean bias. (C) Percent bias plot; the black horizontal dashed line represents mean percent bias.
Abbreviation: AMH, anti-mullerian hormone.

|
5. 비오틴 간섭 검증
Elecsys AMH plus 시약으로 세 가지 검체(저, 중, 고농도 AMH)를검사하였을 때 비오틴 농도를 최대 500 ng/mL까지 높여도 AMH 측정값 변화율은 5% 미만이었다. 기존 시약 Elecsys AMH를 사용한 경우에는 비오틴 농도 13.75 ng/mL일 때 AMH 측정값이 12% 증가했고, 비오틴 농도가 55 ng/mL에서부터는 AMH 측정값이 감소하기 시작하여 비오틴 농도가 500 ng/mL일 때는 AMH 측정값이 90% 이상 감소하였다(
Fig. 3).
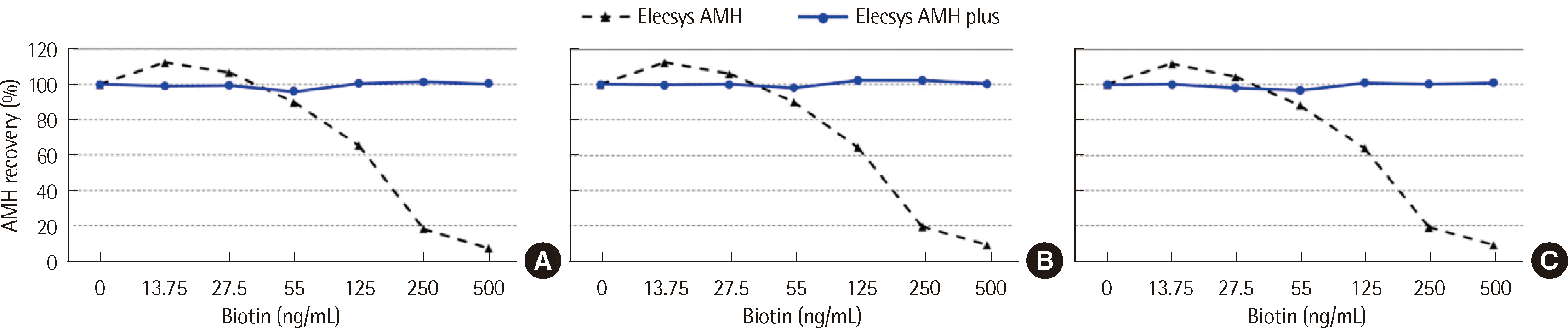 | Fig. 3
Biotin interference test. (A) Low AMH concentration (0.267 ng/mL). (B) Medium AMH concentration (1.810 ng/mL). (C) High AMH concentration (6.815 ng/mL).
Abbreviation: AMH, anti-mullerian hormone.

|
Go to :

고 찰
저자들은 비오틴 간섭 문제를 최소화한 새로운 시약인 Elecsys AMH plus를 CLSI 지침에 따라 평가하였다. 제조사에서 제시한 정밀도, 직선성, 그리고 측정한계가 적절히 검증되었다. 기존 시약Elecsys AMH과 상관성이 우수하였고, 비오틴 간섭효과는 현저히 개선되었다.
Elecsys AMH 와 Elecsys AMH Plus 두 시약 간 상관성 평가에서 상관계수 r은 0.975 이상으로 우수한 상관성을 보였다. 다만, 저농도 AMH 검체에서(0–0.4 ng/mL) 바이어스 백분율이 -10.2%로 전체 바이어스 백분율 -5.89%보다 컸다. 난임 환자 치료로 사용되는 난포자극호르몬 주사제인 폴리트로핀델타(follitropin delta)는 AMH 혈중 농도 2.1 ng/mL (15 pmol/L) 미만인 환자들에게 체중과 무관하게 12 µg의 투약용량이 권고된다[
2,
3]. 따라서 AMH 저농도 검체에서 새 시약 결과가 기존 시약보다 10% 정도 낮게 측정되는 현상은 임상적 치료 결정에 영향을 미치지 않을 것으로 판단되었다. AMH검사는 아직 표준화되지 않았기 때문에 기존 시약과 새 시약 중 어느 결과값이 정확한지 확인하기는 어렵다[
11]. 추후에 매우 낮은 AMH을 가진 환자들에 대한 치료 및 진단적 접근이 개발된다면, 그에 따라 저농도에서의 검사 정확도를 확보한 시약이 개발되어야 할 것이다.
비오틴 간섭효과 비교 분석 결과, 기존 시약에서는 13.75 ng/mL의 비오틴 농도에 대해 저농도, 중간농도, 고농도 검체 모두에서 AMH 측정치가 10% 이상 증가하였고, 500 ng/mL의 비오틴 농도에 대해서는 90% 이상 감소하였다. 새 시약에서는 500 ng/mL의 비오틴을 넣은 검체에서도 측정된 AMH의 농도가 5% 이내의 변화를 보였다. 정상인에서 혈청 비오틴 농도는 0.3–0.8 ng/mL 미만으로 낮으나 최근 머리카락 및 손톱의 성장 개선 등 증명되지 않은 목적으로 비오틴 보충제를 복용하는 사람들이 늘고 있어서 고농도 혈청 비오틴 농도를 보이는 경우도 발견되고 있다[
12]. 미국에서 2016년에 진행된 조사에서 5,647명 중 2.8%가 비오틴 보충제를 1 mg/day 이상, 0.7%가 5 mg/day 이상 복용 중이었다[
12]. 또한, 2018년 Mayo Clinic의 외래환자 1,442명 중 7.4%에서, 2020년 한국인 723명 중 0.41%에서 혈중 비오틴 농도가 10 ng/mL 이상이었다[
13,
14]. 10 mg 비오틴 보충제를 매일 복용한 사람들의 혈청 비오틴 농도는 53–149 ng/mL, 20 mg 비오틴 보충제를 복용하는 경우 80–355 ng/mL까지 증가한다[
15]. 이러한 환자들을 대상으로 Elecsys AMH plus는 보다 정확한 결과 값을 보고할 수 있을 것이다. AMH 외에도 streptavidin-biotin-based immunoassay 방법을 이용해 측정되는 물질들의 비오틴 간섭 현상을 예방할 수 있는 시약들도 필요할 것이다[
5].
Elecsys AMH plus의 수행능 평가 결과 정밀도, 직선성, 측정한계가 제조사에서 제시한 기준에 합당하였고, 기존 시약과의 상관성이 우수하였다. 특히 비오틴 간섭 효과가 크게 개선되었다. 본 시약을 통해 보다 정확한 AMH 검사 결과를 보고할 수 있을 것으로 판단된다.
Go to :






 PDF
PDF Citation
Citation Print
Print





 XML Download
XML Download