This article has been
cited by other articles in ScienceCentral.
Abstract
Background
Nosocomial legionellosis is associated with high mortality. Here, we present the results of an epidemiological investigation and the control measures undertaken for a case of nosocomial Legionella pneumonia at a pediatric hematopoietic stem cell transplantation (HSCT) unit.
Methods
A 22-month-old boy developed nosocomial Legionella pneumonia while at a pediatric HSCT unit. A multidisciplinary team conducted an environmental assessment of the hospital water system and collected water and swab samples from faucets and shower heads from the index patient rooms and nurse stations for Legionella culture.
Results
Legionella was isolated from two swab samples and four water samples out of a total of 24 environmental samples. Follow-up cultures were conducted after replacing the faucets or shower heads which tested positive on Legionella cultures, and point-of-use filters were additionally installed on the sites where Legionella were still isolated. When the water temperature was measured in 20 patient areas, the hot water from the four areas was 50°C or less. Based on the results of the investigation, several interventions including water temperature increase (60°C or higher), flushing out hot water in all patient rooms monthly, cleaning and disinfecting faucets and shower heads monthly, and expanding sampling sites for surveillance were implemented. After the implementation of the control measures, no cases of nosocomial legionellosis occurred, and Legionella was not detected in environmental samples.
Conclusion
Conducting multidisciplinary collaboration and investigation, even for a single nosocomial legionellosis, is important to identify the source and to prevent further transmission. Hospitals should maintain comprehensive water management programs and ensure that control measures are implemented through continuous monitoring.
Go to :

Keywords: Infection control, Legionella, Pneumonia, Surveillance
INTRODUCTION
레지오넬라균(
Legionella species)은 토양이나 냉각탑, 건물의 수계시설 등 환경에 존재하는 그람 음성균으로, 에어로졸 형태로 인체에 흡입되어 감염을 일으킬 수 있다. 50세 이상, 흡연자, 만성 질환자와 면역저하자가 레지오넬라 폐렴의 고위험군으로 알려져 있으며 레지오넬라 폐렴의 경우는 사망률이 약 5-25%로 알려져 있다[
1,
2].
레지오넬라증(Legionellosis) 신고 건수는 국내의 경우 2005년까지는 10명 이내, 2006년 이후 20-30명 수준으로 신고되다가 2016년부터 신고 건수가 증가하여 2020년에는 총 335명의 환자 및 의사환자가 신고되었다[
3]. 레지오넬라증의 주된 감염원은 냉각탑, 건물의 수계시설(샤워기, 수도꼭지), 가습기, 호흡기 치료기기, 온천 등과 같은 에어로졸 발생 시설과 관련되는데 병원 내 감염의 경우 중증 폐렴이 발생할 수 있는 고위험 환자가 많고 집단 발생 가능성이 있어 의료기관 내 수계시설의 오염을 예방하고 관리하는 선제적인 대책이 필요하다[
3-
5]. 본 저자들은 소아 조혈모세포 이식병동에서 병원 내 레지오넬라 폐렴을 경험하여 이후 진행된 역학 조사와 감염관리를 공유하고자 한다.
Go to :

MATERIALS AND METHODS
1. 사례 환자
사례 환자는 생후 22개월 남아로, 만성 육아종증(Chronic granulomatous disease)으로 진단받고 2020년 11월에 제대혈 조혈모세포이식(Cord blood transplantation)을 받았으나 생착 실패로 2021년 5월에 본원 소아청소년과 병동에 입원하여 6월에 반일치 조혈모세포이식을 받았다. 이후에도 혈구 감소증이 회복되지 않아 7월 9일에 추가로 boosting infusion을 시행받고 소아 조혈모세포이식병동에 재원중이었다.
추가 이식 이후 발열이 지속되며 빈호흡이 발생하여 시행한 흉부 전산화 촬영에서 종괴양 음영(
Fig. 1)을 보이는 폐렴 소견으로 경험적인 항생제와 항진균제 투약이 시작되었다. 7월 14일에 환자의 호흡기 검체로 시행한 비정형 폐렴 중합효소 연쇄법 검사에서
Legionella pneumophila가 검출되었고 객담 배양 검사에서도
Legionella pneumophila가 분리되었다. 7월 16일에 시행한 레지오넬라 소변 항원 검사 결과는 음성이었다. 말초 혈액 검사에서 백혈구 0.01×10
3/uL, 혈색소 11.4 g/dL, 혈소판 56×10
3/uL 이었고, C-반응단백 33.81 mg/dL로 증가해 있었다. 그 외 혈청요소질소, 크레아티닌, 간기능 검사는 정상 범위였다.
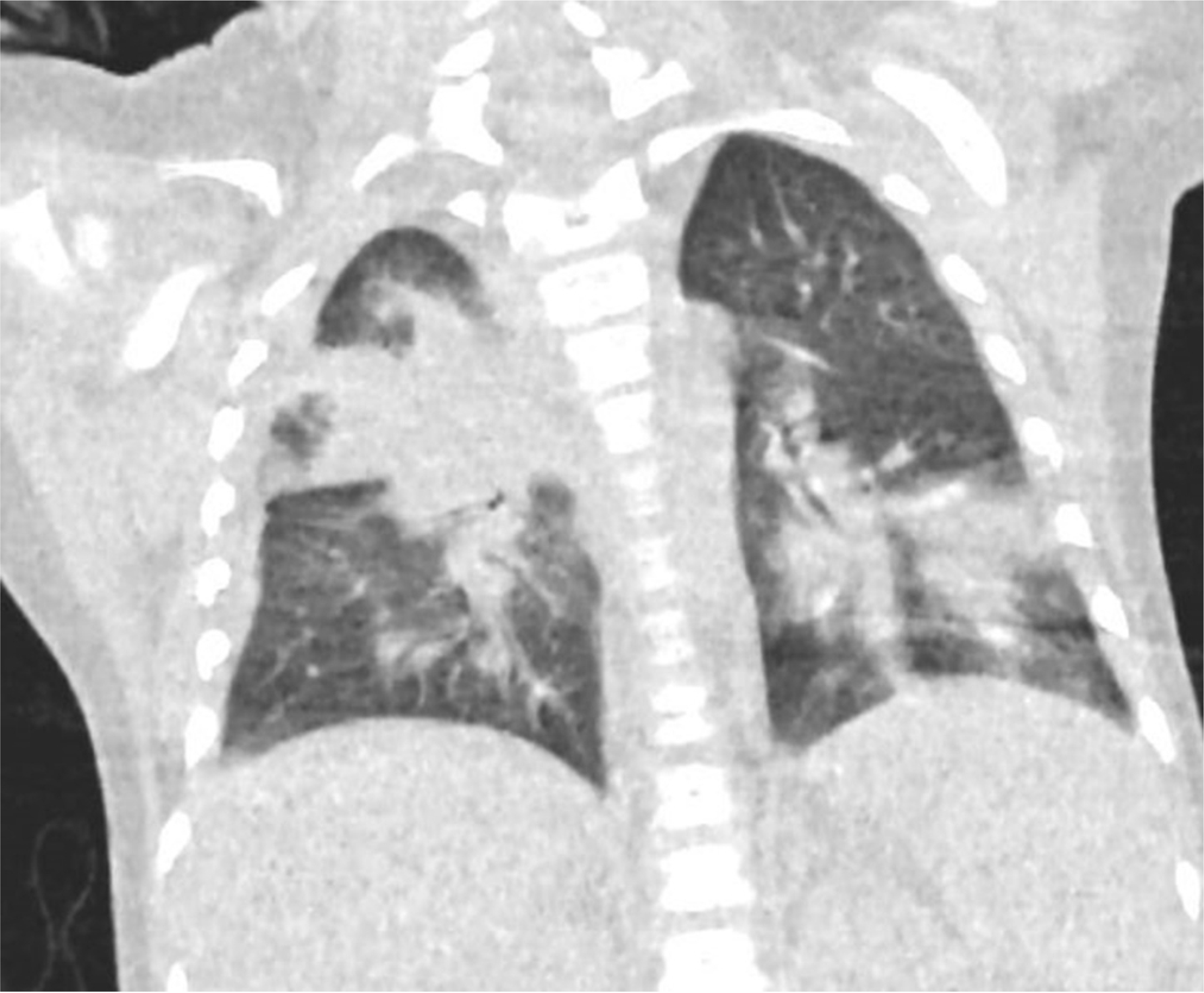 | Fig. 1Chest computed tomography showed multiple mass-like, confluent consolidative lesions in both lungs. 
|
2. 조혈모세포 이식병동의 환경 관리
사례 환자는 2021년 5월 12일 소아청소년과 일반 병동(8E)으로 입원하였고 5월 26일 소아 조혈모세포이식병동 무균실(8S)로 전동되었다. 환자가 사용한 무균실은 총 3명이 사용하는 양압 병실로 환자 병상에는 비닐 커튼이 설치되어 있으며 급기에 헤파 필터가 설치되어 있고 연 2회 공기배양 검사를 시행하고 있었다. 소아 조혈모세포병동의 물은 서울시 아리수에서 인입된 물이 본관 물탱크에 저장되어 있다가 공급되며 병동 내 기계실에 위치한 공급관에 총 3개의 필터(10 mm→1 mm→0.2 mm)가 단계적으로 설치되어 있고 수도꼭지나 샤워기 말단에 필터가 별도 설치되어 있지 않았다.
3. 병원의 수계시설 관리 및 레지오넬라 모니터링
병원의 본관은 20층 건물로 냉온수는 저층부(B3-4층), 중층부(5-12층), 고층부(13-20층)로 나뉘어져 공급되었다(
Fig. 2A). 냉수의 경우 물탱크에 저장되어 있다가 각 병실로 공급되는데 4-28℃로 계절에 따른 온도의 변동이 있으며 재순환하지 않는 반면, 온수는 순간 온수기를 통해 가열되어 각 병실로 공급되며 사용되지 않은 온수는 각 층부 순간 온수기로 다시 돌아와서 사용되었다. 사례 환자 발생 전 순간 온수기에서 공급되는 온수의 온도는 55℃로 설정되어 있었다.
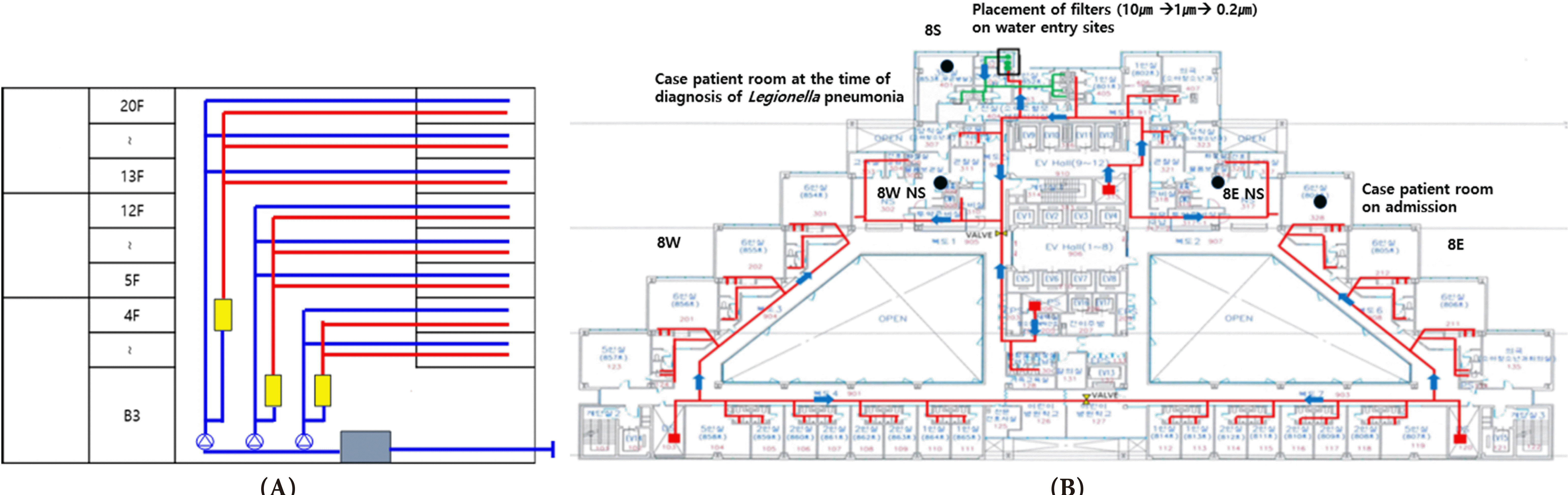 | Fig. 2(A) Schematic representation of the water supplying system at the study hospital (blue line: cold water, red line: hot water, yellow box: water heater and grey box: water tank). (B) Floor plan and water flow of the 8th floor where the case patients was hospitalized (red line and blue arrow: hot water flow and black circle: sampling point of Legionella culture). 
|
병원의 냉각탑수 소독은 연중 주 1회 외부 업체에서 소독제 농도를 확인하고 소독제의 양을 조절하고 있으며 물탱크는 연 2회 청소를 시행하고 있었다. 환경수계검체에 대한 레지오넬라균 배양 검사는 냉각탑수의 경우 연 중 주 1회 시행하고 있으며 병실의 경우 2016년에는 본관과 암병원 각각 1개 병실을 시설팀에서 지정하여 시행하다가 2017년에는 면역저하환자가 주로 치료를 받는 병실로 변경하여 6개 병실(본관 3개, 암병원 3개)로 확대하였으며 2018년에는 별관 건물 1개 병실을 추가하여 2021년에는 총 7개 구역(본관 4개, 별관 1개, 암병원 3개)에 대한 검사를 연중 월 2회 시행하고 있었다. 성인 및 소아 조혈모세포이식 병동의 경우에는 병실로 공급되기 전 필터 3개가 설치되어 있어 해당 병실들의 경우 레지오넬라균 배양 검사를 별도로 시행하지 않았다.
감염관리실에서 연중 레지오넬라증 환자 발생을 모니터하고 있으며 증상 발생 10일전에 의료기관 입원력이 있는 경우를 의료기관 내 감염(확정, 가능성 큼, 가능성 있음을 모두 포함)으로 정의하는 기준에 의하면[
3] 레지오넬라증 원내 발생은 2016년 2건, 2018년 3건, 2019년 2건이었으며 2020년에는 원외 발생 2건 외에 원내 발생은 없었다.
4. 역학조사 및 환경 평가
2021년 7월 16일 원내 레지오넬라 폐렴 발생 건이 확인된 즉시 감염관리실, 소아청소년과, 진단검사의학과, 시설팀에서는 원인 분석 및 추가 환자 발생을 예방하기 위한 역학 조사 및 환경 평가를 시행하였다. 사례 환자가 재실했던 병실의 환자 유입을 중단시키고 레지오넬라균 배양 검사를 위해 해당 병실의 냉온수를 채취하였으며 세면대 수도꼭지와 샤워기 헤드에 대해서 멸균면봉으로 검체를 채취한 후 해당 수전을 교체하였다. 7월 21일에는 해당 환자가 조혈모세포 이식병동으로 전동되기 전 재원하였던 소아청소년과 일반 병동(8E)의 다인실과 간호사실, 조혈모세포 병동에 인접한 소아 혈액암 병동(8W) 간호사실에 대한 환경 검사도 시행하였다(
Fig. 2B). 레지오넬라균 배양 검사는 냉온수에 대해서는 한국종합공해시험연구소에서 시행하였고 멸균면봉으로 채취한 검체는 병원의 미생물 검사실에서 시행하였다. 또한 각 병실에 공급되는 냉온수 온도의 적절성을 평가하기 위해 사례 환자가 재실했던 8층을 포함한 본관 4개 층의 병실 수전 토출 온도를 측정하였다. 사례 환자 외 레지오넬라 폐렴 환자가 있었는지 확인하기 위해 사례 환자가 진단되기 2달전부터 8층에 입원했던 환자들에 대해 의무기록 검토 및 해당 층에서 시행된 레지오넬라증 진단 검사 결과를 검토하였다.
Go to :

RESULTS
1. 환경 배양 검사
사례 환자 발생 이후 시행한 환경수계검체에 대한 레지오넬라균 배양 검사 결과, 사례 환자가 재원했던 소아 조혈모세포 이식병동의 병실과 병실 내 화장실에서 채취한 냉온수에서는 레지오넬라균이 검출되지 않았으나 화장실 세면대의 수도꼭지와 샤워기 헤드 내부에 대한 스왑 검체에서 레지오넬라균이 검출되었다(
Table 1). 해당 시설이 교체된 이후 재검사를 시행하였고 냉온수 및 도말 검체에서 모두 레지오넬라균이 검출되지 않았다. 7월 21일 추가로 시행한 물 검체 16건과 도말 검체 8건의 배양 검사 중 물 배양 4건에서 레지오넬라균이 검출되어 해당 수전을 교체하고 재검사를 시행하였으나 2건에서 다시 재검출되어 해당 수전 외부에 0.2 μm 필터를 설치하였다. 수전 외부에 필터를 설치한 이후 총 2회 레지오넬라 배양 검사를 시행하였으나 더 이상 균이 검출되지 않았으며 2주 간격으로 3개월간 추적 배양 검사를 지속하였다. 추적 검사에서 지속적으로 균 음전이 확인되어 2021년 11월 필터를 제거하였고, 이후에도 2주 간격으로 3개월간, 그 후 1개월 간격으로 3개월 동안 추적 검사를 지속하였으나 균은 검출되지 않았다. 병실로 공급되는 수전 토출 온도 측정 시 본관 4개층의 20개 구역에 대한 수전 온도 측정 시 6개 구역에서는 50℃ 이하의 온도(46.9℃-49.3℃)가 측정되었다(
Table 2). 사례 환자가 재실한 층에 입원한 환자들에 대한 의무기록 및 레지오넬라 진단 검사 검토 결과 사례 환자 외 레지오넬라 폐렴이 의심되는 사례는 확인되지 않았다.
Table 1
Results of environmental surveillance of Legionella
|
Ward |
Sampling points |
Type of samples |
Date of samples collection |
|
July 16*
|
July 21 |
August 11**
|
September 1***
|
|
Pediatric hematopoietic stem cell transplantation ward (8S) |
Faucet of the case patient’s room |
Cold water |
Negative |
Negative |
|
|
|
Hot water |
Negative |
Negative |
|
|
|
Water tap (swab) |
Negative |
Negative |
|
|
|
Bathroom faucet of the case patient’s room |
Cold water |
Negative |
Negative |
|
|
|
Hot water |
Negative |
Negative |
|
|
|
Water tap (swab) |
Positive |
Negative |
|
|
|
Shower of the case patient’s room |
Cold water |
Negative |
Negative |
|
|
|
Hot water |
Negative |
Negative |
|
|
|
|
Shower head (swab) |
Positive |
Negative |
|
|
|
8E |
Faucet of the patient’s room (left) |
Cold water |
|
Negative |
Negative |
|
|
Hot water |
|
Positive (1,000 CFU/L) |
Negative |
|
|
Water tap (swab) |
|
Negative |
|
|
|
Faucet of the patient’s room (right) |
Cold water |
|
Negative |
|
|
|
Hot water |
|
Negative |
|
|
|
Water tap (swab) |
|
Negative |
|
|
|
Shower of the patient's room |
Cold water |
|
Negative |
Negative |
Negative |
|
Hot water |
|
Positive (1,600 CFU/L) |
Positive (200 CFU/L) |
Negative |
|
|
Shower head (swab) |
|
Negative |
|
|
|
Nurse station |
Cold water |
|
Negative |
|
|
|
|
Hot water |
|
Positive (1,200 CFU/L) |
|
|
|
|
Water tap (swab) |
|
Negative |
|
|
|
8W |
Nurse station |
Cold water |
|
Negative |
Negative |
Negative |
|
|
Hot water |
|
Positive (1,200 CFU/L) |
Positive (6,000 CFU/L) |
Negative |
|
|
Water tap (swab) |
|
Negative |
|
|

Table 2
Results of water temperature measured from the faucets and showers on selected wards before and after adjustment
|
Ward |
Location |
Survey temperature, ℃ |
|
Post adjustment, ℃ |
|
Tap (hot/cold) |
Shower (hot/cold) |
Tap (hot/cold) |
Shower (hot/cold) |
|
8E |
Patient room |
- |
48.5/27.7 |
|
- |
51.5/24.0 |
|
8W |
Nurse station |
46.9/27.2 |
- |
|
54.8/24.1 |
- |
|
7E |
Nurse station |
49.3/27.3 |
- |
|
51.1/23.8 |
- |
|
Patient room A |
56.1/27.1 |
56.1/27.1 |
|
61.1/24.0 |
57.9/23.4 |
|
Patient room B |
55.1/27.4 |
54.9/27.3 |
|
62.1/25.6 |
55.5/23.9 |
|
7W |
Nurse station |
47.6/26.3 |
- |
|
52.9/23.9 |
- |
|
Patient room C |
53.5/25.8 |
53.8/26.2 |
|
55.9/24.2 |
54.2/23.5 |
|
Patient room D |
54.0/26.2 |
54.2/26.2 |
|
54.4/24.2 |
55.8/23.1 |
|
12E |
Nurse station |
50.2/26.5 |
- |
|
56.3/24.4 |
- |
|
Patient room E |
54.5/27.5 |
54.1/27.2 |
|
59.6/24.4 |
56.1/25.1 |
|
Patient room F |
55.0/27.4 |
54.6/27.6 |
|
60.7/24.3 |
58.0/24.1 |
|
12W |
Nurse station |
48.5/27.2 |
- |
|
50.7/24.2 |
- |
|
Patient room G |
54.1/27.6 |
54.3/27.2 |
|
60.4/24.0 |
57.0/23.3 |
|
Patient room H |
54.2/27.0 |
53.8/27.3 |
|
60.4/24.0 |
57.0/23.3 |
|
18E |
Nurse station |
51.1/27.3 |
- |
|
54.8/23.8 |
- |
|
Patient room I |
52.4/27.3 |
53.1/27.4 |
|
56.8/24.3 |
56.9/24.4 |
|
Patient room J |
52.2/27.8 |
53.5/28.2 |
|
56.5/24.4 |
54.5/24.3 |
|
18W |
Nurse station |
47.2/27.5 |
- |
|
53.1/24.2 |
- |
|
Patient room K |
51.9/27.1 |
51.2/26.7 |
|
56.2/24.3 |
51.4/23.8 |
|
Patient room L |
51.8/27.0 |
51.8/27.1 |
|
56.4/24.7 |
54.4/22.3 |

2. 환경 관리 개선안
환경수계검체에서 레지오넬라 균이 검출됨에 따라 감염관리실과 시설팀에서는 예방을 위한 환경 관리 개선안을 모색하였다. 각 병실로 공급되는 온수의 온도를 50℃이상으로 유지하기 위해 순간 온수기에서 공급되는 온도를 55℃에서 60℃로 조정하고 월 1회 전 병동의 온수를 20초 이상 방출하여 순환을 개선하도록 하였다. 온수 온도 조정 후 다시 수전과 샤워기 온수 온도를 측정한 결과 56.1℃로 이전(52.5℃)과 비교하여 온수의 평균 온도는 3.6℃ 상승하였고 조정 전 50℃가 넘지 않았던 구역의 온수 온도는 모두 50℃ 이상으로 측정되었다(
Table 2).
모든 병실의 수전 수도꼭지 토출면을 1일 1회 애니오설프 400배 희석 티슈를 사용하여 소독하고, 무균병실 샤워기의 관리 강화를 위해 월 1회 락스 500 ppm을 이용하여 30분간 침적 후 헹구고 100℃로 스팀 소독을 시행하기로 하였다. 또한 수계시설 점검 DAY를 지정하여 시설팀에서 월 1회 점검표를 이용하여 수계시설의 작동 및 외관 상태를 확인하기로 하였다(
Fig. 3). 주기적인 레지오넬라균 배양 검사는 월 1회 시행하되 기존 7개 구역에서 레지오넬라증 고위험군 환자들이 치료를 받는 부서를 포함하여 총 19개 병동으로 확대하고 최소 연 1회 이상 해당 병동 내 모든 병실에 대한 검사가 시행되도록 검사 일정을 정하여 진행하기로 하였다. 환경수계시설 관리 강화 활동 이후 2021년 7월 확인된 본 사례 1건 이외에 전 병동에서 추가적인 레지오넬라증 발생 건은 없었으며 환경 검사에서 레지오넬라균이 검출되지 않았다.
 | Fig. 3Reinforced cleaning, disinfection and maintenance of water system components. 
|
Go to :

DISCUSSION
조혈모세포 이식을 받은 환아에서 발생한 원내 레지오넬라 폐렴에 대해 광범위하고 즉각적인 환경 역학조사를 통해 오염원을 신속하게 파악할 수 있었으며 재발 방지를 위해 환경관리를 강화하였다. 사례 환자의 호흡기 검체에서 분리된 레지오넬라 균과 환경에서 분리된 균에 대해 추가적인 분자역학적 분석은 시행되지 않았으나 환자가 약 2달 동안 병실 밖으로의 이동이 거의 없었으며 보호자가 사례 환자를 해당 화장실에서 몇 차례 목욕을 시킨 적이 있어 오염된 수전 및 샤워기가 감염원이었을 것으로 추정한다. 특히 레지오넬라균에 오염된 샤워기는 사용 중 에어로졸 발생으로 인해 여러 문헌에서 의료기관내 감염과 지역사회 감염으로 발생하는 레지오넬라증 유행의 주 감염원으로 보고되었다[
5-
7]. 사례 환자가 조혈모세포 병동으로 전동되기 전 재실하고 있던 병동의 병실과 간호사실 수전 온수에서 레지오넬라 균이 분리되기는 했으나 레지오넬라 폐렴이 발생하기 6주 전 재실했던 병동으로 감염원이 되지는 않았을 것으로 보인다.
의료기관내 레지오넬라 감염을 예방하기 위한 수질 및 환경관리 방법은 열소독, 자외선 소독, 염소계 소독제를 사용한 소독, 말단 수도꼭지 등에 필터를 설치하는 방법 등이 있는데 각 방법마다 장단점이 있는 것으로 알려져 있다[
3,
8,
9]. 열소독은 추가적인 시설을 설치하지 않고도 시행할 수는 있으며 건물 전체 수계시스템에 효과가 있다는 장점이 있다. 상시에 수전에서 토출되는 온수의 온도는 국내외 지침에서는 50℃ 이상(가능하다면 55℃ 이상) 유지하도록 하는데 이를 충족하기 위해서는 온수기에서 60℃ 이상으로 공급이 이루어져야 하며, 레지오넬라증 유행이 의심되거나 환경 검체에서 레지오넬라가 검출되는 건수가 증가할 경우 온수기의 온도를 70-80°C까지 올려 최소 한 시간 이상 온수시스템을 순환하도록 하는 고열가열-세척법(Superheat and Flush)을 사용할 수 있는데 화상의 위험이 있어 소독하는 동안 병동 내 물을 사용하지 않도록 관리해야 한다. 자외선 소독의 경우 바이오필름 생성에 효과가 없으며 잔류 효과가 없어 건물 전체의 수질관리에는 충분하지 않으나 수술실 스크럽 싱크 등 사용하기 직전에 설치하여 사용할 수 있다. 염소계 소독제를 사용하는 소독법은 물에서 소독 냄새가 나며 배관을 부식시킬 수 있고 일부 소독제는 투석환자에게는 탄소 필터와 같은 보호가 필요하다. 수도꼭지나 샤워기 헤드 말단에 설치하는 필터는 물리적 장벽의 역할을 하며 말단에 설치하므로 설치가 용이하고 냉온수 모두에 적합하나 단기간 사용하고 주기적으로 교체를 해야 하므로 대형 건물의 여러 지점을 관리하기 위해서는 비용 소모가 크므로 일부 고위험 구역이나 원내 레지오넬라증 유행 시 적용할 수 있다.
사례 환자 발생 이후 각 관리법에 대해 검토 후 온수기의 온도를 60℃로 높이며 월 1회 전 병동의 온수를 20초 이상 방출하여 순환을 개선하도록 하였다. 일부 구역에서는 수전 교체 후에도 균이 검출되어 말단 필터를 설치하였고 이후 균은 분리되지 않았다. 이는 말단 부위 오염보다는 순환되는 온수가 레지오넬라에 오염되었다는 것을 시사하며 이후 온수 온도를 올리는 조치를 시행한 후 필터 제거 후에도 균이 분리되지 않은 것을 확인하여 온수 온도를 50-55℃ 이상으로 유지하는 조치가 효과를 보인 것으로 보인다.
소아 조혈모세포이식 병동의 경우 수도꼭지와 샤워기 헤드 내부 스왑 검사에서 레지오넬라균이 검출되고 해당 시설 교체 후 분리되지 않았는데 이 병동은 기존에 병실로 공급되기 전 내부 필터가 설치되어 있어 수전 말단에 별도의 필터를 설치하는 것은 고려하지 않기로 하였고, 대신 수전과 샤워기에 대한 주기적인 소독과 레지오넬라 배양검사를 시행하면서 관리하기로 하였다.
환경 관리 개선안 중 하나로 수계시설의 말단 부위에 대한 세척 및 소독을 강화하였는데, 유럽의 질병관리센터 권고안에서는 말단 부위에 유기물 침착으로 인한 바이오필름이 생성되는 것을 막기 위해 샤워기 헤드, 호스 등 수계 시스템을 구성하는 각 장치에 대해 정기적으로 오염물을 제거하고 세척 및 소독을 하는 것을 권고하고 있다[
9]. 그러나 레지오넬라균에 대한 효과적인 소독제에 대한 연구는 대부분 물에 있는 레지오넬라균에 대한 것으로 주로 염소계 소독제가 추천되나 환경 표면에 대한 소독에 대해서는 적절한 소독제 및 소독 방법에 대해서는 제시하고 있지 않다. 본원에서는 수전 토출면 부위의 유기물 제거와 세척 등의 목적으로 편의성을 고려하여 병원의 일반적인 환경 소독시 사용하는 4급 암모늄계 소독제인 애니오설프를 사용하였다. 샤워기의 경우 통상적으로 낮은 수준의 소독에서 사용되는 락스 500 ppm을 사용하기로 하였으며 샤워기 내부는 100℃로 스팀 소독을 하기로 결정하였다. 의료기관에서는 각 수계시설의 위생 상태를 주기적으로 살피며 위험도에 따라 일정한 주기로 수전과 샤워기를 세척하고 소독해야 한다.
크고 복잡한 대형 병원의 수계 시스템에서 레지오넬라균이 상재하는 것을 완벽하게 막을 수 있는 효과적인 방법은 없기 때문에 수계 환경에 대한 주기적인 레지오넬라균 배양 검사는 중요하다[
8-
13]. 본 병원에서는 지정된 7개 병실에 대해 월 2회씩 환경 배양 검사를 시행하고 있었으나 이번 사례 환자의 발생 이후 지정된 일부 병실을 자주 검사하기보다는 고위험 환자들이 재실하는 모든 병실이 최소 연 1회 이상 검사될 수 있도록 검사 장소를 대폭 확대하기로 하였다. 의료기관에서의 주기적인 환경 검사에 대한 권고는 다양하게 제시되고 있는데, 2022년 질병관리청 호흡기감염병 관리지침에서 지자체에서 노인인구 재원시설 등 고위험시설에 대해 연 1회 이상 수계 환경 검사를 시행하도록 되어 있으나[
3] 각 의료기관의 정기적인 환경 검사 시행에 대해서는 구체적으로 언급하고 있지 않다. 국외의 경우 미국 질병관리센터에서 의료기관에서 레지오넬라균 전파 위험을 낮추고 수질 관리 프로그램이 잘 운영되는지 확인하는 목적으로 정기 환경 검사를 고려할 수 있으며 특히 이식병동에서는 정기적인 환경 검사를 시행하도록 권고하고 있고[
12], 이탈리아에서는 의료기관의 경우 위험 구역은 연 1-2회 환경 검사를 시행하며 고위험구역은 분기별로 환경 검사를 시행하도록 권고하고 있다[
13]. 의료기관에서의 정기적인 수질 환경에 대한 레지오넬라균 배양 검사의 시행 장소 및 주기 등은 각 기관의 상황과 위험도 평가를 통해 결정할 수 있을 것으로 보인다.
면역저하환자를 주로 진료하는 병원에서는 한 건의 원내 레지오넬증 발생시에도 신속히 다부서간 협조를 통해 오염원을 찾아 추가적인 전파를 막기 위해 신속한 역학조사 및 환경 평가를 시행하여야 한다. 또한 원내 레지오넬라증 위험을 감소시키기 위해서는 체계적인 수질 관리 프로그램을 갖추어야 하며 이런 프로그램이 잘 운영되고 있는지 지속적으로 환자와 환경에 대한 모니터링을 통해 평가해야 한다.
Go to :






 PDF
PDF Citation
Citation Print
Print





 XML Download
XML Download