Abstract
Clinical microbiological test results are fundamental in preventing of healthcare-related infections, but the test methods and interpretative criteria for antimicrobial susceptibility tests vary, depending on the period. Therefore, to effectively utilize the automated epidemic notification system based on the results of the clinical microbial test, it is necessary to build a test code system that can be expanded and allows the management of history to reflect changes in the clinical microbial tests. The level and scope of the establishment of the infection epidemic monitoring system depends on the characteristics of the medical institution, policy direction of the hospital decision-making management, details of the computer hardware, peripheral devices, and the software and personnel supporting it.
의료관련감염에 대한 사회적 시각은 매우 많은 변화가 있어 왔고, 의료기관에서의 접근 방향도 달라질 수밖에 없는 실정이다. 예전에는 병원에 입원하면 병원감염을 피할 수 없고 최선의 감염관리 활동을 하면 병원감염의 1/3 정도를 예방할 수 있다는 다소 수동적인 견해를 가졌으나 2000년대에 들어서는 치명적인 의료관련감염의 3/4을 예방할 수 있다고 생각하고 있다[1]. 또한 2000년대 초반부터 시도된 중심정맥관 삽관 과정을 단순하게 표준화한 시술의 적용으로 카테터-연관 혈류감염의 빈도가 획기적으로 감소한 결과[2]는 대부분의 의료관련감염을 예방할 수 있다는 패러다임 변화를 가져오게 되었다. 더불어 감염관리실무자의 역할도 단순히 의료관련감염을 관리하는 데 멈춰 있는 것이 아니라 의료관련감염이 발생하지 않도록 예방적 조치를 개발하고 적용해야 하는 패러다임 변화가 오게 되었다.
의료관련감염의 예방을 위해서는 감염 발생 전에 위험도가 있는 환자를 예측하여 선별 집중 관리하는 시스템을 구축하는 것이 바람직하다. 이러한 예방적 조치의 적용 수준은 병원 체계와 이를 지원하는 환경과 역량에 따라 다를 것이다. 의료관련감염 위험도 평가와 관리 방법은 의료관련감염 발생 자료를 자체 분석 또는 문헌을 참조하여 위험도가 있는 변수들을 추린 후 지속해서 평가와 관리를 할 수 있는 것들을 목록화한 다음에 위험도 변수별로 응급실(센터), 외래, 병동, 중환자실 등으로 구분하여 점검표, 알고리즘 순서도 등을 제작하여 사용하거나 전산화할 수 있다[3,4]. 감염원의 전파와 확산 방지는 감염관리실무자의 가장 중요한 책무이다. 임상미생물 검사 결과는 의료관련감염의 예방과 감염의 전파와 확산 방지의 바탕이 되는 기본 항목이지만 그 활용 정도에 따라 얻어지는 효과는 다르다. 이에 임상미생물 검사 결과의 유형, 관리 방법과 활용에 대하여 알아보고자 한다.
의료관련감염 발생과 위험도 요인을 정확히 확인하기 위해서는 의료기관의 환자 관련 자료인 의료정보시스템(HIS, Healthcare Information System)의 표준화가 선행되어야 한다. 의료정보시스템에는 처방전달시스템(OCS, Order Communication System), 전자의무기록시스템(EMR, Electronic Medical Record), 진료지원부서시스템이 있고, 진료지원부서시스템에는 검사정보시스템(LIS, Laboratory Information System), 영상정보시스템(RIS, Radiology Information System), PACS (Picture Archiving and Communication System), 약품정보시스템(Pharmacy Information System)이 있으며 이러한 단위별 정보시스템을 연결하여 분석하는 의료관련감염관리시스템이 있다. 의료관련감염관리시스템 구축을 위한 데이터베이스 구성 요소는 다음과 같다.
외래와 입원의 구분이 필요하며 이는 보험급여 기준과는 다를 수 있다. 응급실과 관련된 병실로는 선제구역, 관찰병동, 응급실 전용 병실 등이 있으며, 신장실, 분만실, 단기입원, 재활병동, 낮병동 등은 별도로 관리하는 것이 혼란을 줄일 수 있다. 입퇴원일자 시간도 보험급여 기준과는 다를 수 있다. 의료관련감염의 정의는 입원 48시간 이후, 퇴원 후 14일 이내, 수술 후 30일 이내로 되어 있었으나 대부분의 병원에서는 오후 12시를 기준으로 입원일을 산정하므로 감염이행기간(Infection Window Period)은 입원 후 3 역일(calendar days)을 기준으로 변경되었다[5].
주증상과 증후는 표준 의무기록을 적용하며 간호 전자의무기록시스템을 활용하면 도움을 받을 수 있다. 진단명은 SNOMED CT (Systematized Nomenclature of Medicine-Clinical Terms), UMLS (Unified Medical Language System), MSD (Medical Subject Headings), ICD (International Statistical Classification of Diseases) 등을 사용한다. ICD는 역학과 의료 관리의 목적으로 사용되는 국제 표준 진단 분류체계로서 한국에서는 ICD를 기반으로 만든 KCD (Korean Standard Classification of Disease; 한국표준질병사인 분류, 통계청)를 사용하고 있다.
항균제, 처치, 수술 등으로 구분되며, 항균제 코드는 심평원 코드와 각 기관의 약물정보시스템을 이용하여 투여 시기와 기간, 용량 등을 분석하고, 처치는 카테터 종류, 내시경과 환기기의 종류와 개별 식별 번호를 부여하여 관리하며, 수술은 수술명, 수술 시간, 집도의 등을 구분한다.
임상미생물검사는 검체, 균종, 항균제감수성검사로 크게 나눠지며 대부분 문자형 자료이므로 이를 코드화하는 것이 중요하다. 또한 병원마다 검체 정의와 균 분리 방법과 결과 보고 표준화가 완전하지 않으므로 이에 대한 표준화가 필요하다. 또한 지속적으로 균종명이 추가되며 같은 균종이 이름이 변경되고 항균제감수성검사 판정 기준이 해마다 달라지므로 이에 대한 이력 관리가 필요하다.
대분류는 의료보험 분류에 맞춰 구강, 기도, 호흡기/소화기/비뇨,생식기/혈액,체액/기타부위로 나누고 중분류는 부위(왼쪽, 오른쪽/첫째, 둘째, 등), 소분류는 채취 시기와 방법(예로 protected specimen brush bronchoscopy, Indwelling catheter, Swab 등)으로 분류할 수 있으나 표준화가 미흡하다. 예로 피부와 피부 구조 감염(bacterial skin and skin structure infection, BSSSI)은 합병증이 없는 감염(uSSSI)에는 소농양, 고름딱지증(impetigo), 종기(furuncle), 연조직염(cellulitis)이 해당되고, 합병증이 있는 감염(cSSSI)에는 감염된 궤양, 화상 감염, 대농양, 치료가 어려운 질환의 피부감염이 속하며, 대농양은 고름의 가장자리 경계에서 발적과 부종(경화 포함)이 최소 5 cm 이상 확장된 경우로 정의되며, 피부와 연조직감염(skin and soft tissue infection, SSTI)은 근막(fascia) 또는 근육까지 침범하는 경우로서 일부 연조직염, 괴사근막염(necrotizing fasciitis), 근육괴사(myonecrosis)가 포함된다. 또한 창상과 농양 감염에 대한 용어도 wound, pus, abscess 등이 다양하게 사용된다. 임상미생물검사에는 혈액배양이나 객담배양처럼 2-3차례 연속으로 의뢰할 때와 상부호흡기, 하부호흡기, 창상 검체 등과 같이 유사 부위에서 채취한 검체는 어떻게 처리할 것인가도 고려해야 한다(Supplementary Fig. 1).
같은 균종을 서로 다르게 명명함으로써 발생하는 혼란을 없애기 위해 1980년에 Approved Lists of Bacterial Names를 발행하였고, 이 목록에 있는 균종명만을 인정하며, 새로운 균종명은 International Journal of Systematic and Evolutionary Microbiology 학술지에 실린 것만 유효한 것으로 판정하여 International Code of Nomenclature of Bacteria에 등록된다(https://www.bacterio.net/). 동일 균종이 새로운 균종명으로 변경될 때에 이를 새로운 균종 코드로 만들면 결과를 분석할 때 오류를 초래하게 된다. 참고로 Pseudomonas maltophilia는 Xanthomonas maltophilia로 바뀌고 다시 Stenotrophomonas maltophilia로 변경되었으며, Pseudomonas pickettii도 Burkholderia pickettii에서 Ralstonia pickettii로 변경되었다. 그러므로 균동정 검사 장비에서 새로운 균종명이 보고될 때는 이전 균종명이 있는지를 확인해야 한다(Supplementary Fig 2).
항균제감수성검사에 사용하는 항균제 명칭은 Clinical and Laboratory Standards Institute (CLSI) 기준을 따른다. 항균제 코드는 제원과 함께 표준화하며 대표이름-방법-용량-제조사를 포함한다(AMP1: Ampicillin, Disk diffusion, 10 μg, AMP2: Ampicillin, Micro broth dilution, 10 μg, Vitek, AMP3: Ampicillin, Micro broth dilution, 10 μg, Microscan). 또는 검사한 항균제의 변경 사항에 대한 이력 관리를 철저히 한다. 항균제감수성검사 방법은 항균제 코드 목록과 연동시킨다. 항균제감수성검사 판독 기준은 시기에 따라 달라지므로 이력관리를 해야 하며, 감수성, 중간, 내성으로 보고하는 것보다 억제대 지름이나 최소억제농도를 입력한다(Supplementary Fig. 3).
Supplementary Fig. 4는 임상미생물 결과 관리를 위한 기본 코드 관리 화면이다. Supplementary Fig. 5는 감염관리와 법정감염병 자동 검출을 위한 조건 설정 기초 파일이며 Supplementary Fig. 6은 조건 설정 기초 파일로 만든 데이터베이스이다. Supplementary Fig. 7은 감염환자 관리를 위한 화면이며, Supplementary Fig 8은 조회 화면이다. 환경 배양은 의뢰한 병동과 과에 따라 당일 검사와 누적 결과를 조회할 수 있게 만든다. 항균제감수성검사 rule-based management system은 균 규칙과 항균제 규칙을 설정한 후 이에 따른 주석을 임상과 검사자에게 표시되는 화면으로 나누어 구성한다(Supplementary Fig. 9). 항균제감수성검사 결과 여과는 항균제감수성검사의 실제 결과와는 상관없이 내성 기전이나 임상 치료 효과에 근거하여 결과를 조정하여 보고하는 방식이다(Supplementary Fig. 10). 미생물검사결과의 delta check는 이전의 결과와 현재의 미생물 결과에 차이가 있을 때 검사자가 다시 확인하는 일종의 정도관리 방법으로 동일 검체(군)에서 다른 균종이 분리되거나 동일 균종이 분리되었을 때 항균제감수성검사 결과에 차이가 있으면 표시된다(Supplementary Fig. 11).
법정감염병은 보고 주석에 감염관리 방법을 추가한다(Supplementary Fig. 12, 13). 항균제감수성검사 결과를 보고할 때 동일 환자에서 발생하는 다음과 같은 상황 ① 반복하여 동일 균종이 분리될 때 항균제감수성검사를 매번 해야 하는가? ② 반복 분리 균종에 대하여 항균제감수성검사를 생략한다면 생략할 수 있는 기간은 얼마이며, 균종별로 달리 적용해야 하는가? ③ 균종명이 같다고 같은 균으로 간주할 수 있는가? ④ 항균제감수성검사 결과가 다르면 균종명이 같아도 다른 균인가? ⑤ 항균제감수성검사에서 시행한 항균제 중 몇 개까지, 어느 수준 내의 오차(very major error, major error, minor error)가 있으면 동일 균으로 간주할 수 있는가? 등에 대한 표준화된 지침이 없다.
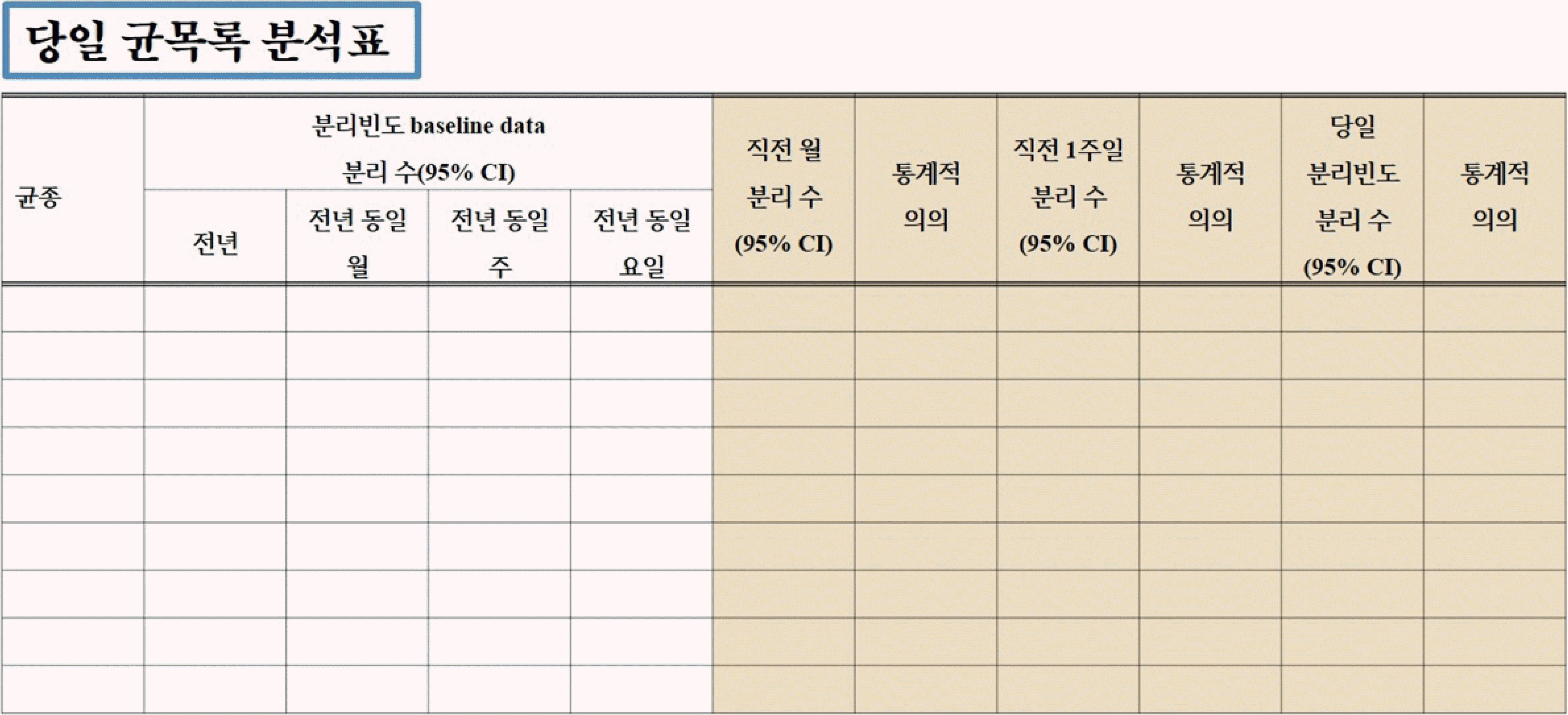
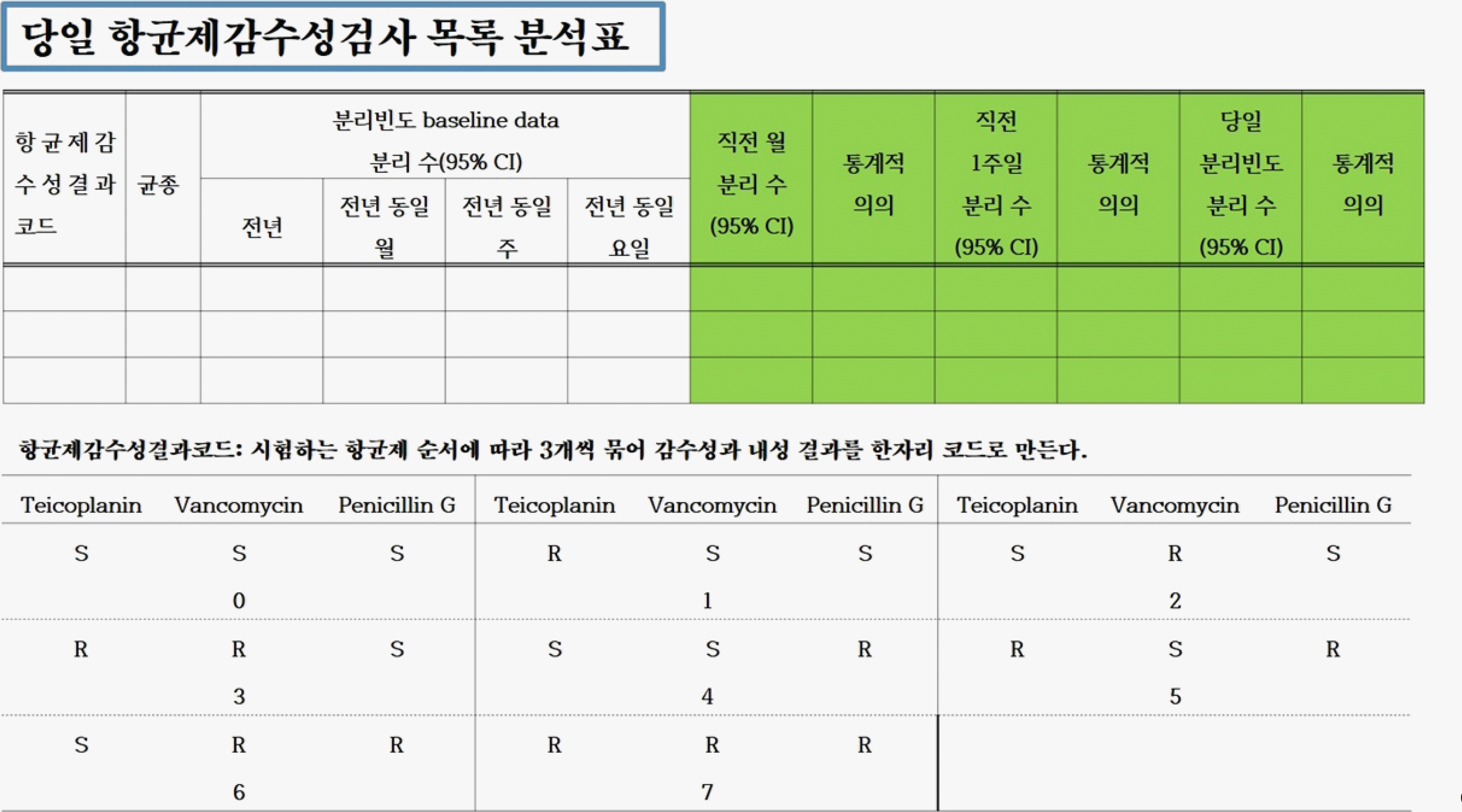
유행의 신속 검출을 위해서는 역학과 임상 자료를 체계적이고 정확하게 모으고 분석할 수 있는 병원 체계와 미생물검사 결과와 다른 검사 정보 결과를 정확하게 해석할 수 있는 능력 있는 인적 자원이 필요하다. 기본적으로 유행의 인지는 통상적인 발생 빈도를 추정하는 것이 선행되어야 하므로 이를 위해서는 각 의료기관의 균 분리 빈도 데이터베이스를 구축하고(Supplementary Fig. 14-16) 매일의 통상적 균 목록의 철저한 검토가 필요하며, 당일 균 목록과 항균제감수성검사 목록 분석표에서 95% 신뢰구간이 겹치지 않으면 통계적으로 의의가 있는 것으로 초기 판단할 수 있다(Fig. 1, 2).
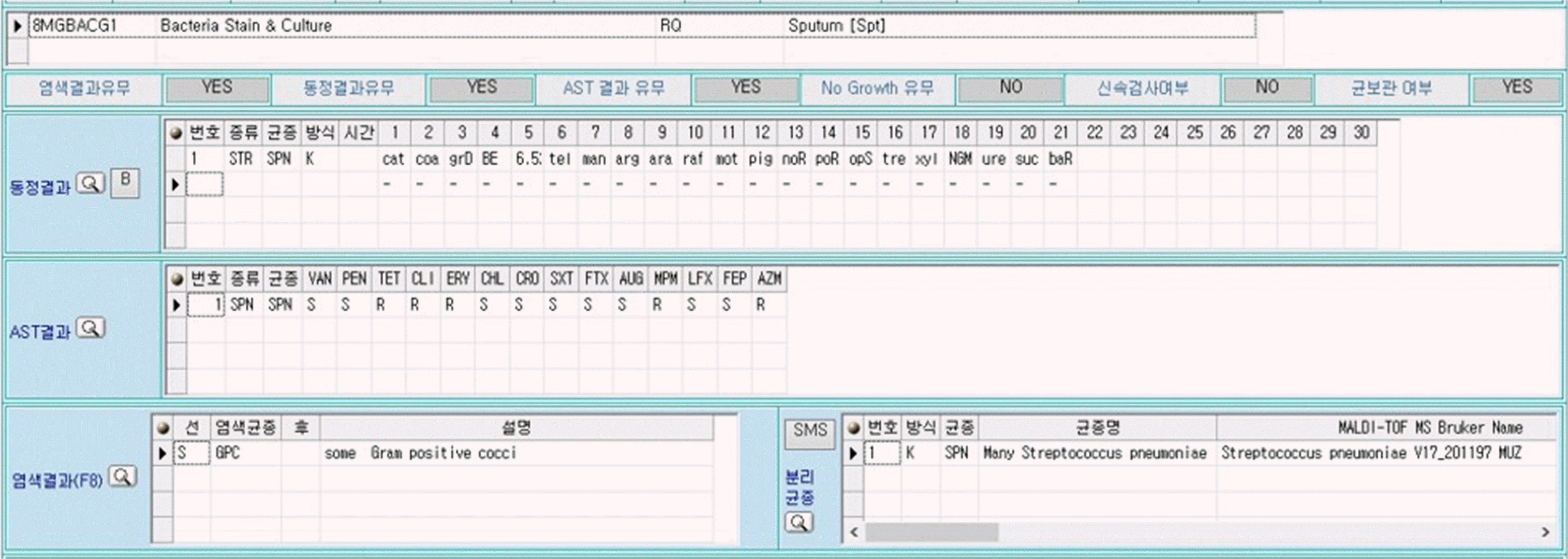
세균의 단백질 분자의 질량을 측정하여 그 패턴으로 균을 동정하는 MALDI-TOF MS (Matrix-Assisted Laser Desorption Ionization-Time-of-Flight Mass Spectrometer)를 이용하는 기관에서는 동정된 동일 균종의 단백질 성분 차이를 분석하면 유행을 확인하는 데 도움을 줄 수 있다. 이러한 시스템을 구축하기 위해서는 먼저 MALDI-TOF MS의 균종별 library 코드를 균종명과 함께 데이터베이스를 구축하고(Fig. 3) 자료 전송 프로그램으로 균종명과 library 코드를 함께 전송하며(Fig. 4) 전체, 균종별, 검체별로 자료를 분석하여 유행을 선별한다(Fig. 5-7).
자동 유행 모니터링 시스템은 해당 병원과 지역, 나라에서의 시계열적인 감염병의 통상 발생 빈도를 기초 자료로 하여 유행의 기준점을 설정한 후 감염병별로 기준점에 근접하면 경고하는 알림 시스템을 구축할 수 있다. 의료관련감염의 예방 알림 시스템도 기존의 의료관련감염의 발생 위험 인자를 분석하여 위험인자별 점수를 코드화한 후 의료관련감염의 위험도가 높은 환자를 모니터링할 수 있다. 임상연구지원(CDW, Clinical DataWarehouse) 시스템이 구축되어 있다면 의료관련감염 레지스트리를 추가할 수 있다. 근거리에 있는 스마트 기기를 자동으로 인식하여 필요한 데이터를 전송할 수 있는 무선 통신 장치인 비콘(beecon)을 이용한 역학관리 RIB (Rapid Identification of contact points and pathways using Bluetooth low energy) 시스템 또는 실시간 위치 추적 시스템(RTLS, Real Time Location System)을 구축하면 감염 환자와의 접촉자들의 접촉 시간, 공간과 거리에 따른 감염 위험도 리스트도 확인할 수 있다[6,7].
감염 유행 모니터링 시스템의 구축의 수준과 범위는 의료기관의 특성과 병원 경영진의 의지, 세부적으로는 컴퓨터 하드웨어와 주변 장치, 이를 뒷받침하는 소프트웨어와 인력 구성에 따라 달라진다. 국가의 정책적 보상 지원도 매우 중요하다.
Supplementary material can be found via https://doi.org/10.14192/kjicp.2022.27.2.118.
REFERENCES
1. Alliance for Human Research Protection. Unhealthy Hospitals: 103,000 preventable deaths in 2000. Chicago Tribune. AHRP. https://ahrp.org/unhealthy-hospitals-103000-preventable-deaths-in-2000-chicago-tribune/. Updated on 9 December 2022.
2. Berenholtz SM, Pronovost PJ, Lipsett PA, Hobson D, Earsing K, Farley JE, et al. 2004; Eliminating catheter-related bloodstream infections in the intensive care unit. Crit Care Med. 32:2014–20. DOI: 10.1097/01.CCM.0000142399.70913.2F. PMID: 15483409.

3. Evans RS, Burke JP, Classen DC, Gardner RM, Menlove RL, Goodrich KM, et al. 1992; Computerized identification of patients at high risk for hospital-acquired infection. Am J Infect Control. 20:4–10. DOI: 10.1016/S0196-6553(05)80117-8. PMID: 1554148.

4. Glenister HM, Taylor LJ, Bartlett CL, Cooke EM, Sedgwick JA, Mackintosh CA. 1993; An evaluation of surveillance methods for detecting infections in hospital inpatients. J Hosp Infect. 23:229–42. DOI: 10.1016/0195-6701(93)90028-X. PMID: 8099097.

5. Louisiana Department of Health. NHSN overview. Infectious Disease Epidemiology 2017. https://ldh.la.gov/assets/oph/Center-PHCH/Center-CH/infectious-epi/HAI/HAIworkshop2017/handoutsD2/NHSNOverview_Final.pdf. Updated on 15 May 2022.
6. Curtis SJ, Rathnayaka A, Wu F, Al Mamun A, Spiers C, Bingham G, et al. 2022; Feasibility of Bluetooth Low Energy wearable tags to quantify healthcare worker proximity networks and patient close contact: a pilot study. Infect Dis Health. 27:66–70. DOI: 10.1016/j.idh.2021.10.004. PMID: 34810151. PMCID: PMC8963530.

7. Ng GY, Ong BC. 2022; Contact tracing using real-time location system (RTLS): a simulation exercise in a tertiary hospital in Singapore. BMJ Open. 12:e057522. DOI: 10.1136/bmjopen-2021-057522. PMID: 36192104. PMCID: PMC9535253.





 PDF
PDF Citation
Citation Print
Print





 XML Download
XML Download