Abstract
Purpose
The efficacy and safety of low-dose pregabalin and alpha lipoic acid in diabetic neuropathy were evaluated and analyzed.
Materials and Methods:
Materials and This study designed a retrospective study that included patients with diabetic neuropathic pain. From 2009 to 2022, 100 patients who suffered from diabetic neuropathic pain were included in this study. The patients were divided into group I (pregabalin 150 mg/day with alpha lipoic acid 600 mg/day) and group II (pregabalin 300 mg/day with alpha lipoic acid 600 mg/day). The visual analogue scale (VAS), medication side effects, and neurometer results were compared.
Results
The mean follow-up period of the above patients was 120.23 weeks in group I and 149.05 weeks in group II. The average VAS score in group I decreased by 3.23 points, and the average VAS score in group II decreased by 2.86 points. Approximately 24.3% of group I had side effects, such as dizziness, sleepiness, and gastrointestinal trouble, while 76.7% of patients in group II had side effects. Sixtyseven patients had a neurometer examination before and after the medication, and there is no statistical difference between the two groups.
Conclusion
The combination of low-dose pregabalin (pregabalin 150 mg/day) and alpha lipoic acid in diabetic neuropathy had a similar clinical effect and less frequent medication side effects than regular dose pregabalin (pregabalin 300 mg/day) and alpha lipoic acid. Therefore, low-dose pregabalin (pregabalin 150 mg/day) and alpha lipoic acid should be considered in treating diabetic neuropathy.
Go to : 
당뇨병성 말초 신경병증(diabetic polyneuropathy)은 제 1형 및 2형 당뇨 환자에게서 증상을 유발하는 장기적인 합병증으로 신경 섬유의 점진적인 소실을 특징으로 하며, 이로 인해 체성 신경계와 자율 신경계 모두에 영향을 끼쳐 통증, 감각 이상, 감각 상실과 같은 증상을 유발한다.1) 이 중 신경병증성 통증은 당뇨병 환자의 약 16%에게 영향을 미치며 수면이나 여가 생활 등의 삶의 질에 상당한 영향을 미친다.2) 당뇨병성 신경병증의 병리 기전은 산화성 및 질산화성 스트레스, 고혈당증, 허혈, 신경 영양 장애 및 자가면역성 신경 파괴 등으로 설명되며 이는 모두 미세혈관 질환과 신경 기능 장애에 영향을 미친다. 따라서 당뇨병성 신경병증을 치료할 때에는 단순히 통증만을 호전시키는 것은 손상된 신경이 회복되는 것이 아니며 최종적으로 산화 스트레스를 감소시키고 미세 혈관의 순환을 호전시키는 것이 중요하다고 할 수 있다.3)
Pregabalin은 신경전달체인 γ-aminobutyric acid 유사체로서 presynaptic calcium channels의 α2δ subunit에 작용하여 항경련 효과를 가진 약물로 주로 당뇨병성 신경병증 또는 대상포진 후 신경통이나 섬유근육통을 가진 환자에게 효과가 있는 것으로 알려져 있다. Lesser 등4)은 당뇨병성 신경병증을 가진 338명의 환자들에게 있어서 pregabalin 300 mg/day 및 600 mg/day를 투여하여 weekly pain score, sleep interference score 등이 위약(placebo)에 비해 호전되었다고 보고하였다. 하지만 pregabalin은 부종, 어지러움, 졸음, 두통, 근육 경련 등과 같은 많은 부작용이 있으며 이로 인해 300 mg/day의 pregabalin 복용은 순응도가 상당히 낮지만 pregabalin의 효능을 평가하기 위하여 시행한 다양한 임상 시험들은 대부분 300 mg/day 이상의 용량에 대한 연구이며 300 mg/day 미만 용량에 대한 연구는 부족하다. 일부 연구에서는 300 mg/day 미만에서도 통증 조절과 약 부작용에 대해 좋은 결과를 얻었다고 보고하기도 하였으나5) 일반적으로 대부분의 연구들은 300 mg/day를 적정 용량으로 생각하며 150 mg/day로는 적절한 신경병증성 통증에 대한 효과를 보기 어렵다고 판단했다. Derry 등6)의 systemic review에 따르면 다른 약제와의 병용 없이 pregabalin 300 mg/day가 당뇨병성 신경병증을 비롯한 신경병증성 통증에 유의미한 효과가 있음을 보고하였으나 150 mg/day으로는 적절한 신경병증성 통증에 대한 효과를 보기 어렵다고 판단했다.
Alpha lipoic acid (ALA)는 통증을 동반한 당뇨병성 신경병증의 치료에 있어 가능성을 보여왔다.7) ALA는 항산화 효과를 가진 약제로 당뇨병성 신경병증에서 superoxide anion와 peroxynitrite에 의한 산화 스트레스에 영향을 주어 당뇨병성 신경병증의 주된 병리 기전인 미세순환에 대한 산화 스트레스를 감소시키는 효과가 있다고 알려져 있다.8) 또한 ALA 사용이 당뇨병성 신경병증에서의 감각신경 전도 속도 회복에도 효과가 있다고 보고되었다.9,10) McIlduff와 Rutkove11)는 당뇨병성 다발 신경병증의 환자들에 경구 ALA 600 mg/day를 투여하였을 때 임상적으로 중요한 합병증 발생 없이 증상 호전을 보였다고 보고하였다.
이에 저자들은 본 연구에서 국내 환자를 대상으로 당뇨병성 말초 신경병성 통증에 대해 단일 약제 요법을 통한 통증 조절보다 ALA 600 mg/day와 150 mg/day의 저용량 pregabalin을 병용 투여하여 약제 부작용도 감소시키는 동시에 만족스러운 통증 조절 효과를 얻을 수 있는지 확인하고자 한다.
Go to : 
2009년 1월 1일부터 2022년 10월 31일까지 본원에서 당뇨병성 신경병증의 조절을 위해 pregabalin과 ALA를 병용하여 처방받은 환자 100명을 대상으로 하였다. 1군(pregabalin 150 mg/day+ALA 600 mg/day)은 70명, 2군(pregabalin 300 mg/day+ALA 600 mg/day)은 30명이었으며 평균 추시 기간은 1군 120.23주 (12∼248주), 2군 149.05주(12∼298주)였다(Table 1).
18세 이상의 성인을 대상으로 2형 당뇨병으로 진단받아 약물 치료를 시행 중인 환자 중 유병 기간이 6개월 이상인 당뇨병성 신경병증 환자를 대상으로 하였다. 이전에 당뇨와 상관없는 신경학적 질환이 있었던 환자, 당화혈색소가 11% 이상으로 조절되지 않는 당뇨병 환자, 기존에 진단받았던 신기능 장애(혈청 크레아티닌 >1.5 mg%)가 있는 환자, 간기능 장애(혈청 총 빌리루빈 >2.5 mg%)가 있는 환자, 기존의 만성 B형 간염 환자, 이전 3개월 이내의 B형 간염 또는 HIV 감염이 있었던 환자, 그리고 호흡기 계통이나 혈액학적인 이상이 있는 환자는 대상에서 제외하였다. 불안정 관상동맥 질환 및 증상을 동반한 말초 혈관 질환, 스크리닝으로 시행한 심전도상에서 이상 소견을 보이는 환자, 임신 혹은 수유 중인 여성들도 연구 대상에서 제외하였다.
당뇨병성 말초 신경병증에 의한 감각 신경 이상은 양측 발목에서의 반사 감소 혹은 결여, 또는 양측 하지 말단부에서 진동 감각이나 찌르기 감각, 미세 접촉 감각, 온도 감각의 감소로 정의하였다.12) 각 환자들의 의무 기록을 참고하여 약제 복용 전후의 통증 정도를 visual analogue scale (VAS)로 확인하였으며 약제 복용 전후 각각 시기에 시행한 neurometer 측정값을 이용하여 감각 기능을 평가 및 비교하였다.
Neurometer 검사는 Neuromter CPT/C (Neurotron Inc., Baltimore, MD, USA) 모델을 사용하였으며, 환자의 엄지발가락에 전극을 설치한 후 환자가 자극을 감지할 수 있을 때까지 전류를 올린 후 느끼지 못하는 시점까지 내리며 환자가 자극을 느낄 수 있는 최소 역치값(current perception threshold)을 얻는 방법으로 검사하며 0에서 12까지의 결괏값을 갖는다(Fig. 1).
약제 복용 기간 동안 발생한 부작용들을 의무 기록을 통하여 후향적으로 조사하였으며 약제 부작용으로는 어지러움, 졸림, 오심, 구토, 변비, 말초 부종 등이 확인되었다.
연구의 프로토콜, 사례 기록 양식, 사전 동의 양식 및 피험자 정보지는 윤리 위원회에서 검토 및 승인되었으며 헬싱키 선언(2013년 개정)에 따른 윤리 원칙과 International Conference of Harmonization Good Clinical Practices에 따라 수행되었다.
Paired t-test를 통하여 약물 복용 전후 각 군별의 통증 VAS 점수를 비교하였으며 군 사이의 비교를 위하여 independent two sample t-test 를 사용하였다. 또한 각 군에서 약제 복용 전후 neurometer 결과의 차이를 구하여 이를 이용한 independent t-test를 사용하였다. 통계적 유의 수준은 p-value가 0.05 미만일 경우 의미 있는 결과로 판정하였으며 모든 분석에는 IBM SPSS Statistics ver. 22.0 (IBM Corp., Armonk, NY, USA)을 이용하였다.
Go to : 
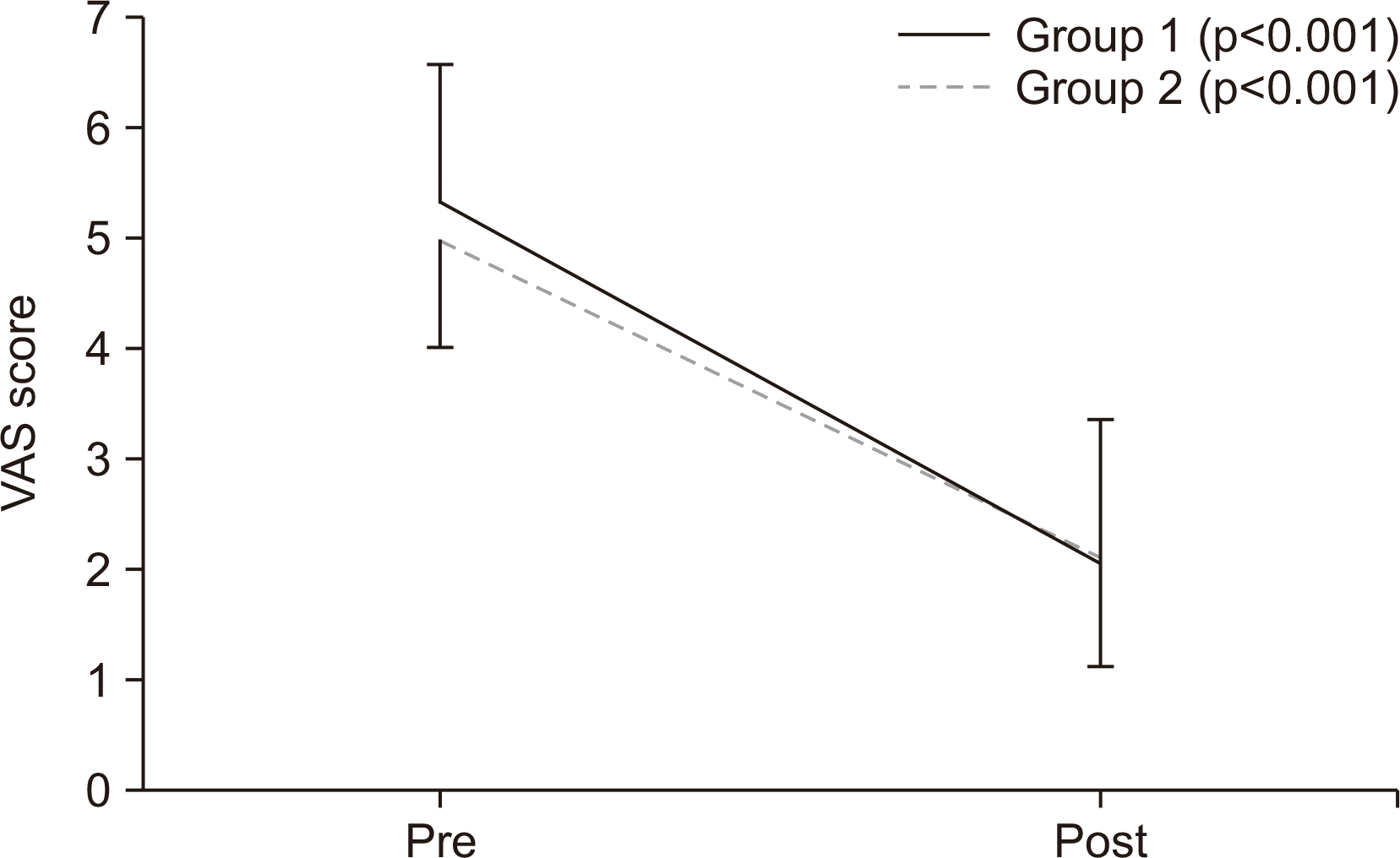
약제 복용 전후의 VAS 점수를 paired t-test를 통하여 비교하였을 때 1군에서는 평균 VAS 점수 3.23점의 유의미한 감소가 있었으며(p<0.001), 2군에서는 평균 VAS 점수 2.86점의 유의미한 감소가 있었다(p<0.001) (Fig. 2). 또한 1군과 2군의 약제 복용 전과 후의 VAS 점수, 그리고 전후의 VAS 점수 차이의 평균이 통계적으로 의미 있는 차이를 보이는지에 대해 independent two sample t-test를 통하여 분석하였으나 p-value는 각각 0.284, 0.912, 0.248로 두 군 간에 유의미한 차이를 보이지는 않았다.
또한 신경병증성 통증 조절에 대한 효과 분석 외에도 각 군에서 약물의 부작용을 확인하였다. 전체 40건의 부작용이 보고되었으며 그중 1군의 70명 환자 중에서는 17건(24.3%), 30명의 2군 환자 중에서는 23건(76.7%)이 발생하였다. 각 군에서 가장 흔하게 발생한 부작용은 어지러움으로 1군에서는 6건(35.3%), 2군에서는 10건(43.5%)으로 가장 많았다. 그다음으로는 졸림, 부종, 위장관계 증상 순서로 부작용이 발생하였다(Table 2).
Neurometer 검사는 1군에서 47예, 2군에서는 20예가 시행되었다. 1군에서 약제 복용 전후의 neurometer 값의 평균값은 각각 7.826±4.047, 7.417±4.324였고, 2군에서는 각각 4.48±5.093, 평균값은 5.91±4.979이었다. 두 군의 복용 전후 neurometer 결괏값 간의 차이를 약제 복용 전 시행한 검사에서 약제 복용이 종료된 후에 시행한 검사의 값을 뺀 값으로 분석을 진행하였다. 감각 이상이 호전을 보이는 경우 양수의 값을 보이게 되는데 1군에서는 0.41±3.21, 2군에서는 –1.43±4.02의 평균값을 보였고, 약제 복용 전후의 neurometer 차이에 대하여 independent two sample t-test를 이용하여 분석한 결과 통계적으로 의미 있는 차이는 없었다(p=0.089). 즉, 2군보다 1군에서 neurometer를 이용한 감각 이상의 호전 정도가 더 양호하게 나타났으나 이는 통계적으로 유의미한 차이를 보이지 않았다(Table 3).
Go to : 
Pregabalin는 미국 Food and Drug Association에서 당뇨병성 신경병증과 헤르페스 후 발생되는 신경통에 대해 승인받은 약제로 국내에서는 말초 및 중추 신경병증성 통증, 간질 또는 섬유근육통 투여하는 것으로 허가되어있다.13) 특히 당뇨병성 신경병증성 통증에 대해서는 일차 약물로 권고되는 약제로, 일반적으로 초회 150 mg/day로 시작한 후 3∼7일에 걸쳐 300 mg/day로 증량하고 최대 600 mg/day까지 투여할 수 있는 것으로 알려져 있다.14)
보고된 이중 맹검 무작위 대조군 연구에 따르면 당뇨병성 말초 신경병증에 대해 pregabalin 300 mg/day를 8주간 투여함으로써 유의미한 통증 및 수면 방해의 호전을 보였다고 하였으며,15) Richter 등16)은 246명을 대상으로 6주간 시행한 무작위 대조군 연구에서 pregabalin 600 mg/day와 위약을 비교하였을 때 신경병증성 통증에 대해 50% 이상의 유의미한 통증 호전을 확인하였다. 또한 pregabalin의 용량에 대해 150 mg/day, 300 mg/day, 600 mg/day 그리고 위약을 비교한 이중 맹검 무작위 대조군 연구에서는 600 mg/day를 투여한 군에서는 유의미한 통증 호전을 확인할 수 있었으나 150 mg/day 및 300 mg/day를 투여한 군에서는 위약과 비교했을 때 유의미한 차이가 없었다고 보고하여 고용량의 pregabalin 투여를 권고한 바 있다.17) 하지만 pregabalin은 어지러움, 졸림, 구토, 오심, 말초 부종 등과 같은 많은 부작용이 보고되어 있으며 이로 인해 환자의 약물 순응도에 문제가 있는 것으로 알려져 있어 당뇨병성 말초 신경병증에 일차 약물로 고용량의 pregabalin을 처방하기에는 어려움이 있는 것이 사실이다.
본 연구에서는 당뇨병성 말초 신경병증을 가진 환자들에게 pregabalin 150 mg/day와 ALA 600 mg/day 또는 pregabalin 300 mg/day와 ALA 600 mg/day를 투여하였는데 초기에는 300 mg/day의 pregabalin을 주로 처방하였고 이로 인한 약제 부작용이 환자들에게 빈번하게 발생하여 약물 순응도가 현저히 떨어지는 것을 확인한 후에는 주로 150 mg/day의 pregabalin을 처방하였다. 신경병증성 통증에 대해서는 VAS 점수를 비교하였고, 감각에 대한 치료 효과에 대해서는 neurometer 검사를 이용해 확인하였다. 일반적으로 권고되는 정상 용량보다 저용량인 pregabalin 150 mg/day와 ALA 600 mg/day를 병용하여 사용한 군에서 약물 사용 후 평균 3.23점의 VAS 점수 감소가 있었고(p<0.001), pregabalin 300 mg/day와 ALA 600 mg/day를 병용한 군에서도 평균 2.86점의 VAS 점수 감소가 있었으며(p<0.001) 두 군 모두에서 통계적으로 유의미한 정도의 통증 감소를 확인할 수 있었다. 그러나 이러한 각 군 사이의 VAS 점수 호전 정도를 비교한 통계적 분석에서 유의미한 통계적 차이는 없었다(p=0.248).
신경병증성 통증을 호소하는 한국인에게 pregabalin의 적정 용량에 대한 무작위 이중 맹검 연구에 따르면 300 mg/day 투여 시 최대 43.8%까지 어지러움, 졸림, 안면부종 등의 부작용이 나타난 것으로 보고되었다.18) 또한 pregabalin의 부작용뿐만 아니라 ALA의 경우에도 두드러기, 습진 등의 피부 병변 또는 감각 이상과 함께 혈당 감소에 의한 증상이 나타날 수 있다고 알려져 있다. 본 연구에서는 각 군에서 약물의 부작용 빈도를 확인하였는데 어지러움, 졸림, 위장관계 증상, 말초 부종 등이 보고되었으며 이는 주로 pregabalin에 의한 부작용으로 생각되지만 저용량의 pregabalin 투여군에서 훨씬 적은 빈도의 약물 부작용이 나타나는 것으로 확인되어 저용량의 pregabalin 투여는 환자의 약물 순응도를 높이는 데 도움이 될 것으로 판단된다.
Neurometer는 당뇨병성 말초 신경병증 또는 다른 신경병증 등의 환자들에게 있어서 비침습적으로 감각 신경의 손상 정도를 확인하는 방법이다.19,20) 신체의 한 부위에서 서로 다른 전기 자극을 준 뒤(2,000, 250, 5 Hz) 전류 인지 역치값을 측정하여 양적으로 감각신경 손상을 확인하며 0에서 12까지의 결괏값을 갖는다21).
본 연구에서 100명의 당뇨병성 신경병증 환자들 중 neurometer를 약물 복용 전후에 시행한 환자는 총 67명이었으며, 약제 복용 전후의 neurometer 차이값의 평균값을 각 군에서 분석하였다. Pregabalin 300 mg/day와 ALA 600 mg/day를 복용한 환자군에 비하여 pregabalin 150 mg/day와 ALA 600 mg/day를 복용한 1군에서 더 양호한 감각 이상의 호전 경향을 보이는 것으로 분석되었으나 통계적으로는 유의하지 않았다(p=0.089).
본 연구 결과에 따르면 pregabalin 150 mg/day와 함께 ALA 600 mg/day를 병용 투여하였을 때 pregabalin 300 mg/day와 ALA 600 mg/day를 함께 복용하는 것에 비해 VAS 점수로 측정한 통증 호전 정도에서 더 좋은 결과를 보였으며, 이는 두 군 사이의 비교에서 유의한 통계적 의미는 없었으나 통증 호전의 정도가 최소한 대등한 것으로는 볼 수 있다. 또한 pregabalin 300 mg/day와 ALA 600 mg/day를 복용한 환자군에 비하여 pregabalin 150 mg/day와 함께 ALA 600 mg/day를 병용 투여한 군에서 약물 복용으로 인한 부작용의 빈도가 훨씬 더 적은 것으로 나타났으며, neurometer를 이용하여 측정한 감각 이상 호전 정도의 결과에서도 통계적으로 유의한 차이는 없지만 더 좋은 결과를 보여 주고 있어 이상의 결과를 감안할 때 ALA와 저용량의 pregabalin 투여는 이전 보고된 연구 결과와는 다르게 당뇨병성 말초 신경병증의 치료에 있어 의미 있는 임상 결과를 보여준다고 하겠다.
본 연구의 제한점으로는 약제의 효과를 판단하기 위해 이중 맹검, 무작위 대조군 연구가 아닌 의무 기록을 이용해 후향적으로 연구하였다는 것이다. 또한 pregabalin 150 mg/day와 ALA 600 mg/day를 복용한 군은 70명, pregabalin 300 mg/day와 ALA 600 mg/day를 복용한 군은 30명이며, neurometer를 시행한 환자 수 역시 pregabalin 150 mg/day와 ALA 600 mg/day를 복용한 군은 47명, pregabalin 300 mg/day와 ALA 600 mg/day를 복용한 군은 20명으로 군별 환자 수의 차이가 있어 통계적인 오차나 선택 오류(selection bias) 등이 발생하였을 가능성이 있다. 그 외 약물 복용에 대한 순응도를 변수로서 고려하지 않았으며 상기 기술한 변수들은 본 연구의 결과에 영향을 줄 수 있어 결과 분석에 제한된다고 할 수 있겠다. 앞으로 이러한 문제점을 보완하여 많은 환자를 대상으로 전향적인 이중 맹검 연구가 시행되어야 할 것으로 판단된다.
Go to : 
당뇨병성 말초 신경병증에 대해 ALA 600 mg/day와 함께 일반적으로 투여되는 용량보다 더 작은 용량인 pregabalin 150 mg/day를 병용 투여하는 것은 유의미한 신경병증성 통증의 호전을 보였고, ALA 600 mg/day와 pregabalin 300 mg/day 병용 투여했을 때와 비교하여 부작용 발생 빈도는 작고 신경병증의 호전 정도는 차이가 없었다. 따라서 당뇨병성 말초 신경병증성 통증 환자에 있어서 ALA 600 mg/day와 pregabalin 150 mg/day를 병용 투여하는 것도 임상적으로 고려되어야 할 것으로 판단된다.
Go to : 
References
1. Boulton AJ, Vinik AI, Arezzo JC, Bril V, Feldman EL, Freeman R, et al. 2005; Diabetic neuropathies: a statement by the American Diabetes Association. Diabetes Care. 28:956–62. doi: 10.2337/diacare.28.4.956. DOI: 10.2337/diacare.28.4.956. PMID: 15793206.
2. Young MJ, Boulton AJ, MacLeod AF, Williams DR, Sonksen PH. 1993; A multicentre study of the prevalence of diabetic peripheral neuropathy in the United Kingdom hospital clinic population. Diabetologia. 36:150–4. doi: 10.1007/BF00400697. DOI: 10.1007/BF00400697. PMID: 8458529.
3. Pirart J. 1978; Diabetes mellitus and its degenerative complications: a prospective study of 4,400 patients observed between 1947 and 1973. Diabetes Care. 1:168–88. doi: 10.2337/diacare.1.3.168. DOI: 10.2337/diacare.1.3.168.
4. Lesser H, Sharma U, LaMoreaux L, Poole RM. 2004; Pregabalin relieves symptoms of painful diabetic neuropathy: a randomized controlled trial. Neurology. 63:2104–10. doi: 10.1212/01.wnl.0000145767.36287.a1. DOI: 10.1212/01.WNL.0000145767.36287.A1. PMID: 15596757.
5. Daniel SR, Badyal DK, Jacob JJ, Kaur J. 2018; Efficacy and safety of pregabalin versus amitriptyline in patients with painful diabetic neuropathy. Int J Adv Med. 5:716–21. doi: 10.18203/2349-3933.ijam20182129. DOI: 10.18203/2349-3933.ijam20182129.
6. Derry S, Bell RF, Straube S, Wiffen PJ, Aldington D, Moore RA. 2019; Pregabalin for neuropathic pain in adults. Cochrane Database Syst Rev. 1:CD007076. doi: 10.1002/14651858.CD007076.pub3. DOI: 10.1002/14651858.CD007076.pub3. PMCID: PMC6353204.
7. Ziegler D, Reljanovic M, Mehnert H, Gries FA. 1999; Alpha-lipoic acid in the treatment of diabetic polyneuropathy in Germany: current evidence from clinical trials. Exp Clin Endocrinol Diabetes. 107:421–30. doi: 10.1055/s-0029-1212132. DOI: 10.1055/s-0029-1212132. PMID: 10595592.
8. Ziegler D. 2004; Thioctic acid for patients with symptomatic diabetic polyneuropathy: a critical review. Treat Endocrinol. 3:173–89. doi: 10.2165/00024677-200403030-00005. DOI: 10.2165/00024677-200403030-00005. PMID: 16026113.
9. Ziegler D, Low PA, Litchy WJ, Boulton AJ, Vinik AI, Freeman R, et al. 2011; Efficacy and safety of antioxidant treatment with α-lipoic acid over 4 years in diabetic polyneuropathy: the NATHAN 1 trial. Diabetes Care. 34:2054–60. doi: 10.2337/dc11-0503. DOI: 10.2337/dc11-0503. PMID: 21775755. PMCID: PMC3161301.
10. Ametov AS, Barinov A, Dyck PJ, Hermann R, Kozlova N, Litchy WJ, et al. 2003; The sensory symptoms of diabetic polyneuropathy are improved with alpha-lipoic acid: the SYDNEY trial. Diabetes Care. 26:770–6. doi: 10.2337/diacare.26.3.770. Erratum in: Diabetes Care. 2003;26:2227. DOI: 10.2337/diacare.26.3.770. PMID: 12610036.
11. McIlduff CE, Rutkove SB. 2011; Critical appraisal of the use of alpha lipoic acid (thioctic acid) in the treatment of symptomatic diabetic polyneuropathy. Ther Clin Risk Manag. 7:377–85. doi: 10.2147/TCRM.S11325. DOI: 10.2147/TCRM.S11325. PMID: 21941444. PMCID: PMC3176171.
12. Thomas PK. 1997; Classification, differential diagnosis, and staging of diabetic peripheral neuropathy. Diabetes. 46 Suppl 2:S54–7. doi: 10.2337/diab.46.2.s54. DOI: 10.2337/diab.46.2.S54. PMID: 9285500.
13. Verma V, Singh N, Singh Jaggi A. 2014; Pregabalin in neuropathic pain: evidences and possible mechanisms. Curr Neuropharmacol. 12:44–56. doi: 10.2174/1570159X1201140117162802. DOI: 10.2174/1570159X1201140117162802. PMID: 24533015. PMCID: PMC3915349.
14. Handelsman Y, Bloomgarden ZT, Grunberger G, Umpierrez G, Zimmerman RS, Bailey TS, et al. 2015; American Association of Clinical Endocrinologists and American College of Endocrinology--clinical practice guidelines for developing a diabetes mellitus comprehensive care plan--2015--executive summary. Endocr Pract. 21:413–37. doi: 10.4158/EP15672.GL. DOI: 10.4158/EP15672.GL. PMCID: PMC4959114.
15. Rosenstock J, Tuchman M, LaMoreaux L, Sharma U. 2004; Pregabalin for the treatment of painful diabetic peripheral neuropathy: a double-blind, placebo-controlled trial. Pain. 110:628–38. doi: 10.1016/j.pain.2004.05.001. DOI: 10.1016/j.pain.2004.05.001. PMID: 15288403.
16. Richter RW, Portenoy R, Sharma U, Lamoreaux L, Bockbrader H, Knapp LE. 2005; Relief of painful diabetic peripheral neuropathy with pregabalin: a randomized, placebo-controlled trial. J Pain. 6:253–60. doi: 10.1016/j.jpain.2004.12.007. DOI: 10.1016/j.jpain.2004.12.007. PMID: 15820913.
17. Tölle T, Freynhagen R, Versavel M, Trostmann U, Young JP Jr. 2008; Pregabalin for relief of neuropathic pain associated with diabetic neuropathy: a randomized, double-blind study. Eur J Pain. 12:203–13. doi: 10.1016/j.ejpain.2007.05.003. DOI: 10.1016/j.ejpain.2007.05.003. PMID: 17631400.
18. Moon DE, Lee DI, Lee SC, Song SO, Yoon DM, Yoon MH, et al. 2010; Efficacy and tolerability of pregabalin using a flexible, optimized dose schedule in Korean patients with peripheral neuropathic pain: a 10-week, randomized, double-blind, placebo-controlled, multicenter study. Clin Ther. 32:2370–85. doi: 10.1016/j.clinthera.2011.01.014. DOI: 10.1016/j.clinthera.2011.01.014. PMID: 21353106.
19. Park JH, Won JC. 2018; Patterns of nerve conduction abnormalities in patients with type 2 diabetes mellitus according to the clinical phenotype determined by the current perception threshold. Diabetes Metab J. 42:519–28. doi: 10.4093/dmj.2018.0068. Erratum in: Diabetes Metab J. 2019;43:381. DOI: 10.4093/dmj.2018.0068. PMID: 30398037. PMCID: PMC6300437.
20. Park KS, Kwon YC, Youn M, Park YS, Hong YH, Sung JJ. 2017; Current perception threshold in diabetic sensory polyneuropathy with normal routine nerve conduction study. Ann Clin Neurophysiol. 19:125–30. doi: 10.14253/acn.2017.19.2.125. DOI: 10.14253/acn.2017.19.2.125.
21. Prendergast JJ, Miranda G, Sanchez M. 2004; Improvement of sensory impairment in patients with peripheral neuropathy. Endocr Pract. 10:24–30. doi: 10.4158/EP.10.1.24. DOI: 10.4158/EP.10.1.24. PMID: 15251618.
Go to : 




 PDF
PDF Citation
Citation Print
Print




 XML Download
XML Download