Abstract
Severe fever with thrombocytopenia syndrome (SFTS) is an emerging tick-borne infectious disease caused by a novel Dabie bandavirus belonging to the genus Bandavirus. The incidence of SFTS has been increasing in East Asia, posing a great concern to public health in endemic areas. Although SFTS has a high case-fatality rate, there is currently no effective treatment for SFTS. Therefore, early diagnosis and prevention of SFTS are essential. Primarily, SFTS is a tick-borne zoonosis, but human-to-human transmission can also occur in healthcare workers or family members by exposure to patients’ blood or body fluids. We review the current epidemiological characteristics of SFTS in Korea and the key infection control measures in hospitals and household settings.
중증열성혈소판감소증후군(Severe fever with thrombocytopenia syndrome, SFTS)은 SFTS virus (SFTSV)에 의한 열성 출혈 질환으로 진드기 매개에 의해 발생하는 인수공통 신종감염병이다[1]. 2009년 중국 중부의 허베이와 동북부의 허난성 시골 지역에서 혈소판 감소를 동반한 고열, 소화기 증상, 백혈구감소증을 보이는 원인 불명의 발열 환자들이 다수 발생하였는데 2년간의 역학 조사와 병원체 연구를 통해 환자의 혈액에서 원인 병원체 분리하였고 2011년에 단일가닥 RNA virus에 속하는 SFTS bunyavirus를 학계에 최초로 보고하였다[2]. 이후 2012년 한국, 일본에서도 감염 사례들이 보고되었고 최근에는 대만, 베트남 등에서도 SFTS감염 사례를 보고하였다[3-6]. SFTS의 발생과 유행을 감시하고 대처하기 위해 우리나라에서는 2013년 4월부터 SFTS를 4군 법정감염병으로 지정하여 환자 발생에 대한 감시를 시작하였고 2020년부터는 제3급 법정감염병으로 분류되어 발생과 유행 감시가 이루어지고 있다. 인체 감염은 주로 SFTSV에 감염된 진드기에 물려서 감염이 되는 것으로 알려져 있는데 중국에서 처음 SFTS가 발생할 당시에 환자가 거주하는 지역의 가축에서 채집한 작은소피참진드기(Haemaphysalis longicornis)에서 SFTSV RNA가 검출되어 작은소피참진드기가 SFTSV의 유력한 매개체로 인식되기 시작하였다[2]. 또한 SFTS 환자의 혈액이나 체액에 노출되어 감염되는 사람 간의 전파 사례와 SFTSV에 감염된 가축이나 개, 고양이를 통한 감염이 의심되는 사례도 보고되었다[7-19]. 특히 의료기관에서 중증의 SFTS 환자와 접촉한 의료진이나 환자의 가족 등에서도 2차감염 사례가 보고되면서 의료기관종사자들의 감염 관리에 각별한 주의가 요구되고 있다. 본 종설에서는 SFTS의 국내 발생 현황과 국내 의료관련감염 사례를 살펴보고 전파 경로에 따른 의료관련감염관리를 중심으로 소개하고자 한다.
SFTS를 일으키는 원인 바이러스의 이름은 2014년에 Bunyaviridae과 Phlebovirus속 SFTS virus 로 처음 명명되었고 이후 여러 차례의 수정을 거쳤다[1,20]. 현재 국제 바이러스 분류위원회(The International Committee on Taxonomy of Viruses: ICTV)에서 사용하는 공식 이름은 Bunyavirales목 Phenuiviridae과 Bandavirus속에 속하는 Dabie bandavirus이며 흔히 Severe Fever with Thrombocytopenia Syndrome Virus (SFTSV)로 불린다[21]. SFTSV의 유전자형은 A, B, C, D, E, F 총 6개로 알려져 있으며 국내 확진자들로부터 검출된 SFTSV에서는 6가지 유전자형이 모두 검출되었다. 특히 유전형B가 77.6%로 가장 많았고 D (10.5%), A (6.3%) 순이었다[22,23]. 중국은 유전형F (43.6%)가 가장 많고 A (20.1%), B (19.5%), D (15.4%) 순이며 일본은 한국과 마찬가지로 유전자형 B가 주로 확인된다[22,23]. SFTSV를 전파시키는 주된 매개체는 작은소피참진드기(H. longicornis)로 알려져 있으며 개피참진드기(H. flava), 뭉뚝참진드기(Amblyomma testudinarium), 일본참진드기(Ixodes nipponensis)도 SFTS을 매개할 수 있는 것으로 알려져 있다[2,21,24-27]. 국내에는 작은소피참진드기가 매개체의 96-99%를 차지하며 전국에 걸쳐 분포한다[28]. SFTSV는 참진드기의 침샘, 중장 및 난소 조직에 널리 분포하는데 SFTSV에 감염된 진드기가 흡혈 하는 동안 진드기의 침샘을 통하여 숙주 동물이나 인체에 전파되는 것으로 추정하고 있다[24,25,29]. 국내 작은소피참진드기의 SFTSV 최소감염률(minimum infection rate)은 0.2-11.1%로 보고되었는데, 특히 제주도에서 채집된 참진드기에서 가장 높은 감염률을 보였다[30-33]. 작은소피참진드기는 유충(larva), 약충(nymph), 성충(adult)의 모든 단계에서 흡혈을 하는데, 유충과 암컷 성충에서 SFTSV 양성률이 높았으며 월별로는 4월-10월에 양성률이 높은 것으로 조사되었다[30-33]. 흡혈 숙주 동물은 주로 포유류와 조류이며 소, 염소, 양, 개, 돼지, 닭 및 고슴도치와 같은 여러 종에서 SFTSV 특이적 항체가 발견되어 SFTSV에 감염된 동물이 SFTSV를 유지하고 전파시키는데 중요한 역할을 할 것으로 생각된다[34-38]. 국내에서 조사한 동물의 SFTSV 항체 유병률 연구에서는 염소(6.9-14.4%), 개(13.9%), 고라니(23.8%), 멧돼지(1.9%) 등에서 SFTSV 특이 항체가 확인되었다[21,35,39]. 국내 인구집단의 SFTSV 항체의 혈청 유병률은 대상 지역과 인구 집단 별로 다소 차이는 있지만 1.4-2.1%의 항체 유병률을 보이며 특히 농촌 지역에서는 2.4-7.7%로 도시 지역에 비해 높고, 연령이 증가함에 따라 유병률이 높게 나타났다[40-42]. 진드기 교상 후 잠복기는 평균 9일(5-14일)이며 SFTS환자와 직접 접촉했거나 환자의 체액이나 혈액에 노출 후에는 평균 10일(7-12일)의 잠복기를 거친다[1,43]. 주요 증상은 발열, 쇠약감, 두통과 구역, 구토, 설사 등 위장관계 증상 등이며 피부 발진, 점상출혈이 나타나기도 한다[1]. 혈소판감소증이 동반되며 백혈구감소증, 간수치 상승도 흔히 동반되고 의식 저하, 경련 등의 신경학적 증상 등의 중증 사례도 나타난다[1,2,44,45]. 경과가 좋은 경우에는 바이러스 부하가 점차 감소하면서 발병 후 2주 정도에 회복되지만 치명적인 경우에는 혈액 중에 계속 높은 바이러스 농도를 유지하면서 점차 악화되어 발병 후 7-14일 정도에 다발성장기부전으로 악화되고 사망에 이르게 된다[1,43]. 진단은 혈액 등의 검체에서 배양 검사로 SFTSV를 분리하거나 실시간 역전사 중합효소연쇄반응(real-time RT-PCR)을 통해 SFTSV 유전자를 검출하거나 회복기 혈청에서 SFTSV 특이 항체가 급성기의 4배 이상 증가한 경우 진단이 가능하다[26,46]. 현재까지 정립된 치료법은 없어 보존적 치료가 주를 이루며 ribavirin, favipiravir등의 항바이러스제 투여, 스테로이드, 면역글로불린 투여나 혈장교환술 등의 방법이 시도되고 있다[26,46].
국내에서는 2012년 8월에 강원도에서 첫 사례가 발생한 것으로 보고되었는데 당시 환자는 원인 불명의 고열과 혈소판감소증, 백혈구감소증을 보이면서 다발성장기부전으로 사망하였고 환자의 사후에 보관 혈액을 후향적으로 분석하여 원인 병원체가 SFTSV임을 확인하였다[3]. 2013년 5월에 제주도에서 가축을 기르는 농부가 발열로 내원하여 SFTS로 진단받고 치료 도중 다발성장기부전으로 사망하는 사례가 발생하여 법정감염병 지정 이후 국내 첫 등록 환자가 되었다[47]. 하지만 2010년도에 일개 병원에 내원한 환자들의 혈액 보관 검체에서도 SFTSV가 확인되어 현재까지 국내에서는 2010년도부터 SFTS가 발생했던 것으로 추정하고 있다[48]. 2013년에 총 36건의 SFTS 환자가 확인되었고 이후 5년간 확진자 수가 급증하여 2017년에는 연간 발생 건수가 272건으로 증가하였다. 2018년부터는 연간 200-250명 수준으로 발생하다가 2021년에는 178명으로 감소하였다(Fig. 1) [49]. 2013년에 법정감염병으로 신고가 시작된 이후부터 2021년까지 신고된 확진 환자는 1498명이며 의사 환자와 검사 거부자 13명을 포함하여 총 1510명이 신고되었다[50]. 여자가 780명(51.7%), 남자가 730명(48.3%)이었으며, 평균 연령은 67세이고 50대 이상이 전체의 91.1%으로 대부분을 차지하며 그 중 70대 이상이 44.2%로 고령에서 이환율이 높게 나타나고 있다(Fig. 2). 2013년부터 국내 SFTS 환자의 거주지 별 누적 발생 현황을 살펴보면 경기도 263명(17.4%), 경상북도 219명(14.5%), 강원도 202명(13.4%) 순으로 환자가 발생했다. 인구 10만명 당 누적 발생률은 제주도가 16.31명으로 가장 발생빈도가 높고 강원도(13.11명), 경상북도(8.11명), 세종시(7.65명), 충남(6.53명) 순이며 전국적으로는 10만명 당 2.96명의 환자가 발생하였다(Fig. 3) [50]. 계절 및 월별로는 1월과 12월을 제외하고 2월부터 11월까지 환자가 발생하고 있으나 주로 봄부터 가을까지 많이 발생하며 6-10월 동안의 발생이 97%로 집중되고 있다(Fig. 3) [50,51]. 특히 10월 발생이 전체 건수의 26.4%로 가장 많은 환자가 발생하고 있다(Fig. 4) [50]. 이러한 계절과 지역에 따른 환자 발생의 편향은 SFTSV 매개체인 진드기 성장 역학과 관련된 기온, 상대습도 등의 기후 요인과 관련이 있으며 또한 사람이 진드기에 노출되는 기회에 영향을 주는 직업, 연령, 야외활동 등의 인구학적 요인과 밀접한 관련이 있다고 추정할 수 있다[52-54]. 우리나라는 9월과 10월 추석 시기에 성묘∙벌초 작업 및 야외활동 증가로 인해 진드기에 노출되는 기회 빈도가 증가하는 것도 가을철 SFTS의 높은 발생률과 관련이 있을 것으로 생각된다. 국내 SFTS의 치명률은 2013년 유행 초기에는 36명의 환자 중 17명이 사망하여 47.2%의 높은 치명률을 보였으나 점차 감소하는 추세이며 2021년에는 28명이 사망하여 15.7%로 감소하였다(Fig. 1) [50]. 2013년부터 2021년까지 누적 사망자 수는 총 279명으로 18.5%의 치명률을 보여주고 있다[50].
SFTS의 사람 간 전파 경로에 대해서는 아직까지 정확하게 밝혀진 바는 없으나 위험 요인은 주로 중증 또는 사망 환자와의 접촉 및 환자의 혈액 또는 체액에 대한 노출이다. Ye 등[27]의 연구에서 89건의 사람 간 2차 감염 사례 중 82%가 SFTS 지표 환자의 혈액에 노출된 적이 있었고 환자의 혈액에 접촉 후 2차 감염률은 62.4%로 SFTS 환자의 혈액에 대한 노출 경험이 사람 간 전파의 주된 위험 요인이었다. 또한 SFTS 지표 환자의 중증도가 높고 출혈이 있거나 사망한 경우에도 접촉자의 2차 감염 위험이 증가한다. 환자의 혈액 중의 바이러스 농도는 중증도나 사망과 밀접한 관련이 있는 것으로 알려졌는데 중증 환자나 사망 환자의 혈액에는 SFTSV가 고농도로 유지되고 있을 가능성이 높아 이런 환자의 혈액이나 혈성 분비물에 노출되는 것은 SFTSV 2차감염의 위험 요인이 된다[55,56]. 국내에서 발생했던 SFTS의 의료관련감염 사례를 살펴보면 2014년 9월 서울의 상급종합병원 응급실에서 SFTS 환자의 심폐소생술을 시행했던 의료진 7명 중 4명이 감염되는 사례가 발생하였고 역학조사 결과 호흡기 분비물, 혈액 또는 체액에 대한 노출이 2차 감염과 유의한 관련성이 있었다[57]. 2015년 10월에는 강원도의 상급종합병원에서 SFTS 환자의 심폐소생술, 혈액투석도관 삽입 시술을 한 의료인 및 사망 후 사체에 접촉한 장례지도사의 감염 사례가 있었으며, 접촉자 15명 중 5명의 감염이 확인되었다[13]. 감염된 사람은 모두 환자가 출혈 증상이 나타난 후 환자와 접촉했고 환자의 혈액에 노출되었던 것으로 확인되었다[13]. 2017년 10월 경기도의 상급종합병원에서는 SFTS 환자에게 기도삽관을 시행했던 의사와 환자 사망 후 사체를 수습했던 장례지도사의 감염 사례가 있었다[58]. 2차감염이 확인된 의사는 기도삽관 시에 방수마스크와 장갑을 착용하였음에도 감염이 발생하여 기도삽관 및 기도흡인술 도중 발생한 에어로졸에 의한 감염으로 추정하였다[58]. 2018년 10월 제주도의 종합병원에서는 SFTS로 사망한 환자의 혈액에 직접 노출되었던 환자 가족에서 2차 감염이 발생한 것을 계기로 밀접접촉자에 대한 조사를 시행하였고 그 결과, 중환자실에서 환자와 접촉했던 의료진 4명 중 2명에서 2차 감염이 확인되었다[59]. 2020년 8월 대구의 상급종합병원 응급실에서는 심폐소생술에 참여했던 의료진 59명 중 17명이 집단 감염되는 사례가 발생하였고 환자의 혈액 및 체액 접촉이 2차 감염의 유의미한 위험 요인으로 확인되었다[60]. 이상의 사례 들에서 공통적으로 감염된 의료진들이 SFTS 지표 환자들을 접촉할 당시에 환자들은 모두 중증 상태였으며 결국 모두 사망하였다(Table 1). 2차 감염이 확인된 의료진들은 직ㆍ간접적으로 환자의 혈액 또는 체액과 접촉하는 상황을 경험하였으며 환자 접촉 시에 대부분 마스크 또는 장갑 등 일부 보호장비만을 착용한 경우가 많았다(Table 1). 그러나 비말전파 주의에 준한 개인보호구를 착용했음에도 불구하고 2차 감염이 발생한 경우도 있었다[58,60]. SFTSV는 환자의 혈액뿐만 아니라 기도흡인액, 위액, 소변에서도 발견된다[61]. 사람 간의 직접적인 전파 경로는 환자의 혈액이나 체액 중의 바이러스가 접촉자의 피부의 상처, 결막, 구강이나 비강 점막을 통해 전파되는 것으로 추정되기 때문에 환자 접촉 시에는 장갑, 방수 가운을 착용하여 환자의 손상된 피부나 점막, 혈액, 분비물, 배설물과의 직접 접촉을 피해야 한다[11]. 하지만 사람 간의 2차 감염이 일어났던 사례에서 접촉자의 피부 상처가 있었던 경우는 흔하지 않아서 분변-경구 감염(fecal to oral transmission) 가능성이나 에어로졸을 통한 전파 가능성도 제기되고 있다[27,58,62]. 따라서 중증환자, 바이러스혈증 가능성이 있는 환자, 호흡기 질환이 동반된 환자, 체액이나 혈액의 누출이 있는 환자, 특히 응급실이나 중환자실에서 심폐소생술, 기도삽관, 기도분비물 흡인술 등 환자의 혈액을 포함하는 체액과 에어로졸에 노출될 가능성이 있는 경우에는 눈, 코, 입 등의 점막을 보호하기 위해 N95마스크, 안면보호구, 고글을 착용하고 몸통을 덮는 가운과 장갑을 착용하여 환자의 분비물과 접촉을 방지하는 조치가 필요하다. 현재 질병관리청 지침에 따른 SFTS의 의료기관 감염관리는 표준주의와 접촉주의 준수이며 특히 고농도의 바이러스를 배출할 것으로 예상되는 중증환자의 관리 시에는 철저한 비말 전파 지침 준수가 권고된다[63]. 공기매개전파에 대해 정확한 근거는 없으나 여러 경로로 전파될 수 있는 가능성이 있기 때문에 에어로졸이 발생할 수 있는 시술이나 처치 시에는 공기매개전파 주의에 준하는 보호 조치를 권장한다.
일반적으로 SFTS 환자를 반드시 격리하도록 권고하지는 않으나 표준 및 접촉주의가 필요하며, 환자의 혈액 및 체액의 노출이 예상되는 중증환자의 경우에는 의료진의 판단에 따라 비말격리 수준 이상의 격리가 필요할 수 있다[63]. 환자의 혈액에서 SFTSV가 검출되지 않을 때까지 적절한 격리 수준을 유지하고 특히 객혈과 신체 외부로 출혈을 동반한 중증 환자의 경우에는 음압병실 또는 1인실 음압병실에서 격리를 권장한다[1,63]. 접촉주의 지침에 따라 의학적으로 필요한 경우를 제외하고 환자의 이동과 이송을 가급적 제한하고 환자를 이송해야 하는 경우에는 이송 요원과 도착지의 의료종사자에게 주의사항을 알리고 개인보호구를 착용하도록 한다. 환자에게는 청결한 옷 및 가운을 착용할 수 있도록 하고 창상이나 손상된 피부는 개방되지 않도록 적절하게 소독하며 요실금이 있는 경우는 방수 기저귀 등을 이용한다. 출혈 가능성이 있는 시술이나 처치 시에는 비말매개 전파 이상 수준의 주의 지침을 마련하도록 하고 가능하면 마지막 일정으로 검사 및 시술 처치를 할 수 있도록 일정을 조정한다.
매개물에 의한 간접 전파나 에어로졸에 의한 공기매개 전파의 위험성도 꾸준히 제기되고 있어 치료 장비, 기구 및 환경관리에 대해서도 주의가 필요하다[27]. 중증 환자에게 사용한 청진기 등의 물품, 중증 환자가 입원했던 병실의 TV, 가구, 싱크, 문 손잡이 등에서도 SFTSV가 검출되어 매개물이나 오염된 환경에 의한 간접전파의 잠재적인 가능성이 있음을 주지해야 한다[64]. 환자가 사용한 장비, 기구 및 장치의 관리는 표준주의에 따르고 환자의 치료를 위해 필요한 물품은 접촉주의에 따라 가능한 일회용품과 환자 전용 의료용품(혈압계, 체온계 등)을 사용해야한다. 환자의 병실은 접촉주의에 준하여 다른 병실보다 더 자주 청소하고 소독해야 하며, 특히 환자가 자주 만지는 표면과 물건은 철저히 청소하고 소독한다. 심폐소생술 및 기관 흡인술, 기관 삽관술 등 환자를 직접적으로 접촉한 의료기관 종사자의 의류는 분리 세탁을 해야 한다. 환자에게 사용한 모든 장비와 의류, 환자의 혈액, 분비물 및 배설물로 오염된 기구, 물품과 환경에 대해도 반드시 적절한 환경 전반의 소독(terminal cleaning)과 세탁을 시행해야 한다. SFTSV는 산, 열, 에테르(ether), 데옥시콜산나트륨(sodium deoxycholate), 기타 일반적인 소독제 및 자외선 조사에 민감하며 빠르게 비활성화되므로 적절한 소독제를 선택하여 사용하면 된다[1]. 또한 최근 연구에서는 심자외선 발광다이오드(deep-ultraviolet light-emitting diode, DUV-LED) 조사에 의한 SFTSV의 신속한 불활성화를 보고하였는데 약 5초의 자외선 노출에도 바이러스 감염력이 99.8% 이상 감소되어 병원 내에서 기구 및 환경 소독에 DVU-LED도 활용할 수 있을 것으로 생각한다[65].
제주도 종합병원에 내원한 17명의 SFTS 환자들의 17명의 가족구성원에 대한 전수조사 연구에서 총 4명의 가족구성원의 무증상 SFTS 감염이 확인된 사례가 있었다[66]. SFTSV는 환자의 혈액, 체액, 분비물, 배설물 등에 의해 일상적인 접촉으로도 손상된 피부나 점막을 통해 2차 감염이 발생할 수 있기 때문에 집에서 환자 간병 시, 환자의 체액이나 토사물 등에 직접 접촉을 피하기 위하여 마스크, 비닐 장갑, 비닐 가운 등을 착용하는 것이 권장된다. 밀접 접촉자나 간병 중에 접촉된 사람은 즉시 비누와 물로 오염된 피부를 철저히 씻고 결막에 노출된 경우 충분한 물이나 생리식염수로 15분 이상 충분히 세척해야 한다. 접촉자에 대한 추가 역학 조사나 관리는 일반적으로 필요하지 않지만 환자 접촉 후 잠복기 동안은 발열 유무를 모니터링하는 것이 권장된다[1]. 위험 요인에 노출되었다면 마지막 노출일로부터 15일 동안 하루 2회씩 발열 감시를 포함한 추적관찰 시행하고 잠복기 내에 발열이 있다면 SFTS에 대한 진단 검사와 추가 역학 조사를 실시해야 한다.
SFTS 환자의 사망 후 사체를 수습하는 과정에서 시신으로부터 나오는 혈액 및 체액에 노출된 후 2차 감염이 발생한 사례는 국내외에서 이미 여러 건이 보고되었다[8, 9, 11, 13, 58]. 사체는 높은 농도의 SFTSV를 배출할 수 있으므로 사망한 환자의 사체를 다루는 의료종사자, 장례시술자 및 이송요원 등은 감염에 주의하여야 한다. 시신을 이송하거나 처리하는 경우 반드시 개인보호구(마스크, 장갑, 고글 또는 안면보호구, 방수가 되는 1회용 가운 등)를 착용한다. 시신으로부터 혈액 및 체액의 누출이 있는 경우 개인보호구를 철저하게 착용한 상태에서 의료용 솜 및 거즈 등을 이용하여 누출부위를 막으며, 누출이 심한 경우 시신을 방수용 시신백에 넣고 70% 이상의 알코올을 이용하여 표면을 소독한다. 담당 의료진은 장례시술자 및 사망환자 이송요원에게 시신의 혈액과 체액을 통한 감염 위험성이 있음을 알려야 한다[63].
SFTS는 주로 참진드기를 매개로 발생하는 열성 바이러스 질환으로 봄부터 가을까지 전국적으로 발생한다. 일부 환자군에서는 여전히 높은 치명률을 보이나 현재까지는 확립된 치료제나 백신이 없어 감염 예방과 전파 관리가 매우 중요하다. SFTSV는 진드기 교상을 통한 감염 뿐만 아니라 혈액, 체액, 호흡기 및 소화기 분비물 등을 통한 사람 간의 전파가 가능하다. 따라서 SFTS 환자 및 의심환자를 접촉할 때에는 철저한 표준주의, 접촉주의 지침 준수가 필요하며 중증 환자를 접촉할 경우에는 비말주의 지침을 준수해야 한다. 특히 중증 환자의 시술이나 처치 시 에어로졸이 발생할 가능성이 있다면 공기매개전파 주의에 해당하는 지침 준수가 필요하다. SFTS 환자를 접촉했던 의료종사자들의 2차 감염이 계속 보고되고 있고 SFTS는 검사 진행 후 결과 확인까지도 수 시간 이상이 소요되기 때문에 발열, 혈소판감소증, 백혈구감소증과 소화기증상을 동반한 환자에 대해서는 야외 활동력이나 동물 접촉력을 확인하고 SFTS가 의심된다면 선제적인 감염관리와 철저한 주의 지침 준수가 필요하다. 특히 중증 SFTS 환자나 사망 환자는 혈액이나 체액 중에 고농도의 바이러스가 유지되고 있을 가능성이 높아 의료진 뿐만 아니라 가족 및 접촉하는 모든 사람들은 2차 감염 예방을 위해 한층 강화된 주의와 감염관리가 요구된다.
REFERENCES
1. Liu Q, He B, Huang SY, Wei F, Zhu XQ. 2014; Severe fever with thrombocytopenia syndrome, an emerging tick-borne zoonosis. Lancet Infect Dis. 14:763–72. DOI: 10.1016/S1473-3099(14)70718-2. PMID: 24837566.

2. Yu XJ, Liang MF, Zhang SY, Liu Y, Li JD, Sun YL, et al. 2011; Fever with thrombocytopenia associated with a novel bunyavirus in China. N Engl J Med. 364:1523–32. DOI: 10.1056/NEJMoa1010095. PMID: 21410387. PMCID: PMC3113718.

3. Kim KH, Yi J, Kim G, Choi SJ, Jun KI, Kim NH, et al. 2013; Severe fever with thrombocytopenia syndrome, South Korea, 2012. Emerg Infect Dis. 19:1892–4. DOI: 10.3201/eid1911.130792. PMID: 24206586. PMCID: PMC3837670.

4. Takahashi T, Maeda K, Suzuki T, Ishido A, Shigeoka T, Tominaga T, et al. 2014; The first identification and retrospective study of Severe Fever with Thrombocytopenia Syndrome in Japan. J Infect Dis. 209:816–27. DOI: 10.1093/infdis/jit603. PMID: 24231186. PMCID: PMC7107388.

5. Peng SH, Yang SL, Tang SE, Wang TC, Hsu TC, Su CL, et al. 2020; Human case of severe fever with thrombocytopenia syndrome virus infection, Taiwan, 2019. Emerg Infect Dis. 26:1612–4. DOI: 10.3201/eid2607.200104. PMID: 32568054. PMCID: PMC7323535.

6. Tran XC, Yun Y, Van An L, Kim SH, Thao NTP, Man PKC, et al. 2019; Endemic severe fever with thrombocytopenia syndrome, Vietnam. Emerg Infect Dis. 25:1029–31. DOI: 10.3201/eid2505.181463. PMID: 31002059. PMCID: PMC6478219.

7. Silvas JA, Aguilar PV. 2017; The emergence of severe fever with thrombocytopenia syndrome virus. Am J Trop Med Hyg. 97:992–6. DOI: 10.4269/ajtmh.16-0967. PMID: 28820686. PMCID: PMC5637595.

8. Liu Y, Li Q, Hu W, Wu J, Wang Y, Mei L, et al. 2012; Person-to-person transmission of severe fever with thrombocytopenia syndrome virus. Vector Borne Zoonotic Dis. 12:156–60. DOI: 10.1089/vbz.2011.0758. PMID: 21955213.

9. Bao CJ, Guo XL, Qi X, Hu JL, Zhou MH, Varma JK, et al. 2011; A family cluster of infections by a newly recognized bunyavirus in eastern China, 2007: further evidence of person-to-person transmission. Clin Infect Dis. 53:1208–14. DOI: 10.1093/cid/cir732. PMID: 22028437.

10. Yoo JR, Heo ST, Park D, Kim H, Fukuma A, Fukushi S, et al. 2016; Family cluster analysis of severe fever with thrombocytopenia syndrome virus infection in Korea. Am J Trop Med Hyg. 95:1351–7. DOI: 10.4269/ajtmh.16-0527. PMID: 27928083. PMCID: PMC5154449.

11. Jiang XL, Zhang S, Jiang M, Bi ZQ, Liang MF, Ding SJ, et al. 2015; A cluster of person-to-person transmission cases caused by SFTS virus in Penglai, China. Clin Microbiol Infect. 21:274–9. DOI: 10.1016/j.cmi.2014.10.006. PMID: 25687766.

12. Jia B, Wu W, Huang R, Wang G, Song P, Li Y, et al. 2018; Characterization of clinical features and outcome for human-to-human transmitted severe fever with thrombocytopenia syndrome. Infect Dis (Lond). 50:601–8. DOI: 10.1080/23744235.2018.1449962. PMID: 29542384.

13. Jung IY, Choi W, Kim J, Wang E, Park SW, Lee WJ, et al. 2019; Nosocomial person-to-person transmission of severe fever with thrombocytopenia syndrome. Clin Microbiol Infect. 25:633.e1–4. DOI: 10.1016/j.cmi.2019.01.006. PMID: 30677496.

14. Zhu Y, Wu H, Gao J, Zhou X, Zhu R, Zhang C, et al. 2017; Two confirmed cases of severe fever with thrombocytopenia syndrome with pneumonia: implication for a family cluster in East China. BMC Infect Dis. 17:537. DOI: 10.1186/s12879-017-2645-9. PMID: 28774267. PMCID: PMC5541732.

15. Chen H, Hu K, Zou J, Xiao J. 2013; A cluster of cases of human-to-human transmission caused by severe fever with thrombocytopenia syndrome bunyavirus. Int J Infect Dis. 17:e206–8. DOI: 10.1016/j.ijid.2012.11.006. PMID: 23218674.

16. Tsuru M, Suzuki T, Murakami T, Matsui K, Maeda Y, Yoshikawa T, et al. 2021; Pathological characteristics of a patient with severe fever with thrombocytopenia syndrome (SFTS) infected with SFTS virus through a sick cat's bite. Viruses. 13:204. DOI: 10.3390/v13020204. PMID: 33572914. PMCID: PMC7912689.

17. Yamanaka A, Kirino Y, Fujimoto S, Ueda N, Himeji D, Miura M, et al. 2020; Direct transmission of severe fever with thrombocytopenia syndrome virus from domestic cat to veterinary personnel. Emerg Infect Dis. 26:2994–8. DOI: 10.3201/eid2612.191513. PMID: 33219655. PMCID: PMC7706950.

18. Matsuno K, Nonoue N, Noda A, Kasajima N, Noguchi K, Takano A, et al. 2018; Fatal tickborne phlebovirus infection in captive cheetahs, Japan. Emerg Infect Dis. 24:1726–9. DOI: 10.3201/eid2409.171667. PMID: 30124411. PMCID: PMC6106400.

19. Miyauchi A, Sada KE, Yamamoto H, Iriyoshi H, Touyama Y, Hashimoto D, et al. 2022; Suspected transmission of severe fever with thrombocytopenia syndrome virus from a cat to a veterinarian by a single contact: a case report. Viruses. 14:223. DOI: 10.3390/v14020223. PMID: 35215817. PMCID: PMC8874511.

20. International Committee on Taxonomy of Viruses (ICTV). Taxonomy history. https://talk.ictvonline.org/taxonomy/p/taxonomy-history?taxnode_id=202000166. (Updated on 30 March 2022).
21. Casel MA, Park SJ, Choi YK. 2021; Severe fever with thrombocytopenia syndrome virus: emerging novel phlebovirus and their control strategy. Exp Mol Med. 53:713–22. DOI: 10.1038/s12276-021-00610-1. PMID: 33953322. PMCID: PMC8178303.

22. Yun SM, Park SJ, Park SW, Choi W, Jeong HW, Choi YK, et al. 2017; Molecular genomic characterization of tick- and human-derived severe fever with thrombocytopenia syndrome virus isolates from South Korea. PLoS Negl Trop Dis. 11:e0005893. DOI: 10.1371/journal.pntd.0005893. PMID: 28937979. PMCID: PMC5627960.

23. Fu Y, Li S, Zhang Z, Man S, Li X, Zhang W, et al. 2016; Phylogeographic analysis of severe fever with thrombocytopenia syndrome virus from Zhoushan Islands, China: implication for transmission across the ocean. Sci Rep. 6:19563. DOI: 10.1038/srep19563. PMID: 26806841. PMCID: PMC4726339.

24. Yun SM, Lee WG, Ryou J, Yang SC, Park SW, Roh JY, et al. 2014; Severe fever with thrombocytopenia syndrome virus in ticks collected from humans, South Korea, 2013. Emerg Infect Dis. 20:1358–61. DOI: 10.3201/eid2008.131857. PMID: 25061851. PMCID: PMC4111194.

25. Luo LM, Zhao L, Wen HL, Zhang ZT, Liu JW, Fang LZ, et al. 2015; Haemaphysalis longicornis ticks as reservoir and vector of severe fever with thrombocytopenia syndrome virus in China. Emerg Infect Dis. 21:1770–6. DOI: 10.3201/eid2110.150126. PMID: 26402039. PMCID: PMC4593435.
26. Seo JW, Kim D, Yun N, Kim DM. 2021; Clinical update of severe fever with thrombocytopenia syndrome. Viruses. 13:1213. DOI: 10.3390/v13071213. PMID: 34201811. PMCID: PMC8310018.

27. Ye C, Qi R. 2021; Risk factors for person-to-person transmission of severe fever with thrombocytopenia syndrome. Infect Control Hosp Epidemiol. 42:582–5. DOI: 10.1017/ice.2020.1258. PMID: 33161921.

28. Song BG, Lee WG, Ju YR. 2017; Geographical distribution of Ixodid ticks in the Republic of Korea, 2015. Public Health Wkly Rep. 10:239–45.
29. Zhuang L, Sun Y, Cui XM, Tang F, Hu JG, Wang LY, et al. 2018; Transmission of severe fever with thrombocytopenia syndrome virus by Haemaphysalis longicornis ticks, China. Emerg Infect Dis. 24:868–71. DOI: 10.3201/eid2405.151435. PMID: 29664718. PMCID: PMC5938789.
30. Park SW, Song BG, Shin EH, Yun SM, Han MG, Park MY, et al. 2014; Prevalence of severe fever with thrombocytopenia syndrome virus in Haemaphysalis longicornis ticks in South Korea. Ticks Tick Borne Dis. 5:975–7. DOI: 10.1016/j.ttbdis.2014.07.020. PMID: 25164614.

31. Seo MG, Noh BE, Lee HS, Kim TK, Song BG, Lee HI. 2021; Nationwide temporal and geographical distribution of tick populations and phylogenetic analysis of severe fever with thrombocytopenia syndrome virus in ticks in Korea, 2020. Microorganisms. 9:1630. DOI: 10.3390/microorganisms9081630. PMID: 34442708. PMCID: PMC8399818.

32. Jo YS, Kang JG, Chae JB, Cho YK, Shin JH, Jheong WH, et al. 2019; Prevalence of severe fever with thrombocytopenia syndrome virus in ticks collected from national parks in Korea. Vector Borne Zoonotic Dis. 19:284–9. DOI: 10.1089/vbz.2018.2338. PMID: 30481146.

33. Yoo JR, Heo ST, Song SW, Bae SG, Lee S, Choi S, et al. 2020; Severe fever with thrombocytopenia syndrome virus in ticks and SFTS incidence in humans, South Korea. Emerg Infect Dis. 26:2292–4. DOI: 10.3201/eid2609.200065. PMID: 32818414. PMCID: PMC7454071.

34. Jiao Y, Zeng X, Guo X, Qi X, Zhang X, Shi Z, et al. 2012; Preparation and evaluation of recombinant severe fever with thrombocytopenia syndrome virus nucleocapsid protein for detection of total antibodies in human and animal sera by double-antigen sandwich enzyme-linked immunosorbent assay. J Clin Microbiol. 50:372–7. DOI: 10.1128/JCM.01319-11. PMID: 22135253. PMCID: PMC3264160.

35. Lee SH, Kim HJ, Lee MJ, Byun JW, Kim DY, Kim NH, et al. 2018; Prevalence of antibodies against severe fever with thrombocytopenia syndrome virus in shelter dogs in the Republic of Korea. Ticks Tick Borne Dis. 9:183–7. DOI: 10.1016/j.ttbdis.2017.09.002. PMID: 28899663.

36. Kimura T, Fukuma A, Shimojima M, Yamashita Y, Mizota F, Yamashita M, et al. 2018; Seroprevalence of severe fever with thrombocytopenia syndrome (SFTS) virus antibodies in humans and animals in Ehime prefecture, Japan, an endemic region of SFTS. J Infect Chemother. 24:802–6. DOI: 10.1016/j.jiac.2018.06.007. PMID: 30017796.

37. Li Z, Hu J, Bao C, Li P, Qi X, Qin Y, et al. 2014; Seroprevalence of antibodies against SFTS virus infection in farmers and animals, Jiangsu, China. J Clin Virol. 60:185–9. DOI: 10.1016/j.jcv.2014.03.020. PMID: 24793967.

38. Chen C, Li P, Li KF, Wang HL, Dai YX, Cheng X, et al. 2019; Animals as amplification hosts in the spread of severe fever with thrombocytopenia syndrome virus: a systematic review and meta-analysis. Int J Infect Dis. 79:77–84. DOI: 10.1016/j.ijid.2018.11.017. PMID: 30500443.

39. Yu KM, Yu MA, Park SJ, Kim YI, Robles NJ, Kwon HI, et al. 2018; Seroprevalence and genetic characterization of severe fever with thrombocytopenia syndrome virus in domestic goats in South Korea. Ticks Tick Borne Dis. 9:1202–6. DOI: 10.1016/j.ttbdis.2018.05.001. PMID: 29748119.

40. Kim KH, Ko MK, Kim N, Kim HH, Yi J. 2017; Seroprevalence of severe fever with thrombocytopenia syndrome in southeastern Korea, 2015. J Korean Med Sci. 32:29–32. Erratum in: J Korean Med Sci 2018;33:e225. DOI: 10.3346/jkms.2017.32.1.29. PMID: 27914128. PMCID: PMC5143294.

41. Han MA, Kim CM, Kim DM, Yun NR, Park SW, Han MG, et al. 2018; Seroprevalence of severe fever with thrombocytopenia syndrome virus antibodies in rural areas, South Korea. Emerg Infect Dis. 24:872–4. DOI: 10.3201/eid2405.152104. PMID: 29664384. PMCID: PMC5938763.

42. Yoo JR, Heo ST, Kim M, Song SW, Boo JW, Lee KH. 2019; Seroprevalence of severe fever with thrombocytopenia syndrome in the agricultural population of Jeju Island, Korea, 2015-2017. Infect Chemother. 51:337–44. DOI: 10.3947/ic.2019.51.4.337. PMID: 31668024. PMCID: PMC6940373.

43. Gai ZT, Zhang Y, Liang MF, Jin C, Zhang S, Zhu CB, et al. 2012; Clinical progress and risk factors for death in severe fever with thrombocytopenia syndrome patients. J Infect Dis. 206:1095–102. DOI: 10.1093/infdis/jis472. PMID: 22850122.

44. Guo CT, Lu QB, Ding SJ, Hu CY, Hu JG, Wo Y, et al. 2016; Epidemiological and clinical characteristics of severe fever with thrombocytopenia syndrome (SFTS) in China: an integrated data analysis. Epidemiol Infect. 144:1345–54. DOI: 10.1017/S0950268815002678. PMID: 26542444.

45. He Z, Wang B, Li Y, Du Y, Ma H, Li X, et al. 2020; Severe fever with thrombocytopenia syndrome: a systematic review and meta-analysis of epidemiology, clinical signs, routine laboratory diagnosis, risk factors, and outcomes. BMC Infect Dis. 20:575. DOI: 10.1186/s12879-020-05303-0. PMID: 32758175. PMCID: PMC7409422.

46. Li JC, Zhao J, Li H, Fang LQ, Liu W. 2022; Epidemiology, clinical characteristics, and treatment of severe fever with thrombocytopenia syndrome. Infect Med. 1:40–9. DOI: 10.1016/j.imj.2021.10.001.

47. Heo ST, Yoo JR, Lee KH, Ko KS. 2015; The first case of non-retrospective clinical identification of severe fever with thrombocytopenia syndrome patient in 2013 in South Korea. J Bacteriol Virol. 45:155–8. DOI: 10.4167/jbv.2015.45.2.155.

48. Kim YR, Yun Y, Bae SG, Park D, Kim S, Lee JM, et al. 2018; Severe fever with thrombocytopenia syndrome virus infection, South Korea, 2010. Emerg Infect Dis. 24:2103–5. DOI: 10.3201/eid2411.170756. PMID: 30334706. PMCID: PMC6199997.

49. Choi SJ, Park SW, Bae IG, Kim SH, Ryu SY, Kim HA, et al. 2016; Severe fever with thrombocytopenia syndrome in South Korea, 2013-2015. PLoS Negl Trop Dis. 10:e0005264. DOI: 10.1371/journal.pntd.0005264. PMID: 28033338. PMCID: PMC5226827.

50. Korea Disease Control. Infectious Disease Portal. https://www.kdca.go.kr/npt/biz/npp/ist/simple/simplePdStatsMain.do#. (Updated on 30 March 2022).
51. Jeong SJ, Hwang JH, Kim HS, Kwon GY. 2021; Epidemiological characteristics of patients with Severe Fever with Thrombocytopenia Syndrome (SFTS) from 2013 to 2020. Public Health Wkly Rep. 14:2561–72.
52. Yoo JR, Heo ST. 2018; Strategies against severe fever with thrombocytopenia syndrome increasing in Korea. Korean J Blood Transfus. 29:117–29. DOI: 10.17945/kjbt.2018.29.2.117.

53. Sun J, Lu L, Yang J, Liu K, Wu H, Liu Q. 2018; Association between severe fever with thrombocytopenia syndrome incidence and ambient temperature. Am J Trop Med Hyg. 98:1478–83. DOI: 10.4269/ajtmh.17-0991. PMID: 29557340. PMCID: PMC5953393.

54. Cho G, Lee S, Lee H. 2021; Estimating severe fever with thrombocytopenia syndrome transmission using machine learning methods in South Korea. Sci Rep. 11:21831. DOI: 10.1038/s41598-021-01361-9. PMID: 34750465. PMCID: PMC8575988.

55. He F, Zheng X, Zhang Z. 2021; Clinical features of severe fever with thrombocytopenia syndrome and analysis of risk factors for mortality. BMC Infect Dis. 21:1253. DOI: 10.1186/s12879-021-06946-3. PMID: 34906106. PMCID: PMC8669668.

56. Kwon JS, Jin S, Kim JY, Ra SH, Kim T, Park SY, et al. 2021; Viral and immunologic factors associated with fatal outcome of patients with severe fever with thrombocytopenia syndrome in Korea. Viruses. 13:2351. DOI: 10.3390/v13122351. PMID: 34960620. PMCID: PMC8703577.

57. Kim WY, Choi W, Park SW, Wang EB, Lee WJ, Jee Y, et al. 2015; Nosocomial transmission of severe fever with thrombocytopenia syndrome in Korea. Clin Infect Dis. 60:1681–3. DOI: 10.1093/cid/civ128. PMID: 25694652.

58. Moon J, Lee H, Jeon JH, Kwon Y, Kim H, Wang EB, et al. 2019; Aerosol transmission of severe fever with thrombocytopenia syndrome virus during resuscitation. Infect Control Hosp Epidemiol. 40:238–41. Erratum in: Infect Control Hosp Epidemiol 2019;40:620. DOI: 10.1017/ice.2018.330. PMID: 30565531.

59. Yoo JR, Choi JH, Kim YR, Lee KH, Heo ST. 2019; Occupational risk of severe fever with thrombocytopenia syndrome in healthcare workers. Open Forum Infect Dis. 6:ofz210. DOI: 10.1093/ofid/ofz210. PMID: 31139678. PMCID: PMC6527088.

60. Bae S, Chang HH, Kim SW, Kim Y, Wang E, Kim CK, et al. 2022; Nosocomial outbreak of severe fever with thrombocytopenia syndrome among healthcare workers in a single hospital in Daegu, Korea. Int J Infect Dis. 119:95–101. DOI: 10.1016/j.ijid.2022.03.048. PMID: 35358725.

61. Jeong EJ, Song JY, Lim CS, Lee I, Park MS, Choi MJ, et al. 2016; Viral shedding from diverse body fluids in a patient with severe fever with thrombocytopenia syndrome. J Clin Virol. 80:33–5. DOI: 10.1016/j.jcv.2016.04.018. PMID: 27135388.

62. Gong Z, Gu S, Zhang Y, Sun J, Wu X, Ling F, et al. 2015; Probable aerosol transmission of severe fever with thrombocytopenia syndrome virus in southeastern China. Clin Microbiol Infect. 21:1115–20. DOI: 10.1016/j.cmi.2015.07.024. PMID: 26255811.

63. Korea Disease Control. 2022 Guideline for infection control of tick-borne and rodent borne disease. https://kdca.go.kr/board/board.es?mid=a20507020000&bid=0019. (Updated on 15 April 2022).
64. Ryu BH, Kim JY, Kim T, Kim MC, Kim MJ, Chong YP, et al. 2018; Extensive severe fever with thrombocytopenia syndrome virus contamination in surrounding environment in patient rooms. Clin Microbiol Infect. 24:911.e1–4. DOI: 10.1016/j.cmi.2018.01.005. PMID: 29355730.

65. Kaneko C, Saito A, Inagaki H, Sugiyama H, Mazimpaka E, Fujimoto S, et al. 2022; Rapid inactivation of Dabie bandavirus (SFTSV) by irradiation with deep-ultraviolet light-emitting diode. J Med Virol. 94:3438–41. DOI: 10.1002/jmv.27698. PMID: 35246855.
66. Yoo JR, Lee KH, Heo ST. 2018; Surveillance results for family members of patients with severe fever with thrombocytopenia syndrome. Zoonoses Public Health. 65:903–7. DOI: 10.1111/zph.12481. PMID: 29862661.

67. Reece LM, Beasley DW, Milligan GN, Sarathy VV, Barrett AD. 2018; Current status of Severe Fever with Thrombocytopenia Syndrome vaccine development. Curr Opin Virol. 29:72–8. DOI: 10.1016/j.coviro.2018.03.005. PMID: 29642053.

68. Robles NJC, Han HJ, Park SJ, Choi YK. 2018; Epidemiology of severe fever and thrombocytopenia syndrome virus infection and the need for therapeutics for the prevention. Clin Exp Vaccine Res. 7:43–50. DOI: 10.7774/cevr.2018.7.1.43. PMID: 29399579. PMCID: PMC5795044.

69. Kwak JE, Kim YI, Park SJ, Yu MA, Kwon HI, Eo S, et al. 2019; Development of a SFTSV DNA vaccine that confers complete protection against lethal infection in ferrets. Nat Commun. 10:3836. DOI: 10.1038/s41467-019-11815-4. PMID: 31444366. PMCID: PMC6707330.

Fig. 1
Annual number of cases and case fatality of severe fever with thrombocytopenia syndrome in Korea from 2013 to 2021.
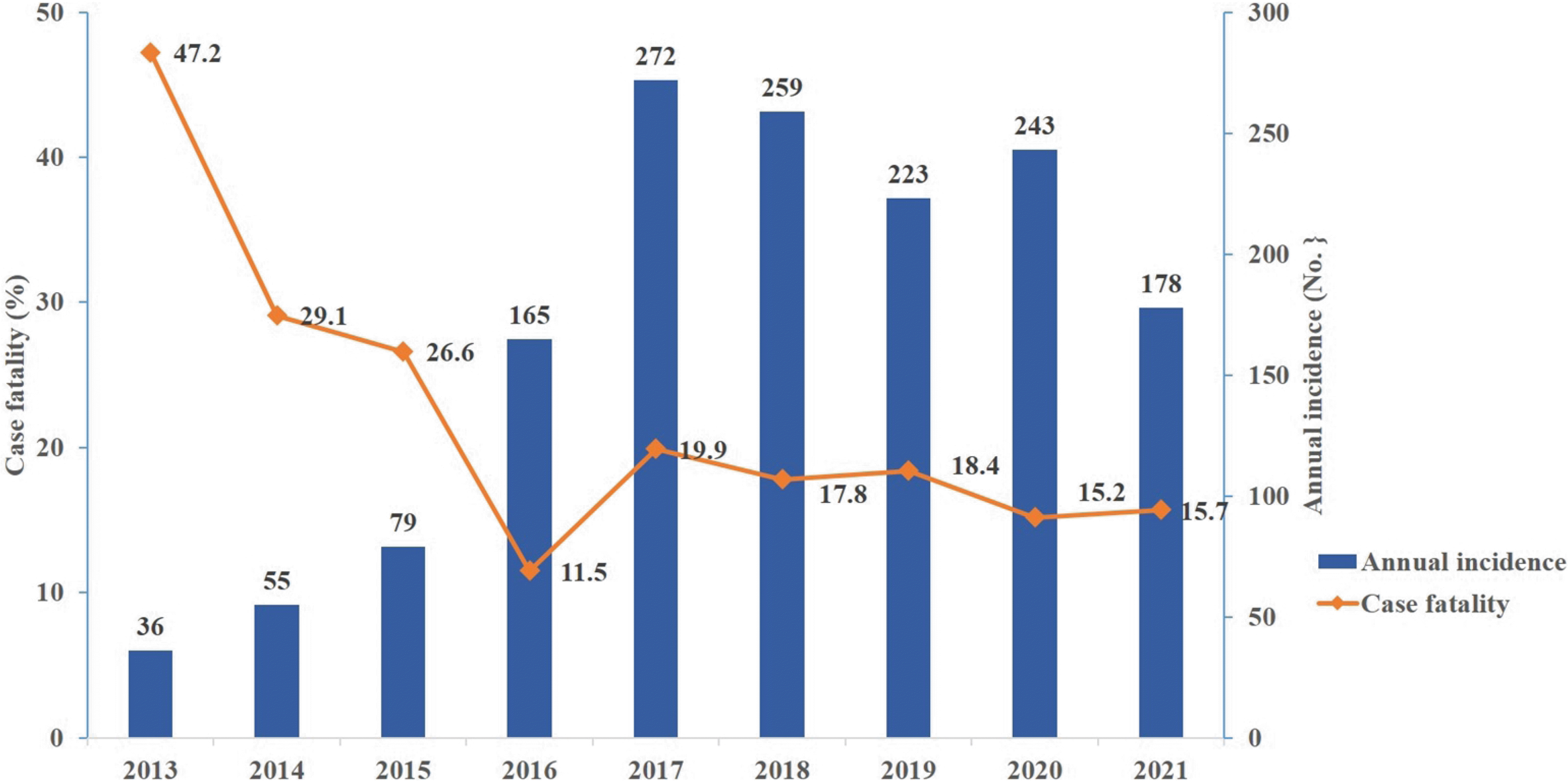
Fig. 2
Cumulative number and case fatality of patients with severe fever with thrombocytopenia syndrome according to the age groups in Korea from 2013 to 2020.
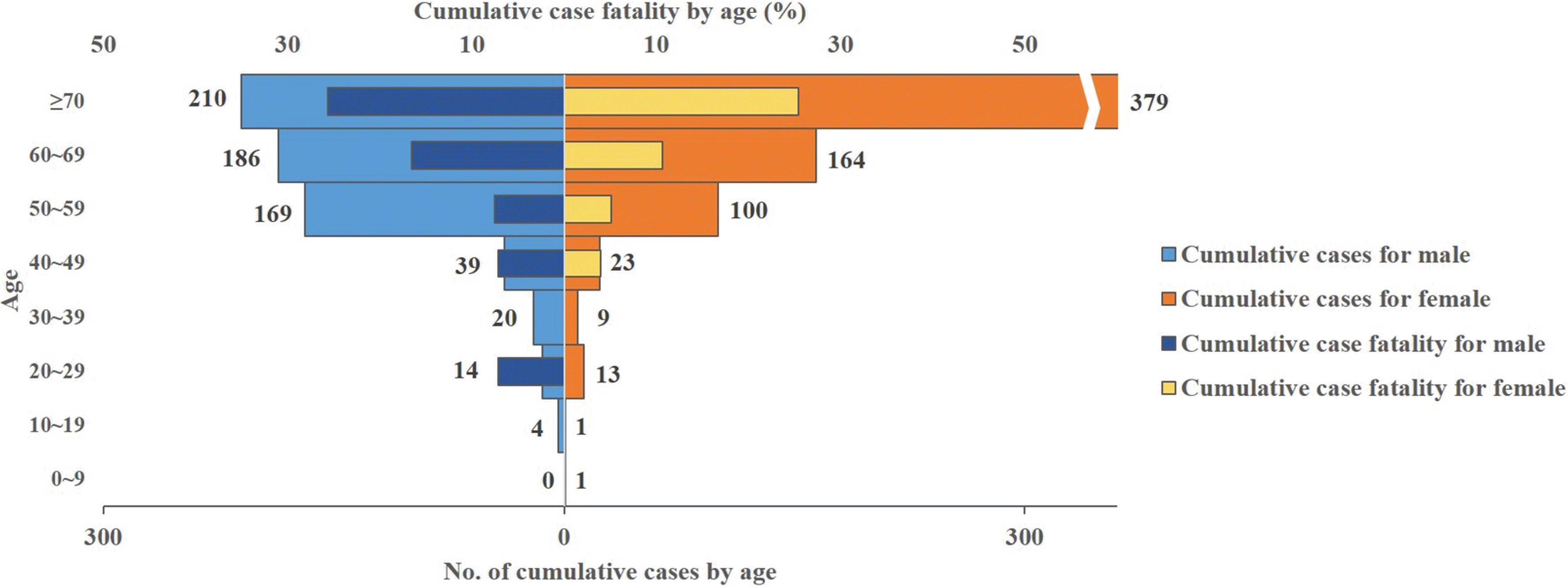
Fig. 3
Average annual incidence of indigenous severe fever with thrombocytopenia syndrome cases in Korea from 2013 to 2021 (per 100,000 population).
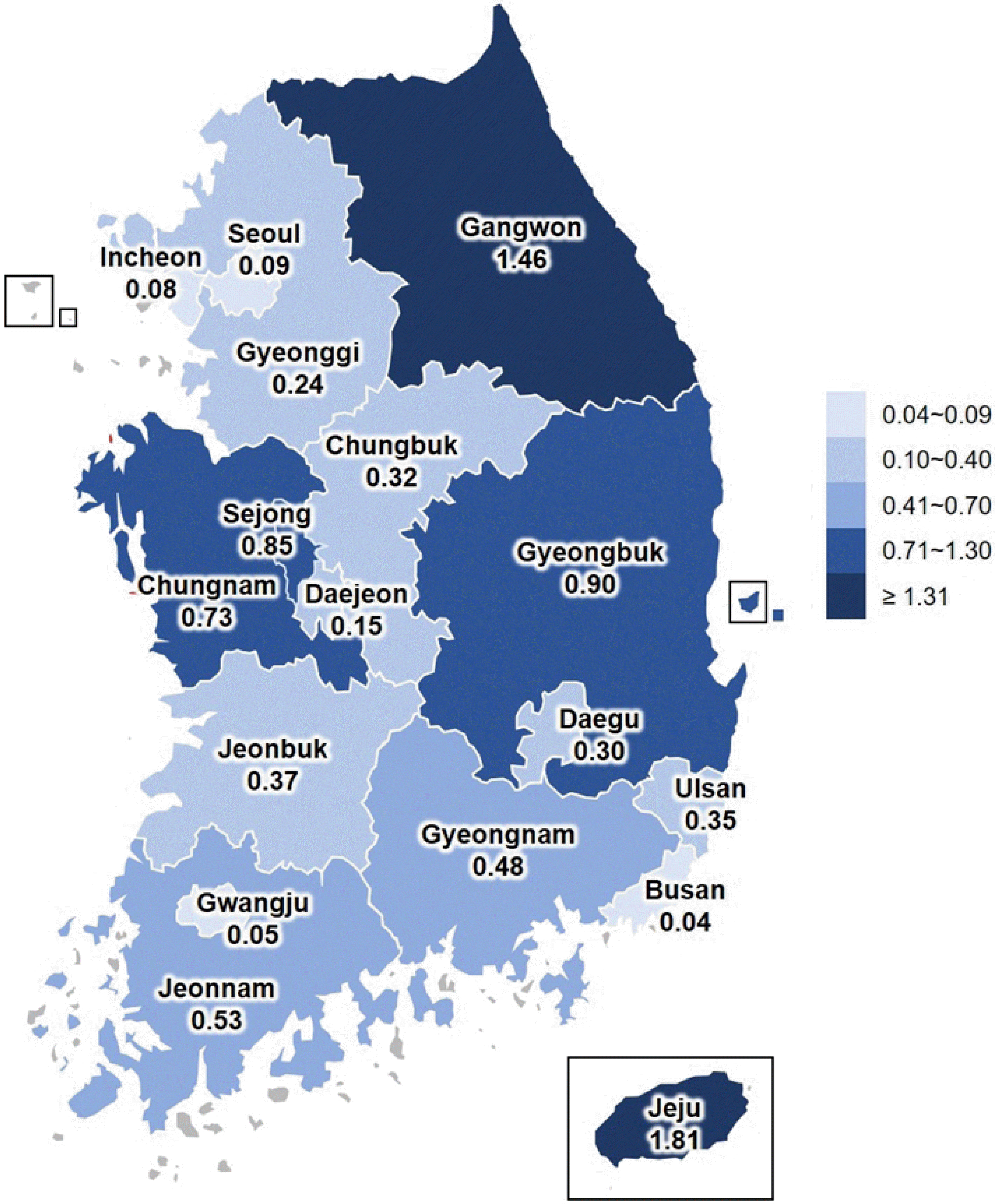
Fig. 4
Monthly incidence of patients with severe fever with thrombocytopenia syndrome in Korea from 2013 to 2021.
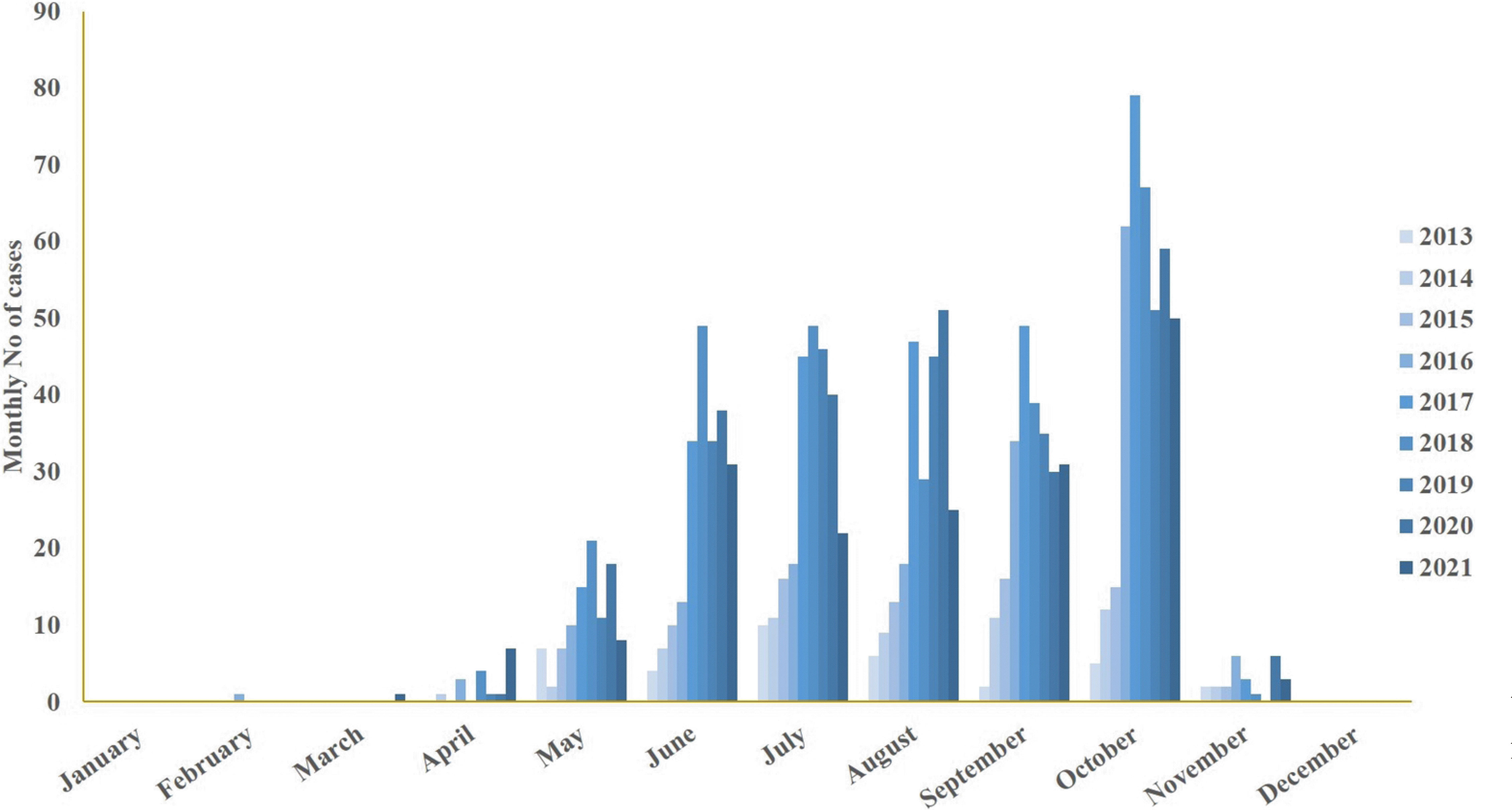
Table 1
Cases on the nosocomial infection of severe fever with thrombocytopenia in Korea
| Cases | Outcome of index patient | No. of infected HCW | Total No. of exposure HCW | From contact to symptom onset (days) | Index patient’s viral load | Hospital events | No. of wearing PPE among the infected HCW |
|---|---|---|---|---|---|---|---|
| Kim et al. [57] | Death | 4 | 7 | 5-12 | 3.7×108 copies/mL | CPR |
Mask: 4 Gloves: 2 Facial shield/goggles: 0 Gown: N/A |
| Jung et al. [13] | Death | 5 | 15 | 8-11 | N/A | CPR, HD catheter insertion, endotracheal suction, cleansing the corpse |
Mask: 0 Gloves: 3 Facial shield/goggles: 0 Gown: N/A |
| Moon et al. [58] | Death | 2 | 14 | 10 | 1.9×106 copies/mL | Endotracheal intubation, clean the deceased |
Mask: 1 Gloves: 1 Facial shield/goggles: N/A Gown: 1 |
| Yoo et al. [59] | Death | 2 | 4 | N/A | N/A | CVC insertion, lumbar puncture | N/A |
| Bae et al. [60] | Death | 17 | 59 | N/A | N/A | CPR, cleaning up around the patient’s bed |
Mask: 16 Gloves: 13 Facial shield/goggles: N/A Apron: 2 |




 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download