Abstract
Background and Objectives
Microtia is a congenital deformity where the pinna and middle ear structures are underdeveloped. Auricular reconstruction in microtia is one of the most difficult surgeries in otolaryngology due to the complex three-dimensional structure of the auricle. This study investigated the post-operative results in total auricular reconstruction performed by otologic surgeons in a single institution.
Subjects and Method
We analyzed data from 27 microtia patients who underwent auricular reconstruction in our institution from 2011 to 2019. The post-operative results were evaluated in terms of the shape of the auricle, the symmetry of the ear, and the degree of auriculocephalic sulcus stricture. The type and frequency of post-operative complications associated with the reconstruction were also evaluated.
Results
Of the 24 patients, the shape of the auricle was good in 11 (40.7%), moderate in 11 (40.7%), and poor in 5 (18.6%) patients. The symmetry of the ear size was symmetric in 24 (88.9%) and asymmetric in 3 (11.1%) patients. The degree of auriculocephalic sulcus stricture was good in 11 (40.7%), partial stricture in 12 (44.4%), and severe stricture in 4 (14.8%) patients. Postoperative complications included skin necrosis, suture material exposure, and wound infection with cartilage deformation.
Conclusion
Total auricular reconstruction is a complex and sophisticated operation utilizing either autologous rib cartilage or artificial implant material. Considering that microtia is often accompanied by ear canal stenosis and hearing impairment, otolaryngologists should be more interested in the field of auricular reconstruction.
소이증(microtia)은 이개가 불완전하게 발달하여 작거나 흔적으로 남는 선천성 기형으로 대부분 중이의 기형을 동반하며, 0.01%-0.2%의 발생율을 보인다[1-3]. 일측성이 더 흔하고 여성보다 남성에서 더 흔하며(2.5:1.0) 두개안면기형과 50% 이상에서 연관되어 있는 것으로 알려져 있다[1,2]. 선천성 이개기형에 대한 분류는 Marx가 1926년 처음으로 소이증의 분류를 제시하였으며, 이후에 1977년 Tanzer에 의해 널리 사용되는 분류법이 정립되었고 Weerda와 Siegert가 1988년 이 분류법들을 치료적 관점에서 1-4단계로 다시 정리하여 분류하였다[1]. 소이증은 Weerda와 Siegert가 치료적 관점에서 분류한 이개 기형 중 2, 3단계에 해당하며[1], Nagata [4]는 이를 이개강형(concha type), 소이개강형(small concha type), 이수형(lobule type)의 세 가지 형태로 분류하였다. 이개강형 소이증은 이개의 일부 상부구조와 이수, 이개강, 이주, 주간절흔 및 외이도가 존재하는 기형이고, 소이개강형은 일부 상부구조와 이수 및 작은 이개강만 존재하는 경우, 그리고 이수형은 상부 구조가 거의 형태만 남아있고 정상에 가까운 이수가 존재하는 경우이다. 이 외에도 낮은 두발선을 동반하며 이개의 형태가 전무한 무이증(anotia)이 있다. 현재 International Consensus Recommendations에 따르면 Nagata 분류법의 이개강형은 grade I-II에 해당하며, 소이개강형은 grade II, 이수형은 grade III에 해당하고, 무이증은 grade IV에 해당한다[5].
소이증의 재건에는 대개 6-9번째 자가늑골연골이 널리 사용된다. 자가늑골연골을 이용한 이개재건술은 Brent [6,7]가 4단계로 재건을 시행하는 술식을 고안하였으며, 이후 Nagata [4,8]가 이를 2단계로 압축한 술식을 창안하여 현재 주로 사용되고 있다. 이후에 Nagata [4]의 술식은 Weerda, Siegert, Firmin 등에 의해 이개 기틀의 제작, 피부피판의 디자인 및 이개거상 방법이 조금씩 변형되어 사용되고 있다. 자가늑골연골 외에 인공삽입물은 메드포어(MEDPOR, Stryker, Kalamazoo, MI, USA)가 주로 사용되며, 이를 사용할 경우는 술식과 수술 시 기가 자가늑골연골을 이용할 때와는 차이가 있다. 자가늑골연골을 이용할 경우 이개골조 제작이 가능할 만큼 늑골 연골이 충분히 성장하고, 이개가 성인의 크기에 가깝게 되는 8-10세 이후에 수술을 시행하고, 메드포어 등의 인공재료를 이용할 경우 대개 4-5세 이후에 수술을 시행할 수 있다[9].
현재 국내에서의 이개재건술은 대부분 성형외과에서 시행하고 있으며 이비인후과에서 시행되는 경우는 매우 드물다. 외이의 성형만큼이나 술후 청력재활이 소이증의 치료에 중요하다는 점을 고려했을 때 이개재건술은 이비인후과에서 더 많은 관심을 가져야 할 영역이다. 본 연구에서는 본원에서 시행한 전이개재건술의 결과와 어려움을 조사하여 이비인후과에서 시행하는 귀 성형 및 재건의 활성화에 도움이 되고자 하였다.
2011-2019년까지 연세대학교 세브란스병원에서 전이개재건술을 시행받은 총 27명의 소이증 환자의 수술 결과를 분석하였으며, 이 중 17명이 남성, 10명이 여성이고 연령은 9-63세였다. 소이증의 분류상 13명이 이수형(grade III), 11명이 이개강형(grade I), 2명이 무이증(grade IV)의 형태를 보였고 1명은 타병원에서 수술 후 외형에 대한 불만족으로 재수술을 시행하였으며, 이수형 소이증과 무이증 각 1예에서 편측안면왜소증(hemifacial microsomia)과 낮은 두발선이 동반되어 있었다.
이 연구는 세브란스병원 Institutional Review Board의 승인을 받은 후 진행되었다(IRB No. 4-2022-0074).
재건술의 재료로 자가늑골연골이 26명에서 사용되었으며, 1명의 환자에서는 메드포어를 사용하여 전체이개를 재건하였고, 1명의 환자에서는 메드포어를 2차 재수술 시 이개거상에 사용하였다. 자가늑골연골을 사용하는 외이재건에는 Weerda와 Siegert에 의해 변형된 Nagata 술식을 이용하였으며, 늑골연골 채취는 흉부외과 전문의에 의해 진행되었다. 술식은 이수를 회전시키고 이개기틀을 피하에 삽입하는 1단계 수술을 먼저 시행 후 약 6개월 뒤 이개를 거상시키는 2단계 수술로 나누어 시행되었다. 1단계 수술에서는 이수를 회전시킬 위치를 고려하여 Z형 피부절개를 이수와 유양돌기 상부 쪽으로 가하고, 이를 통하여 이개기틀이 삽입될 위치에 피부피판을 거상하여 피하 주머니를 형성하였다. 이 때 피부피판에는 지방유경(fat pedicle)을 피부의 혈류순환을 위하여 일부 부착한 상태로 남겨두었다. 절개한 이수는 후방으로 회전시켜 봉합하였다. 이후 7-8번 늑골연골을 이용하여 이개기틀의 본체 및 대이륜, 대이륜각, 대주 및 이주를 조각하였으며, 이륜은 9번 늑골연골을 이용하여 제작하여, 각 조각된 세부구조물들은 의료용 5-0 철사로 연결하였다(Fig. 1). 6번 연골은 2차 술식에서 이개거상 시 받침으로 사용하기 위해 늑골을 채취한 흉부의 피하에 삽입하였다. 2차 수술은 1차 수술 후 6개월 가량 지난 뒤 시행하였다(Fig. 2). 형성된 이개의 상부와 후부 1 cm 후방에 절개선을 디자인하고, 이륜 직후방까지 부분 피부편(thick split thickness skin flap)을 모낭을 보존하며 거상하고, 이후부터는 이개기틀 후면의 연조직을 손상시키지 않으면서 이개강 부위까지 이개기틀을 거상하였다. 거상된 이개기틀 후면에 1단계에서 흉부에 삽입해 두었던 6번 연골을 조각하여 연골편을 만든 뒤 5-0 철사로 고정하고, 연골편은 후두부근막피판을 거상하여 덮은 후 이개후면에 부분층 피부이식을 시행하였다[10,11]. 낮은 두발선을 동반한 편측안면왜소증 증례 및 메드포어를 사용한 증례에서는 이수를 후방전위 시키고, 이개가 재건될 위치 후면의 5 cm 가량의 피부피판을 모낭을 보존하며 이개기틀이 삽입될 후방까지 부분층으로 거상하고 이후 전방으로는 피부피판을 전층으로 거상하였다. 늑골연골을 이용하여 이개기틀을 제작하고 이개기틀 후면부에 이개거상에 사용하는 늑골연골편을 부착한 뒤 측두두정근막피판(temporoparietal fascia flap)을 거상하여 이를 덮어준 후 거상된 피부피판으로 이개후면을 덮어주는 단일단계 전이개재건술을 시행하였다(Fig. 3). 메드포어를 이용하는 경우는 위의 술식에서 늑골연골을 이용한 이개기틀 대신 메드포어를 삽입 후 피판은 동일한 술식으로 덮어주었다. 재수술을 시행한 경우는 기존의 이개기틀을 제거하고, 추가로 채취한 늑골연골을 이용해 새로운 이개기틀을 제작하여 삽입한 뒤, 측두두정근막피판으로 이개기틀을 덮은 뒤 모자라는 피부는 부분 피부이식을 시행하였다. 한 환자에서는 이개거상에 사용할 늑골연골편이 부족하여 이개 후면에 늑골연골편 대신 메드포어편을 삽입한 뒤 측두두정근막피판을 이용하여 이를 덮어준 뒤 피부이식을 시행하였다.
이개의 크기는 성인을 기준으로 길이 5.5-6.5 cm, 폭 3-4.5 cm 정도로 폭이 길이의 50%-60% 정도이다 [12]. 이개의 높이는 상단은 윗눈썹 외측, 하단은 비하점(subnasale)이 기준이 될 수 있으며, 이륜각(crus of helix)의 이상기점(otobasion superius)은 측면 안각(lateral canthus)의 높이이다. 외이의 장축은 머리의 수직축을 기준으로 10°-25° 뒤로 기울어 콧등과 평행인 것이 이상적이며[13], 이개의 돌출 정도는 두개이개각(cephaloauricular angle) 혹은 두개이개간격(cephaloauricular distance)으로 평가할 수 있다. 현재까지 소이증의 재건수술의 결과를 평가하는 국제적인 기준은 마련되어 있지 않으며, 많은 저자들이 환자의 주관적인 평가나 수술 후 각자의 기준에 따라 수술 결과를 보고하고 있으며, 이러한 기준도 대부분의 논문에서 명확히 기술되어 있지 않다[10,14-16]. 따라서 본 저자들은 상기에서 기술된 이개의 해부학적인 기준을 토대로, 수술 결과는 이개의 형태, 양측 귀의 대칭성, 이개두부 고랑(auriculocephalic sulcus)의 협착 정도에 따라서 각각 분류하였다. 이개의 모양은 대이륜, 대이륜각, 주상와, 삼각와 및 이개강, 이갑개정의 능과 골이 명확하고 뚜렷하게 형성된 경우는 양호(good), 상기의 구조가 일부는 뚜렷하지만 일부는 뚜렷하지 않거나, 형성은 되었지만 능과 골의 형태가 불완전 한경우는 보통(moderate), 상기의 구조가 뚜렷하게 형성되지 않고 경계가 명확하지 않은 경우는 불량(poor)의 3가지로 분류하였으며(Fig. 4), 대칭성은 좌우 이개의 크기가 상하경계선 3 mm 이하로 차이가 날 경우 대칭, 이보다 크게 차이가 날 경우 비대칭으로 분류하였다(Fig. 5). 이개두부고랑은 후면에서 보았을 때 이개 중앙부의 두부에서 이륜면까지의 높이가 1.5-2.0 cm일 경우 양호(good), 1 cm 이상 1.5 cm 미만의 경우 부분 협착(partial stricture), 1 cm 미만의 경우 심한 협착 (severe stricture)으로 평가하였다(Fig. 6). 이외에 수술 후 발생한 합병증의 종류 및 빈도를 분석하였다.
시간에 따른 수술 숙련도를 분석하기 위하여, 수술에 소요된 시간을 1차 수술, 2차 수술, 단일단계로 계획된 수술별로 분석을 하였다. 수술 소요 시간은 의무기록을 분석하여, 수술 시작 시간부터 수술 종료 시간을 증례별로 분석하였으며, 2개년씩 묶어 평균 소요 시간을 계산하였다. 단 2017년 이후(19증례 이후)로는 어느 정도 숙련도에 올랐다고 판단되어, 한가지로 묶어 평균을 산출하였다. 각 그룹별 수술 소요 시간의 차이는 one-way repeated measures analysis of variance를 이용하여 분석하였다. 단일단계로 시행된 수술은 4증례밖에 없어 통계 분석에는 포함하지 않았다.
이개 형태는 총 27명의 환자 중 11명(40.7%)이 양호, 11명(40.7%)이 보통, 5명(18.6%)이 불량 소견을 보였다. 이개 크기의 대칭성은 24명(88.9%)에서 대칭, 3명(11.1%)에서 비대칭이었다. 이개두부고랑은 11명(40.7%)에서 양호, 12명(44.4%)에서 부분적 협착, 4명(14.8%)에서 심한 협착 양상을 보였다.
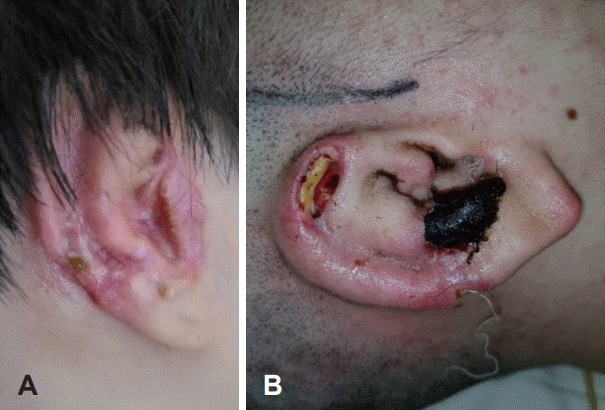
수술 후 합병증으로 8명(29.6%)에서 피부 괴사가 나타났다. 이 중 5명(18.5%)에서는 드레싱을 통하여 괴사부위가 호전되었으나(Fig. 7A), 3명(11.1%)에서는 회복되지 않고 장기간의 연골 노출이 초래되어 국소피부피판술 혹은 측두두정근막과 부분층 피부이식을 시행하여 치료하였다(Fig. 7B). 수술용 철사의 노출은 1명(3.7%)에서 나타났으나 철사를 제거 후 문제없이 치유가 되었고, 수술 부위 감염 및 연골 변형은 1명(3.7%)에서 나타나 재수술을 시행하였다. 모든 합병증은 자가늑골연골을 사용한 환자에서 나타났으며, 메드포어를 이용하여 재건한 예에서는 술후 2년간 합병증의 발생은 없었다.
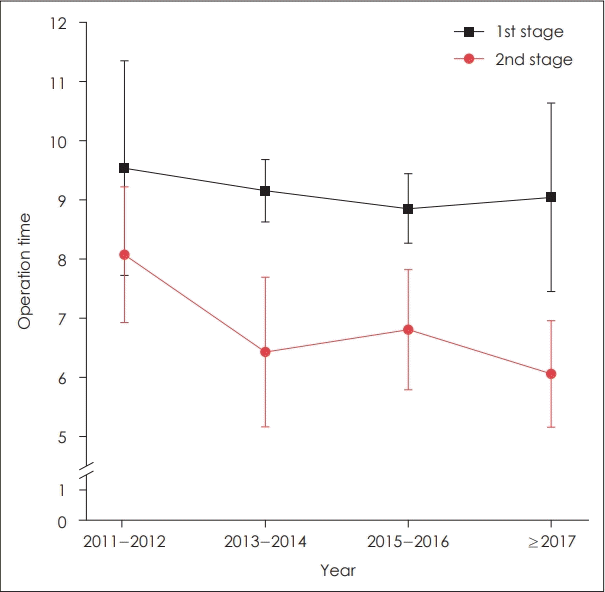
시간에 따른 수술의 숙련도의 향상 정도를 보기 위하여 수술에 소요된 시간을 연도별로 파악하였을 때, 1차 수술은 첫 2년(2011-2012년)은 9.5±1.8시간이 소요되었고, 2017년 이후는 9.0±1.6시간이 소요되어, 시간 경과에 따른 수술 소요 시간은 차이가 없었다(p>0.05) (Fig. 8). 반면 2차 수술은 첫 2년은 8.1±1.2시간에서 2017년 이후는 6.1±0.9시간으로 통계적으로는 차이가 없었지만 1차 수술에 비해 더 감소하는 경향을 보였다(p=0.062) (Fig. 8). 단일단계로 계획되어 시행된 수술은 평균 11.5±2.1시간이었다.
현재까지의 이개재건술의 가장 보편적인 술식은 자가연골을 이용한 이개재건술이다. 자가늑골연골은 수술 시 다듬기가 쉽고, 이물반응이 적어 오랜 기간 동안 널리 사용되어 장기적인 안정성이 확립되었으며, 경우에 따라 측두두정근막 대신 후두부근막피판 사용이 가능하여 피부 절개선이 작아도 되는 장점이 있다. 단점으로는 늑골연골 채취과정에서 발생하는 흉부의 상처 및 결손, 연골 조각 술기가 어려워 술자에 따라 다양한 결과가 나올 수 있다는 점이 있다. 이에 반면 대표적 인공삽입물인 메드포어는 자가늑골연골의 채취 및 이개의 모양을 다듬지 않아도 되어 영구적인 흉터 및 결손이 남지 않고 시간이 크게 절약되는 장점이 있다. 그러나 측두두정피판으로 이식물을 감싸 이물반응을 줄여야 하기 때문에 측두 두피에 큰 절개가 들어가고, 이물반응 및 이식물의 외부노출이 비교적 더 많이 일어나며, 외상에도 더 취약하다는 단점이 있다.
자가연골을 이용한 이개재건술의 술식으로는 Brent와 Nagata의 술식이 가장 널리 쓰인다. Brent 술식에 비하여 Nagata 술식의 경우 미용적인 장점이 있으며, 보다 더 적은 단계를 필요로 하기 때문에, 본원 환자들의 경우 변형된 Nagata 술식을 사용하였다.
소이증 환자의 수술의 시기를 결정하는 것은 매우 중요하다. 메드포어 등의 인공물질을 사용하여 수술을 하는 경우, 수술 재료에 제약을 많이 받지 않기 때문에 5-6세에 이후에는 시행하여도 문제가 없다는 보고들이 있지만[17], 늑골연골을 사용하여 수술을 하는 경우 너무 이른 시기에 수술을 하게 되면 충분한 양의 늑골연골을 채취하지 못할 수 있어 더 늦은 시기에 수술하는 것이 좋다. 자가연골을 이용한 방법에 있어 최적의 수술 시기에 대하여는 여전히 여러 술자마다 논쟁이 있으며, Brent [6]의 경우 7세경, Nagata [4]의 경우 10세경 시행하는 것을 권하고 있으며, 일부의 경우 12세경 시행하는 것을 권하기도 한다[18]. 또한, 늑골연골의 크기를 평가하여 수술의 시기를 결정하고자 하는 시도도 존재한다[19]. International Consensus Recommendations에 따르면, 충분한 양의 늑골연골을 채취할 수 있는 6세 이상에서 수술을 권하나, 사춘기인 12-15세에는 늑골연골의 빠른 성장으로 인해 속이 비어 있는 경우가 많아 9세경 시행하는 것을 권하고 있다[5]. 또한, 성인이 되었을 경우 늑골연골의 석회화(calcification)가 진행되어 연골의 탄성도가 감소하여 수술에 제약이 있을 수 있음을 고려하여야 한다고 하였다[5]. 연골의 크기뿐 아니라, 수술 시기와 방법을 결정함에 있어 환자의 사회심리적, 정신적 스트레스를 개별적으로 고려해야 하며, 보호자의 성향도 종합적으로 고려하여 신중히 결정하여야 한다. 가령, 환자와 보호자가 하루라도 빨리 수술을 원하면서, 여러 번에 걸친 수술을 견뎌낼 수 없다면 인공물질을 사용하여 수술하는 것을 고려해야 하며, 환자 및 보호자가 정서적으로 안정적이며 여러 단계의 수술을 견딜 수 있다면, 10-12세경까지 수술 시기를 늦추어 환자의 치료 순응도를 높이고, 만일에 발생할 수 있는 성장 후 가슴부위의 변형이 생기는 등의 합병증의 발생 확률을 최대한 낮추는 전략을 취할 수 있을 것이다.
이개재건술의 가장 중요한 최종 목표는 술자와 환자 모두 만족할 수 있는 미용적 귀를 만드는 것일 것이다. 평가자와 환자의 주관이 개입된다는 점이 있으나 미용적 불만족은, 술자에 따라 전체의 약 4.8%-21%까지 다양하게 보고된다[20]. 자가조직을 이용한 이개재건술 중 가장 어려운 부분 중 하나로는 1단계 수술 시 늑골연골을 이용하여 이개기틀을 조각하는 과정으로[21], 많은 경험을 필요로 하며, 이를 위하여 다양한 연습 방법이 존재한다[22,23]. 이러한 수술의 만족도를 좌우하는 이개재건술은 새로운 술자가 어느 정도의 경험과 기술을 보유하기까지 매우 가파른 학습 곡선을 보인다. Sabbagh [24]가 4년간 시행한 첫 100건의 이개 재건술을 분석한 논문에서 수술 결과를 불량, 보통, 양호, 매우 양호 4단계로 분류했을 때 첫 1년이 지나서야 불량한 결과가 줄어들었으며 매우 양호는 첫 1년에 1건(3.4%), 2년에 2건(8.0%)만 있었으며 3년이 되어서야 6건(26.1%), 4년에는 10건(43.5%)으로 상승하는 완만한 곡선을 보였다. 본원에서 시행한 환자들의 경우에, 초반에는 경험 부족으로 인하여 만족하지 못할 결과가 비교적 높았으나, 경험이 축적된 후인 2017년부터는 결과가 비약적으로 향상되었으며 선행 문헌과 유사한 결과가 향후 기대된다.
이개 재건술의 합병증은 크게 부위로는 공여부와 이식부의 합병증으로 나눌 수 있으며 발생 시간으로는 초기와 후기 합병증으로 나눌 수 있다. 공여부의 합병증으로는 흉곽의 변형이 대표적이며, 미세한 변형부터 척추 측만증에 이르기까지 6.3%-50.0%까지 다양하게 나타났다[25]. 공여부(늑골연골)을 적게 채취한다면, 변형이 올 위험도는 낮아진다[26]. 흉막의 찢어짐을 보고한 사례도 있었으며, 공여부의 비대반흔이 존재하는 경우도 있다[25]. 이식부의 조기 합병증으로는 피부괴사, 감염, 이개기틀의 흡수 및 괴사, 혈종이 있을 수 있으며, 후기 합병증으로는 이개기틀의 제작 시 이용한 와이어 및 봉합사의 노출, 피부반흔, 이개윤곽의 상실, 재건된 이개의 부적절한 위치, 미용적으로 만족하지 못하는 결과 등이 있을 수 있다. 합병증의 비율은 문헌에 따라 다소 차이가 있으나, 감염 및 피부 괴사가 약 0.9%-6.3% 내외로 가장 흔하게 보고되었다. 조기 합병증은 대개 국소 소독 및 피부나 국소 피판술로 대부분 호전이 되나 지속적인 감염 및 연골의 변형이 일어난 경우 불가피하게 재수술이 필요할 수 있다. Fu 등[27]에 의한 연구에서 이개 재건술에서 술후 합병증은 나이, 성별, 이개의 편위 정도와 상관 없이 Nagata 술식이 Brent 술식에 비해 유의미하게 많았으며, 이는 Nagata 술식이 더 압축적이며 기술적으로 어렵기 때문이라고 설명하였다. 때문에 Nagata 술식을 이용 할 경우에는 피부피판을 더욱 세심하게 디자인하고 조심스럽게 다루는 것이 필요하다[25,28,29]. 본원에서 시행한 이개재건술의 합병증의 빈도도 대개 수술을 개시한 초기 2-3년 이내에 발생하였고, 수술 경험이 누적됨에 따라 줄어들었다. 수술에 소요된 시간은 1차 수술에서는 연도별로 큰 차이를 보이지 않았으나, 2차 수술에서는 약 8시간에서 6시간으로 감소하는 경향을 보였다. 1차 수술에서 수술 시간의 차이가 없는 이유는 기형의 심한 정도와 측두두정근막의 이용 여부 등에 따라 수술 시간의 편차가 크기 때문이라 생각된다. 즉, 연도별로 수술이 시행된 기형의 종류가 차이가 있고, 보다 많은 증례가 있었다면 수술 시간의 감소를 보다 명확하게 파악할 수 있겠으나, 본 연구에서는 총 27개의 증례로 증례 수가 많지 않기 때문에 경향을 정확히 파악하기는 쉽지 않았다. 반면에 2차 수술의 경우는 술식이 거의 일정하므로, 수술 시간의 감소가 확연하였으나, 통계적인 의미는 없었다. 이러한 통계 상의 명확하지 않은 차이 역시 한정된 증례 수에 따른 것이라 생각된다.
이개재건술 술식의 복잡함과 합병증의 처치 등은 이개재건술의 진입 장벽으로 작용하며, 우리나라의 경우 이비인후과보다 성형외과에서 지속적으로 많은 수술이 행해지고 있는 것이 현실이다. 그러나, 많은 경우의 소이증 환자에서 외이도 협착과 난청이 같이 동반되며, 외형뿐 아니라 청력재활도 같이 되어야 환자에게 최선의 치료가 이루어 진다고 볼 수 있다[30-32]. 이비인후과에서는 소이증의 외형적 재건과 청력의 기능적 개선이 모두 가능하기 때문에 환자를 치료함에 있어 보다 포괄적 치료가 가능하며, 추후 소이증 환자의 이개성형술을 포함한 전반적 관리를 적극적으로 시행하기 위해서는 더 많은 훈련과 노력이 필요할 것이다.
결론적으로, 전체 이개재건술은 자가 늑골 연골 혹은 인공 삽입물을 사용하는 복잡하고 정교한 수술이다. 성공적인 이개재건술을 위해서는 피판 및 연골 형태에 대한 세심한 디자인과 수술적 기술의 습득이 중요하며 필수적으로 안면 및 이개에 대한 미적 개념을 확립하고 있어야 하고, 발생 가능한 합병증에 대한 대처 방법의 습득이 필요하다.
REFERENCES
1. Kelley PE, Scholes MA. Microtia and congenital aural atresia. Otolaryngol Clin North Am. 2007; 40(1):61–80. vi.

2. Bartel-Friedrich S. Congenital auricular malformations: Description of anomalies and syndromes. Facial Plast Surg. 2015; 31(6):567–80.

3. Luquetti DV, Heike CL, Hing AV, Cunningham ML, Cox TC. Microtia: Epidemiology and genetics. Am J Med Genet A. 2012; 158A(1):124–39.

4. Nagata S. A new method of total reconstruction of the auricle for microtia. Plast Reconstr Surg. 1993; 92(2):187–201.

5. Zhang TY, Bulstrode N, Chang KW, Cho YS, Frenzel H, Jiang D, et al. International consensus recommendations on microtia, aural atresia and functional ear reconstruction. J Int Adv Otol. 2019; 15(2):204–8.

6. Brent B. Auricular repair with autogenous rib cartilage grafts: Two decades of experience with 600 cases. Plast Reconstr Surg. 1992; 90(3):355–74. discussion 375-6.
7. Brent B. The correction of microtia with autogenous cartilage grafts: II. Atypical and complex deformities. Plast Reconstr Surg. 1980; 66(1):13–21.
8. Nagata S. Modification of the stages in total reconstruction of the auricle: Part II. Grafting the three-dimensional costal cartilage framework for concha-type microtia. Plast Reconstr Surg. 1994; 93(2):231–42. discussion 267-8.
9. Gosain AK, Kumar A, Huang G. Prominent ears in children younger than 4 years of age: What is the appropriate timing for otoplasty? Plast Reconstr Surg. 2004; 114(5):1042–54.

10. Firmin F. State-of-the-art autogenous ear reconstruction in cases of microtia. Adv Otorhinolaryngol. 2010; 68:25–52.

11. Siegert R, Weerda H, Magritz R. Basic techniques in autogenous microtia repair. Facial Plast Surg. 2009; 25(3):149–57.

12. Alexander KS, Stott DJ, Sivakumar B, Kang N. A morphometric study of the human ear. J Plast Reconstr Aesthet Surg. 2011; 64(1):41–7.

13. Skiles MS, Randall P. The anesthetics of ear placement: An experimental study. Plast Reconstr Surg. 1983; 72(2):133–40.
14. Li Q, Zhou X, Wang Y, Qian J, Zhang Q. Auricular reconstruction of congenital microtia by using the modified Nagata method: Personal 10-year experience with 1350 cases. J Plast Reconstr Aesthet Surg. 2018; 71(10):1462–8.

15. Wilkes GH, Wong J, Guilfoyle R. Microtia reconstruction. Plast Reconstr Surg. 2014; 134(3):464e–79e.

16. Xu Z, Zhang R, Zhang Q, Xu F, Li D, Li Y. New strategies for tragus and antitragus complex fabrication in lobule-type microtia reconstruction. Plast Reconstr Surg. 2019; 144(4):913–21.

17. Cabin JA, Bassiri-Tehrani M, Sclafani AP, Romo T 3rd. Microtia reconstruction: Autologous rib and alloplast techniques. Facial Plast Surg Clin North Am. 2014; 22(4):623–38.
18. Beahm EK, Walton RL. Auricular reconstruction for microtia: Part I. Anatomy, embryology, and clinical evaluation. Plast Reconstr Surg. 2002; 109(7):2473–82. quiz following 2482.

19. Moon IY, Oh KS, Lim SY, Pyon JK, Mun GH, Bang SI. Estimation of eighth costal cartilage in surgical timing of microtia reconstruction. J Craniofac Surg. 2015; 26(1):48–51.

20. Limandjaja GC, Breugem CC, Mink van der Molen AB, Kon M. Complications of otoplasty: A literature review. J Plast Reconstr Aesthet Surg. 2009; 62(1):19–27.

21. Brent B. Reconstruction of the auricle. In : Mathes SJ, editor. Plastic Surgery. 2nd ed. Philadelphia: Elsevier;2007. p. 633–98.
22. Murabit A, Anzarut A, Kasrai L, Fisher D, Wilkes G. Teaching ear reconstruction using an alloplastic carving model. J Craniofac Surg. 2010; 21(6):1719–21.

23. Yamada A, Imai K, Fujimoto T, Morimoto K, Niitsuma K, Matsumoto H. New training method of creating ear framework by using precise copy of costal cartilage. J Craniofac Surg. 2009; 20(3):899–902.

24. Sabbagh W. Early experience in microtia reconstruction: The first 100 cases. J Plast Reconstr Aesthet Surg. 2011; 64(4):452–8.

25. Long X, Yu N, Huang J, Wang X. Complication rate of autologous cartilage microtia reconstruction: A systematic review. Plast Reconstr Surg Glob Open. 2013; 1(7):e57.
26. Liu T, Hu J, Zhou X, Zhang Q. Expansion method in secondary total ear reconstruction for undesirable reconstructed ear. Ann Plast Surg. 2014; 73 Suppl 1:S49–52.

27. Fu YY, Li CL, Zhang JL, Zhang TY. Autologous cartilage microtia reconstruction: Complications and risk factors. Int J Pediatr Otorhinolaryngol. 2019; 116:1–6.

28. Park C, Lew DH, Yoo WM. An analysis of 123 temporoparietal fascial flaps: Anatomic and clinical considerations in total auricular reconstruction. Plast Reconstr Surg. 1999; 104(5):1295–306.

29. Zhang Q, Zhang R, Xu F, Jin P, Cao Y. Auricular reconstruction for microtia: Personal 6-year experience based on 350 microtia ear reconstructions in China. Plast Reconstr Surg. 2009; 123(3):849–58.

30. Siegert R. Combined reconstruction of congenital auricular atresia and severe microtia. Adv Otorhinolaryngol. 2010; 68:95–107.

Fig. 1.
First stage of total auricular reconstruction. The outline of the incision (A: anterior surface, B: posterior surface). The construction of the subcutaneous skin pocket after the skin flap elevation (C). The appearance after rotation of ear lobule (D). The outline of the 6th through 9th autologous costal cartilages before fabrication (E). The fabricated costal cartilage units before assembly (F). The completed 3D framework (G). Final appearance after the first stage of auricular reconstruction (H).
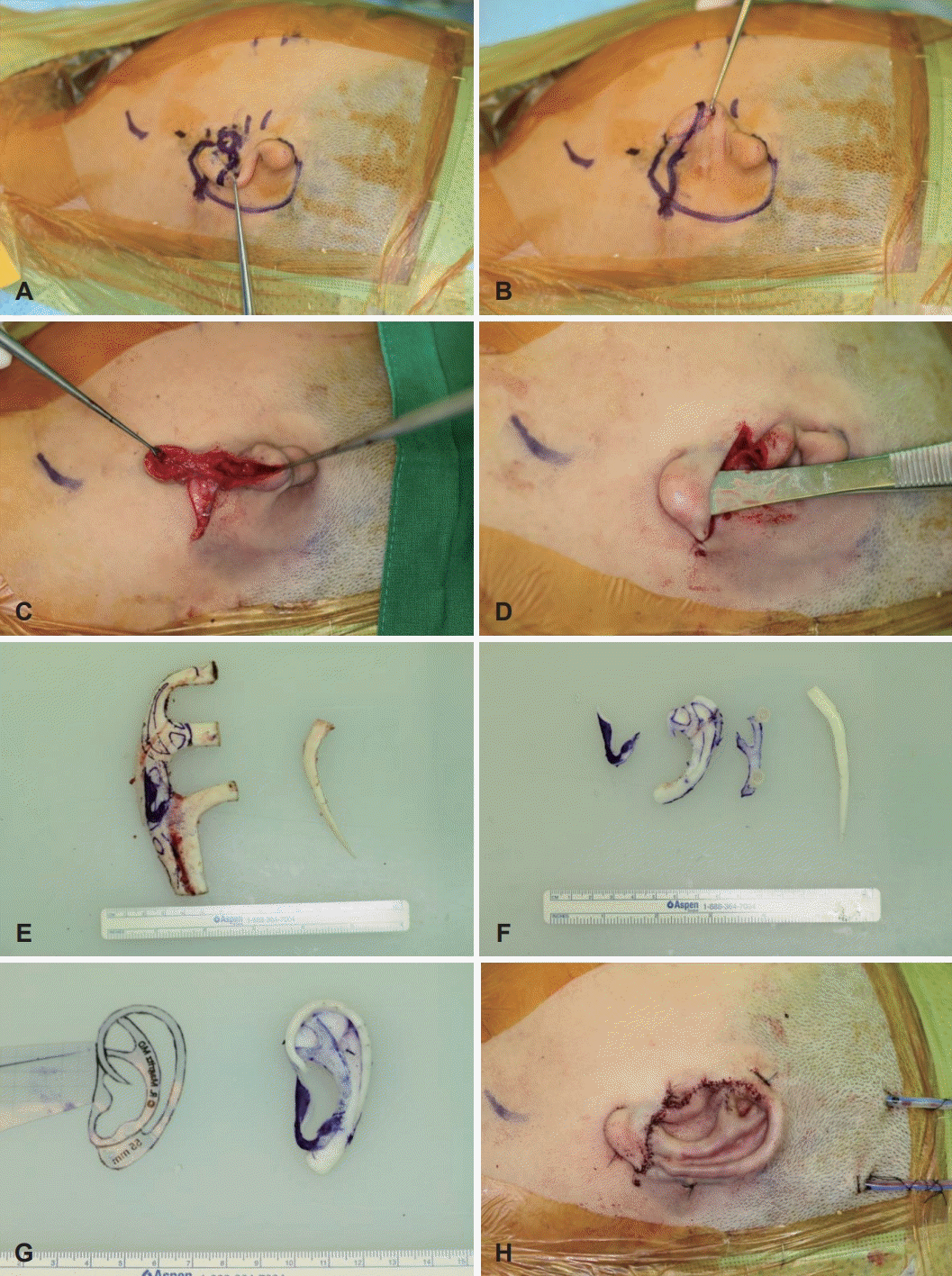
Fig. 2.
Second stage of total auricular reconstruction. The outline of the incision (A). The skin flap elevation along the helical rim (B). The release of the reconstructed auricular framework for the auricular projection (C). The cartilage block for the auricular projection using the remnant 6th costal cartilage from the 1st stage surgery (D). The cartilage block fixation at the posterior surface of 3D frame with 5-0 wire (E). The cartilage block is covered with mastoid galleal flap (F). Formation of auriculocephalic sulcus after covering the exposed surface with skin graft (G and H).
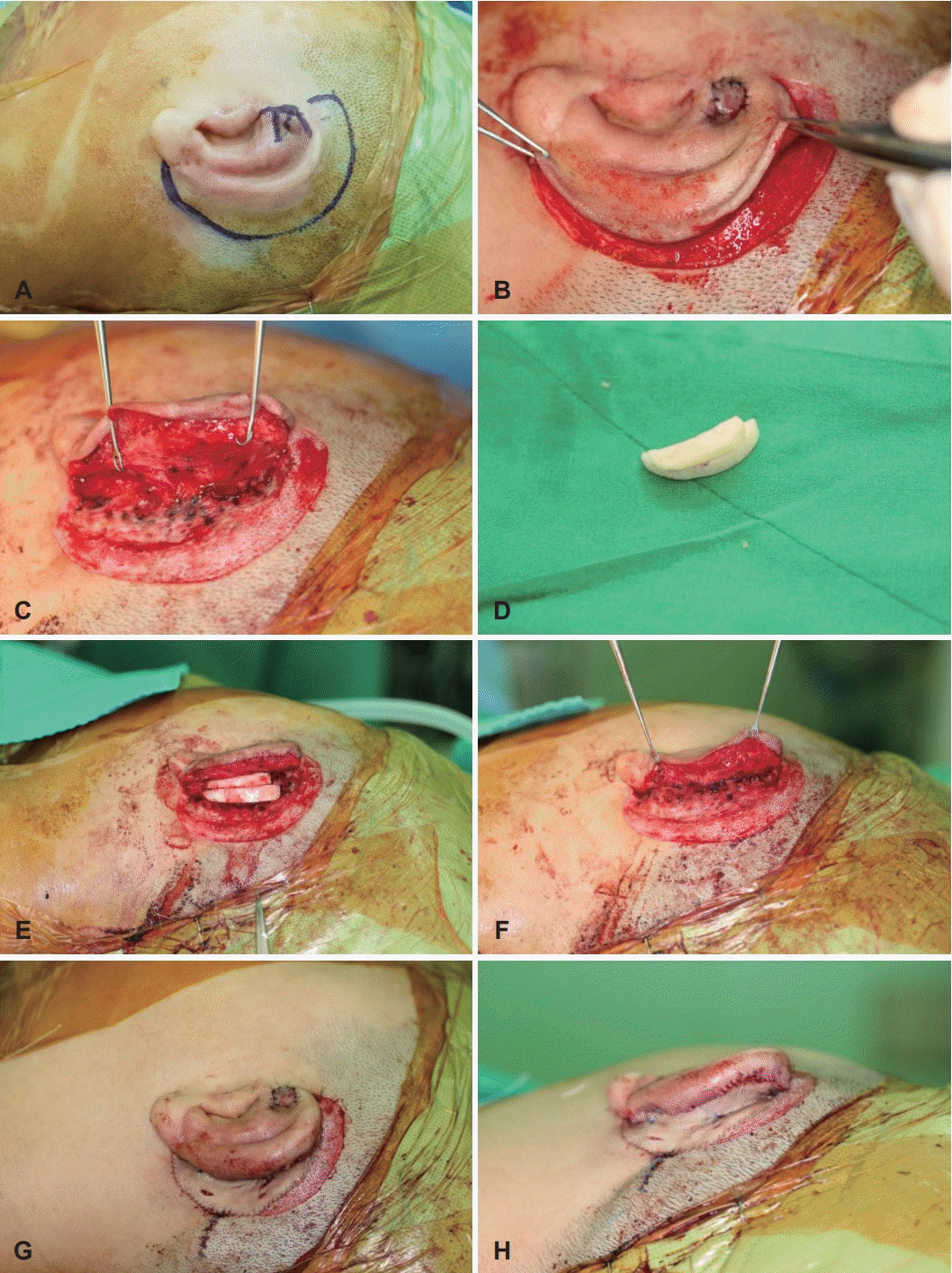
Fig. 3.
Single-stage total auricular reconstruction. Single-stage auricular reconstruction surgeries were performed in the cases of revision surgery, reconstruction with MEDPOR (Styker), or hemifacial microsmia patients. The outline of the incision (A). Elevated skin flap (B). Split-thickness skin flap was elevated from the line indicated by the arrow head (A) preserving the hair follicles in the dermal layer. The anterior surface of the skin covering framework was elevated by full-thickness. Elevation of TPF (C). 3D framework covered with TPF (D). Final appearance after covering the framework with the skin flap. The area where split-thickness skin flap had been elevated was left for secondary healing (E). TPF: temporoparietal fascia flap.
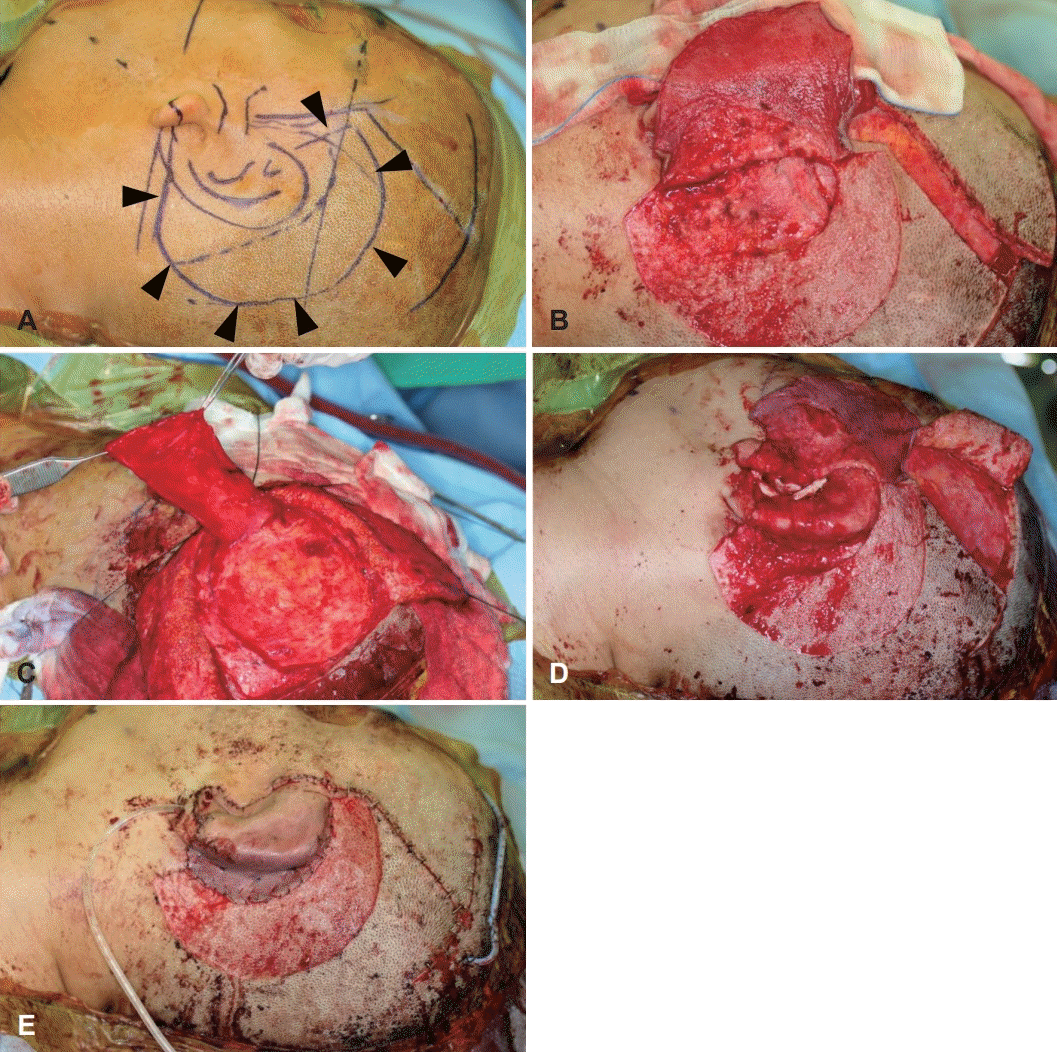
Fig. 4.
Examples of postoperative evaluation for auricle shape. Good (A and B). Moderate (C and D). Poor (E and F).
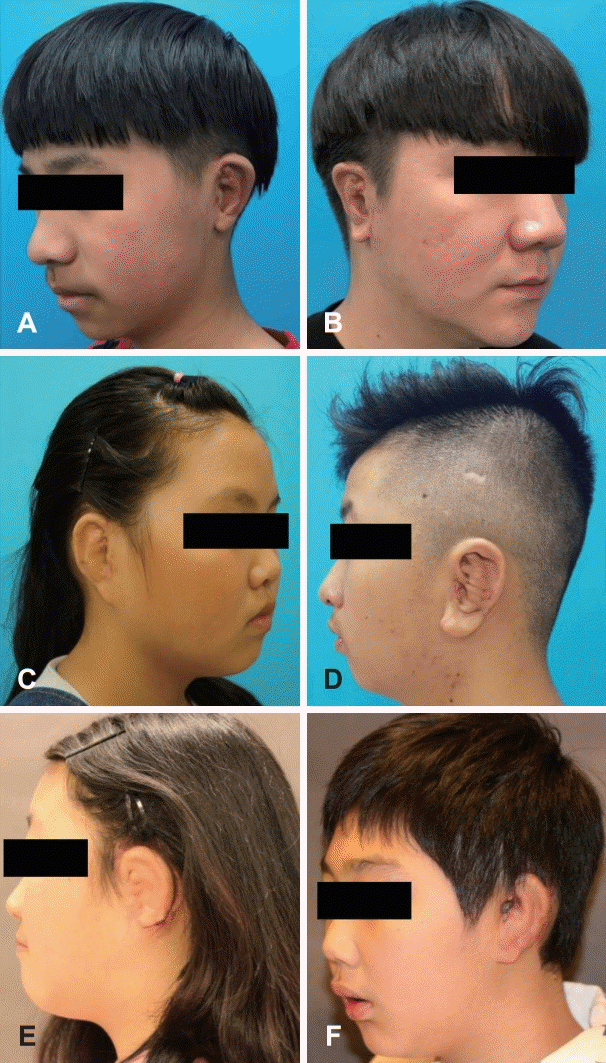
Fig. 5.
Examples of postoperative evaluation for auricle symmetry. Symmetric (A and B). Asymmetric (C and D).
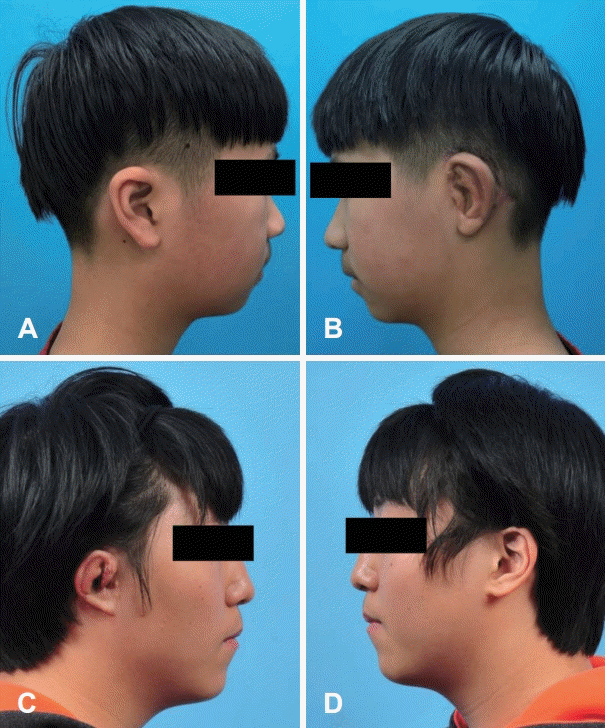
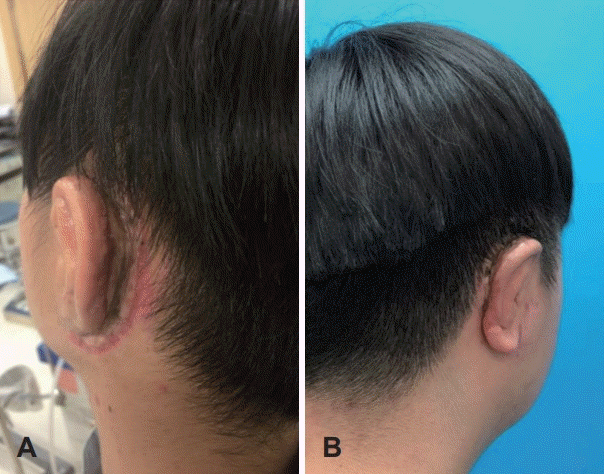
Fig. 6.
Examples of postoperative evaluation for auriculocephalic sulcus. Good (A). Severe stricture (B). Any results between (A) and (B) were considered as ‘partial stricture.’




 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download