Abstract
Purpose
Ultrasonography is widely used for examining breast mass. We used the Breast Imaging-Reporting and Data System (BI-RADS) to characterize breast lesions found on ultrasonography. Among various ultrasound techniques, we used S-DetectTM (Samsung Medison Co., Ltd, Seoul, Korea), which supports the morphological analysis of breast masses found according to BI-RADS. In addition, we compared the breast surgeons’ categorization of breast masses with that by S-DetectTM.
Methods
Breast surgeons evaluated the breast masses found using ultrasonography between April 2016 and December 2016. A total of 139 masses, which were categorized as BI-RADS 3 or 4, from 112 patients were reevaluated by S-DetectTM before performing vacuum-assisted resection or surgical excision.
Results
Of the 139 masses, 118 were benign tumors and 21 were malignant tumors. With regard to the diagnostic performance, the sensitivity of categorization was 95% for breast surgeons, but the sensitivity was relatively lower for S-detectTM (85%). However, the specificity and accuracy of S-detectTM were 70.6% and 74.1%, respectively, which were higher than those values obtained from breast surgeons (18.5% and 30.9%, respectively).
Go to : 
유방암은 여성 암 사망의 가장 흔한 원인이며, 또한 이로 인한 사망률은 점차 증가하고 있다.(1) 유방암의 5년 생존률은 유방암의 병기가 낮을수록 사망률이 더 낮은 경향을 보이는데 2018년 한국유방암학회의 발표에 따르면 조기 유방암으로 분류되는 0, 1, 2기 환자에서는 90% 이상의 5년 생존율을 보이나 전신 전이가 있는 4기 환자는 34%로 상대적으로 낮은 생존율을 보였다.(1) 따라서 유방암의 생존률을 높이기 위해서는 무엇보다도 유방암을 조기에 발견하는 것이 중요하다. 유방암의 선별검사로 유방촬영술이 쓰이고 있지만 우리나라에서는 50세 미만의 여성에서 치밀 유방의 비율이 높아 유방암으로 진단된 환자의 90%이상이 유방초음파를 통해 진단되고 있어 유방초음파의 역할이 크다.(2) 하지만 유방초음파로 관찰된 유방 병변을 유방암으로 조기에 확진하고 악성여부가 불명확한 병변의 경우에 조속히 악성여부를 감별하기 위해서는 조직검사를 적극적으로 시행할 수밖에 없다.(3)
조직검사의 필요성을 명확하게 하기 위한 초음파 판독기준으로 BI-RADS (Breast imaging reporting and data system)가 사용되고 있다. BI-RADS는 초음파시술자와 유방외과 전문의 간에 유방 병변에 대한 표준화된 기준을 제공하여 의사결정에 도움을 준다.(4) 유방초음파상 악성의 가능성이 있는 소견은 불분명한 경계, 미세엽상형, 불규칙 모양, 불균질 내부 에코, 혈류 증가 소견, 주변부 고음영, 각진 변연, 석회화, 유선관 확장 등이 있다.(4) 하지만 표준검사 소견이 있다 하더라도 양성과 악성 종괴의 초음파 소견들은 부분적으로 중복될 수 있으며,(4) 또 시술자에 따라 유방 병변의 판독에 대한 민감도가 떨어질 수 있다. 이러한 단점을 보완하기 위해 인공지능기반 진단보조 프로그램이 등장하였고, S-detectTM (Samsung Medison Co.,Ltd, Seoul, Korea), CADstream (Merge Healthcare Inc., Chicago, IL, USA), 및 DynaCAD for Breast (Invivo, Gainesville, FL, USA) 등이 사용되고 있다.(5) 그 중에서 S-detectTM는 초음파로 측정되는 종양의 형태를 인식하여 평가하는 방식을 취하고 있다.
이 연구는 유방외과 전문의가 평가한 BI-RADS와 S-detectTM의 종괴 분석평가 결과를 비교하고, 절제 후 확인된 병리조직검사와 각각을 비교 분석하여 유방암에 대한 진단 기기로서의 S-detectTM의 성능을 평가하고자 하였다.
Go to : 
이 연구는 후향적 연구로, 본원의 IRB 승인을 받았다 (No. 2019-07-026).
2016년 4월부터 12월까지 유방 종괴를 주소로 본원 외래를 방문한 환자들 중에 유방초음파상 BI-RADS category 3 또는 4에 해당하는 종괴를 갖는 환자들은 121명 이었다. 본 연구는 미세석회화(microcalcification) 3명, 사진이 저장되지 않은 환자 3명, 과거 섬유선종(fibroadenoma) 제거 후 재발한 1명, 중심부바늘생검(core-needle biopsy)을 시행하지 않고 추적관찰 하기 원한 환자 2명 등 9명을 제외한 112명을 대상으로 하였다. 총 112명의 환자에서, 합병 낭종(complicated cystic mass) 양상으로 중심부바늘생검을 시행하지 않고 바로 진공 보조 흡인 생검술을 시행한 종괴 5개와 중심부바늘생검을 시행한 134개의 종괴를 합하여 총 139개의 종괴를 평가하였다.
유방 외과 전문의 3명이 유방 종괴를 1차적으로 평가하였으며, BI-RADS category에 따라 분류하였다. BI-RADS category 3; probably benign; 4a, low suspicion for malignancy; 4b, intermediate suspicion for malignancy; 4c, moderate concern for malignancy에 해당하는 유방 종괴에 대하여 초음파 유도 하 중심부 바늘 생검을 시행하여 양성으로 확인된 종괴는 진공 보조 흡인 생검술을 시행하였고, 악성 종양으로 확인된 경우 수술적 치료를 통해 제거하였다. 진공 보조 흡인 생검술과 수술을 시행하기 전에 S-detectTM를 이용하여 종괴를 재평가하였다. S-detectTM는 종괴의 깊이(depth), 너비(width), 높이(height), 모양(shape), 방향성(orientation), 변연(margin), 병변의 경계(lesion boundary), 후방 특성(posterior feature), 에코 양상(endo patten), 주변 조직(surrounding tissue), 혈관 분포 상태(vascularity), 특별 증례(special case) 등을 분석하여 possibly benign 또는 possibly malignant로 유방 종괴를 분류하였다.
Medical calc version 18.0 (Panmun education, Seoul, Korea)을 이용하였다. 양성 종괴군과 악성 종괴군의 크기 비교 및 유방 종괴 크기에 따른 초음파와 병리조직검사의 일치여부 상관관계를 분석하고 각 환자군의 평균 나이와 1 cm 이상 크기를 가지는 종괴 비율에 대한 통계적 분석을 위하여 T-test를 시행하였다. BI-RADS와 S-detectTM의 결과를 비교하기 위해서 Generalized estimating equation method를 적용하였다. 또한 BI-RADS 및 S-detectTM의 Receiver Operating Characteristic (ROC) curve 비교를 위해 Delong’s method를 사용하여 평가하였다.
Go to : 
전체 139개의 종괴 중에서 양성 종양은 118개(84.2%)였으며, 악성 종양은 21개(15.8%)였다. 연구대상 환자들의 평균나이는 44.4 ± 0.25세였으며, 유방 종괴의 평균크기는 12.1 ± 0.47 mm였다. 유방 종괴 중에서 양성 종괴의 평균 크기는 14.7 ± 7.55 mm였으며, 악성 종괴의 평균 크기는 11.6 ± 0.47 mm였다. 양성 유방병변 중 1 cm 미만은 52개, 1 cm 이상은 66개였고, 악성 유방병변 중 1 cm 미만은 7개, 1 cm 이상은 14개였다(Table 1).
Go to : 
REFERENCES
Korean Breast Cancer Society. Breast Cancer Facts & Figures 2018. Korean Breast Cancer Society;Seoul:
Youn I., Choi S., Kook SH., Choi YJ. 2016. Mammographic breast density evaluation in korean women using fully automated volumetric assessment. J Korean Med Sci. 31:457–62. DOI: 10.3346/jkms.2016.31.3.457. PMID: 26955249. PMCID: PMC4779873.

Stavros AT., Thickman D., Rapp CL., Dennis MA., Parker SH., Sisney GA. 1995. Solid breast nodules: use of sonography to distinguish between benign and malignant lesions. Radiology. 196:123–34. DOI: 10.1148/radiology.196.1.7784555. PMID: 7784555.

Kim YJ., Choi HY., Moon BI., Lee SN. 2006. Categorization and evaluation of usefulness of breast lesions with using ultrasound BI-RADS (Breast Imaging Reporting and Data system). J Korean Radiol Soc. 54:313–8. DOI: 10.3348/jkrs.2006.54.4.313.

Pan J., Dogan BE., Carkaci S., Santiago L., Arribas E., Cantor SB, et al. 2013. Comparing performance of the CADstream and the DynaCAD breast MRI CAD systems : CADstream vs. DynaCAD in breast MRI. J Digit Imaging. 26:971–6. DOI: 10.1007/s10278-013-9602-y. PMID: 23589186. PMCID: PMC3782607.

Kolb TM., Lichy J., Newhouse JH. 2002. Comparison of the performance of screening mammography, physical examination, and breast US and evaluation of factors that influence them: an analysis of 27,825 patient evaluations. Radiology. 225:165–75. DOI: 10.1148/radiol.2251011667. PMID: 12355001.

Kaplan SS. 2001. Clinical utility of bilateral whole-breast US in the evaluation of women with dense breast tissue. Radiology. 221:641–9. DOI: 10.1148/radiol.2213010364. PMID: 11719658.

Brem RF., Lenihan MJ., Lieberman J., Torrente J. 2015. Screening breast ultrasound: past, present, and future. AJR Am J Roentgenol. 204:234–40. DOI: 10.2214/AJR.13.12072. PMID: 25615743.

Kopans DB. 2004. Sonography should not be used for breast cancer screening until its efficacy has been proven scientifically. AJR Am J Roentgenol. 182:489–91. DOI: 10.2214/ajr.182.2.1820489. PMID: 14736687.

Galperin M., Andre MP., Barker CH., Olson LK., O'Boyle M., Richman K, et al. 2009. Reproducibility of image analysis for breast ultrasound computer-aided diagnosis. Acoustical Imaging. 29:397–402. DOI: 10.1007/978-1-4020-8823-0_55.

Sonka M., Hlavac V., Boyle R. 2014. Image Processing, Analysis, and Machine Vision. 4th ed. Cengage Learning;Boston:

Chen CM., Chou YH., Han KC., Hung GS., Tiu CM., Chiou HJ, et al. 2003. Breast lesions on sonograms: computer-aided diagnosis with nearly setting-independent features and artificial neural networks. Radiology. 226:504–14. DOI: 10.1148/radiol.2262011843. PMID: 12563146.

Fujita H., Uchiyama Y., Nakagawa T., Fukuoka D., Hatanaka Y., Hara T, et al. 2008. Computer-aided diagnosis: the emerging of three CAD systems induced by Japanese health care needs. Comput Methods Programs Biomed. 92:238–48. DOI: 10.1016/j.cmpb.2008.04.003. PMID: 18514362.

Choi JH., Kang BJ., Baek JE., Lee HS., Kim SH. 2018. Application of computer-aided diagnosis in breast ultrasound interpretation: improvements in diagnostic performance according to reader experience. Ultrasonography. 37:217–25. DOI: 10.14366/usg.17046. PMID: 28992680. PMCID: PMC6044219.

Kim K., Song MK., Kim EK., Yoon JH. 2017. Clinical application of S-Detect to breast masses on ultrasonography: a study evaluating the diagnostic performance and agreement with a dedicated breast radiologist. Ultrasonography. 36:3–9. DOI: 10.14366/usg.16012. PMID: 27184656. PMCID: PMC5207353.

Shin HJ., Kim HH., Cha JH., Park JH., Lee KE., Kim JH. 2011. Automated ultrasound of the breast for diagnosis: interobserver agreement on lesion detection and characterization. AJR Am J Roentgenol. 197:747–54. DOI: 10.2214/AJR.10.5841. PMID: 21862820.

Go to : 
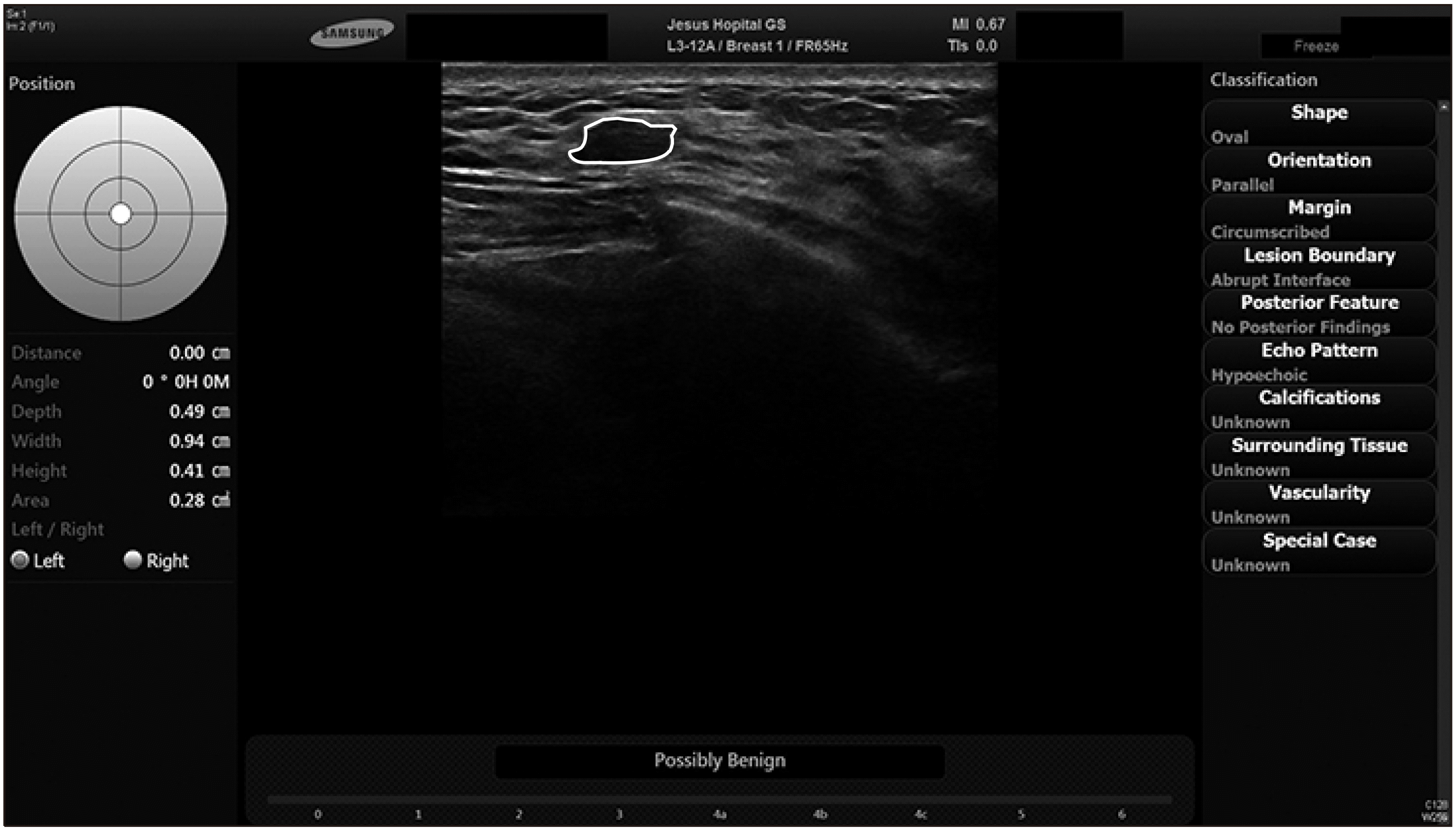 | Fig. 1A 27-year-old woman with left breast mass on B-mode ultrasound. S-DetectTM concluded that it is “Possibly Benign” based on features of the lesion listed on the right column. |
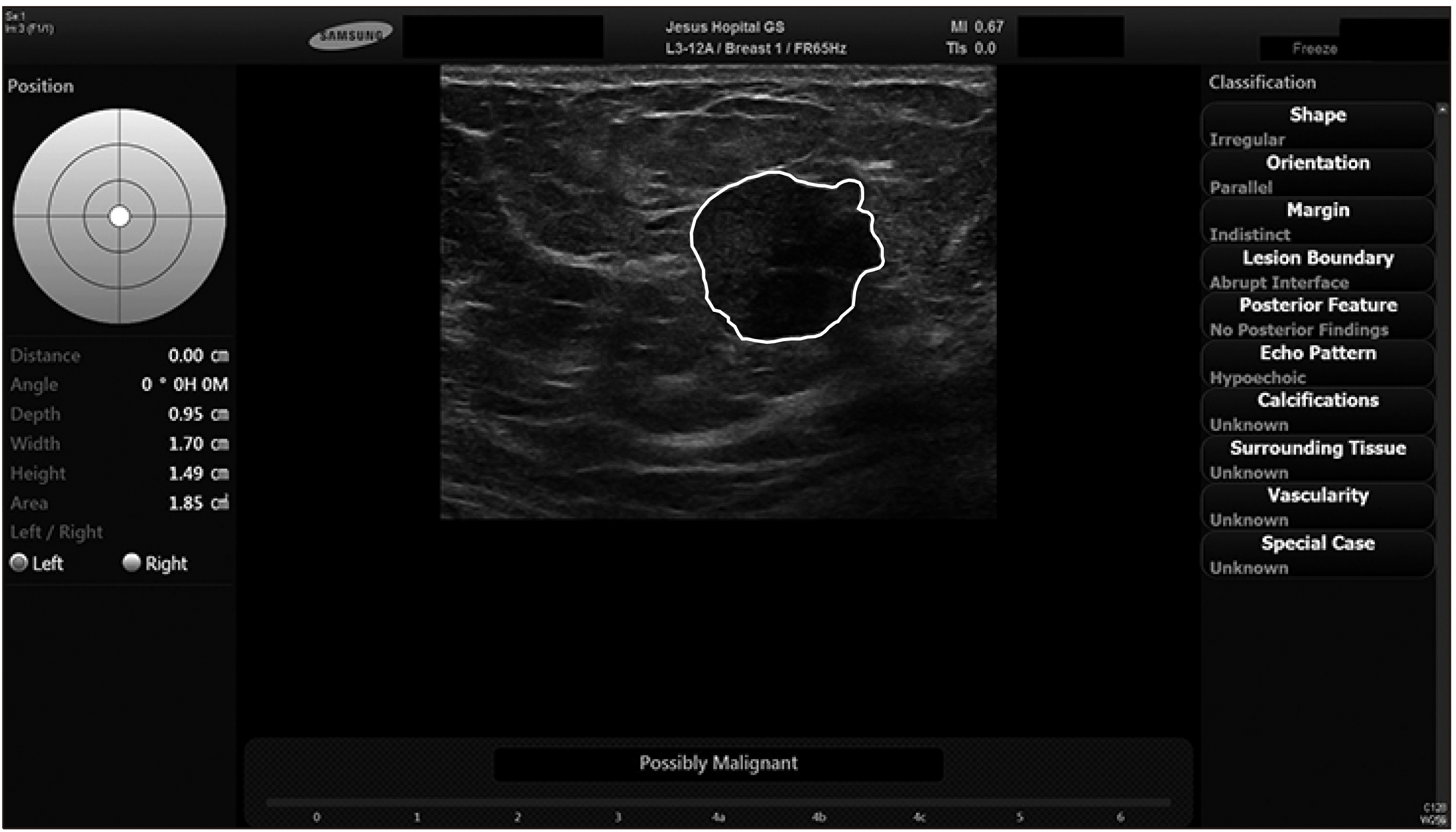 | Fig. 2A 65-year-old woman with left breast mass on B-mode ultrasound. S-DetectTM concluded that it is “Possibly Malignant” based on features of the lesion listed on the right column. |
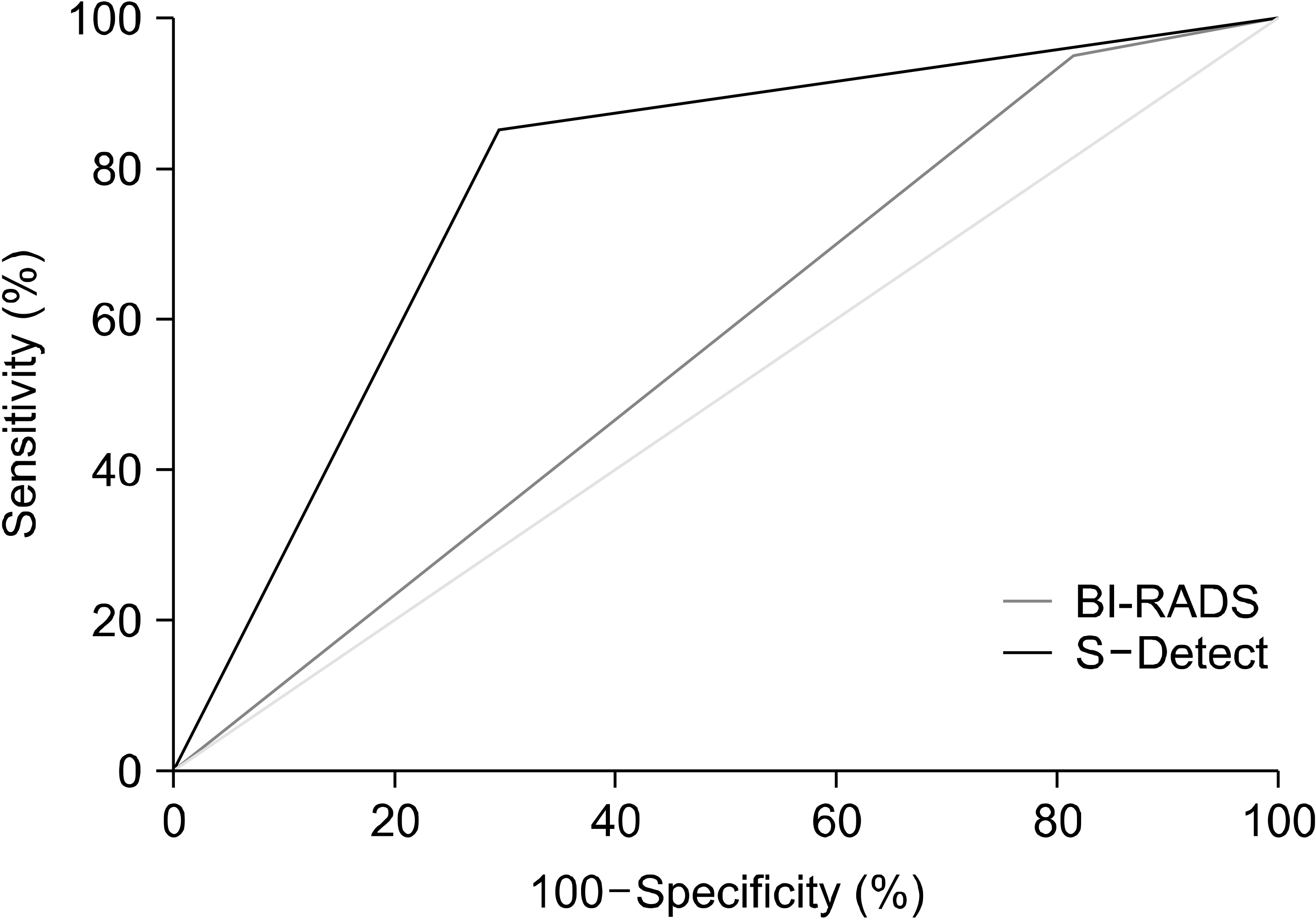 | Fig. 3Receiver operating characteristic curve for breast surgeons (BI-RADS) and S-DetectTM. |
Table 2
Pathologic Diagnosis
Table 3
Distribution of Final Assessments of the 139 Breast Masses according to the Breast Surgeons and S-DetectTM
Table 4
Diagnostic Performance for Breast Surgeons versus S-DetectTM
| Sensitivity (%) | Specificity (%) | Accuracy (%) | PPV (%) | NPV (%) | AUC | |
|---|---|---|---|---|---|---|
| BI-RADS | 95 | 18.5 | 30.9 | 16.4 | 95.7 | 0.567 |
| S-detectTM | 85 | 70.6 | 74.1 | 32.69 | 96.6 | 0.778 |
| P-value | 0.0055 | < 0.0001 | < 0.0001 | 0.0016 | 0.6988 | < 0.0001 |
Table 5
Mean Size of the Masses according to the Results of BI-RADS and S-DetectTM and Histopathological Results




 PDF
PDF Citation
Citation Print
Print


 XML Download
XML Download