This article has been
cited by other articles in ScienceCentral.
초록
목적:
근관 세정제로서 Hydroxyethylidene bisphosphonate (HEBP)가 다른 근관 세정제인 Sodium hypochlorite (NaOCl), Etylenediaminetetraacetic acid (EDTA) 상호 작용 시 조직용해 능력, 항균효과와 온도에 따른 조직 용해 능력의 변화에 대해 알아보았다.
연구 재료 및 방법:
소의 근육으로 제작된 동일한 단면적(2 × 2 × 2 mm)을 가진 80개의 시편을 8개의 그룹(n = 10)으로 임의로 나누었다. 초기 무게 측정 후 각각의 제조된 근관 세정제에 넣어 5분, 10분, 15분 후 무게를 측정하여 무게변화율을 구하였다. 항균 효과 조사를 위해 Enterococcus faecalis를 접종한 agar diffusion test를 시행하였다.
결과:
조직 용해 능력은 NaOCl group (G4, 5)이 가장 뛰어났으며, NaOCl과 HEBP의 혼합물(G7, 8)이 다음으로 나타났다. 또한 가열된(40°C) NaOCl과 NaOCl/HEBP의 혼합물의 경우 실온(25°C)보다 우수한 조직용해 능력이 나타났다. 항균 효과의 경우 EDTA > EDTA + 1% NaOCl > 1% NaOCl ≥ 1% NaOCl + HEBP 순으로 나타났다.
결론:
HEBP는 NaOCl 의 항균 효과를 방해하지 않으며, 조직 용해 능력에도 기존의 킬레이팅 제재에 비해 적은 영향을 미친다. 가열된 NaOCl, NaOCl과 HEBP의 혼합재제는 실온과 비교 시에 효율적으로 조직을 용해할 수 있다.
Abstract
Purpose:
The purpose of this study was to evaluate tissue dissolving capacity, antimicrobial effect of Hydroxyethylidene bisphosphonate (HEBP) interacting with sodium hypochlorite (NaOCl), Ethylenediaminetetraacetic acid (EDTA) as conventional endodontic irrigants and to determine tissue dissolving efficacy depended on temperature.
Materials and Methods:
A total of 80 bovine muscles were randomly distributed into 8 groups (n = 10). After their initial weights determined on a precision scale, the specimens in each group were immersed in the solutions for 5, 10 and 15 min and reweighted at each time period. Agar diffusion test inoculated with Enterococcus faecalis was performed for antimicrobial effect of each endodontic irrigants.
Results:
The ability to dissolve organic matter was greater in NaOCl group following NaOCl and HEBP mixture. Heated NaOCl (40°C) and NaOCl/HEBP mixture was greater tissue dissolving efficacy than room temperature (25°C). Antimicrobial effect was greater and significant in the following order EDTA > EDTA + 1% NaOCl > 1% NaOCl ≥ 1% NaOCl + HEBP.
Conclusion:
HEBP as soft chelating agent does not disturb antimicrobial effect and less affected tissue dissolving efficacy as inherent properties of NaOCl. In the heated NaOCl/HEBP mixture analyzed, it dissolved more the organic matter than room temperature.
Keywords: HEBP (Hydroxyethylidene bisphosphonate), 근관 세정제, 약한 킬레이트 제재, 조직용해능력, 항균 효과
Keywords: HEBP (Hydroxyethylidene bisphosphonate), endodontic irrigants, soft chelating agent, tissue dissolving capacity, antimicrobial effect
서론
근관 치료 영역에서 세척과 성형의 최종적인 목표는 근관 내 미생물과 괴사된 조직의 잔사를 최소한으로 줄이는 것이다. 근관 치료 시 기계적인 기구 조작만 시행한 경우, 근관계의 isthmus나 측방관, fin 등 기구가 도달하지 못하는 해부학적인 영역이 40 - 50% 정도에 달한다.
1 따라서 적절한 근관 치료를 위해서는 기계적인 세정 뿐만아니라 근관 세정제를 이용한 화학적인 세정이 동반되어야 한다.
Sodium hypochlorite (NaOCl)는 근관 치료에서 가장 흔하게 사용되는 근관 세정제로서 항 세균 효과와 유기성분을 용해하는 독특한 성질을 갖는다.
2 근관계에서 NaOCl 세정제의 효과를 개선시키기 위한 방법으로 높은 농도를 사용하거나 가열하여 사용하는 방법이 있다. 낮은 농도를 갖는 NaOCl 용액의 온도를 증가시키면 즉각적인 조직 용해 능력을 높이며, 상아질 잔사로부터 유기질 잔사를 더 효과적으로 제거할 수 있다. Sirtes 등에 의하면 온도가 25°C 오르면 NaOCl의 효과는 100배 증가했다. 또한 45°C에서 1% NaOCl을 사용하여 인간 치수세포를 용해하는 능력은 20°C에서 5.25% 용액을 사용한 것과 같다는 연구 결과를 발표하였다.
3
그러나 NaOCl은 무기 성분으로 구성된 도말층을 제거 할 수 없다는 한계를 갖는다. 이러한 단점을 극복하기 위해서, Etylenediaminetetraacetic acid (EDTA)와 같은 킬레이팅 제재를 이용하여 상아질 벽에 도말층을 제거하고 기구 조작 동안의 경조직 잔사의 축적을 감소시킨다.
4 그러나 EDTA는 NaOCl과 반응하여 NaOCl의 자유 염소기가 소멸되어 특유의 조직용해 능력과 항균 효과를 저해시킨다고 밝혀졌다.
5 따라서 근관 치료 시 NaOCl과 EDTA는 혼합하여 사용해서는 안되며, NaOCl과 EDTA를 각각 교대로 30 - 60초 적용하여 사용해야 한다.
이러한 이유로 1-hydroxyethlidene-1,1,-bisphosphonate(HEBP)와 같은 soft chelating agent 들이 EDTA의 대체제로 소개되고 있다. HEBP는 EDTA 혹은 citric acid와 유사하게 도말층을 제거하는 능력을 가지며, NaOCl과 혼합하여 사용해도 HEBP 고유의 킬레이팅 능력과, 도말층을 제거하는 성질을 저해하지 않고, 자유염소기의 활성에 영향을 받는 NaOCl의 항 세균 효과와 유기성분을 용해하는 성질에도 영향을 미치지 않는다고 알려졌다.
6
이번 연구는 근관 세정제로서 HEBP를 NaOCl, EDTA와 비교 시에 조직용해 능력, 항균효과에 대해 알아보고 각각의 세정제의 상호작용에 대해 평가한다. 또한, 온도에 따른 조직 용해 능력의 변화에 대해 알아보았다.
연구 재료 및 방법
1. 조직 용해 능력
치아의 연조직을 대신하여 소의 근육을 2 × 2 × 2 mm의 크기로 stainless-steel blade를 이용하여 절단하여 표면적과 초기 무게가 같은 80개의 표본을 준비하였다. 표본은 임의로 8개의 그룹(n = 10)으로 나누어, blot dry 한 후 초기 무게를 측정하기 위해 전자저울을 이용하였다. 각 그룹은 다음과 같은 근관 세정제에 넣었다(
Table 1).
Table 1
Solutions for the experiment of tissue dissolving capacity
|
Groups |
Solutions |
|
1 |
Normal saline (control group) |
|
2 |
17% EDTA |
|
3 |
18% HEBP |
|
4 |
2.25% NaOCl (25°C) |
|
5 |
2.25% NaOCl (40°C) |
|
6 |
1:1 5.5% NaOCl + 17% EDTA → finally, 2.25% NaOCl/8.5% EDTA mixture (25°C) |
|
7 |
1:1 5.5% NaOCl + 18% HEBP → finally, 2.25% NaOCl/9% HEBP mixture (25°C) |
|
8 |
1:1 5.5% NaOCl + 18% HEBP → finally, 2.25%NaOCl/9% HEBP mixture (40°C) |
조직 표본을 튜브에 담그기 직전에 그룹 6, 7, 8의 용액은 바로 혼합하였다. 그룹 1, 2, 3, 4, 8은 25°C 실온에서 보관 혹은 혼합되었다. 그룹 5, 8은 혼합 후 40°C 설정된 항온수조에 보관하였다. 각각의 그룹에 해당되는 용액 10 mL를 튜브에 채운 후, 조직 표본을 넣었다. 5분 후, 표본은 즉시 증류수로 옮겨서 30초 동안 용액을 제거하여 blot dry를 시행 후 무게를 재 측정 하였다. 이러한 과정을 5분마다 반복하여, 용액에 침전시킨 5분, 10분, 15분 후의 측정값을 구했다.
2. 항균효과
Brain-heart infusion (BHI) agar를 이용한 8개의 Petri dish를 준비하였다. 한천배지는 제조사의 지시대로 혼합하여, 이 plate는 실온에서 2일간 보관하였다. 동결 건조된
Enterococcus faecalis (KCTC 5290, from dental plaque, human)을 활성화 시킨 후,
E. faecalis를 BHI broth(Sigma-Aldrich, St Louis, USA)에 24시간 동안 배양하고, 박테리아의 성장을 혼탁도의 변화로 확인하였다. 순수하게 배양된
E. faecalis를 BHI broth에 접종한 후 한천 배지에 도말 하였다. 한천이 굳은 후에, 5 mm 직경으로 6개의 동그란 와동을 형성하고, 준비된 와동에 각 용액 10 ㎕를 떨어뜨렸다. 준비된 용액은 6개의 그룹으로 나누었다(
Table 2).
Table 2
Solutions for the experiments of antibacterial efficacy
|
Group |
Solution |
|
A |
1% NaOCl |
|
B |
8.5% EDTA |
|
C |
1:1 2% NaOCl + 17% EDTA → finally, 1% NaOCl/8.5% EDTA mixture |
|
D |
9% HEBP |
|
E |
1:1 2% NaOCl + 18% HEBP → finally, 1% NaOCl/9% HEBP |
|
F |
Saline (control group) |
위 한천배지를 37°C 배양기(
Fig 1)에 48시간 동안 보관한 후, 가장 넓은 너비를 갖는 세균 성장 억제대(zones of microbial inhibition)를 반복해서 측정하여 기록한다.
Fig. 1
(A) General Lan Incubator IB 05-G (60L, Jeio Tech, Inc., Seoul, Korea), (B) Model for Petri dish set up.

3. 통계
무게 변화 측정의 경우 일원 변량 분석(ANOVA)을 사용하였으며 Mann-Whitney test를 이용하여 사후 검정하였다. 항균 효과의 실험은 일원변량분석(ANOVA)와 Kruskal-Wallis’ test를 사용하였으며 Mann-Whitney test를 이용하여 사후 검정하였다. 위의 분석은 모두 SPSS(statistics data editor version 20, IBM, Chicago, USA) 프로그램을 이용하였다.
결과
1. 조직 용해 능력
(1) 시간 경과에 따른 조직 용해 능력
초기 5분 동안 모든 그룹에서 무게의 증가를 보인다(
Fig. 2,
Table 3). 그러나, 5 - 10분 사이에 Group 4와 Group 5에서 무게의 감소가 발생하며, Group 7과 Group 8은 10 - 15분 사이에 감소를 나타낸다. 반면 Group 1, 2, 6에서는 측정 시간 동안 유의미한 무게의 변화가 나타나지 않았다. Group 7은 Group 6에 비해 더 많은 무게의 소실을 관찰할 수 있었고, 15분 후에 더 현저하게 관찰되었다(
P < 0.05,
Fig. 3). Group 4와 비교했을 때는, 10분과 15분 후 모두에서 HEBP를 혼합한 Group 7에서 조직용해능력이 떨어졌다(
P < 0.05).
Fig. 2
The mean rate of weight changes (%) after 5 min, 10 min and 15 min of submersion to the irrigation solutions. EDTA, etylenediaminetetraacetic acid; HEBP, hydroxyethylidene bisphosphonate; NaOCl, sodium hypochlorite.
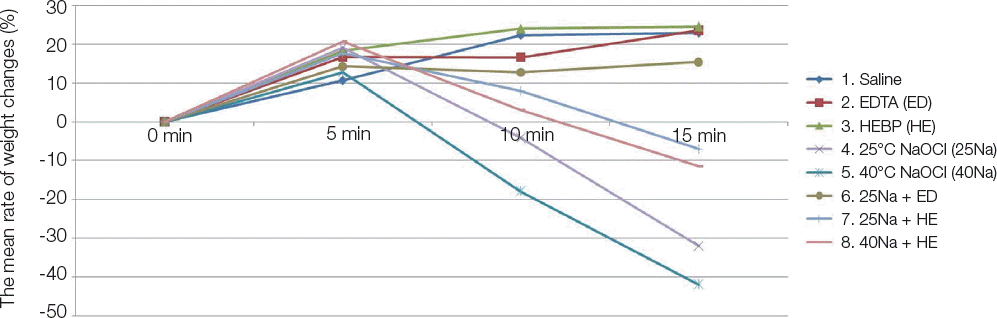
Table 3
Tissue dissolving efficacy depended on time
|
0 min |
5 min |
10 min |
15 min |
|
Group 1 |
0.000% |
10.651% |
22.313% |
22.918% |
|
Group 2 |
0.000% |
16.724% |
16.635% |
23.607% |
|
Group 3 |
0.000% |
18.331% |
23.956% |
24.497% |
|
Group 4 |
0.000% |
19.147% |
-4.103% |
-31.944% |
|
Group 5 |
0.000% |
12.795% |
-17.825% |
-41.853% |
|
Group 6 |
0.000% |
14.321% |
12.770% |
15.447% |
|
Group 7 |
0.000% |
21.551% |
10.260% |
-5.860% |
|
Group 8 |
0.000% |
20.635% |
3.034% |
-11.442% |
Fig. 3
The effect of HEBP. These graphs show comparisons of the mean rate of weight change (%) of Group 4, 6 and 7 after 10 min and 15 min submersion to the irrigation solutions. Values are shown as the mean. NaOCl, sodium hypochlorite; EDTA, etylenediaminetetraacetic acid; HEBP, hydroxyethylidene bisphosphonate.
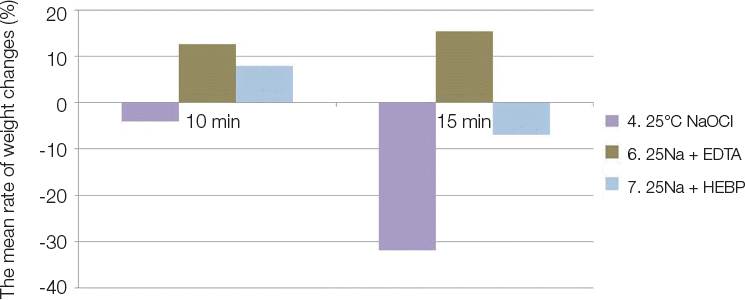
(2) 온도 증가에 따른 조직 용해 능력
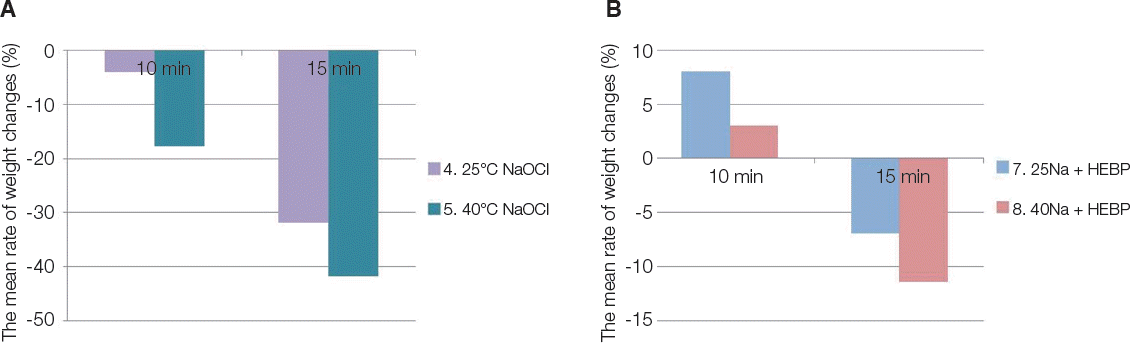
가열된 NaOCl 용액(40°C)은 더 높은 조직용해능력을 갖는다(
Fig. 4). 시간이 지나면서 Group 5는 Group 4 보다 더 큰 무게의 감소를 보이며, 15분 후에는 유의한 차이가 있었다(
P < 0.05). Group 8은 Group 7 보다 더 큰 무게의 감소를 보이나 두 그룹 사이에 유의한 차이는 나타나지 않았다.
Fig. 4
The effect of temperature increase. These graphs show comparisons of the mean rate of weight change (%) of 25°C and 40°C groups after 10 min and 15 min of submersion to G4 and G5 (A), G7 and G8 (B). Values are shown as the mean. NaOCl, sodium hypochlorite; HEBP, hydroxyethylidene bisphosphonate.
2. 항균효과
EDTA group에서 가장 넓은 미생물 억제대를 보였고, 다음으로 1% NaOCl group이 항균효과를 보였다(
Table 4). HEBP 만 사용한 경우와 대조군(증류수)의 경우 미생물 억제의 효과가 나타나지 않았다. NaOCl/EDTA 혼합용액은 EDTA만 사용한 경우와 비교 시 유의미한 감소가 나타났다(
P < 0.05). 반면, NaOCl/HEBP 혼합물은 순수한 NaOCl 용액만 사용한 경우와 비교 시 미생물억제대의 경우 유의한 차이가 나타나지 않았다. 이 혼합물은 전통적인 NaOCl 용액의 항균효과를 저해하지 않는다.
Table 4
Zones of inhibition (mm) against organisms (agar diffusion test)
|
Group A (NaOCl) |
Group B (EDTA) |
Group C (NaOCl/EDTA) |
Group D (HEBP) |
Group E (NaOCl/HEBP) |
Group F (Saline) |
|
Mean |
7.675 |
15.938 |
11.338 |
0.000 |
7.313 |
0.000 |
|
Standard deviation |
1.309 |
1.374 |
1.151 |
0.000 |
0.897 |
0.000 |
고찰
이번 실험에서는 상아질 내 도말층을 제거하기 위한 근관 세정제로서 soft cheating agent 인 1-hydroxyethlidene-1,1,-bisphosphonate (HEBP)를 사용하여 조직 용해 능력과 항균작용에 대하여 평가하였다. HEBP는 독성이 없어 골 질환 치료 시 일반적으로 사용되며, 가정 내에서 건강 보조제와 개인 생활용품으로도 사용된다.
7 HEBP는 NaOCl과 반응하지 않으며 NaOCl과 혼합되어도 킬레이트 능력이 유지되어 기구 조작하는 동안에도 문제 없이 사용할 수 있다.
6 HEBP의 도말층에 대한 작용을 연구한 Kruvilla 등에 의하면 HEBP는 치근의 cervical과 middle 부위에서 EDTA, maleic acid와 유사한 도말층 제거 능력을 보이나, 치근단 부위에서는 EDTA와는 비슷하지만 maleic acid보다는 저하된 도말층 제거 효과를 보인다.
8 하지만 soft chelating agent 임에도 불구하고 근관 내로부터 용출된 칼슘 이온의 양은 약한 알칼리성 환경에서 EDTA와 비슷하다.
9 HEBP로 처리한 치근상아질은 다른 킬레이팅 제재와 비교 시에 가장 높은 미세경도를 보인다.
10 이것은 HEBP로 처리한 경우 EDTA로 처리한 상아질보다 상아세관 면적이 작고 관간 상아질 면적은 더 넓어지기 때문이다. 또한 상아질 접착의 대부분도 상아세관보다는 관간 상아질에 있는 교원질 기질과의 미세 기계적 유지에 의해 얻어지므로 HEBP를 처리한 상아질 접착이 더 유리할 것이다.
11
조직의 용해 능력을 비교한 실험에서, 초기 5분 동안 모든 표본의 무게가 증가하는 것을 관찰할 수 있다. 이것은 조직의 수화과정의 결과로 일어난다. NaOCl만 사용한 그룹에서 가장 빠르게 조직용해가 나타나며 이어서 NaOCl과 HEBP를 혼합하여 사용한 그룹에서 다음으로 큰 무게 변화의 폭이 나타났다. 이 것은 HEBP를 단독으로 사용하였을 때는 조직용해능력을 갖지 못하지만, HEBP와 NaOCl을 혼합하여 사용시에는 NaOCl의 조직용해 능력에 영향을 미치지 않는다는 기존의 연구 결과와 어느 정도 일치하였다.
6 하지만 이번 실험에서는 NaOCl 단독으로 사용했을 때보다는 조직용해능력이 조금 감소하는 효과가 나타났다. NaOCl과 EDTA를 혼합하여 사용한 그룹에서는 거의 무게변화가 나타나지 않았다. Grawher 등의 실험에서 EDTA는 NaOCl 용액 존재하에서도 킬레이트 반응을 일으킬 수 있는 능력이 유지되나 NaOCl 용액은 EDTA의 존재 시 유효 염소 농도가 0.5%에서 0.06%로 현저히 감소되어 조직 용해능력이 감소됨이 밝혀졌다.
5
가열된 NaOCl (40℃)를 사용시에 실온의 NaOCl (25° C)를 사용시 보다 더 큰 조직용해능력을 보였고, NaOCl과 HEBP를 혼합하여 사용한 경우에도 유의미하지는 않지만 가열된 그룹에서 더 큰 조직용해능력이 나타났다.소의 인대에서 추출한 교원질을 이용하여 실온(21°C)과 체온(37°C)에서 2.6%와 5.2% NaOCl 용액의 교원질 용해 능력을 비교한 결과 37°C 2.6% NaOCl 용액은 21°C, 37°C 5.2% NaOCl 용액과 동등한 조직용해 능력을 보였다.
12 조직용해 능력 뿐만 아니라 NaOCl의 항균 효과는 5 - 60 범위 내에서 온도가 5°C 오를 때 두 배 증가한다고 밝혀졌다.
13
이번 실험에서는
E. faecalis에 대한 근관 세정제의 항균 효과를 관찰하였다.
E. faecalis는 구강 내에서 가장 저항성이 높은 세균종이며 종종 근관 내 재감염을 일으키기도 한다. 따라서 근관 세정재 및 첩약제의 항균효과 및 감수성을 평가하는데 흔히 이용되는 세균종이다.
14 이 실험에서는 EDTA group에서 가장 넓은 미생물 억제대가 나타났다. Siqueira 등의 실험에 의하면 agar diffusion model을 이용한 연구에서
E. faecalis에 대한 항균작용은 EDTA group이 0.5% NaOCl보다는 뛰어나나 2.5% NaOCl보다 낮은 값을 나타냈다.
14 이번 실험에 의하면 EDTA의 항균 작용이 1% NaOCl보다도 뛰어난 것으로 추정된다. 하지만 임상적으로 감염된 상아질 내에서 EDTA의 항균효과는 미미하게 나타난다. 그 이유는 근관계 내에서 EDTA는 치아 경조직과 반응하여 비활성화되기 때문이다.
15 이번 실험에서 HEBP 단독적으로 사용시에 항균효과가 나타나지 않았으며 이것은 기존의 연구와도 일치한다.
6 1% NaOCl을 단독으로 사용한 그룹과 NaOCl과 HEBP의 혼합물의 미생물저해영역에는 유의한 차이가 나타나지 않았다. 이것은 항균효과가 활성화된 자유 염소기에만 영향을 받는데, NaOCl과 HEBP를 혼합한 경우에도 활성화된 자유 염소기가 안정적으로 유지되기 때문으로 추정된다. 따라서 NaOCl와 HEBP 혼합물은 근관 치료 동안 혹은 최종 근관 세정제로서 사용될 수 있다.
6
이번 연구에서는 조직용해능력을 평가하기 위하여 소의 근육 조직을 이용하였다. 이전의 다른 조직 용해 능력을 평가하는 연구들에서도 소의 치수조직이나, 돼지의구개 점막, 쥐의 dermal connective tissue 등이 사용되었다. 인간 치수 조직과 다른 유형의 조직을 사용하는 이유는 쉽게 표본을 표준화 시킬 수 있기 때문이다. 그러나 이러한 조직들은 임상적으로 인간의 근관 내의 환경을 재현하지 못한다는 한계가 있어 아쉽다. 조직 용해 능력은 세정제의 양, 실험 조직의 단면적, 교반 횟수 등 여러 가지 요소들에 영향을 받는다.
16 따라서 이번 연구에서 표본의 단면적을 균일하게 하기 위해 노력하였으며, 일정량의 근관 세정제를 사용하기 위해 노력하였다
항균 효과를 평가하기 위해서 agar diffusion test를 사용하였다. 그러나 상아질 기질 내에서 세정제의 항균효과를 배양 방법을 사용하여 평가하는 것은 한계가 있다.이 것은 박테리아가 검출된 곳이 치수강의 어느 부위인지 정확이 알 수 없으며, 근관벽 혹은 상아세관 내부에 잔존하는 부착 biofilm 내에 잔존 박테리아를 확인할 수 없다. 최근에는 confocal microscopy를 사용하여 부착된 세포의 방해 없이 상아세관 내부에 살아있는 박테리아를 확인하고 정량화 하는 방법을 사용하기도 한다.
17 따라서 Biofilm을 확인하는 agar diffusion test 뿐만 아니라 상아세관 내의 박테리아를 확인하는 Confocal laser scanning microscopy 실험이 추가적으로 필요할 것이다.
결론
이번 연구에서 Soft Chelating agent 인 HEBP는 NaOCl의 항균 효과를 방해하지 않는다. HEBP와 NaOCl의 혼합물은 기존의 킬레이팅 제재인 EDTA와 NaOCl의 혼합물과 비교 시, NaOCl의 조직 용해 능력에 미치는 영향이 작다. 하지만 NaOCl 단독으로만 사용했을 때와 비교시에는 저하된 조직 용해 능력이 나타났다. 가열된 NaOCl, NaOCl과 HEBP의 혼합재제는 실온과 비교 시에 효율적으로 조직을 용해할 수 있다. 따라서 근관 치료 동안 NaOCl과 동시에 도말층을 제거하는 근관세정제로서 사용할 수 있다.







 PDF
PDF Citation
Citation Print
Print




 XML Download
XML Download