Abstract
Antibody-drug conjugates (ADCs) represent a promising therapeutic treatment for cancer patients by combining the antigen-targeting specificity of monoclonal antibodies (mAbs) with the cytotoxic potency of chemotherapeutic drugs. ADCs consist of three components, mAbs specific for ad tumor antigen, a linker species, and a cytotoxic payload. ADCs offer selective delivery of cytotoxic agents into targeted cancer cells, thereby allowing for reduced general cellular cytotoxicity caused by chemotherapeutic agents through antibody mediated specific recognition of tumor antigen. Ideally, in blood, after systemic administration, ADCs are nontoxic. Upon binding of the antibody to the targeted tumor antigen and internalization of the complex into the cancer cell, the drug is then released in its active form and in sufficient quantity to kill the cell. ADCs technology has been an active area of research in recent years, resulting in a number of ADCs in development for various tumor types. ADCs are able to be new treatment options for head and neck cancer. The number of ADCs undergoing clinical trial will further increase, possibly replacing some of the existing mAbs, and becoming the next generation of anticancer biotherapeutics.
두경부암은 전 세계적으로 연간 60만 명의 신환자가 발생하는 암으로 기관별 암 발생률이 6번째를 차지하고 있다[1]. 최근 새로운 암 치료법들이 급격히 개발되고 있는 가운데 암에 대한 치료율이 점차 향상되고 있지만, 진행성 두경부암의 경우에서 5년 생존율은 아직 50%를 넘지 못하고 있다. 예후가 좋지 않은 이유로는 암의 공격적인 침습, 림프절 전이, 원격 전이와 이차 암 등을 들 수 있는데, 이를 극복하기 위한 다양한 연구와 치료에도 불구하고 지난 20년간 생존율이 크게 변하지 못한 상태이다. 두경부암에서의 치료는 수술, 방사선 치료, 항암 치료가 주를 이루고 있고, 최근에는 일반적인 항암 치료와 방사선 치료 이상의 효과를 보이고 치료 부작용을 줄일 수 있는 종양세포에 특이적인 표적치료가 크게 주목을 받고 있다. 하지만 개발되는 치료제마다 내인성 혹은 후천성 기전에 의해 다양한 경로로 치료에 대한 저항성이 보고되고 있으며, 이를 극복하려는 방법으로 두 개 이상의 약제 병합치료가 사용되기도 하지만 세포 독성이 증가하는 부작용이 발생한다.
항체-약물 중합체(antibody-drug conjugate)는 항암제의 독성을 줄이고 다양한 기전의 저항성을 극복할 수 있는 새로운 패러다임의 하나로 관심을 받고 있는데, 이는 일반적 항체의 장점인 세포 특이적인 효과를 최대로 활용하여 암세포만을 주로 공격할 수 있는 데 초점을 맞춘 기술로 암세포의 표면에 발현된 특정 항원에 특이적으로 결합하는 항체를 사용하여 세포 독성 약물을 종양세포에만 전달하는 방법이다[2,3]. 두경부암에서도 epidermal growth factor receptor(EGFR)와 같은 발현 증가한 수용체들이 있어 항체-약물 중합체가 치료제로 적용 가능성이 있으므로, 새로운 치료 분야로 자리를 잡기 시작한 항체-약물 중합체에 대해 고찰해 보고자 한다.
항체-약물 중합체의 개념은 1세기경 독일의 Paul Ehrlich가 세포 독성 약물을 선택적으로 세포에 전달하는 개념을 ‘magic bullet’이라고 표현한 것에서 시작했다고 볼 수 있다[4]. 1958년에 methotrexate(MTX)를 백혈병 세포를 표적으로 하는 항체에 결합하여 사용되었다. 1975년 Kohler와 Milstein의 hybridoma 기술을 이용한 생쥐의 단일클론항체(monoclonal antibody, mAb)를 바탕으로 항체 연구가 획기적으로 발전하였고, 1988년 항체 공학의 발전으로 인간화 단일클론항체가 보고되고 생산되기 시작하였다[5]. 이후 치료용 항체 분야가 급속도로 발전하여 키메릭 단일클론항체(chimeric mAb), 인간화 단일클론항체(humanized mAb), 인간 단일클론항체(fully human mAb)의 제조기술은 발전을 거듭하였다. 초기 항체-약물 중합체에는 MTX, 5-fluorouracil 같은 대사길항물질, mitomycin 같은 DNA crosslinker, vinblastine 같은 항미세소관 약제가 사용되었으나 미미한 효과, 정상 세포 독성, 항체-약물 중합체 링커의 불안정성으로 실패를 하였다. 2000년 처음으로 MylotargⓇ(gemtuzumab ozogmicin; Pfizer/Wyeth-Ayerst Pharmaceuticals Inc., Philadelphia, PA, USA)가 FDA 승인을 받았지만, 생존율의 증가가 보이지 않아 임상시험에 실패를 하였으나, 2011년 AdcetrisⓇ(brentuximab vedotin; Seattle Genetics, Bothell, WA, USA)가 두 번째로 FDA 승인을 받아 호지킨 림프종에 사용되고 있다. 최근에는 KadcylaⓇ(trastuzumab ematacin; Genentech, San Fransisco, CA, USA)가 FDA 승인을 받고 Her2 양성 유방암에서 사용되고 있다. 현재까지 30여 가지의 항체-약물 중합체가 개발되고 임상시험 중이며, 곧 새로운 치료의 분야로 자리를 잡을 것으로 보인다[6-12].
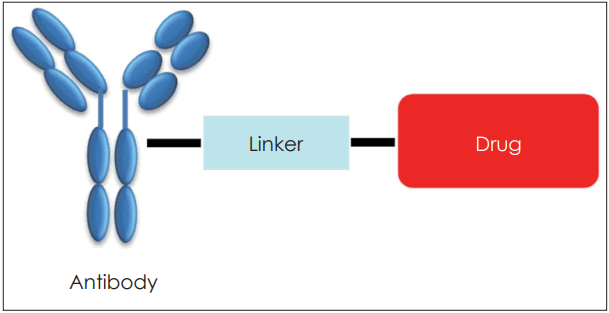
치료용 항체(therapeutic antibodies)는 제약산업에서 가장 빠른 성장을 보이며 2014년 47개의 항체치료제가 생산되었고, 2020년까지 매년 10%의 높은 성장률을 보일 것으로 전망하고 있으며, 70여 개의 항체치료제가 생산될 것으로 예상한다[13]. 이러한 항체치료제와 더불어 항체 공학기술의 발달 때문에 보다 새로운 항체의약품이 개발되고 있다. 항체의 치료 효과를 높이기 위한 것으로 항체와 약물을 결합해 암세포 특이항원에 선택적으로 항체 결합하여 효율적으로 항체와 약물이 동시에 암세포를 공격할 방법이 있다. 이러한 기술을 항체-약물 중합체 합성이라 하는데, 항체-약물 중합체는 단일클론항체, 약물 그리고 항체와 약물을 연결하는 링커를 포함한 세 가지 구성요소로 되어 있다(Fig. 1).
항체-약물 중합체에 사용될 항체는 암세포에서는 발현이 높고, 정상 세포에서 발현이 낮은 항원에 결합할 수 있는 것으로 선택되어야 효과적이다. 이는 암세포에 특이적으로 작용하고 적은 용량으로도 치료 효과를 볼 수 있을 뿐만 아니라 정상 세포에 대한 세포 독성을 줄일 방법이기도 하다. 링커는 항체와 약물의 양쪽에 결합할 수 있어야 하는데, 항체의 cysteine이나 lysine에 결합하거나 항체의 이황화 결합부위에 결합할 수 있다[3]. 링커는 혈액 내에서 안정해야 하며 암세포에 도달하기 전까지 약물이 항체로부터 분리되는 것을 막을 수 있어야 한다. 항체-항원 결합에 영향을 주지 않기 위해서 약물과 결합하기 전의 항체와 같은 친화력을 유지할 수 있도록 해야 하며, 항원과 결합한 이후에는 분리될 수 있어야 한다. 또한, 약물과 항체의 비율(drug antibody ratio)은 항체-약물 중합체의 효능에 중요한 요건이다. 다시 말해 항체에 많은 약물이 붙어 있을수록 항체-약물 중합체는 효과적이라고 할 수 있다[14,15].
항체-약물 중합체가 암세포에 결함한 후에는 수용체 매개세포내섭취(receptor-mediated endocytosis)에 의해 세포 내로 인터널리제시션(internalization)되는데, 충분한 농도의 활성 약물이 세포 내로 들어가야 하지만 일반적으로 항체-항원의 인터널리제이션은 비효율적이고 세포 표면에 있는 항원의 수도 일반적으로 1×105 receptors/cell 이하로 제한되어 있어서 매우 강력한 약물을 사용하여 낮은 농도의 약물에서도 충분히 암세포를 죽일 수 있어야 한다[14,15]. 항체에 결합되어 항체-약물 치료제로 사용될 약물은 보편적으로 사용되는 항암제보다 100~1000배 이상 세포 독성이 있는 약물을 선정하는 이유이다. 유사분열에 관여하는 미세소관(microtubule)을 억제하는 약물이 AdcetrisⓇ와 KadcylaⓇ에서 사용되었고, DNA 구조를 파괴하는 약물이 MylotargⓇ에서 사용되었다.
현재 항체의 대량생산은 미국, 유럽에서 진일보하여 상용화되었지만, 안정적이면서 목표지점에 원하는 양만큼 방출시킬 수 있는 링커 개발은 현재까지는 몇몇 회사에 국한되어 있다. 항체-약물 중합체의 링커는 절단 가능한 링커(cleavable linker)와 절단 불가능한 링커(noncleavable linker)로 분류할 수 있다. 절단 가능한 링커는 세 가지가 다른 메커니즘으로 분류할 수 있다[16,17]. 1) 리소좀 단백질가수분해효소(protease)를 활용한 링커는 특정 dipeptide를 인식하는 cathepsin B 효소의 특성을 활용하여 약물을 방출하는 방법이고, 이 링커는 체액내 안정성과 세포 내 단백질가수분해 절단의 적합한 균형을 잘 이룬 연구로서 valine-citrulline dipeptide linker가 사용되며, 이러한 기전을 이용하여 AdcetrisⓇ가 개발되었다. 2) 산도 변화에 따른 링커 기술(acid cleavable linker)은 혈액의 pH 7.3~7.5에서는 안정적인 상태로 존재하다가 리소좀의 낮은 pH 4.5~5에서는 링커 안에 있는 하이드라존(hydrazone) 부분이 산에 반응하여 가수분해됨으로 약물을 방출하는 기술이다. MylotargⓇ(anti-CD33 calicheamicin conjugate) 개발에 사용되었고 최근에는 inotuzumab ozogamicin(anti-CD22 calicheamicin conjugate)에 하이드라존 링커가 사용되었다. 3) 글루타싸이온 반응 링커(Glutathione sensitive linker)는 혈액과 비교했을 때 세포 내 농도가 높은 glutathione을 활용해 혈액 내 순환을 할 동안에는 안정성을 유지하다가 세포 내로 들어오면 글루타싸이온이 링커 안에 있는 disulfide-bond를 환원시킴으로 약물을 방출하는 기술로써, 더 안정성을 부여하기 위하여 메틸기(methyl group)을 도입했으며, 이 링커를 활용하여 SAR3419(anti-CD19 maytansine), IMGN901(anti-CD56 maytansine)과 AVE9633(anti-CD33 maytansine) 등이 임상 시험 중이다[18-24].
비절단 링커(non-cleavable linker)를 사용하는 것으로 이 방법은 항체-약물 중합체가 세포 내 인터널리제이션이 되면 항체가 온전히 리소좀 안에서 분해됨으로써 약물을 방출하는 방법으로써 이 링커의 최대 장점은 혈액 내 링커가 안정하다는 것이고, 이 방법을 활용하여 KadcylaⓇ가 개발되었다. 링커의 개발은 계속 발전되고 있으며, 암 관련 효소인 legumain과 단백질 분해효소는 아니지만, 선택적 절단 능력이 있는 β-glucuronidase, β-galactosidase를 활용한 링커들도 현재 개발 중이다[17-19].
차세대 항체-약물 중합체는 현재까지 개발된 링커보다 암세포에 도달할 때까지 분해되지 않고 더 안정하게 암세포에 도달할 수 있게 개발하는 것이 핵심이다. 또한, 기존의 항체-약물 중합체는 약물로 세포 독성항암제를 사용했다면 차세대 항체-약물 중합체에는 표적 항체와 표적항암제의 결합형태라 할 수 있다. 새로 개발되고 있는 표적치료제들을 이용하여 항체-약물 중합체 개발이 가능할 것으로 보고 있다[25,26]. 최근에는 면역항암제가 개발되고 많은 관심이 집중되고 있으며, 다양한 면역항암제가 신약으로 개발되고 있어서, 항체-약물 중합체의 파이프라인이 증가한다고 할 수 있다. 다양한 형태로의 항체-약물 중합체의 개발은 기존 항암제들이 갖지 못한 새로운 항암 효과에 대한 적응증 확대의 가능성을 열어두고 있을 것으로 생각한다. 항체 기술이 급속히 발전하고 있지만, 단백질과 저분자 물질에 대한 연구가 활발히 이루어지고 있어서 단백질-약물 중합체(protein-drug conjugate)가 항체-약물 중합체가 차세대로 사용될 수 있는 새로운 약물이라고 할 수 있다.
두경부 편평상피암종의 대부분은 EGFR이 높게 발현되어 있어 EGFR 표적치료제에 효과가 있다고 알려져 있다. 하지만 EGFR 표적치료에 10~20%에서만 반응을 보이고 대부분에서 유의한 반응을 보이지 않는다. 초기에 효과가 있는 경우에도 EGFR 표적치료제를 투여하게 됨에 따라서 후천성 저항성을 보이게 된다. EGFR 표적치료제의 한계를 보이기 때문에 항EGFR 항체에 약물을 중합해서 사용하는 항체-약물 중합체는 이론적으로 두경부암 치료에서는 획기적인 방법일 수 있다. 이 경우에는 항EGFR 항체는 치료적 효과를 보이는 경우도 있겠지만, 운반체 역할을 담당할 것으로 생각된다. 향후 두경부암에 대한 더 효과적인 항EGFR 표적치료제가 개발된다면 더욱더 효과적인 항체-약물 중합체가 개발될 수 있을 것이다[27-29].
항EGFR 항체에 결합한 약물로 두경부암에서 많이 쓰이는 cisplatin, paclitaxel 같은 항암제를 사용하여 항체-약물 중합체를 만들 수 있다. 하지만 이러한 약제보다는 더 효능이 좋은 항암제가 항EGFR 항체에 결합하는 것이 두경부암 치료에 의미가 있을 것으로 생각되며, 두경부암에 사용가능하나 세포 독성이 심해서 사용할 수 없었던 항암제를 발굴해서 후보물질로 사용할 수 있을 것으로 보인다. 링커에 대한 기술이 발전한다면 항체-약물 중합체가 혈액 내에서 덜 분해되고, 암세포에 결합한 후에도 효과적으로 세포 내로 들어가 작용할 수 있을 것으로 보이며, 기존에 사용하고 있던 항암제로도 충분한 효과를 보일 수 있을 것으로 생각된다.
항체-약물 중합체는 암세포에 특이적으로 작용하고, 약물에 대한 효과를 최대화하며, 정상 세포에 부작용을 최소화할 수 있는 특징이 있다. 또한, 재발하거나 전이가 있는 암에서도 암세포 독성이 높은 약물을 사용할 수 있어서 효과를 기대해 볼 수 있다는 장점이 있다. 항체-약물 중합체는 치료 영역을 확대하고 발전해 나가고 있다는 과정에 있으며, 암 치료제의 발전과 함께 더욱더 효과적인 항체-약물 중합체들이 개발되고 있다. 항체-약물 중합체는 재발 암이나 전이성암 등 치료가 잘 안 되는 암에 있어서 치료 효과를 거둘 수 있다고 본다. 진행성 두경부암에서 현재까지의 다양한 치료에도 불구하고 만족스러운 결과를 얻고 있지 못하고 있으므로 새로 개발되고 있는 치료법들을 두경부암에서도 적용할 수 있어야 할 것이다. 항체-약물 중합체도 링커 기술개발과 함께 항체치료제의 발전과 더불어 암 치료의 영역으로 자리를 잡을 수 있을 것이다. 향후 두경부암 영역에서의 치료에도 항체-약물 중합체를 사용할 시기가 다가올 것으로 생각된다.
REFERENCES
2. Parslow AC, Parakh S, Lee FT, Gan HK, Scott AM. Antibody-drug conjugates for cancer therapy. Biomedicines. 2016; 4(3):E14.

3. Panowski S, Bhakta S, Raab H, Polakis P, Junutula JR. Site-specific antibody drug conjugates for cancer therapy. MAbs. 2014; 6(1):34–45.

5. Perez HL, Cardarelli PM, Deshpande S, Gangwar S, Schroeder GM, Vite GD, et al. Antibody-drug conjugates: current status and future directions. Drug Discov Today. 2014; 19(7):869–81.

6. Sievers EL, Larson RA, Stadtmauer EA, Estey E, Löwenberg B, Dombret H, et al. Efficacy and safety of gemtuzumab ozogamicin in patients with CD33-positive acute myeloid leukemia in first relapse. J Clin Oncol. 2001; 19(13):3244–54.

7. Linenberger ML, Hong T, Flowers D, Sievers EL, Gooley TA, Bennett JM, et al. Multidrug-resistance phenotype and clinical responses to gemtuzumab ozogamicin. Blood. 2001; 98(4):988–94.

8. Younes A, Bartlett NL, Leonard JP, Kennedy DA, Lynch CM, Sievers EL, et al. Brentuximab vedotin (SGN-35) for relapsed CD30-positive lymphomas. N Engl J Med. 2010; 363(19):1812–21.

9. Senter PD, Sievers EL. The discovery and development of brentuximab vedotin for use in relapsed Hodgkin lymphoma and systemic anaplastic large cell lymphoma. Nat Biotechnol. 2012; 30(7):631–7.

10. LoRusso PM, Weiss D, Guardino E, Girish S, Sliwkowski MX. Trastuzumab emtansine: a unique antibody-drug conjugate in development for human epidermal growth factor receptor 2-positive cancer. Clin Cancer Res. 2011; 17(20):6437–47.

11. Verma S, Miles D, Gianni L, Krop IE, Welslau M, Baselga J, et al. Trastuzumab emtansine for HER2-positive advanced breast cancer. N Engl J Med. 2012; 367(19):1783–91.

12. Mullard A. Maturing antibody-drug conjugate pipeline hits 30. Nat Rev Drug Discov. 2013; 12(5):329–32.

13. Ecker DM, Jones SD, Levine HL. The therapeutic monoclonal antibody market. MAbs. 2015; 7(1):9–14.

14. Ritchie M, Tchistiakova L, Scott N. Implications of receptor-mediated endocytosis and intracellular trafficking dynamics in the development of antibody drug conjugates. MAbs. 2013; 5(1):13–21.

15. Tsuchikama K, An Z. Antibody-drug conjugates: recent advances in conjugation and linker chemistries. Protein Cell. 2016; Oct. 14. [Epub ahead of print]. https://doi.org/10.1007/s13238-016-0323-0.

16. Sassoon I, Blanc V. Antibody-drug conjugate (ADC) clinical pipeline: a review. Methods Mol Biol. 2013; 1045:1–27.

17. McCombs JR, Owen SC. Antibody drug conjugates: design and selection of linker, payload and conjugation chemistry. AAPS J. 2015; 17(2):339–51.

18. Dubowchik GM, Firestone RA. Cathepsin B-sensitive dipeptide prodrugs. 1. A model study of structural requirements for efficient release of doxorubicin. Bioorg Med Chem Lett. 1998; 8(23):3341–6.

19. Dubowchik GM, Firestone RA, Padilla L, Willner D, Hofstead SJ, Mosure K, et al. Cathepsin B-labile dipeptide linkers for lysosomal release of doxorubicin from internalizing immunoconjugates: model studies of enzymatic drug release and antigen-specific in vitro anticancer activity. Bioconjug Chem. 2002; 13(4):855–69.

20. Doronina SO, Toki BE, Torgov MY, Mendelsohn BA, Cerveny CG, Chace DF, et al. Development of potent monoclonal antibody auristatin conjugates for cancer therapy. Nat Biotechnol. 2003; 21(7):778–84.

21. Ducry L, Stump B. Antibody-drug conjugates: linking cytotoxic payloads to monoclonal antibodies. Bioconjug Chem. 2010; 21(1):5–13.

22. Hamann PR, Hinman LM, Hollander I, Beyer CF, Lindh D, Holcomb R, et al. Gemtuzumab ozogamicin, a potent and selective anti-CD33 antibody-calicheamicin conjugate for treatment of acute myeloid leukemia. Bioconjug Chem. 2002; 13(1):47–58.

23. Sapra P, Hooper AT, O’Donnell CJ, Gerber HP. Investigational antibody drug conjugates for solid tumors. Expert Opin Investig Drugs. 2011; 20(8):1131–49.

24. Ciardiello F, Tortora G. EGFR antagonists in cancer treatment. N Engl J Med. 2008; 358(11):1160–74.

25. Vankemmelbeke M, Durrant L. Third-generation antibody drug conjugates for cancer therapy--a balancing act. Ther Deliv. 2016; 7(3):141–4.
26. Gébleux R, Casi G. Antibody-drug conjugates: current status and future perspectives. Pharmacol Ther. 2016; 167:48–59.

27. Wheeler DL, Huang S, Kruser TJ, Nechrebecki MM, Armstrong EA, Benavente S, et al. Mechanisms of acquired resistance to cetuximab: role of HER (ErbB) family members. Oncogene. 2008; 27(28):3944–56.





 PDF
PDF Citation
Citation Print
Print


 XML Download
XML Download