Abstract
Dermatofibrosarcoma protuberans is a rare type of cancer, a soft tissue sarcoma that develops in the deep layers of skin. It is a locally aggressive tumor with a high recurrence rate but the metastasis rarely occurs. The first sign of dermatofibrosarcoma protuberans is often a small bump on the skin. It may resemble a deep-seated pimple of rough patch of skin. The tumor typically grows slowly and can become a raised nodule. Therefore, it is likely to be misdiagnosed as keloid, basal cell carcinoma and scleroderma. We recently experienced a case of dermatofibrosarcoma protuberans in a 63-year-old man, who presented with anterior lower neck mass. We present this case with a review of the literature.
융기성 피부섬유육종(deromatofibrosarcoma protuberans)은 진피와 지방조직에 걸쳐 섬유아세포가 파괴성으로 증식되어 발생하는 드문 종양으로 연조직 육종의 5% 미만, 두경부 육종의 4~10%를 차지하는 저등급의 피부육종이다[1]. 30~40 세에 호발하고, 남성에서 7:3의 비율로 많다. 두피에 가장 많이 발생하고, 그 외 안면부과 경부에 발생한다[2].
융기성 피부섬유육종은 붉은색이나 청색을 띠고 손가락으로 누르면 창백해지는, 융기되고 경화된 무통성의 판 또는 결절로 나타난다. 국소재발률이 매우 높은 반면, 원격전이는 아주 드물고 천천히 자라기 때문에 진단이 늦어지고 결절 형태를 보이므로 켈로이드, 기저세포암, 피부경화증으로 오진 되기 쉽다[3]. 그 결과 경부에서 발생하는 경우는 단순 양성종양으로 생각하고 적절한 치료시기를 놓치기가 쉽다.
본 증례는 단순 켈로이드로 진단되고 치료받은 융기성 피부섬유육종 증례를 경험하였기에 문헌고찰과 함께 보고하는 바이다.
63세 남자 환자가 내원 8년 전부터 서서히 커지는 경부 전하방종물을 주소로 본원 피부과에 내원하였다. 환자는 과거력상 당뇨병으로 투약 중이었으며 10여 년 전에 전경부에 작은 상처를 경험한 일이 있었다. 신체검사상 경부 전하방 부위에 약 8×4 cm 크기의 무통성이며 단단한 종괴가 촉지되었다(Fig. 1).
지속적인 피부과적 치료에도 불구하고 종물은 점점 커져 본원 성형외과에 의뢰되었다. 환자의 과거 병력과 경험상 켈로이드(Keloid)로 의심되어 종물절제 후 피부 이식을 통한 재건을 계획하였다. 수술 전 시행한 경부전산화단층촬영에서 조영증강이 되는 8×4 cm의 종물이 경부 전하방부에 있었고 우측 피대근(strap muscle)으로 침윤이 의심되었으나 켈로이드로 의심하고 이에 대한 추가 평가는 이루어지지 않았다(Fig. 2).
성형외과에서 종물 절제생검을 계획하였고 전신마취하에 종물을 절제하였고, 술 중 시행한 동결절편 병리검사결과 육종(sarcoma)으로 의심되는 결과를 받았다. 그러나 성형외과에서는 켈로이드가 너무나도 확실해 보였고, 동결절편 병리 검사 결과가 확실한 육종으로 확진할 수 없기에, 추후 악성 진단이 내려지면 추가 수술을 고려하고 절제 부위에 대한 재건 없이 그대로 수술을 마쳤다(Fig. 3). 이후 조직 생검에서 융기성피부섬유육종(deromatofibrosarcoma protuberans)으로 진단되었다. 조직검사상 진피층의 방추형 세포(spindle cell)가 나선형으로 밀집되어 있었으며 핵의 다형성(nuclear pleomophism)이나 유사분열은 거의 관찰되지 않았다(Fig. 4A). 면역조직화학적 검사에서 CD34에 양성 반응을 보인 반면(Fig. 4B), CD31, smooth muscle actin(SMA), S-100 protein 에는 음성 반응을 보여 융기성 피부섬유육종에 합당한 소견을 보였다(Fig. 4C and D). 심부 및 외측 절제연에서 악성세포가 발견되었고 광범위절제와 향후 치료 위해 이비인후과에 의뢰되었다.
이비인후과적 검사에는 특이소견이 없었으며 경부 CT, MRI 에서 특별한 소견은 관찰되지 않았다. 양전자단층촬영에서는 수술에 의한 것으로 보이는 표준섭취계수 2.8의 과대사 병변만 관찰되었다. 피부섬유육종은 절제부위에서 자주 재발하는 특성을 가진 종양이므로 최초의 CT 소견을 기준으로 종양에서 3 cm의 절제연을 두고 종양을 제거하는 계획을 세웠으며, 양측 피대근(strap muscle), 흉쇄유돌근(sternocleidomastoid muscle)의 내측부위, 양측 갑상선의 내측부위 및 협부(isthmus)부위를 절제하였다. 이어 양측 경부 level III, IV, VI 림프절 곽청술을 시행하였다(Fig. 5). 동결절편 결과 절제연의외측, 상부, 하부 및 심부절제연에서 악성세포는 발견되지 않았다.
이후 대흉근피판(pectoralis major myocutaneous flap)을 이용하여 결손부위를 재건하였다(Fig. 6). 국소 재발이 많은 종양이기에 재발 방지를 위해 방사선 치료를 시행하였으며 외래 경과 관찰 결과 수술 후 3개월이 지난 현재까지 재발의 증거는 보이지 않고 있다.
융기성 피부섬유육종은 비교적 드문 중등도의 악성 종양으로 0.5 cm에서부터 20 cm에 이르기까지 다양한 크기로 보고 되며, 전체 종양의 0.1% 이하를 차지한다[4]. 증상은 주위 피부의 모세혈관확장증이 동반된 분홍색의 판(plaque)형태로 시작하여 결절(nodule)의 형태로 성장한다. 서서히 자라기 때문에 진단되기까지 대부분 오랜 시간이 경과된다[5].
융기성 피부섬유육종의 병인은 확실히 알 수 없으나 외상의 경력을 10~20%에서 찾아볼 수 있으며[6], 화상을 입은 부위나 수술 후 반흔조직에서 이 종양이 발생되었다는 보고들이 있다[7]. 따라서 켈로이드와 감별이 어렵다.
융기성 피부섬유육종은 자라면서 점차 피부뿐만 아니라 피부 아래의 근막, 근육, 골까지도 침범한다. 말기에는 성장률이 가속화되고 궤양, 출혈, 그리고 통증을 일으킨다[4].
최근에는 보다 정확한 진단을 위해 Aiba 등[8]이 항 CD34 항체를 이용한 면역조직화학염색으로 융기성 피부 섬유 육종의 진단과 감별에 사용되고 있다. 수술 전 조직생검이 가장 확실한 진단방법이며 본 증례에서는 절제생검을 실시하였다.
감별진단으로는 켈로이드, 피부섬유종(dermatofibroma), 양성 섬유성조직구종(benign fibrous histiocytoma) 등의 중간엽 종양(mesenchymal tumor)이 있으며 면역조직화학검사가 감별에 도움이 된다. 방추세포는 특징적으로 피부섬유종에 양성인 factor XIIIa, 멜라닌 세포에 양성인 S-100, 평활근종양에 양성인 SMA에 염색되지 않는 반면, CD34에 대하여서는 세포질 내에 강하게 염색된다. 본 증례에서도 CD34에 대하여 양성인 반면, S-100 및 SMA에 대하여 음성이었다. 반면 켈로이드는 조직학적으로 비정상적으로 많은 콜라겐 다발 복합체(collagen bundle complexes)를 확인할 수 있다[9].
치료는 광범위 절제가 치료원칙이며 발생부위에 관계없이 2.5~5.0 cm의 경계로 근막을 포함하여 아래의 피하조직을 일괄 제거한다[10]. 절제 후엔 기능적이고 미용적인 면을 고려하여 재건술을 시행하게 되며 피부이식술이나 국소피판, 근피판, 유리피판 등의 피판술이 주로 쓰인다[11,12]. 본 증례에서는 3 cm의 절제연을 두고 전경부광범위 절제술을 실시하였고 동결 조직 절편검사에서 절제연과 기저부에서의 종양세포 침윤이 없음을 확인하였다. 수술 후 피부 결손부위가 커서 대흉근피판(pectoralis major myocutaneous flap)을 이용하여 결손 부위를 재건하였다.
융기성 피부섬유육종의 재발률은 11~55% 정도로 다양하게 보고되어 있다[12].
재발의 양상은 원격 전이보다는 국소재발이 흔하며 국소 재발률은 보고자에 따라 0~60%로 큰 차이를 보이나 대개 2.4%에서 8.3%로 보고하고 있으며 재발한 환자에서 약 반수는 외과적 절제술 후 2년 이내에, 80%는 3년 이내에 발생하지만 시간이 지나서 발생하는 경우도 보고되었다[5].
환자는 수술 후 적어도 첫 3년 동안 3~6개월마다 추적관찰이 필요하고 그 후 1년에 한번씩 추적관찰이 필요하다[11]. 국소재발은 수술 후 방사선 치료를 병행함으로써 유의하게 감소시킬 수 있다고 알려져 있으며 특히 절제연이 불충분하거나 절제연이 양성일 경우 유용하다[13]. 또한 절제가 불가능한 경우에도 방사선 치료는 종양 크기를 줄일 수 있다[5]. 본 증례에서는 절제연이 충분하였지만 국소재발이 흔한 종양이기에 국소재발을 예방하기 위해 수술 후 방사선 치료를 병행하였다. 전이는 대부분 관찰되지 않으나 Bowne 등[14]은 1%의 전이율을 보고하였다. 전이성 종양에서 항암치료의 효과는 분명하지 않으나 타이로신 키나아제 억제제인 글리벡(Glivec, imatinib)이 절제 불가능한 재발성 또는 전이성 종양에서 종양의 크기를 감소시킬 수 있다고 보고되고 있다[15].
본 증례는 전경부에 발생한 융기성 피부섬유육종을 켈로이드로 오인해 단순절제만으로 치료하려다 육종으로 진단된 경우로, 향후 단순 켈로이드 양상의 종물도 주위조직으로 침윤이 의심될 경우 융기성 피부섬유육종도 고려해 보아야 하며 유사한 증례의 진단 및 치료 방법을 결정하는 데 도움이 되고자 증례를 보고하는 바이다.
REFERENCES
1. Le Vay J, O’Sullivan B, Catton C, Cummings B, Fornasier V, Gullane P, et al. An assessment of prognostic factors in soft-tissue sarcoma of the head and neck. Arch Otolaryngol Head Neck Surg. 1994; 120(9):981–6.
2. Gayner SM, Lewis JE, McCaffrey TV. Effect of resection margins on dermatofibrosarcoma protuberans of the head and neck. Arch Otolaryngol Head Neck Surg. 1997; 123(4):430–3.

4. Lee PK, Kim HT, Kim YJ. A case of Dermatofibrosarcoma Protuberans in a breast. J Korean Soc Plast Reconstr Surg. 2002; 29(3):221–4.
5. Lindner NJ, Scarborough MT, Powell GJ, Spanier S, Enneking WF. Revision surgery in dermatofibrosarcoma protuberans of the trunk and extremities. Eur J Surg Oncol. 1999; 25(4):392–7.

6. Taylor HB, Helwig EB. Dermatofibrosarcoma protuberans. A study of 115 cases. Cancer. 1962; 15:717–25.
7. Simstein NL, Tuthill RJ, Sperber EE, Kovalcik PJ, Mullen JT. Dermatofibrosarcoma protuberans--case reports and review of literature. South Med J. 1977; 70(4):487–9.

8. Aiba S, Tabata N, Ishii H, Ootani H, Tagami H. Dermatofibrosarcoma protuberans is a unique fibrohistiocytic tumour expressing CD34. Br J Dermatol. 1992; 127(2):79–84.

9. Blackburn WR, Cosman B. Histologic basis of keloid and hypertrophic scar differentiation. Clinicopathologic correlation. Arch Pathol. 1966; 82(1):65–71.
10. Vásconez HC, Sengezer M, McGrath PC. Flap coverage of a large defect after excision of a massive dermatofibrosarcoma protuberans. Plast Reconstr Surg. 1995; 95(1):136–41.
11. Smola MG, Soyer HP, Scharnagl E. Surgical treatment of dermatofibrosarcoma protuberans. A retrospective study of 20 cases with review of literature. Eur J Surg Oncol. 1991; 17(5):447–53.
12. Kang SY, Yang WY, Yoo YC, Park J. Treatment of wide dermatofibrosarcoma protuberans with tissue expander. J Korean Soc Plast Reconstr Surg. 2003; 30(3):338–41.
13. Mendenhall WM, Zlotecki RA, Scarborough MT. Dermatofibrosarcoma protuberans. Cancer. 2004; 101(11):2503–8.

14. Bowne WB, Antonescu CR, Leung DH, Katz SC, Hawkins WG, Woodruff JM, et al. Dermatofibrosarcoma protuberans: a clinicopathologic analysis of patients treated and followed at a single institution. Cancer. 2000; 88(12):2711–20.
Fig. 1.
8×4 cm sized, erythematous protruding mass was noted on the anterior lower neck. Frontal view (A). Right lateral view (B). Left lateral view (C).

Fig. 2.
Pharynx CT shows 5.5 cm enhancing mass on the anterior lower neck subcutaneous area. Axial view, Suspicious invasion of right strap muscle (A). Coronal view, 5.5 cm enhancing mass on the anterior A B lower neck (B).
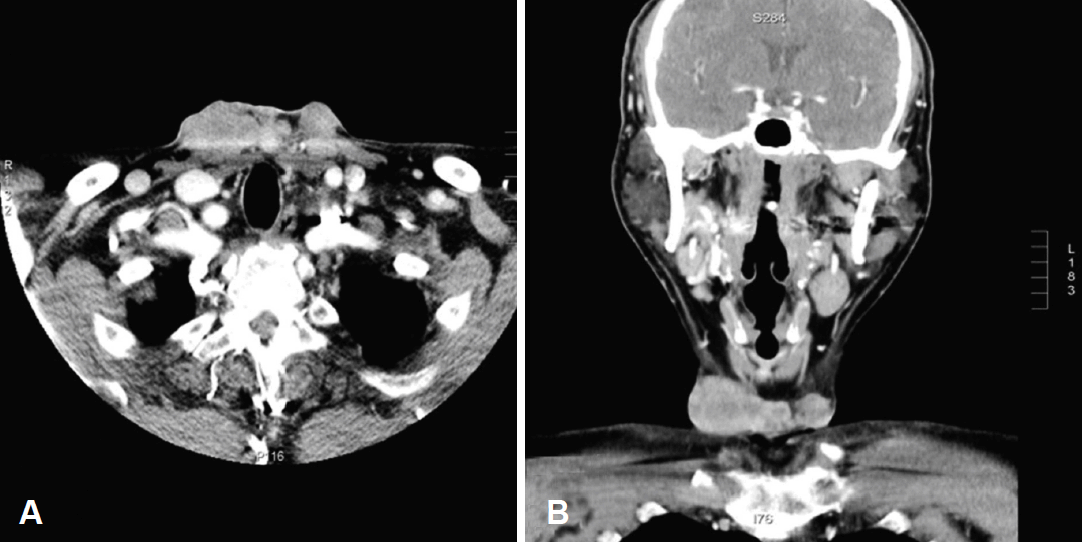
Fig. 4.
Histopathology and immunochemistry showing dermatofibrosarcoma protuberans. Histologic finding shows slender spindle cells arranging in storiform pattern (H&E stain ×100) (A). Immunohistochemical stain reveals tumor cells showing positive reaction for CD34 (CD34 immunostain×100) (B). This photograph shows negative for S-100 protein (S-100 immunostain ×200) (C). This photograph shows negative for anti-SMA antibody (SMA immunostain ×100) (D). SMA: smooth muscle actin.





 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download