서 론
만니톨은 포도당과 매우 유사한 구조를 가지고 있는 비전해질성 삼투성이뇨제로서[1], 혈액뇌장벽(blood-brain barrier) 사이에 삼투압 차이를 만들어 뇌조직에서 혈관내로 수분을 이동시키게 하고, 결국 이 수분을 신장으로 배설시켜 두개내압을 감소시킨다[2]. 또한 혈액 점도를 감소시키고, 자유라디칼을 제거하여 신경을 보호하는 효과도 가지고 있는 것으로 알려져 있어 뇌부종을 동반하는 중증 신경계 질환에 광범위하게 적용된다.
급성 뇌졸중의 치료에서 만니톨 치료의 효과는 불분명하다. 만니톨이 뇌졸중 후 증가된 두개내압을 감소시켜 주고, 결과적으로 뇌관류압을 증가시켜 산소공급에 도움을 주는 것은 사실이나 임상연구에서 효과를 입증하지 못했다. 그러나, American Heart Association/American Stroke Association guideline에서는 ‘급성기 뇌경색 환자에서 뇌부종 때문에 임상 증상이 악화된다면 만니톨 사용은 타당하다(reasonable).’라고 기술되어 있으며[3], 한국 뇌졸중 진료 지침에는 ‘뇌경색 이후 악성 뇌부종에 삼투압요법(osmotherapy)을 포함한 여러 약물적인 두개내압 강화요법을 사용할 수 있다’ 라고 명시하고 있고[4], 실제 임상에서도 사용되고 있다.
만니톨 사용에 있어 가장 잘 알려진 부작용은 급성신부전이다. 지금까지 보고된 바에 의하면 뇌경색 환자들에게 만니톨을 사용했을 경우 11.6% 정도에서 급성신부전이 발생하였다[5]. 주로 용량 의존성(dose dependent)으로 발생하는 것으로 설명되어 혈청 삼투농도가 320 mOsm/L 이상이면 신부전을 유발할 수 있기 때문에 만니톨 사용을 중지할 것을 권고하고 있다[6]. 하지만 뇌졸중 환자에서 만니톨 때문에 발생하는 신부전의 원인, 발생 정도, 위험인자 그리고 결과에 대한 정보가 알려진 것이 거의 없다[7]. 저자들은 이 연구를 통해 큰 영역의 급성기 뇌경색 환자들에서 사용한 만니톨과 신부전의 연관성 및 예후 등을 확인하고자 하였다.
Go to : 
대상 및 방법
2008년 1월부터 2010년 12월 사이 본 병원 신경과에 뇌경색으로 입원한 환자 중 뇌부종으로 만니톨을 투여 받은 환자를 연구 대상으로 하여 의무 기록을 바탕으로 후향적으로 분석하였다. 대상 환자들 중 만니톨을 3일 이내로 짧게 투여 받았던 환자들과 두개골절제술을 받았던 환자들은 연구 대상에서 제외하였다. 인구 통계학적 속성(나이, 성별, 몸무게)과 병력(뇌졸중, 고혈압, 당뇨, 심혈관질환, 흡연)을 조사하였고, 뇌경색의 중증도는 만니톨 치료를 시작할 당시의 National Institute of Health Stroke Scale (NIHSS) 점수로 평가하였다. 신장 기능에 영향을 미칠 수 있는 약제인 vancomycin, ciprofloxacin, levofloxacin, furosemide, angiotensin-converting enzyme inhibitor의 사용 여부를 조사하였으며, 사용한 전체 만니톨 용량도 조사하였다. 혈액요소질소(blood urea nitrogen, BUN)와 크레아티닌(creatinine), 혈청 전해질 농도, 혈당(glucose)은 mannitol 투여 기간 중 하루에 한번 이상 측정하였으며, 혈청 삼투압은 나트륨(Na), 혈당, 혈액요소질소를 이용하여 ([NaX2]+[glucose/18]+[BUN/2.3])와 같이 계산하였다. 신부전은 만니톨 투여 전 크레아티닌이 2 mg/dL 이하이면 0.5 mg/dL 이상 증가했거나, 2 mg/dL 이상이면 1 mg/dL 이상 증가한 경우로 정의하였다[8].
모든 환자는 본 병원의 뇌졸중 진료 지침에 따라 같은 방법으로 치료를 받았다[9]. 15% 또는 25% 만니톨을 Kg당 0.5-1.0 g을 한꺼번에 준 이후 kg당 0.12-0.5 g씩 6번, 하루에 200 g이 넘어가지 않게 5일간 투여한 다음 이틀에 2차례씩 감량하여 유지 기간이 2주를 넘지 않게 하였다. 투여 기간 중 혈청 삼투압이 320 mOsm/L 이상이거나 혈청 전해질 농도, 혈액요소질소, 크레아티닌에 변화가 있을 시 횟수를 감소하여 투여하거나 사용을 중단하였다. 만니톨 투여 기간 중 폴리카테터를 삽입하여 체내의 수분평형을 엄격하게 조절하였다.
자료의 분석은 신부전이 있는 군과 없는 군으로 나누어 인구통계학적 속성과 병력 및 혈액 검사 결과를 비교 분석하였다. 기본적으로 범주형일 경우 각 군 간 카이제곱검정으로 비교하였으며, 변수가 5 미만인 경우는 Fisher 정확검증을 이용하였다. 연속형 자료에 대해서는 독립표본 t 검정을 이용하여 비교하였으며, 비모수적 자료에 대해서는 맨-휘트니 검정을 하였다. 신부전을 유발하는 독립적인 인자를 찾기 위해, 단변량 분석에서 P 값이 0.1 이하인 군을 변수로 하여 로지스틱 회귀분석을 이용하여 독립인자와 교차비를 구하였다. 본 연구에서의 모든 분석은 SPSS 21.0 version (IBM Corp., Armonk, NY, USA)를 이용하였고, 통계적 유의 수준은 P 값은 0.05 미만으로 정의하였다.
Go to : 
결 과
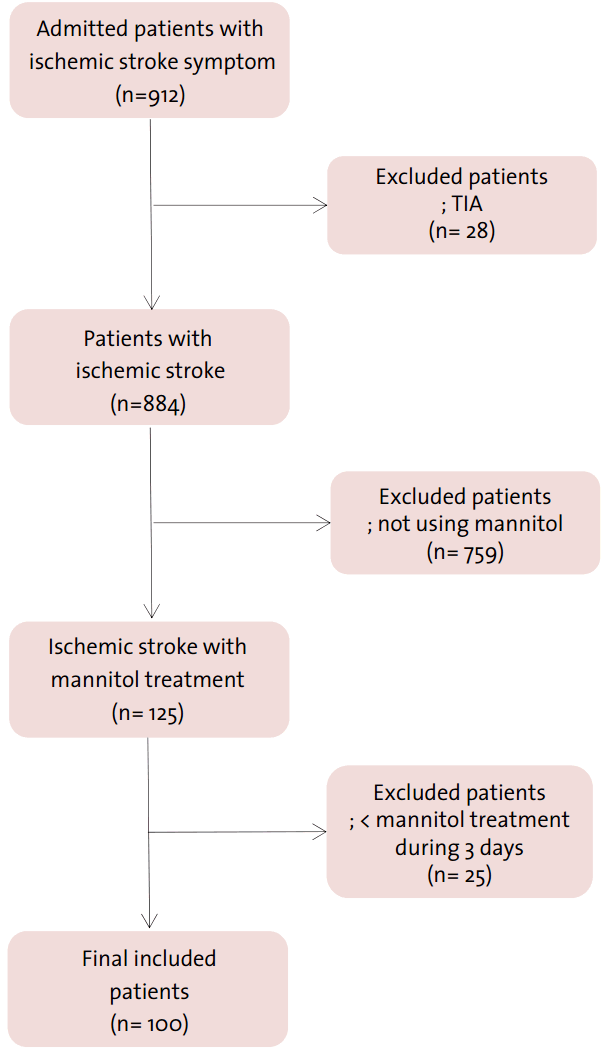
3년 동안 뇌경색으로 입원한 전체 환자 912명 중, 만니톨 치료를 받은 환자는 총 125명(13.7%)이었으며, 투여 기간이 3일 이내인 환자 25명을 제외하고, 100명(10.9%)의 환자를 분석하였다(Fig. 1). 1명을 제외한 모든 환자들은 만니톨 치료를 받기 전 컴퓨터단층혈관조영술과 자기공명혈관조영술을 위한 조영제를 투여 받았다.
최종 분석 대상 100명 중 14명(14%)의 환자가 만니톨에 의한 급성신부전 진단을 받았으며, 만니톨 투여 이후 급성신부전이 발생하기까지의 평균일수는 중앙값(사분위수범위)으로 5(3-9)일이 걸렸다. 급성신부전 발병군과 발병하지 않은 군 사이에 성별, 평균 나이, 평균 몸무게의 유의한 차이는 보이지 않았다. 고혈압, 당뇨, 흡연력, 뇌졸중 과거력 및 심혈관질환 과거력은 양 군에서 유의한 차이가 없었으며, 만니톨 투여 당시의 NIHSS 또한 차이가 없었다. 만니톨 평균 투여 기간은 오히려 신부전 발생군(4.79일)이 발생하지 않은 군(6.63일)에 비해 짧았으며, 총 투여량 또한 발생군이 668.14 g으로 772.61 g을 보인 발생하지 않은 군에 비해 적었으나 통계적으로 유의하지는 않았다(Table 1). 이는 만니톨 투여 도중 크레아티닌 수치에 이상 소견을 보여 투여 횟수를 감소하거나 끊었기 때문으로 생각한다. 급성신부전 발생군에서 발생하지 않은 군에 비해 levofloxacin (50% vs. 23.3%; P =0.041)과 furosemide (28.6% vs. 9.3%; P =0.042)를 투여받은 환자의 비율이 통계적으로 유의하게 높았다. 만니톨 투여 직전 시행한 혈액요소질소, 크레아티닌, 혈청 삼투압, 나트륨은 양 군에서 차이를 보이지 않았지만, 혈당은 급성신부전 발병군(167.76 mg/dL)이 발병하지 않은 군(128.37 mg/dL)에 비해 유의하게 높았으며(P =0.006), 만니톨 치료 중 최고 혈청 삼투압도 발병하지 않은 군(301.43 mOsm/L)에 비해 발병군(344.37 mOsm/L)에서 높았다 (P =0.032)(Table 1). 다변량 분석에서도 만니톨 투여 전 혈당과 투여 도중 최고 혈청 삼투압은 발병군에서 유의 있게 높았다(P =0.043, 0.010)(Table 2).
Table 1.
Demographics and characteristics of ischemic stroke patients who had mannitol treatment with and without ARF
| ARF (n=14) | No ARF (n=86) | P-value* | |
|---|---|---|---|
| Demographics | |||
| Age (year old) | 74.71±9.72 | 70.63±11.74 | 0.220 |
| Male | 5 (35.7) | 49 (57.0) | 0.139 |
| Body weight (kg) | 58.29±13.9 | 59.66±11.10 | 0.761 |
| NIHSS | 17.01±7.86 | 15.27±7.43 | 0.484 |
| Total mannitol dose (g) | 668.14±436.0 | 772.61±420.0 | 0.415 |
| Duration of mannitol treatment (days) | 4.79±2.42 | 6.63±4.38 | 0.129 |
| Stroke risk factors | |||
| Hypertension | 10 (71.4) | 46 (53.5) | 0.210 |
| Diabetes mellitus | 5 (35.7) | 13 (15.1) | 0.125 |
| Smoking | 1 (7.1) | 21 (24.4) | 0.294 |
| Coronary heart disease | 2 (14.3) | 10 (11.6) | 0.674 |
| Previous stroke | 3 (21.4) | 13 (15.1) | 0.693 |
| Additional drugs | |||
| Vancomycin | 0 (0) | 1 (1.2) | 1.000 |
| Any ofloxacin | 7 (50) | 61 (70.9) | 0.133 |
| Levofloxacin | 7 (50) | 20 (23.3) | 0.041 |
| Furosemide | 4 (28.6) | 8 (9.3) | 0.042 |
| Angiotensin II receptor blocker | 5 (35.7) | 23 (26.7) | 0.527 |
| Laboratory | |||
| Initial creatinine (mg/dL) | 1.20±0.76 | 0.98±0.37 | 0.092 |
| Peak creatinine (mg/dL) | 2.69±1.34 | 1.05±0.37 | 0.001 |
| Discharge creatinine (mg/dL) | 2.17±0.98 | 0.93±0.34 | 0.001 |
| Initial BUN (mg/dL) | 21.83±112.44 | 17.07±12.73 | 0.196 |
| Initial sodium (mEq/L) | 140.9±4.3 | 140.6±5.3 | 0.866 |
| Initial glucose (mg/dL) | 167.76±55.62 | 128.37±47.0 | 0.006 |
| Initial serum osmolality (mmoL/kg) | 300.53±11.72 | 295.76±14.52 | 0.246 |
| Peak serum osmolality (mmoL/kg) | 344.37±66.94 | 301.43±16.88 | 0.032 |
| Creatinine phosphokinase (U/L) | 338.15±383.16 | 282.52±368.50 | 0.615 |
Table 2.
Factors associated with the occurrence of acute renal failure
혈청 삼투압이 320 mOsm/L을 넘는 환자들과 넘지 않는 환자들의 차이를 비교해 보았을 때 혈청 삼투압이 높았던 환자들은 NIHSS가 상대적으로 더 높았고, 사용된 약들 중에서는 levofloxacin이 많이 사용되었으며, 내원 당시 혈당이 높았다(Table 3).
Table 3.
Comparison of characteristics of ischemic stroke patients who had serum osmolality less than 320 mmoL and more than 320 mmoL
| Osmolality ≤ 320 (n=84) | Osmolality > 320 (n=16) | P-value* | |
|---|---|---|---|
| Demographics | |||
| Age (year old) | 70.81±11.81 | 73.13±9.87 | 0.464 |
| Female | 37 (44.0) | 10 (62.5) | 0.274 |
| Body weight (kg) | 58.55±11.54 | 63.50±7.77 | 0.075 |
| NIHSS | 14.79±7.10 | 19.31±7.21 | 0.022 |
| ARF | 8 (9.5) | 6 (37.5) | 0.009 |
| Duration of mannitol treatment (days) | 6.27±4.11 | 6.19±3.50 | 0.938 |
| Stroke risk factors | |||
| Hypertension | 44 (53.0) | 12 (75.0) | 0.167 |
| Diabetes mellitus | 15 (18.1) | 3 (18.8) | 1.000 |
| Smoking | 21 (25.3) | 1 (6.3) | 0.112 |
| Coronary heart disease | 8 (9.6) | 4 (25.0) | 0.101 |
| Previous stroke | 12 (14.5) | 3 (18.8) | 0.705 |
| Additional drugs | |||
| Vancomycin | 1 (1.2) | 0 (0) | 1.000 |
| Any ofloxacin | 5 (6) | 0 (0) | 1.000 |
| Levofloxacin | 19 (22.6) | 8 (50.0) | 0.033 |
| Furosemide | 9 (10.7) | 3 (18.8) | 0.402 |
| Angiotensin II receptor blocker | 24 (28.6) | 4 (25.0) | 1.000 |
| Laboratory | |||
| Initial creatinine (mg/dL) | 1.02±0.31 | 1.42±0.86 | 0.082 |
| Peak creatinine (mg/dL) | 1.13±0.64 | 2.00±1.21 | 0.013 |
| Discharge creatinine (mg/dL) | 0.95±0.37 | 1.75±1.04 | 0.008 |
| Initial BUN (mg/dL) | 15.51±6.40 | 27.83±24.90 | 0.067 |
| Initial Sodium (mEq/L) | 141.90±3.43 | 145.13±6.07 | 0.055 |
| Initial Glucose (mg/dL) | 148.08±55.32 | 182.50±63.37 | 0.028 |
| Initial serum osmolality (mmoL/kg) | 298.78±8.50 | 312.49±20.78 | 0.019 |
| Creatinine phosphokinase (U/L) | 281.24±358.44 | 325.94±421.75 | 0.658 |
그리고 급성신부전 환자 14명 중 4명(28.6%)만이 퇴원 전까지 신기능이 완전히 회복되었지만, 신부전 발생 이후 평균 입원 기간은 중앙값 (사분위수범위)으로 9 (3-59)일 밖에 되지 않았다.
Go to : 
고 찰
만니톨은 두개내압 상승과 뇌부종의 치료에 효과적이지만, 약물 자체의 신독성 때문에 그 사용에 제한을 가지게 된다. 만니톨이 급성신부전을 일으키는 기전은 확실하지 않지만, 콩팥요세관 세포 상피에 광범위한 공포형성(삼투압성 신장증 [Osmotic nephrosis])과 세포 부종으로 인한 사구체여과율의 감소한다는 기전이 있고[10], 다량의 만니톨 투여가 원위세관으로 이동하는 전해질의 양을 증가시켜 세뇨관 압력이 증가하기 때문에 사구체여과율이 감소하게 된다는 가설이 있다[11,12]. 또한, 혈청의 삼투압이 증가하여 사구체를 여과시키는 힘보다 커지게 되면, 전체 사구체 간의 압력차가 감소하여 사구체여과율이 감소한다는 가설도 있다[13]. 본 연구에서 저자들은 뇌부종을 동반하는 중증 뇌경색 환자들에서 만니톨의 사용이 어떤 신체적, 약물적 원인으로 신부전을 일으키는지 알아보고자 했다.
본 연구 대상 환자들은 가이드라인에서 제시한 방법에 따라 치료 받은 환자들임에도 14%에서 신부전이 발생하였다. 우리의 연구 결과는 뇌출혈 때문에 만니톨을 사용한 환자의 76%에서 급성신부전이 발생하였다는 대규모 연구 결과와는 차이가 있었지만[14], 뇌경색, 거미막밑출혈, 경막밑출혈, 외상성 출혈, 엽출혈 환자를 대상으로 한 연구의 유병률인 11.6%와는 유사하였다[5]. 두 연구 모두 신부전의 정의를 본 연구와 같게 정의하였고, 수액 균형을 위해 매일 수액양을 조절하였다. 또한 혈청 삼투압이 320 mOsm/L 이상이 되거나, 크레아티닌이 신부전의 정의에 맞게 상승한 경우 만니톨 양을 줄였거나 투여를 중지하였다. 따라서 이러한 유병률의 차이는 환자 관리의 차이 보다는 환자군의 특성에 따른 것으로 해석된다. 대부분의 연구에서 만니톨 치료를 중단하면 모두 신기능을 회복하는 것으로 보고하였지만, 본 연구에서는 28.6%만이 퇴원 전까지 신기능이 완전히 회복되었다. 하지만 신부전 발생 이후 평균 입원 기간이 9일밖에 되지 않아 이를 정확히 평가하기는 어려우며, 실제 모든 환자는 신기능이 회복되는 과정에서 퇴원을 하였다.
단변량 분석에 따른 위험 인자는 만니톨 자체의 효과인 투여 중 최고 혈청 삼투압과 함께 신독성 약물인 levofloxacin과 furosemide 사용 여부였다. 또한 당뇨 여부와는 상관이 없었지만, 만니톨 치료 시작 당시의 혈당 또한 위험 인자로 생각되었다. 하지만, 다변량 분석에서는 이러한 모든 위험 인자 중 최고 혈청 삼투압과 투여 전 혈당이 신부전과 관련이 있다고 분석되었다. 결국 신독성 약물은 만니톨로 인한 신부전에 독립적인 영향을 주기는 어려운 인자라 생각되며, 치료 시작 전 혈당이 높았던 환자들은 당뇨가 있던걸 몰랐던 환자들이거나 이제 막 당뇨가 시작되는 환자들이었을 것으로 생각되었다. 그래서 기존에 당뇨를 알고 있었던 환자들에 비해 혈당 조절이 잘 안되었을 것이고, 이러한 이유로 만니톨 때문에 발생하는 급성신부전은 당뇨와 별다른 상관 관계를 보이지 않았지만, 내원 당시의 고혈당과 밀접한 관련을 보였다고 생각한다. 고혈당이 신부전을 일으키는 이유로는 산화 스트레스(oxidative stress)의 상승, 염증 수치의 증가, 또는 내피 기능이상(endothelial dysfunction)이 발생하여 신장 기능에 장애를 유발할 수 있다[15].
일반적으로 삼투압이 320 mOsm/L 이상 상승하게 되면 만니톨 투여를 주의하게 되는데, 이러한 내용은 Brain Trauma Foundation 지침에도 권고되고 있다[9]. 본 연구에서도 만니톨 치료를 시작할 시점에서는 혈청 삼투압의 차이를 보이지 않았지만, 투여 중 최고 혈청 삼투압은 신부전 발생군이 발생하지 않은 군에 비해 유의하게 높았다(Table 1). 또한, 삼투압이 320 mOsm/L을 넘는 환자들만을 따로 분석해 본 바로 뇌경색의 중증도가 높았고, 초기 혈당과 혈청 삼투압이 높았기 때문에 이러한 특성을 가진 환자들이 내원하여 mannitol 치료를 해야 할 경우 치료 중 혈청 삼투압이 높아져 mannitol을 중단하는 경우가 발생할 가능성이 높아 주의를 기울여야 할 것으로 생각한다. 따라서 본 연구는 만니톨 투여시 혈청 삼투압을 주의 깊게 감시하여야 하며, 320 mOsm/L 이상시 용량을 줄이거나 중단해야 한다는 기존의 주장을 뒷받침하고, 초기 혈당과 삼투압이 높은 큰 영역의 뇌경색 환자들에게 mannitol 치료를 함에 있어 주의해야 함을 보여주고 있다.
만니톨은 체내에서 거의 대사가 되지 않기 때문에 소변으로의 배출양보다 주입양이 많을 때 세포외액에 축적되게 되고, 따라서 신장 기능 이상자에서 부작용이 좀 더 많이 발생한다고 알려져 있다[12]. 본 연구에서는 신부전 발병군의 투여 전 크레아티닌 수치가 1.20 mg/dL로, 발병하지 않은 군의 0.98 mg/dL에 비해 높기는 하지만 유의성을 보이지 않았다. 이는 투여 전 신기능이 떨어져 있으면 처음부터 만니톨 투여량을 조절하는 본원 뇌졸중 진료 지침에 따른 것으로 해석된다. 하루에 200 g 이상 투여하고 전체 축적 농도가 1,000 g 이상일 때, 신혈관의 수축이 발생하면서 사구체여과율이 떨어지고, 이로 인해 급성신부전의 발생에 영향을 미치는 것으로 알려져 있다[12,16]. 본 연구의 대상자들은 사례별로 총 양이 1,000 g을 넘는 경우는 있지만, 하루 투여량이 200 g 이상 되지 않도록 엄격하게 관리되었으며, 투여량과 발병은 상관 관계를 보이지 않았다.
Go to : 
결 론
요약하자면, 만니톨 때문에 발생하는 신부전은 드문 일은 아니다. 본 연구에서는 내원 당시의 혈당과 만니톨 투여시 최고 혈청 삼투압이 위험 인자로 분석되었다. 우리는 투여 전 신장 기능과 전체 투여량의 관련성은 찾을 수 없었다. 이는 만니톨 투여시 환자별로 신장 기능을 고려하여 투여량을 조절하였으며, 하루 투여량이 200g 넘지 않게 엄격하게 조절한 결과로 해석된다. 따라서 급성기 뇌경색 환자에서 만니톨 투여시 혈당을 엄격하게 조절하면서 혈청 삼투압 및 크레아티닌의 지속적인 감시가 필요하며, 엄격하게 투여량을 조절하고 체액 균형을 맞추는 것이 중요하다.
Go to : 




 PDF
PDF Citation
Citation Print
Print


 XML Download
XML Download