Abstract
Purpose
In general orthopedic surgery, the use of prophylactic antibiotics to prevent infection is recommended to be administered within 24 hours. However, there was no analysis on the incidence of surgical site infection according to the duration of use of prophylactic antibiotics for upper extremity fractures. This study aims to derive the appropriate prophylactic antibiotic using time by analyzing the incidence of infection according to the time of prophylactic antibiotic use in distal radius fractures.
Methods
We retrospectively analyzed patients who used prophylactic antibiotics among patients who underwent open reduction and internal fixation for distal radius fractures from April 2018 to May 2021. The time of use of prophylactic antibiotics was classified into the 1-day group used, from 1 hour before surgery to 24 hours after the first administration, and the long-term group, continuously administered until discharge after surgery. Demographic characteristics, infection rate, C-reactive protein, risk factors for surgical site infection, and bone union were compared between the two groups.
Results
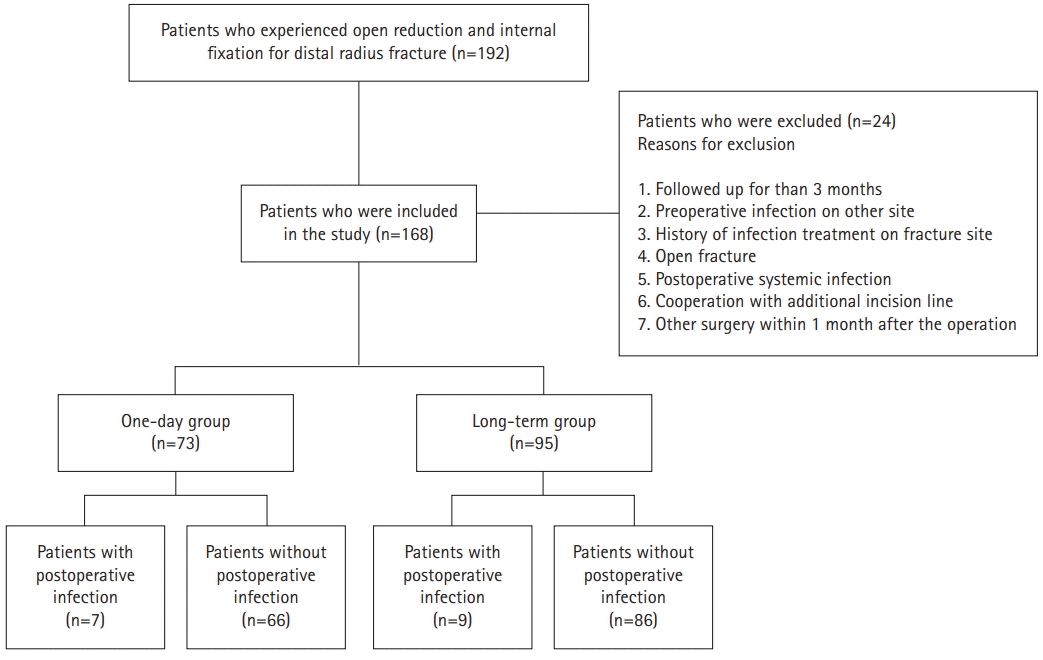
A total of 168 patients were included in the study, 73 in the 1-day group and 95 in the long-term group. Superficial infection occurred in seven patients in the 1-day group and nine in the long-term group, and there was no statistically significant difference in the incidence rates of the two groups (p=0.980).
병원내감염(nosocomial infection)은 선진국의 경우 7%, 개발도상국의 경우 10% 정도 보고되고 있다[1]. 수술부위감염(surgical site infection)은 병원내감염의 가장 흔한 원인으로, 병원내감염 전체의 약 20% 정도를 차지한다[2]. 내고정물(implant) 삽입이 많은 정형외과 수술은 감염에 더욱 취약하다. 내고정물은 체내 이물로 미생물막(biofilm) 형성이 쉽기 때문에 100개 미만의 황색포도상구균(Staphylococcus aureus) 집락 형성(colony-forming unit)에도 감염이 발생할 수 있어 적절한 무균적 수술이 이루어졌다고 하더라도 수술부위감염이 발생할 수 있다[3]. 골절 후의 관혈적 정복술과 내고정술 후 감염률은 0.4%에서 16.1%로 보고되고 있다[4,5]. 정형외과 수술에서 수술부위감염이 발생하면 환자의 예후를 나쁘게 할 뿐 아니라 사망률은 2배 상승, 의료비는 약 300% 증가, 재원기간은 평균 2주 연장 및 재입원률은 5배 증가하므로 주의를 요한다[6,7].
수술 전후의 예방적 항생제 사용은 수술부위감염을 막기위한 효과적인 방법이다[8,9]. 내고정물 삽입이 없는 청결수술(clean surgery)의 경우 예방적 항생제 사용이 필요 없지만, 내고정물이 들어가는 수술은 예방적 항생제 사용이 권장된다[10]. 예방적 항생제의 선택과 사용방법에는 주의가 필요하다. 흔히 감염되는 병원체를 포괄적으로 막을 수 있어야 하고, 부작용이 적어야 하며, 항생제 내성균의 발생과 악화에 대한 고려가 필요하다. 미국정형외과학회에서는 일반 정형외과 수술(general orthopedic surgery)에 대해 예방적 항생제로 1세대 세팔로스포린(cefazolin) 혹은 2세대 세팔로스포린(cefuroxime)을 권장하고 만약 베타락탐 계열에 대한 알레르기가 있을 경우 클린다마이신(clindamycin)이나 반코마이신(vancomycin)을 추천하였으며, 절개 전 한 시간 이내에 투여하고 수술 후 24시간 이내에 중단할 것을 권장하였다[10]. 고관절과 슬관절의 인공관절 치환술, 개방성 골절 등의 세부 파트는 독립적인 예방적 항생제 사용에 대해 가이드라인을 제시하였으나, 원위 요골 골절을 포함한 상지 골절에 대해서는 아직 구체적인 가이드라인이 없이 일반 정형외과 수술 권고를 따르고 있다[11-13].
본 연구는 후향적 의무기록 연구로 연구 기관의 기관생명윤리위원회의 승인(No. 30-2020-217) 후 진행하였으며 심의 과정에서 환자동의서의 수령을 면제받았다. 2018년 4월부터 2021년 5월까지 원위 요골 골절로 본 기관에서 수술받은 환자들을 대상으로 후향적 의무기록을 분석하였다. 연구의 포함기준은 만 18세 이상으로 본 기관에서 원위 요골 골절로 수술받았으며 예방적 항생제를 사용한 환자이다. 제외기준은 추시기간이 3개월 미만인 자, 수술 전 상기도, 비뇨기계 등 다른 부위의 감염을 동반한 자, 골절 부위에 전 생애에 걸쳐 골수염 등의 감염치료를 받은 과거력이 있는 자, 개방성 골절 환자, 고관절, 원위 척골 골절 등의 동반으로 추가적인 절개선을 넣어 다른 수술을 함께 시행한 자, 수술 후 수술 부위와 별개의 기타 전신적 감염이 동반된 자, 수술 후 1개월 이내에 다른 수술을 시행받은 자, 베타락탐 계열 항생제에 대한 알레르기 과거력이 있는 자는 연구 대상에서 배제하였다. 후향적 의무기록 분석을 통하여서 환자 나이, 성별 및 수술방향, 감염 여부, 항생제 사용기간 및 감염 치료적 목적의 항생제 재사용 여부, 수술부위감염의 위험인자(흡연, 65세 이상 고령, 당뇨, 말기신질환, 간경화, 체질량지수(body mass index, BMI) >35 kg/m2 이상의 비만, 3시간 이상의 수술시간), C-반응 단백질, 최종 추시시 골 유합 여부를 파악하였다.
수술부위감염은 미국 국가의료안전관리네트워크(National Healthcare Safety Network) 기준을 따라 표재성과 심부로 나누어 정의하였다[20]. 표재성 수술부위감염은 수술 후 30일 이내 발생한 감염으로 피부 및 피하조직을 침범하여, 표재성 절개부위의 표재성 화농성 삼출물이나 미생물을 식별하였거나, 균 배양이 없더라도 수술 부위의 압통, 국소부종, 홍반, 열감 등의 임상징후로 인하여 의료진이 표재성 수술부위감염으로 정의한 것을 말한다. 심부 감염은 수술 후 30–90일 사이에 발생한 것으로, 절개 부위의 근막 및 근육층과 같은 심부조직에 침범하여 38°C 이상의 발열을 동반한 현저한 국소 통증 및 압통을 동반한 임상증상과, 수술실에서의 심부 절개를 통하여 부위에서 화농성 삼출물 및 병리검사나 균 배양검사에서 감염이 식별된 경우를 말한다. 표재성 감염처럼 항생제를 재시작했거나, 상위 항생제로 바꾸었더라도 조절되지 않고 이후 수술적 처치가 필요하였다면 심부 감염으로 분류하였다. 균 동정은 수술실에서 무균적으로 시행한 것만을 수집하였으며, 심부 감염에서는 일반적으로 균 동정을 시행하였으나, 표재성 감염은 균 동정을 시행하지는 않았다.
예방적 항생제는 1세대 세팔로스포린계 항생제인 세파졸린(cefazolin)을 사용하였다. 1회 용량은 70 kg 체중 기준으로 그 이하에서는 1 g, 그 이상에서는 2 g을 사용하였다. 예방적 항생제의 시작은 피부 절개 시작 전 한 시간 이내, 토니켓(tourniquet) 사용 10분 전에 투여하였으며 수술이 3시간 이상 길어질 경우에는 1회 추가 투여하였다.
예방적 항생제의 사용기간은 하루사용군(1-day group)과 1일 이상 사용한 장기사용군(long-term group)으로 분류하였다. 하루사용군은 첫 투여 후 8시간 간격으로 24시간 동안 총 3회 투여하였으며, 장기사용군은 수술 후 퇴원시까지 첫 투여 후 12시간 간격으로 하루 2회, 5일에서 14일까지 지속 투여하였다. 예방적 항생제의 하루사용군과 장기사용군은 의료진의 사용방식의 변화에 따라 다른 기간에 의무기록이 수집되었다. 2018년 4월부터 2019년 5월까지는 예방적 항생제의 장기사용군이었고, 2020년 4월부터 2021년 5월까지는 예방적 항생제의 하루사용군이었으며, 동일한 2인의 전문의의 집도 아래 수술적 치료가 이루어졌다. 하루사용군에 73명, 장기사용군에 95명, 총 168명의 환자가 연구 대상에 포함되었다(Fig. 1).
통계 분석은 independent samples t-test 및 chi-square test를 사용하였으며, chi-square test에 대한 사후검정을 위하여 Fischer exact test를 사용하였다. IBM SPSS Statistics ver. 26 (IBM Corp., Armonk, NY, USA)를 통해 분석하였고, p-value가 0.05 미만인 경우 통계적으로 유의하다고 정의하였다.
연구에 포함된 환자의 평균 연령은 65.7세, 여성은 79.2%였다(Table 1). 전체 168명의 환자 중 9.5%인 16명이 수술부위감염이 있었으며 모든 감염은 표재성 감염으로 수술적 처치 없이 해결되었다. 16명의 감염 환자 중 한 명을 제외한 15명이 항생제를 재시작하였으며 평균 8.53일간 항생제를 추가적으로 투약하였다. 연구에 포함된 모든 환자들이 최종 추시시에 골 유합을 얻었다. 하루사용군과 장기사용군 간의 성별, 나이, 수상 부위, 기저질환, BMI, 수상 후 수술까지 소요기간 및 수술 전 후 C-반응 단백질의 농도를 포함한 모든 수치는 통계적으로 유의한 차이를 보이지 않았다. 감염의 유무에 따른 환자군 분석에서 흡연 이외의 위험인자들의 통계적 차이는 없었다(Table 2).
수술부위감염에 이환된 환자는 73명의 하루사용군 중에서 7명(9.6%), 95명의 장기사용군에서 9명(9.5%)으로 통계적으로 유의한 차이를 보이지는 않았다. 하루사용군과 장기사용군의 위험인자의 분포 및 수술 후 2주 내의 1차 외래 방문시 C-반응 단백질의 농도는 통계적 차이가 없었다(Table 3).
정형외과 수술 후 예방적 항생제 사용은 수술부위감염을 줄이는 효과적인 방법이다[8,9]. 미국정형외과학회에서는 상지의 골절에 대한 세부 권고안을 제시하지는 않았으나 일반 정형외과 수술(general orthopedic surgery)에 대한 예방적 항생제 사용시간에 대해서 수술 후 24시간 내에 중단할 것을 권장하고 있다[10]. 이런 권고안에도 불구하고 투여량과 시간에 대해서는 정형외과의마다 사용 편차가 있다. Lundine 등[21]의 보고에 의하면 골절 환자의 32%만이 용량과 시간에 대한 권장사항대로 예방적 항생제 처방을 받았으며, 예방적 항생제 처방을 권고대로 하지 않은 61%는 명확한 이유가 없다고 하였다. Thonse 등[15]은 고관절 골절 수술 환자들의 76%가 권장된 항생제 용량과 시간을 지키지 못한다고 보고하였다. Yeap 등[14]은 정형외과 수술 후 92%가 수술 후 예방적 항생제를 사용하였으나 항생제 사용시간은 상이하였다고 보고하였다. 이런 보고들은 정형외과의들이 예방적 항생제 사용의 용량과 시간에 대한 중요성을 간과하고 있음을 시사한다.
장기간의 항생제 사용은 감염을 줄이는 이점이 없을뿐더러 항생제 내성균을 증가시키고 추가적인 비용이 발생하기 때문에 적절한 항생제 사용기간을 정하는 것이 중요하다[16-18]. 몇몇 술자들은 수술 부위에 드레인(drain)을 거치한 기간 동안 예방적 항생제를 연장하여 사용하기도 하나, 이는 감염률을 떨어뜨리지 못하는 것으로 알려졌다[22,23]. 본 연구도 이전의 연구들의 유사하게 원위 요골 골절 환자들에서 하루사용군과 하루 이상의 장기사용군 간의 수술부위감염 발생률이 차이가 없음을 증명하였다.
최근에는 예방적 항생제의 수술 전과 수술 후 사용으로 나누어 수술 후 사용에 대한 필요성을 검증하는 연구들도 보고되면서 예방적 항생제의 수술 전 단회(single-dose) 사용이 권장되는 추세이다. Southwell-Keely 등[24]이 수행한 고관절 골절 환자에 대한 메타분석에서는, 수술 전 예방적 항생제가 수술부위감염을 줄여주긴 하지만 수술 후 항생제 투여는 감염 위험성을 줄여주지 못하는 것으로 결론지었다. Gillespie와 Walenkamp [25]는 체계적 문헌고찰을 통하여 근위 대퇴골 골절을 포함한 장골 골절에서 반감기가 12시간보다 긴 항생제를 수술 전에 단일 용량으로 사용하는 것이 효과적이라고 보고하였다. 본 연구에서는 모든 환자에게 수술 후 항생제를 사용하여 단회 사용에 대한 검증은 하지 못하였다. 추후에는 예방적 항생제의 수술 전 단회 사용에 대한 추가 연구가 필요할 수 있다.
본 연구는 상지 골절에서의 예방적 항생제 사용기간에 대한 첫 근거를 제시하였다는 점에서 의미가 있다. 상지는 하지에 비하여 측부순환(collateral circulation) 등의 혈류가 풍부하고 기능상 위생 관리가 쉬우며, 당뇨 등 기저질환에 의한 영향이 적은 편이다[26,27]. 이런 해부학적 차이로 상지와 하지의 수술에 따른 감염 예방과 관리 방법에 차이를 둘 수 있으며, 상지의 경우 불필요한 예방적 항생제 사용을 최소화할 수 있는 근거가 된다[28]. Murphy 등[29]은 메타분석을 통하여 압궤 손상이나 개방성 골절을 제외한 수부의 일반 외상 수술에서 예방적 항생제가 필요없다고 하였다. 하지만 이 연구는 단순 열상 등 순수 연부조직 수술까지 포함한 것으로 내고정물이 삽입되는 골절 수술을 완전히 대변하지는 못한다. 상지 골절에서의 예방적 항생제 사용에 대한 원저(original article)는 없으며 일반 정형외과 수술이나 인공관절 수술, 전체 골절이나 고관절 등의 연구 결과를 인용하여 사용해왔다[10,15]. 본 연구는 손목의 골절에 대하여 예방적 항생제의 사용시간을 조사한 첫 논문으로 원위 요골 골절에서 24시간 이내 예방적 항생제 사용이 안전함을 증명하여 상지에서의 예방적 항생제 사용에 대한 근거를 제시하고 있다.
본 연구는 몇 가지 한계점을 가지고 있다. 첫 번째, 후향적 연구로 근거의 강도가 떨어지며, 의무기록의 누락이나 선택 편향의 가능성이 있다. 두 번째, 샘플수가 적어서 수술부위감염 증례가 적고 모든 예가 표재성 감염이었다. 이로 인하여 수술부위감염군에 대한 더 세부적인 분석이 부족하고 통계적 힘이 약하였다. 세 번째, 최근 상지의 예방적 항생제 연구는 수술 전 단일 투여만 하는 것이나 투여하지 않는 것에 대해 활발히 연구되고 있으나, 본 연구는 후향적 연구의 한계로 이를 반영하지 못하였다.
REFERENCES
1. Danasekaran R, Mani G, Annadurai K. Prevention of healthcare-associated infections: protecting patients, saving lives. IJCMPH. 2014; 1:67–8.

2. Owens PL, Barrett ML, Raetzman S, Maggard-Gibbons M, Steiner CA. Surgical site infections following ambulatory surgery procedures. JAMA. 2014; 311:709–16.

3. Trampuz A, Zimmerli W. Antimicrobial agents in orthopaedic surgery: prophylaxis and treatment. Drugs. 2006; 66:1089–105.
4. Chen AF, Schreiber VM, Washington W, Rao N, Evans AR. What is the rate of methicillin-resistant Staphylococcus aureus and Gram-negative infections in open fractures? Clin Orthop Relat Res. 2013; 471:3135–40.

5. Zimmerli W. Clinical presentation and treatment of orthopaedic implant-associated infection. J Intern Med. 2014; 276:111–9.

6. Whitehouse JD, Friedman ND, Kirkland KB, Richardson WJ, Sexton DJ. The impact of surgical-site infections following orthopedic surgery at a community hospital and a university hospital: adverse quality of life, excess length of stay, and extra cost. Infect Control Hosp Epidemiol. 2002; 23:183–9.

7. Kirkland KB, Briggs JP, Trivette SL, Wilkinson WE, Sexton DJ. The impact of surgical-site infections in the 1990s: attributable mortality, excess length of hospitalization, and extra costs. Infect Control Hosp Epidemiol. 1999; 20:725–30.

8. Burnett JW, Gustilo RB, Williams DN, Kind AC. Prophylactic antibiotics in hip fractures. A double-blind, prospective study. J Bone Joint Surg Am. 1980; 62:457–62.

9. Gatell JM, Riba J, Lozano ML, Maña J, Ramon R, García SanMiguel J. Prophylactic cefamandole in orthopaedic surgery. J Bone Joint Surg Am. 1984; 66:1219–22.

10. Prokuski L. Prophylactic antibiotics in orthopaedic surgery. J Am Acad Orthop Surg. 2008; 16:283–93.

11. American Academy of Orthopaedic Surgeons. Recommendations for the use of intravenous antibiotic prophylaxis in primary total joint arthroplasty [Internet]. Rosemont, USA: American Academy of Orthopaedic Surgeons;c2004. [cited 2014 Mar 1]. Available from: https://www.aaos.org/about/bylaws-policies/statements--resolutions/information-statements/.
12. Bedouch P, Labarère J, Chirpaz E, et al. Compliance with guidelines on antibiotic prophylaxis in total hip replacement surgery: results of a retrospective study of 416 patients in a teaching hospital. Infect Control Hosp Epidemiol. 2004; 25:302–7.

13. Gosselin RA, Roberts I, Gillespie WJ. Antibiotics for preventing infection in open limb fractures. Cochrane Database Syst Rev. 2004; (1):CD003764.

14. Yeap JS, Lim JW, Vergis M, Au Yeung PS, Chiu CK, Singh H. Prophylactic antibiotics in orthopaedic surgery: guidelines and practice. Med J Malaysia. 2006; 61:181–8.
15. Thonse R, Sreenivas M, Sherman KP. Timing of antibiotic prophylaxis in surgery for adult hip fracture. Ann R Coll Surg Engl. 2004; 86:263–6.

16. Li JT, Markus PJ, Osmon DR, Estes L, Gosselin VA, Hanssen AD. Reduction of vancomycin use in orthopedic patients with a history of antibiotic allergy. Mayo Clin Proc. 2000; 75:902–6.

17. Terpstra S, Noordhoek GT, Voesten HG, Hendriks B, Degener JE. Rapid emergence of resistant coagulase-negative staphylococci on the skin after antibiotic prophylaxis. J Hosp Infect. 1999; 43:195–202.

18. Harbarth S, Samore MH, Lichtenberg D, Carmeli Y. Prolonged antibiotic prophylaxis after cardiovascular surgery and its effect on surgical site infections and antimicrobial resistance. Circulation. 2000; 101:2916–21.

19. Na YG, Kim Y, Park E, et al. Outcomes research and physician perceptions on antibiotic prophylaxis in total knee arthroplasty [Internet]. Seoul, KR: National Evidence-based Healthcare Collaborating Agency;c2018. [cited 2018 May 31]. Available from: https://www.neca.re.kr/lay1/program/S1T11C145/report/view.do?seq=244&.
20. Centers for Disease Control and Prevention.. National Healthcare Safety Network: surgical site infection (SSI) event [Internet]. Atlanta, USA: Centers for Disease Control and Prevention;c2010. [cited 2010 Jun 26]. Available from: http://www.cdc.gov/nhsn/PDFs/pscManual/9pscSSIcurrent.pdf.
21. Lundine KM, Nelson S, Buckley R, Putnis S, Duffy PJ. Adherence to perioperative antibiotic prophylaxis among orthopedic trauma patients. Can J Surg. 2010; 53:367–72.
22. Oishi CS, Carrion WV, Hoaglund FT. Use of parenteral prophylactic antibiotics in clean orthopaedic surgery. A review of the literature. Clin Orthop Relat Res. 1993; (296):249–55.

23. Bratzler DW, Houck PM; Surgical Infection Prevention Guidelines Writers Workgroup, et al. Antimicrobial prophylaxis for surgery: an advisory statement from the National Surgical Infection Prevention Project. Clin Infect Dis. 2004; 38:1706–15.

24. Southwell-Keely JP, Russo RR, March L, Cumming R, Cameron I, Brnabic AJ. Antibiotic prophylaxis in hip fracture surgery: a metaanalysis. Clin Orthop Relat Res. 2004; (419):179–84.
25. Gillespie WJ, Walenkamp GH. Antibiotic prophylaxis for surgery for proximal femoral and other closed long bone fractures. Cochrane Database Syst Rev. 2010; 2010:CD000244.

26. Ryan DJ, Minhas SV, Konda S, Catalano LW. Surgical site infection after open upper extremity fracture and the effect of urgent operative intervention. J Orthop Trauma. 2020; 34:258–62.

27. Greenblatt DY, Rajamanickam V, Mell MW. Predictors of surgical site infection after open lower extremity revascularization. J Vasc Surg. 2011; 54:433–9.

Table 1.
Demographic features of patients
| Variable | Total (n=168) | One-day group (n=73) | Long-term group (n=95) | p-value |
|---|---|---|---|---|
| No. of patient | 168 | 73 | 95 | |
| Age (yr) | 65.73±13.64 | 63.78±13.92 | 64.92±13.32 | 0.592 |
| >65 yr | 100 (59.5) | 41 (56.2) | 59 (62.1) | 0.605 |
| Sex | 0.146 | |||
| Male | 35 (20.8) | 19 (26.0) | 16 (16.8) | |
| Female | 133 (79.2) | 54 (74.0) | 79 (83.2) | |
| Smoking | 9 (5.4) | 4 (5.5) | 5 (5.3) | >0.999 |
| Body mass index > 5 kg/m2 | 2 (1.2) | 2 (2.7) | 0 (0) | 0.187 |
| Fracture side | 0.709 | |||
| Right | 81 (48.2) | 34 (46.6) | 47 (49.5) | |
| Left | 87 (51.8) | 39 (53.4) | 48 (50.5) | |
| Comorbidity | ||||
| Diabetes mellitus | 25 (14.9) | 11 (15.1) | 14 (14.7) | 0.952 |
| End-stage renal disease | 2 (1.2) | 1 (1.4) | 1 (1.1) | >0.999 |
| Liver cirrhosis | 8 (4.8) | 3 (4.1) | 5 (5.3) | >0.999 |
| Operation time >3 hr | 0 (0) | 0 (0) | 0 (0) | - |
| Duration from injury to surgery (day) | 4.96±5.61 | 5.39±6.84 | 4.63±4.47 | 0.416 |
| C-reactive protein (mg/L) | ||||
| Preoperative | 0.26±0.62 | 0.24±0.38 | 0.28±0.75 | 0.649 |
| At the first follow-up visiting | 0.27±0.72 | 0.25±0.48 | 0.28±0.86 | 0.772 |
| Duration of antibiotic use (day) | - | 1.00±0.00 | 10.44±1.99 | <0.001* |
| Infection | 0.980 | |||
| Superficial | 16 (9.5) | 7 (9.6) | 9 (9.5) | |
| Deep | 0 (0) | 0 (0) | 0 (0) | |
| Bone union at the last follow-up | 168 (100) | 73 (100) | 95 (100) | - |
Table 2.
Relationship between comorbidities and infection
| Risk factor | Infection (n=16) | Non-infection (n=152) | p-value |
|---|---|---|---|
| Smoking | 3 (33.3) | 6 (66.7) | 0.042* |
| Age >65 yr | 12 (12.0) | 88 (88.0) | 0.185 |
| Diabetes mellitus | 5 (20.0) | 20 (80.0) | 0.067 |
| ESRD | 1 (50.0) | 1 (50.0) | 0.182 |
| Liver cirrhosis | 1 (12.5) | 7 (87.5) | 0.559 |
| BMI >35 kg/m2 | 0 (0) | 2 (100) | >0.999 |
| Operation time >3 hr | 0 (0) | 0 (0) | - |
Table 3.
Comparison of infected groups between 1-day and long-term groups




 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download