서론
클로자핀(clozapine)이 정신과 임상에 등장한 후 40여년이 되었다. 그 동안 다양한 새로운 항정신병약물의 도입이 지속되었지만, 클로자핀은 현재까지도 다른 항정신병약물에 의한 치료 효과 부족을 해결할 수 있는 약제로서 그 자리를 지키고 있다. 다만, 우월한 치료 효과에도 불구하고 무과립구증(agranulocytosis) 발생의 위험으로 인해 일차 치료제로 사용될 수는 없다. 우리나라 조현병 약물치료 지침서에서 클로 자핀은 3단계에 위치하여 다른 항정신병약물의 치료 반응이 제한적인 경우 사용하며, 각국의 조현병 치료 가이드라인에서도 비슷한 상황이다[1]. 클로자핀의 처방이 인가된 적응증은 치료 저항성 조현병, 심한 추체외로 부작용 또는 지연성 운동장애로 인해 다른 약물을 사용할 수 없는 경우, 자살행동 위험성이 높은 조현병 또는 조현정동장애 등이다[1,2]. 본 종설에서는 클로자핀이 치료 저항성 조현병 치료에서 점하고 있는 위치와 임상적 의미 등에 대해서 고찰해 보기로 한다.
Go to : 
클로자핀의 개발과 도입 과정
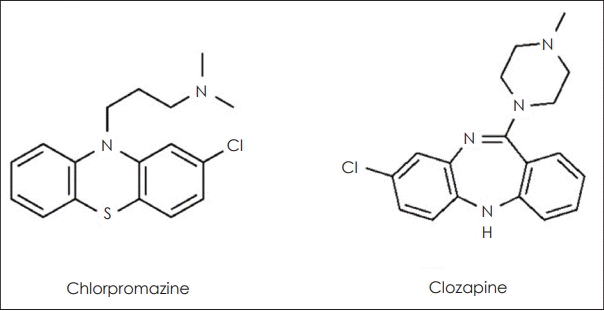
항정신병약물 시대는 클로르프로마진(chlorpromazine)의 정신병적 증상에 대한 치료 효과의 발견으로부터 시작되었다. 클로르프로마진은 원래 마취보조제로 개발되었으나, 외과 의사였던 앙리 라보리(Henri Laborit)에 의해 정신병적 증상에 대한 치료 효과가 최초로 확인되었다. 프랑스 제약회사 론풀랑(Rhone-Poulenc)에 의해 라각틸(Largactil)이라는 상표명으로 1952년에 시장에 첫 등장을 하였다[3]. 다른 한편, 클로르프로마진 화합적 변형체의 하나인 G22355는 정신병 증상에 대한 효과를 시험하던 중 우연히 항우울 효과가 확인되었으며, 향후 이미프라민(imipramine)이라는 이름으로 1958년 판매가 시작되었다[4]. 현재 사용되고 있는 많은 항정신병약물과 항우울제는 클로르프로마진의 화학적 변형에 기반한다.
이와 같이 클로르프로마진과 삼환계 항우울제의 도입과 확산이 이루어지던 1950년대 유럽의 제약사들은 유사한 화학물질을 기반으로 새로운 약을 찾고 있었다. 스위스 제약사 Wander AG는 이와 같은 과정에서 1959년 클로자핀의 화학물질을 개발하였으며(그림 1), 1972년 Sandoz 사에서 “LeponoxⓇ” 란 상품명으로 스위스와 오스트리아에서 처음 시장에 발매하였고, 1974년 독일, 1975년 핀란드에서 판매를 시작하였다. 1975년 핀란드에서 클로자핀이 사용되기 시작하고 4개월 만에 18명의 환자에서 무과립구증이 발생하였고 그 중 9명이 사망하였으며, 클로자핀은 핀란드에서 판매금지 되었다[5,6]. 당시 미국에서 시행 중이던 임상시험 역시 중단되었다. 클로자핀의 효과에 대해서 잘 알려진 상황에서 1984년 미국에서 임상시험이 재개되었고, 연구 결과 확실한 효능이 확인되었다. 무과립구증에 대한 위험이 재차 확인되기도 하였지만, 조기 발견에 따른 중단으로 치명적인 부작용은 막을 수 있다는 것 역시 확인하였다. 이미 1977년에 클로자핀 시작 후 18주 동안 매주 혈액검사를 하는 방안이 제안되어 있었다. 미국 식품의약품청(Food and Drug Administration, FDA)은 1989년 “ClozarilⓇ” 상품명으로 미국 내 클로자핀의 시판을 허가하였다. Sandoz 제약사는 “Clozaril Patient Monitoring System (CPMS)”를 시작하여 클로자핀을 투여 받는 모든 환자로부터 혈액샘플을 받아 직접 검사를 수행하고 혈액 수치를 관리하였다. 당시에는 혈액 샘플을 공급하지 않으면 클로자핀 처방도 할 수 없게하여, 엄격한 관리 체계 하에 클로자핀 시판이 본격적으로 시작되었다[5]. 물론 현재의 CPMS는 직접 검사를 주관하지는 않고 혈액 검사 수치만을 모니터링한다. 우리나라에서는 1995년 10월에 시판이 허가되었으며, 그 해 12월부터 발매되었다. 우리나라에서도 CPMS가 운영되고 있으며, 혈액검사를 시행하는 조건에서 건강보험심사에서 삭감 없이 처방될 수 있다. 이와 같이 클로자핀은 긴 역사 속에서 살아남아 CPMS라는 제도적 보완까지 하면서 현재 우리의 정신과 치료 현장에서 자리를 차지하고 있다. 이는 조현병 치료에서 주요한 부분을 차지하고 있는 치료 저항성 환자군에 대한 클로자핀의 우수한 효과에 그 근거가 있다.
Go to : 
치료저항성 조현병에 대한 클로자핀의 효과
치료저항성 조현병(treatment resistant schizophrenia, TRS)은 서로 다른 종류의 항정신병약물을 두 가지 이상 적절하게 시도한 후에도 치료반응에 실패한 경우를 일컫는다. 국내 조현병 학회 약물치료 지침서 내용을 소개하면, 화학적으로 상이한 최소 두 가지의 항정신병약물(최소 하나는 반드시 비정형 항정신병약물)을 충분 용량(일일 chlorpromazine 등가용량 600 mg 이상)으로 각각의 약물마다 4~8주의 충분 기간 동안 치료 반응 치료했음에도 치료 반응이 없다면 치료 저항성 조현병으로 판단한다고 하였다[1]. 상세한 내용은 본 학회지 지난 호에 실린 종설 “치료저항성 조현병: 정의와 임상양상”을 참고하면 되겠다[7]. 조현병으로 치료받는 환자들 중 약 30~50%가 치료저항성을 가지고 있을 것으로 추정되고 있어, 대략 1/3 정도의 환자는 두 가지 이상의 항정신병약물에 반응하지 않는다. 클로자핀은 이러한 치료저항성 조현병 환자에서 탁월한 효과를 보이며, 이는 오랜 기간 다양한 약물과의 비교임상 연구에서 반복 확인되었다[2].
미국 FDA에서 클로자핀 판매를 허가한 결정적 임상연구는 1988년에 Kane 등[8]이 발표한 연구였다. 기존에 세 가지 이상의 항정신병약물에 반응하지 않았던 조현병 환자를 대상으로 하여 무작위 배정을 하여 클로르프로마진과 클로자핀을 투여하여 비교한 결과, 클로르프로마진 투약은 4% 환자만이 효과가 있었던 반면, 클로자핀은 30% 정도에서 치료 반응이 있어 매우 명확한 우위가 확인되었다. 또한 양성 증상뿐 아니라 음성, 인지, 불안, 우울 증상 등의 다양한 영역에서의 호전이 확인되었다.
정형 항정신병약물에 대한 비교효과에 대한 메타분석에서 클로자핀은 단기 및 장기 효과, 재발방지, 환자의 만족도 등의 다양한 영역에서 우월한 효과를 보이는 것으로 확인되었으며, 그 차이는 비교적 명확한 편이다[9]. 비정형 약물들과의 비교 효과는 그에 비해 복잡하다. Cost Utility of the Latest Antipsychotic Drugs in Schizophrenia Study (CUtLASS) 연구에서 클로자핀은 다른 비정형 항정신병약물들에 비해 유의한 차이의 우수한 성적을 내는 것으로 확인되었으며[10], Clinical Antipsychotic Trials for Intervention Effectiveness (CATIE) 연구에서 클로자핀은 다른 비정형 항정신병약물에 비해 정신병적 증상의 가장 큰 폭의 호전을 유발하였으며, 탈락율 역시 가장 낮았다[11]. 그러나 네트워크 메타분석(network meta-analysis)을 통해 클로자핀이 치료 저항성 조현병 치료에서 다른 비정형 항정신병약물에 비해 과연 유의한 우월성을 보이는가에 대해서 부정적인 결과가 제시되기도 하였다[12]. 물론 다수의 메타분석을 포함한 연구 보고들은 클로자핀의 우월성을 반복적으로 확인시켜 주었다. 비정형 항정신병약물들과의 비교에서는 통계법의 차등적 적용, 목표 증상 영역, 연구 조건 등에 따라 유의성 수준에서의 다양한 결과는 있으나, 클로자핀이 치료저항성 조현병 치료에 있어서 ‘gold standard’ 로서 간주된다는 점은 경험적으로나 학술적으로 인정되는 것이 사실이다[2,13,14].
양성 증상에 대한 명확한 효과 외에도 클로자핀은 음성 증상 및 인지 기능에도 부분적으로나마 개선 효과를 나타내는 것으로 보인다. 초창기 연구에서 정형 항정신병약물에 비교하여 클로자핀의 음성 증상 호전 효과가 명확하게 드러났었는데, 추후 분석을 통해 양성 증상 호전 및 추체외로 부작용 감소에 의한 이차적인 호전의 부분이 있었던 것으로 시사되기도 하였다[15]. 다른 비정형 항정신병약물과의 비교에서도 일차적인 음성 증상에 대한 효과가 있는 것으로 확인되어 오고 있다[13,14]. 다만, 음성 증상에 대한 호전 효과의 판단에는 장기간의 관찰이 필요하지만, 음성 증상에 대한 효과가 주로 12주 이내의 단기간 연구에 국한되어 있어 추가 확인이 필요하겠다[14]. 인지기능 측면에서 클로자핀은 언어 유창성, 실행기능, 정신운동속도 등에서 부분적인 호전 효과를 보이는 것으로 보고되었다. 그러나 다른 비정형 항정신병약물에 비한 비교 우위성이 확인되는 편은 아니며, 클로자핀의 인지기능에 대한 효과가 동반된 항콜린 작용 및 진정 작용으로 상쇄되는 부분도 있는 것으로 예상된다[16,17].
Go to : 
적절한 클로자핀 사용 가이드라인에 기반한 클로자핀 저항성의 판단
클로자핀을 적정 용량으로 충분한 기간 동안 투여했음에도 대략 40~70% 환자가 클로자핀 저항성을 보인다. 이와 같은 경우 많은 조현병 치료반응 연구 그룹에서 클로자핀 저항성 조현병(clozapine-resistant schizophrenia, CRS)로 명명하며 이에 대한 정의, 치료반응 판단 기준, 향후 대책 등에 대해서 제안을 해 오고 있다[7,18]. 클로자핀 저항성의 정의를 위한 기준은 결국 클로자핀의 적절한 사용에 대한 가이드라인으로서의 역할을 하므로 이에 대한 상세한 고찰이 필요하다.
이미 다수의 다른 항정신병약물에 의한 치료 실패로 클로자핀을 처방받고 있는 단계로서 클로자핀 저항성을 정의하는 데에는 세심한 임상적 판단이 필요하다. 극저항성(ultra-resistance) 으로 명명되고 제안된 Mouaffak 등[19]의 정의는 널리 인용된 클로자핀 저항성 가이드라인의 대표격으로서 인용을 해 보면 다음과 같다. 클로자핀을 8주 이상 혈중농도 350 ng/mL 이상으로 유지함에도 불구하고, Brief Psychiatric Rating Scale (BPRS) 기준으로 20% 미만으로 호전을 보이며, 두 가지 이상의 양성 증상이 중등도 이상으로 지속하며, BPRS 총점 45점 이상에 Clinical Global Impression (CGI) 점수 4점 이상인 경우를 말한다. 또한 5년 이상의 기간 동안 사회적 직업적 기능에서 안정적인 기간을 보이지 않은 경우로 Global Assessment of Functioning (GAF) 점수 40점 이하의 기준을 포함한다.
이후 S chizophrenia Patient O utcomes Research Team (PORT), Treatment Response and Resistance in Psychosis (TRRIP), World Federation of Societies of Biological Psychiatry (WFSBP), Canadian guidelines for the Pharmacotherapy of Schizophrenia in Adults 등의 다양한 조현병 치료 반응 연구 그룹에서 제안한 가이드라인에서도 기본적으로 클로자핀 혈중 농도와 충분한 사용 기간을 강조한다. 혈중농도의 경우 마찬가지로 350 ng/mL 이상 유지한 상태에서, 치료 혈중 농도에 도달한 이후 적어도 8~12주 이상의 치료 기간 이후 판단을 하도록 한다[20-23].
혈중 농도 350 ng/mL 기준은 많은 연구 그룹에서 공통적으로 동의가 이루어져 있다. 그러나 실제 임상에서 클로자핀 혈중 농도를 측정하는 것이 용이하지 못한 경우가 많은데다가, 더욱이 클로자핀 용량과 혈중 농도의 상관관계는 개인에 따른 편차가 상당히 크기 때문에 임상 현장에서 실질적인 활용은 어려운 것이 현실이다. 클로자핀 용량에 대한 가이드라인 역시 있으나, 그룹별로 상당히 다양하여 적절한 일일 용량으로서 100~900 mg 정도로 상당히 넓게 제시하고 있다. TRIPP은 혈중 농도 측정이 어려운 경우 클로자핀 일일 용량 500 mg 이상을 사용하여 치료 효과를 확인하길 권장하며, 이는 클로자핀 일일 용량 400 mg 이상인 경우 효능의 우월성이 확인되었다는 보고에 의거한다[21,24]. 그러나 아시아인은 서구인에 비해 대사율이 낮고 부작용에 더 민감한 경우가 많아[25], 이보다는 훨씬 낮은 용량이 사용되고 있어 우리나라 환자에게는 잘 맞지 않는다. 우리나라 연구에 따르면 치료적 유효 혈중농도 350~400 ng/mL 유지에 필요한 클로자핀 용량은 300~400 mg/일이었다[26,27].
클로자핀의 치료 반응 발현은 다른 항정신병약물에 비해 더 시간이 오래 걸리는 것으로 알려져 있다. 따라서 클로자핀 시작 후 적어도 3개월의 기간 이상을 지속한 후 치료 반응을 판단하도록 제안된다. 또한 유효 혈중 농도에 이르기까지의 기간도 개인차가 크고 오랜 기간이 걸리므로, 정확히 판단하기 위해서는 1주일 이상 용량이 유지된 상태에서 2회 이상 350 ng/mL 이상의 혈중 농도 유지를 확인하고 이로부터 12주 정도 후까지의 반응을 확인하여 클로자핀 저항성을 확인하도록 하고 있다. 클로자핀 시작 후 50% 정도의 환자가 6개월 이내에 유효한 치료 반응이 있었으나, 6개월 이후에도 10~20%의 환자가 추가적인 치료 반응이 나타났다는 보고도 있어, 클로자핀 치료 반응을 판단하는 기간의 기준을 확장적으로 고려하는 것이 필요하겠다[18,28].
전술한 바와 같이 클로자핀을 충분 용량, 충분 기간 사용하며 증상 심각도에 대해 천천히 확인하는 것은 클로자핀 반응성 평가에 반드시 필요하다(표 1). 그러나 클로자핀의 증량 과정은 졸림, 어지러움, 침분비과다, 변비 등의 부작용 증가로 순응도 감소의 원인이 되며, 높은 용량까지의 증량은 경련 역치를 낮추거나 심전도 이상 등의 위험성 또한 증가시킨다[29]. 다른 한편, 경도 내지 중등도 수준의 정신병적 증상의 환자군이 아닌 심각한 수준의 정신병적 증상이 지속되는 경우 클로자핀 단독 치료로 충분 기간을 기다린다는 것은 현실적으로 어려워 대안적 방안이 필요하다. 다른 약물과의 병용 치료는 클로자핀 저항성의 다음 방안이며, 위와 같은 상황에 대한 현실적 방안이 된다.
Table 1.
Requirements for assessment of adequate treatment response for clozapine
| Plasma clozapine level | ≥350 ng/mL |
| Treatment duration | More than 8-12 weeks after achieving clozapine plasma level 350 ng/mL |
| Clozapine dose | More than 400-500 mg/day if plasma level unavailable* |
| Symptom severity | No more than moderate level of individual psychotic symptoms |
Go to : 
클로자핀과 다른 항정신병약물의 병용 치료
클로자핀 저항성이 확인된 경우라도 이미 두 가지 이상의 항정신병약물에 대한 치료 실패 후 클로자핀 치료를 시작한 경우가 대부분이므로 다른 항정신병약물로의 변경을 통해 성공적인 치료 반응 증진을 도모하기는 현실적으로 어려운 경우가 많다. 클로자핀을 3~6개월 정도 충분 기간 사용하고도 반응이 부족하다면 다른 항정신병약물의 병용을 시도해 볼 수 있다. 클로자핀을 복용하는 조현병 환자의 18~35% 정도가 다른 항정신병약물을 함께 복용하는 것으로 보고되었다. 많은 병용 치료의 효과 보고가 비록 소규모 연구를 통해 도출되었으며 대규모 이중맹검 연구를 통한 확실한 증거를 확보하지 못하여 그 효과 크기(effect size)가 크지는 못하지만, 유효한 양성 증상의 감소 뿐 아니라 인지기능 호전 등 측면에서 이점을 무시할 수 없다[30-32]. 병용 치료를 통해 클로자핀의 부작용 을 경감시킬 수 있는 경우도 있지만, 대부분의 병용 치료는 비용 및 부작용의 부담을 증가시킬 위험성을 높여 적절한 병용 투여를 위한 노력이 반드시 필요하다[33].
병용 요법의 기본적 요건의 하나는 약물별 작용 기전을 보완하여 다중 표적에 작용하도록 하는 것이다. 클로자핀은 다른 항정신병약물들에 비해 D2보다 5-HT2A 수용체에 대한 결합능이 높으며 이는 낮은 추체외로 부작용 기전의 이유로 제시되었으며, 소위 D2/5-HT2A 가설은 후속 비정형 항정신병약물의 기본적인 기전으로 자리 잡았다. 클로자핀은 용량을 지속적으로 높여도 D2 수용체 점유율이 60% 이하이며, 이로 인해 5-HT2A/D2 수용체 점유율 비는 클로자핀이 상대적으로 가장 높은 편이다. 그 외에도 클로자핀은 도파민 D1 수용체, α1, α2-아드레날린 수용체, H1 히스타민 수용체, M1 아세틸콜린 수용체 등에도 높은 결합력을 보인다[34].
따라서 클로자핀과 다른 항정신병약물 병용의 이론적 근거의 대표적 개념 중 하나는 클로자핀의 부족한 D2 수용체 차단 효과를 다른 약물로 보충한다는 것이다. 따라서 도파민 수용체 친화도가 높은 약제에 대한 시도가 많이 되어 왔다. 그런 의미에서 정형 항정신병약물 병용의 부가적 효과가 기대될 수 있으며, 할로페리돌, 설피라이드, 피모자이드, 플루페나진 등의 병용 요법 효과가 알려졌다[30-32]. 그러나 정형 항정신병 약물 병용 요법에 대한 체계적 연구는 제한적인 편이다. 설피라이드의 경우, 클로자핀과 병용하게 되면 클로자핀 단독 투여에 비해 부가적인 치료 효과를 낳는 것으로 통제된 비교임상 연구를 통해 확인되었으며, 클로자핀에 할로페리돌과 아리피프라졸 병용 투여를 하여 비교한 연구에서 할로페리돌은 아리피프라졸과 유사한 정도의 부가적인 치료 효과를 유발하였다[35,36].
병용 약물로서 제안된 비정형 항정신병 약물은 상당히 다양하다. 리스페리돈, 아미설프라이드, 아리피프라졸, 서틴돌, 지프라시돈, 팔리페리돈, 퀘티아핀, 올란자핀 등 대부분의 비정형 약물이 포함되며, 대표적 약물들은 리스페리돈, 아미설프라이드, 아리피프라졸이 있다. 대부분의 개방연구에서는 비정형 항정신병약물 병용 요법의 효과가 확인되었으나, 무작위 배정 임상시험(randomized controlled trial, RCT)은 그에 비해 부족하여, 이를 대상으로 한 메타분석 결과에 따르면 해당 약제들 병용 효과의 근거가 큰 편이 아닌 것으로 나타나기도 한다. 그러나 병용 치료 자체의 효과 이득은 작지만 확실한 편이다. 메타 분석 결과들에 따르면 특히 아리피프라졸, 리스페리돈, 아미설프라이드의 효과가 부각된다. 리스페리돈의 경우 RCT를 통해 양성 증상에 대한 추가 효과가 반복 확인되었다. 아리피프라졸 및 아미설프라이드 병용의 경우에는 양성 증상 호전 외에도 음성 및 우울 증상 호전에 효과가 좋은 편으로 보고되었다[30-32].
최근 핀란드에서 처방된 약제에 따른 조현병 환자들의 재입원율을 분석한 연구 보고에서, 클로자핀과 아리피프라졸 병용 요법이 가장 우월한 효과를 보이는 것으로 보고되었다. 그 외에도 올란자핀, 리스페리돈, 퀘티아핀 등의 병용 치료가 클로자핀 단독 치료에 비해서 재입원율을 더 낮추었으며, 장기지속형 주사제 제형으로 처방 가능한 모든 항정신병약물 성분의 병용을 합쳐서 분석한 결과에서도 클로자핀 단독 치료에 비해 재입원율을 감소시켰다. 클로자핀과 수용체 결합 프로파일이 유사한 올란자핀의 병용 역시 많이 처방되고 있었으며, 재입원율의 추가적 감소를 보여 도파민 수용체 작용만을 병용의 기준으로 삼기는 어려워 보인다[37].
다양한 연구에서 클로자핀과 아리피프라졸 병용 요법의 부가적 효과가 반복 확인되고 있다. 클로자핀과 아리피프라졸 병용은 양성, 음성, 기분 증상에 대한 효과 뿐 아니라 강박 및 불안 증상에도 호전 효과를 보인다. 더욱이 추체외로 부작용이나 프로락틴 증가의 부가적 위험성이 적으며, 클로자핀에 의한 대사계 부작용 역시 오히려 경감시키는 것으로 보여 내약성 면에 있어서도 긍정적인 효과가 있다. 이와 같은 다각적 증상 영역에 대한 추가 효능 및 내약성 증진이 병용 투여에 의한 재입원 감소 효과로 이어지는 것으로 보인다. 아리피프라졸의 D2, 5-HT1A, 5-HT2C 수용체 부분 효현(partial agonism) 작용 및 5-HT2A수용체에 대한 길항 작용은 양성, 음성, 우울 증상에 대한 추가적 효과를 일으키면서도 진정작용, 체중증가 및 대사증후군의 위험성을 유발할 위험성은 적은 기전으로 제안되고 있어, 클로자핀 병용제로서 아리피프라졸의 역할이 주목되는 바이다[30,31,38].
클로자핀과 아리피프라졸 병용 치료의 효과에 대해 우리나라에서 시행된 2008년 연구 발표가 있었다. 클로자핀 복용 중인 환자에서 양성 증상의 호전 정도는 아리피프라졸 병용군과 대조군 사이에 큰 차이가 없었으나, 음성 증상 및 강박 증상의 호전에서는 유의한 차이가 있었다. 프로락틴과 중성지방의 혈중농도는 아리피프라졸 병용군에서 유의하게 낮았다. 이후 발표된 52주간 장기 추적 연구에서도 양성 증상 외에도 음성, 우울, 강박 증상 감소 및 대사 증후군 지표의 호전이 지속되었다. 아리피프라졸은 일일 5~30 mg 범위로 사용되었으며, 평균 용량은 약 10 mg로 높은 용량이 아닌 편이었다. 이는 우리나라 치료저항성 조현병 환자들을 대상으로 한 연구 결과로서 실제적 임상 사용에서의 가치를 지닐 수 있겠다[39,40].
Go to : 
적절한 클로자핀의 활용
산술적으로 대략 20~30% 조현병 환자가 치료저항성이며, 그 중 약 60%의 환자가 클로자핀에 의한 치료 효과가 있다고 가정해 볼 수 있다. 이에 따르면, 매우 단순화된 계산이지만, 전체 조현병 환자의 대략 12~18% 환자는 클로자핀을 복용하고 있다고 예상할 수 있다[41]. 덴마크, 핀란드 등의 북유럽 국가에서 주로 10% 이상의 조현병 환자가 클로자핀을 사용하고 있으나, 그 외 대부분의 국가에서는 클로자핀 처방률이 상당히 낮은 편이다[41]. 미국의 경우 주(state)마다 그 통계에 차이가 있으나 50% 이상의 주에서 5% 이내의 조현병 환자에게 클로자핀이 처방되고 있는 것으로 조사되었다[42]. 클로자핀 도입 이후, 많은 비정형 항정신병약물들이 발매되어 왔으나 역설적으로 클로자핀의 처방 비율은 최근 10여년간 더 증가하는 추세로 보고되기도 하였다[43]. 종합하면, 클로자핀 처방 비율이 기대 예상에 미치지는 못하지만, 새로운 항정신병약물의 지속적 도입 과정 속에서도 늘어나고 있다는 것이다. 다른 한편, 클로자핀 필요성의 지속적 증가에도 불구하고, 처방에 대한 장애물의 존재가 시사되는 바이다.
대표적인 장애물은 호중구 감소증 및 무과립구증과 같은 혈액학적 부작용에 대한 우려이다. 클로자핀 사용 후 호중구 감소증은 약 2.7%, 무과립구증은 약 0.7~0.8% 정도의 환자에서 나타난다. 무과립구증의 발견이 늦는 경우 사망으로 이어질 수 있는 치명적인 부작용이지만, 무과립구증의 발생 비율이 처음 클로자핀 도입 당시의 우려에 비해 높은 편은 아니며 CPMS의 적용으로 효과적인 예방이 이루어진 것 또한 사실 이다[44,45]. 의미있는 호중구 감소는 주로 치료 1년 이내에 발생한다. 그러나 클로자핀 사용 10년이 지나서 발생하는 혈액학적 이상에 대한 사례 보고는 매우 드물긴 하지만 있기는 하다. 한국에서 6,782명의 클로자핀 투여 환자를 조사한 바에 따르면 투여한지 6년이 지난 이후에 무과립구증이 나타난 사례는 없었다[46]. 2015년 미국 FDA는 혈액 검사 모니터링 기준을 다소 완화하여 absolute neutrophil count (ANC) 1,000~1,499/μL구간을 ‘경한 호중구 감소증(mild neutropenia)’으로 간주하고 혈액 검사를 더 자주하여 확인하면서 클로자핀 치료를 유지하는 것으로 두었다[45]. 네덜란드의 클로자핀 연구자들(Netherlands Clozapine Collaboration Group)의 경우, 정신병적 증상으로 문제가 되지 않고 적절하게 정보를 제공받은 환자들이 클로자핀 사용 시작 6개월 이후 정기적인 혈액검사 검사 시행을 거부하는 경우 수용할 수 있는 것으로 제안하기도 하였다. 물론 무과립구증의 위험이 의심되는 경우 혈액검사를 반드시 시행하며, 적어도 1년에 4회 정도의 검사는 필요할 것으로 언급하였다[47]. 클로자핀의 사용 경험이 축적되면서 전반적으로 혈액 검사 기준의 완화가 이루어지는 편으로 보인다. 물론 정기적 혈액 검사는 국가별로 지정된 규정에 맞추어 반드시 수행되어야 하며, 혈액학적 부작용 위험성을 간과해서는 안 된다[48,49].
혈액학적 부작용 외에 클로자핀에 의한 주된 부작용은 침 분비 과다, 졸림, 어지러움, 변비 등이 있으며, 클로자핀 치료 초기 몸살과 같은 주관적 불편감과 발열 등이 있어 초기 증량 시 환자들의 불편감이 있다. 또한 클로자핀은 체중 증가, 당 및 지질 대사 이상 등을 포함한 대사 증후군 유발 비율이 다른 항정신병약물에 비해 높은 편이다. 이와 같은 부작용들에 대해서는 정기적인 신체검진 및 실험실 검사들이 필요하다[29]. 그러나 무엇보다 의사와 환자가 협력적으로 부작용으로 인한 불편감과 용량 조정 등의 치료 과정 등을 논의하고 계획해 가는 과정이 부작용의 경감을 통한 최적의 치료에 가장 중요하다고 생각된다.
본 논문에서는 치료저항성 조현병에서 클로자핀 사용과 클로자핀 저항성 및 이에 대한 항정신병약물 병용 치료 방안을 살펴 보았다. 실질적인 처방 방법 및 개별 부작용과 그 중재 방안 등에 대해서는 본 논문에 포함되지 못하였으나, 이는 클로자핀의 적절한 처방에 주요한 부분으로 반드시 숙지가 필요하겠다. 특히 클로자핀과 기타 항정신병약물의 병용 투여 시 상호작용, 부작용 발현 등에 대해서 더 세심한 주의가 요구된다. 다른 한편, 클로자핀의 작용 기전에 대한 이해 증진은 조현병이 나아가는 과정을 이해하고 더 나은 치료제를 만드는데 기반이 될 것이다. 축적된 임상 경험과 연구 결과 보고들의 적절한 통합에 기반하여 클로자핀의 치료 이익을 최적화시킬 수 있는 노력들이 이어지고 있어, 조현병 치료의 향상이 기대되는 바이다.
Go to : 




 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download