서론
임신 기간 중 산모의 인슐린저항성은 지속적으로 증가한다[1]. 임신 중의 인슐린저항성 증가는, 산모 체내의 당 이용을 억제하여 태아로의 당의 이행이 효과적으로 되기 위한 생리적인 변화이다[2]. 산모의 인슐린저항성 정도는 태아로 전달되는 당의 양과 밀접히 관련되므로[1], 임신 주수가 늘수록 산모의 인슐린저항성은 증가한다. 임신 초기 인슐린감수성(sensitivity) 변화는 개인차가 있고 임신 전의 인슐린저항성 정도에 따라 결정되지만, 정상 내당능을 보이는 산모의 경우에도 인슐린저항성은 임신 후기로 갈수록 증가하여[3] 임신 전보다 약 33∼78% 정도 증가한다고 보고되어 있다[4,5]. 증가된 인슐린저항성은 산모에서 태아로의 당 운반을 효과적으로 이뤄지게 하지만, 임신 중 식후 혈당 상승의 주된 원인이 된다.
Go to : 
임신기간 중 혈당 변화
정상 임신 기간 중 혈당 변화는, 공복 혈당의 경우 임신 8주부터 감소하기 시작하여 12주 때 가장 낮은 반면, 식후 혈당은 지속적으로 상승하는 경향을 보인다[6,7]. 이는 임신 기간 중 인슐린감수성과 인슐린 분비능 변화의 결과이다.
가장 중요한 인체 내 당 생산(endogenous glucose production) 기관은 간으로, 간의 당 생산은 글리코겐 분해(glycogenolysis)와 당신생(gluconeogenesis)을 통해 이뤄지는데, 이는 주로 인슐린에 의해 억제된다. 임신 중에는 인슐린저항성으로 인해 공복 상태의 인슐린 농도가 높음에도 불구하고 간의 당 생산이 증가하여[3,8], 정상 산모의 경우, 임신 34주 이후는 임신 전에 비해 30% 정도 증가한다[3].
공복 상태에서 당 합성과 당 소모가 평형을 이루면 혈당은 약 90 mg/dL 정도를 유지하게 된다. 임신 중에는 간의 당 생산이 증가함에도 불구하고[3,8] 대개 공복 혈당은 감소하는데[4,5], 이는 임신 중 혈액량이 증가하면서 희석되는 효과[5], 신장으로 제거되는 당의 증가(renal clearance) [9], 태아-태반 당 소모 증가[5], 기초대사율의 증가[10,11] 등이 그 원인으로 생각된다.
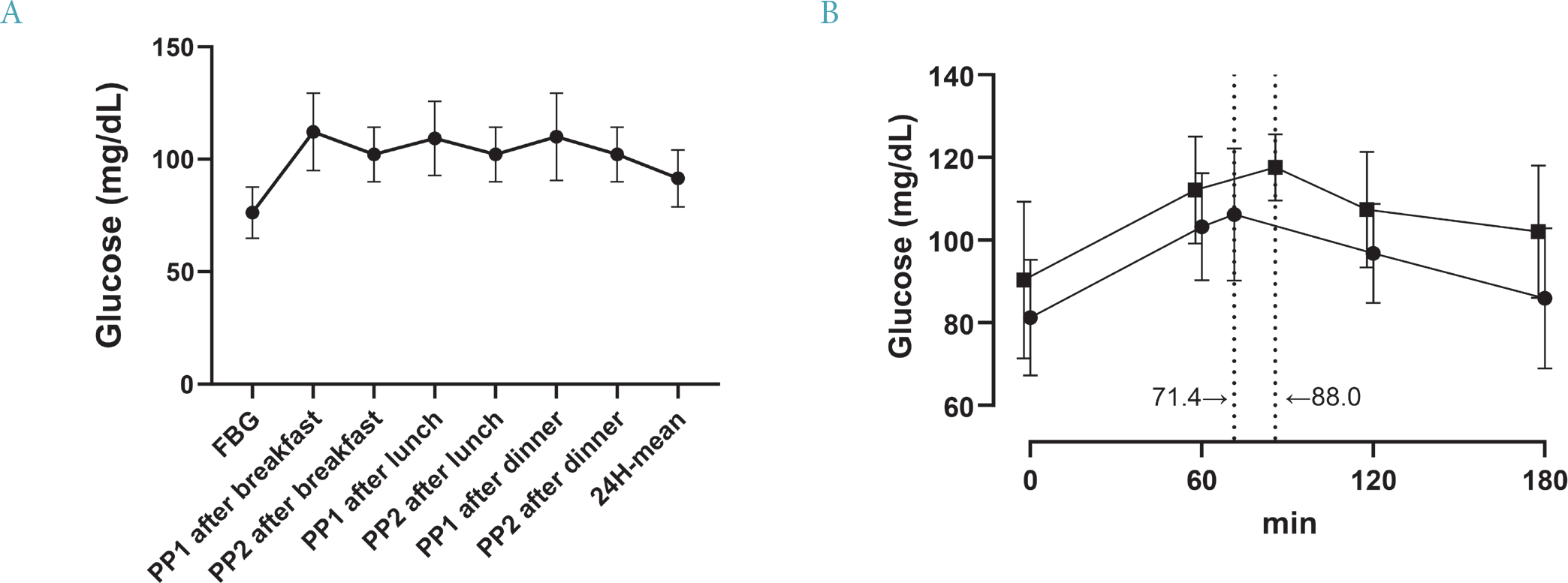
임신 28∼36주의 정상 산모의 연속측정 혈당을 메타분석해 보면, 아침 공복 혈당은 76.3 ± 11.4 mg/dL, 아침 식후 혈당은, 1시간 후, 2시간 후 각각 112.2 ± 17.2 mg/dL, 102.2 ± 12.1 mg/dL였다(Fig. 1A) [12]. 이런 혈당의 변동은 정상 산모에서도 비만 여부에 따라 차이가 있었는데(Fig. 1B), 임신 30주 정상 산모에서 공복 혈당도 비만한 산모에서 높았고(90.3 ± 19 mg/dL vs. 81.2 ± 14.0 mg/ dL), 식후 최고 혈당(peak glucose)도 비만한 산모에서 높았다(117.6 ± 8 mg/dL vs. 106.2 ± 16 mg/dL) [13]. 또한 식사 후 최고 혈당에 이르는 시간도 차이가 있었는데, 비만한 산모에서 88.0분으로, 비만하지 않은 산모(71.4분)에 비해 유의하게 길었다[13].
Go to : 
임신중 인슐린감수성의 변화
정상 산모에서도 임신 기간 중 산모의 인슐린감수성은 지속적으로 감소하지만[1], 인슐린감수성 변화를 임신 주수별로 확인하는 것은 쉽지 않다. 제1형 당뇨병 산모의 임신 중 인슐린 요구량 변동을 보면, 임신 중 인슐린감수성의 변화를 간접적으로 확인할 수 있는데, 임신 11∼16주에는 임신 전에 비해 인슐린 요구량이 약 –1%에서 –4% 정도 감소한다[14]. 이후 임신 20주부터 36주까지는 지속적으로 인슐린 요구량이 증가하는데, 임신 33∼36주에는 임신 전에 비해 약 70% 정도 인슐린 요구량 증가가 있다[14].
정상 산모에서 고인슐린 정상 혈당 클램프(hyperinsulinemic euglycemic clamp)로 측정한 인슐린감수성 변화 연구 결과도 위와 비슷한데, 임신 12∼14주 경은 임신 전과 인슐린감수성에 차이가 없으나, 임신 34주 이후에는 임신 전의 50∼60% 정도로 인슐린감수성이 감소한다[3]. 또한 Homeostatic Model Assessment for Insulin Resistance로 확인한 인슐린저항성의 경우, 정상 산모에서 임신 14주에 비해 임신 28주 경, 30% 이상 증가한다[15]. 임신성 당뇨병 산모의 경우, 임신 전부터 정상 산모에 비해 인슐린감수성은 감소해 있고[3], 임신 주수가 늘어남에 따라 인슐린감수성이 지속적으로 감소하지만, 일반적으로 정상 산모에 비해 임신기간 중 감소 폭이 크지 않다고 알려져 있다[3,15].
임신 중에는 간뿐만 아니라 근육 및 지방세포의 인슐린감수성도 감소하기 때문에[16,17], 인슐린에 의해 매개되는 근육, 지방세포의 당 축적(disposal)은 임신 기간 중 약 50% 감소한다[17]. 이는 인슐린수용체 이후의 신호전달과 관련되는데, 직접적으로는 인슐린수용체기질(insulin receptor substrate 1, IRS-1)의 티로신(tyrosine)기의 인산화 감소가 원인으로[18], 정상 산모의 경우에는 출산 후 회복된다[18]. 인슐린수용체 신호전달의 감소 기전은 확실히 규명되지는 않았으나, 임신 중 모체에서 분비되는 호르몬과 시토카인(cytokine)으로 일부를 설명하고 있다. 모체의 인슐린저항성을 높인다고 생각되는 인자로는 human placental lactogen (hPL), human placental growth hormone (hPGH), human chorionic gonadotropin (hCG), 코티솔(cortisol), 프로게스테론(progesterone), 프로락틴(prolactin), 종양괴사인자-α (tumor necrosis factor-α [TNF-α]) [19,20], 자유지방산(free fatty acid) [21] 등이다.
태반은 정상 산모의 인슐린저항성 증가에 매우 중요한 역할을 할 것으로 생각되며, 출산 직후 당 대사가 급속히 정상화되는 것은 그 간접적인 증거일 수 있다. 그러나 아직은 분자적인 기전이 잘 알려져 있지 않다. 또한 태반의 여러 호르몬(hPL, hPGH 등)은 기전 상 인슐린감수성을 감소시킬 수 있지만, 실제로 산모에서 태반 호르몬 농도와 인슐린저항성 사이에 뚜렷한 상관성은 없다고 알려져 있다[19]. 이는 태반 호르몬 외 다른 기전이 존재함을 시사하며, 지방세포 및 태반에서 분비되는 각종 시토카인과 아디포카인도 임신 중 인슐린저항성 증가에 기여할 것으로 생각된다. 특히 TNF-α는 임신 중 IRS-1의 세린(serine)기를 인산화함으로써 인슐린 신호전달을 감소시킬 수 있다[19,22]. 이외 엑소좀(exosome) [23], 장내세균총[24]의 역할이 대두되고 있으나, 더 연구가 필요하다.
Go to : 
임신중 인슐린 분비의 변화
인슐린 분비는 임신 기간 중 공복 상태와 식후 모두에서 증가하는데, 임신 후기의 인슐린 하루 평균 분비량은 임신 전의 2배에 가깝다[25]. 임신 기간 중 증가하는 인슐린저항성을 극복하고자 하는 반응으로 생각되고 있다. 동물모델에서 임신 기간 동안 모체의 췌도 크기가 증가하고 인슐린 분비가 증가함을 확인되었다[26].
공복 상태의 인슐린 농도는 임신 전 기간 동안 증가한 상태로 유지된다[27,28]. 기저 인슐린과 기저 C-peptide를 측정해 보면, 임신 초는 임신 전과 유의한 차이가 없지만, 임신 후반으로 갈수록 증가하여, 30주 이후, 임신 전에 비해, 약 65% 기저 인슐린 분비 증가가 보고되었다[29]. 이런 증가 양상은 정상 산모와 임신성 당뇨병 산모에서 차이는 없으나[29], 증가 폭은 임신성 당뇨병 산모에서 정상 산모보다 크다[3].
경구당부하 후 1기(1st phase; 당부하 후 0∼5분), 2기 (2nd phase; 당부하 후 5∼60분)의 식후 인슐린 분비도 임신 주수가 증가할수록 증가한다[3]. 그러나 임신 주수에 따른 인슐린 분비량의 증가 폭은 서구인에 비해 동양인에서 적고[15] 임신성 당뇨병 산모에서 정상 산모에 비해 적다[15].
Go to : 
결론
임신 중 정상 포도당 대사의 변화를 이해하는 것은, 임신성 당뇨병의 발병 원인을 이해하는 데 도움이 된다. 임신성 당뇨병도 다른 당뇨병과 같이 인슐린저항성과 인슐린 분비능의 장애가 모두 문제가 된다. 임신 시의 인슐린저항성은 앞서 기술한 임신 중 유발되는 생리적인 인슐린저항성 외에, 임신 전 개인이 가지고 있는 소인에 따른 인슐린저항성이 더해지게 되는데, 임신성 당뇨병 산모의 경우, 임신 전부터 인슐린저항성이 높다[8]. 임신성 당뇨병 산모의 경우도 임신 기간 중 인슐린 분비량이 증가하지만[30], 정상 내당능의 산모에 비교했을 때, 증가된 인슐린저항성 정도에 비해 인슐린 분비능이 낮다[3,5,30]. 즉, 베타세포의 상대적인 기능 저하로 인해, 임신 중 생리적으로 증가하는 인슐린저항성 및 이에 더해진 임신 전의 만성적인 인슐린저항성을 극복하지 못할 때 내당능 장애가 발생한다고 정리할 수 있다.
Go to : 




 PDF
PDF Citation
Citation Print
Print


 XML Download
XML Download