This article has been
cited by other articles in ScienceCentral.
초록
배경
수술 중 무손상부갑상선호르몬(intact parathyroid hormone, iPTH) 농도 측정은 부갑상선절제술에서 항진된 부갑상선이 완전히 절제되었는지 확인하거나 갑상선절제술 시 부갑상선 손상을 확인하는 데 도움이 된다. 수술 중 신속하게 결과를 얻기 위해 일반적으로 사용하는 혈청 검체 대신 혈장 검체를 사용함으로써 혈액응고 과정을 생략하여 검사소요시간(turnaround time, TAT)을 단축시킬 수 있다. 따라서, 본 연구에서는 혈장 iPTH와 혈청 iPTH의 검사결과를 비교하여 혈장 iPTH의 유용성을 평가하고, 혈장 iPTH 검사의 분석능을 검증하였다.
방법
2019년 3월 원자력병원 진단검사의학과에 의뢰된 혈장과 혈청 iPTH 검사의 검사소요시간을 비교하였다. 혈장 iPTH 검사의 분석능 평가를 위해 ADVIA Centaur iPTH assay (Siemens Healthineers, Germany)로 반복정밀도, 검사실 내 정밀도, 직선성 검증을 실시하였다. 또한 20명의 건강한 성인으로 참고범위를 검증하였다. 검체 간 비교를 위해 환자 100명의 같은 날 채혈된 혈장과 혈청 검체로 iPTH 농도를 비교하였다.
결과
혈장 iPTH 분석에서 혈청보다 짧은 검사소요시간을 나타내어(P <0.001) 검사시간 단축에 유용함을 알 수 있었다. 혈장 iPTH의 분석능 평가에서 반복정밀도와 검사실 내 정밀도는 제조사의 기준을 만족하였다. 혈장 iPTH 농도는 5.1 pg/mL부터 1,670.0 pg/mL까지의 범위에서 직선성을 보였다(R2 =0.999). 20명의 건강한 성인의 검사결과는 모두 시약 제조사의 참고범위 안에 들어 참고범위가 검증되었다. 검체 간 iPTH 농도 비교에서는 혈장이 혈청에 비해 높았다(P <0.001). 또한 혈장과 혈청 iPTH 농도는 강한 양의 상관관계를 보였다.
결론
결론적으로 혈장 iPTH 농도는 혈청보다 높고 강한 양의 상관관계를 갖는다. 또한, 혈청 검체와 비교했을 때 검사소요시간을 단축시킬 수 있으므로 신속한 검사결과 확인이 필요한 경우 유용하게 사용할 수 있다.
Go to :

Abstract
Background
Intraoperative measurement of intact parathyroid hormone (iPTH) levels is crucial for confirming complete removal of hyperfunctioning parathyroid glands during parathyroidectomy and for detecting parathyroid gland damage during thyroidectomy. The use of plasma samples can shorten the turnaround time (TAT) for iPTH. The present study explored the effectiveness of using plasma samples for iPTH quantitation by comparison with the corresponding serum samples. We also evaluated the analytical performance of iPTH.
Methods
The TAT of plasma and serum samples analyzed in March 2019 was compared. In addition, comparative evaluation of the iPTH levels in 100 paired plasma and serum samples were performed. Analytical performances including within-run and within-laboratory precision, and linearity were evaluated in plasma samples using the ADVIA Centaur iPTH assay (Siemens Healthineers, Germany). The reference range was verified with plasma samples collected from 20 healthy adults.
Results
Plasma iPTH tests showed shorter TAT values (P <0.001) and higher iPTH levels (P <0.001) than serum. Correlation analysis between plasma and serum iPTH levels showed a strong positive correlation (r=0.925). The within-run and within-laboratory precision values were within the manufacturer’s recommendation. iPTH showed linearity from 5.1 to 1,670.0 pg/mL (R2 =0.999). The plasma iPTH levels from 20 healthy adults were within the reference range, thus validating our method.
Conclusions
The plasma iPTH levels were higher than the serum levels, with a strong positive correlation. The TAT of plasma samples was considerably shorter than that of serum. iPTH quantitation from plasma samples is preferable when rapid results are required.
Go to :

Keywords: Intact parathyroid hormone, Comparison, Plasma, Serum
서 론
부갑상선호르몬(parathyroid hormone, PTH)은 부갑상선에서 생성되며 세포 외 칼슘농도 조절에 가장 중요한 물질이다[
1]. 부갑상선호르몬은 84개의 아미노산으로 이루어진 펩타이드이다. 체내에서는 부갑상선호르몬이 84개의 아미노산 중 일부만 가지고 있는 분절형태로도 존재하는데, 무손상부갑상선호르몬(intact parathyroid hormone, iPTH)은 84개의 아미노산을 모두 가지고 있다. iPTH는 간의 쿠퍼 세포에 의해 분절로 분해되고 신장을 통해 배출되며 반감기는 4분 미만이다[
1,
2].
부갑상선호르몬 농도는 일차성 부갑상선항진증과 위장관 기능장애, 비타민D 결핍, 만성신부전, 골대사 장애, 유전적 질환, 약물(비스포스포네이트) 등의 원인으로 발생할 수 있는 이차성 부갑상선항진증 시 높아지고, 갑상선 절제술이나 부갑상선 절제술로 인한 손상, 자가면역질환, 혈색소침착증, 저마그네슘혈증, 유전적 원인으로 인한 부갑상선저하증 시에는 낮아지는 것으로 알려져 있다[
3-
5]. 부갑상선호르몬 농도 측정은 대사성골질환, 고칼슘혈증, 저칼슘혈증과 신성골이영양증의 진단과 관리에 필수적이다[
3,
4,
6]. 또한 iPTH는 일차성 부갑상선항진증 환자에서 부갑상선 절제 직후 측정하여 부갑상선절제술의 평가에 사용될 수 있으며[
7-
9], 갑상선전절제술 시행 후 저칼슘혈증의 발생을 예측하는데 유용하다[
10-
13].
혈청 검체로 iPTH 검사를 실시할 경우 검체 준비 과정에서 혈액응고에 30분, 원심분리(1,000 g)에 15분이 소요된다. 반면, 혈장 검체는 혈액응고 과정 없이 원심분리만으로 검사를 실시할 수 있으므로 혈액응고에 소요되는 시간인 30분이 단축되어 더 신속하게 결과를 도출할 수 있다[
14]. 그러므로 혈장 검체로 iPTH 검사를 할 경우 부갑상선절제술이나 갑상선전절제술과 같이 신속하게 iPTH 검사결과가 필요할 때 도움이 될 수 있다.
이에 본 연구에서는 Siemens ADVIA Centaur XP (Siemens Healthineers, Erlangen, Germany) 기기와 두 부위 비경쟁 면역측정법(two-site, noncompetitive immunoassay)을 원리로 하는 ADVIA Centaur iPTH assay (Siemens Healthineers) 시약을 이용하여 혈청과 혈장의 iPTH 측정 시 검사소요시간(turnaround time, TAT)과 검사결과를 비교하고 혈장 검체로 iPTH의 분석능을 검증하여 혈장 iPTH의 유용성을 평가하고자 한다.
Go to :

재료 및 방법
1. 혈장과 혈청의 iPTH 농도 비교를 위한 검체 선정
국가방사선혈액자원은행(Korea Institute of Radiological and Medical Sciences Radiation Biobank, KRB)이 보유하고 있는 췌장암 환자 15명, 전립선암 환자 20명, 위전절제술 후 위암 환자 25명과 갑상선전절제술 후 갑상선 암 환자 40명의 같은 날 채혈된 100명의 혈장(100건)과 혈청(100건) 검체를 분양받았다(
Table 1).
Table 1
General and clinical information of patients participating in this study
|
Characteristics |
Patients (N=100) |
|
Age (yr) |
60 (21-83)*
|
|
Sex (%) |
|
Male |
54 |
|
Female |
46 |
|
Clinical diagnosis (%) |
|
Pancreatic cancer |
15 |
|
Prostate cancer |
20 |
|
Gastric cancer status post total gastrectomy |
25 |
|
Thyroid cancer status post total thyroidectomy |
40 |

분양받은 검체 중 검체량이 100 µL 미만으로 부족하거나 육안검사 시 고지방 혼탁, 황달, 용혈이 확인된 검체는 연구에서 제외하였다. 이 연구는 원자력병원 임상연구심의위원회의 승인(KIRAMS 2018-12-007)을 받아 진행하였다.
2. 검사소요시간(Turnaround time, TAT) 비교
2019년 3월 한 달간 원자력병원 진단검사의학과에 의뢰된 혈청과 혈장 iPTH 검사를 대상으로 검체 접수시각부터 검사결과 보고까지 소요되는 시간을 검사소요시간으로 정하여 비교하였다. 혈장의 평균 검사소요시간이 혈청보다 적고 두 검체의 검사소요시간의 평균이 유의한 차이를 보이면 혈장 iPTH 검사가 검사소요시간 단축에 유용하다고 평가하였다.
3. 분석능 검증
1) 정밀도(Precision)
Siemens ADVIA Centaur XP system (Siemens Healthineers)의iPTH 검사의 전용 정도관리물질인 ADVIA Centaur PTH Quality Control (Siemens Healthineers)을 사용하여 정밀도를 검증하였다. 본 정도관리 물질은 총 3가지 농도(low, medium, high)의 물질을 제공하고 있다. Clinical and Laboratory Standards Institute (CLSI) EP15-A3 지침에 따라 3가지 농도의 정도관리물질을 1일 5회, 5일간 측정하여 반복(within-run) 정밀도와 검사실 내(within-laboratory) 정밀도를 검증하였다[
15].
2) 직선성(Linearity)
제조사에서 제시한 측정가능범위는 4.6-2,000 pg/mL이다. iPTH가 저농도(5.1 pg/mL)와 고농도(1,670.0 pg/mL)인 보정물질(calibrator)을 혼합하여(0:4, 1:3, 2:2, 3:1, 4:0) 제조한 5가지 농도의 물질을 2회 반복 측정하였다. 다항회귀분석을 실시하여 최적합 다항식모델을 구하였고, 모델의 차수가 2차 이상일 경우 1차식과 최적합모델과의 예측값 차이가 5%의 허용범위 이내이면 직선성을 만족하는 것으로 판정하였다[
16].
3) 참고범위 검증(Reference range validation)
일상검사 후 발생한 잔여검체 중 건강한 성인의 혈장 검체를 참고범위 검증에 사용하였다. 20세에서 70세 사이의 성인의 검체 중 전혈구계산치, 칼슘, 크레아티닌, 유리티록신, 갑상선자극호르몬 검사결과가 모두 참고범위 이내인 검체 20개를 선별하여, iPTH 농도를 측정하여 제조사에서 제공하는 참고범위를 검증하였다[
17]. 제조사에서 제공하는 혈청과 혈장 iPTH 농도의 참고범위는 각각 18.5-88.0 pg/mL, 18.4-80.1 pg/mL이었다.
4. 혈장과 혈청의 iPTH 농도 비교
대상 환자의 혈청과 혈장 검체로 대응표본 Wilcoxon 검정을 이용하여 iPTH 결과에 유의한 차이를 보이는지 확인하고, 상관분석하여 상관계수(r) 및 유의확률(P)을 확인하였다.
5. 통계 분석
정량적인 결과의 비교에는 대응표본 Wilcoxon 검정과 독립표본 T검정과 독립표본 Mann-Whitney U 검정을 이용하였으며, 통계분석을 위해 Microsoft Office 365 Excel (Microsoft Corp., Redmond, WA, USA), SPSS v21.0 (SPSS Inc., Chicago, IL, USA)과 Origin pro 2018 (OriginLab Corp., Northampton, MA, USA) 프로그램을 이용하였다.
Go to :

결 과
1. 검사소요시간(Turnaround time) 비교
혈장과 혈청 검사소요시간은 각각 45.5±15.4분과 89.7±22.8분으로 혈장에서 유의하게 짧은 검사소요시간을 나타냈다(P<0.001) (
Table 2).
Table 2
Comparison of TAT values between plasma and serum iPTH measurements from independent samples
|
TAT values |
Parameter from t-test |
|
|
|
Mean±SD (min) |
P-value |
|
Plasma iPTH |
45.5±15.4 |
<0.001 |
|
Serum iPTH |
89.7±22.8 |
|

2. 분석능 검증
1) 정밀도(Precision)
3가지 농도(low, medium, high)에서 구한 반복정밀도는 각각1.8%, 1.5%, 1.3%로 시약 제조사에서 제공하는 기준인 6%를 만족하였고, 검사실 내 정밀도는 각각 2.6%, 2.4%, 2.1%로 시약 제조사의 기준인 8%를 만족하였다(
Table 3).
Table 3
Precision of the Siemens ADVIA Centaur XP immunoassay system for iPTH quantitation
|
Mean±SD (pg/mL) |
Within-run precision (%CV) |
Within-laboratory precision (%CV) |
|
Low |
31.7±0.8 |
1.8 |
2.6 |
|
Medium |
175.9±4.0 |
1.5 |
2.4 |
|
High |
661.8±13.3 |
1.3 |
2.1 |

2) 직선성(Linearity)
다항회귀분석에서 최적합 다항식 모델이 1차 다항식으로 분석되었고 5.1 pg/mL부터 1,670.0 pg/mL까지의 범위에서 직선성을 만족하였다(R
2 =0.999) (
Fig. 1).
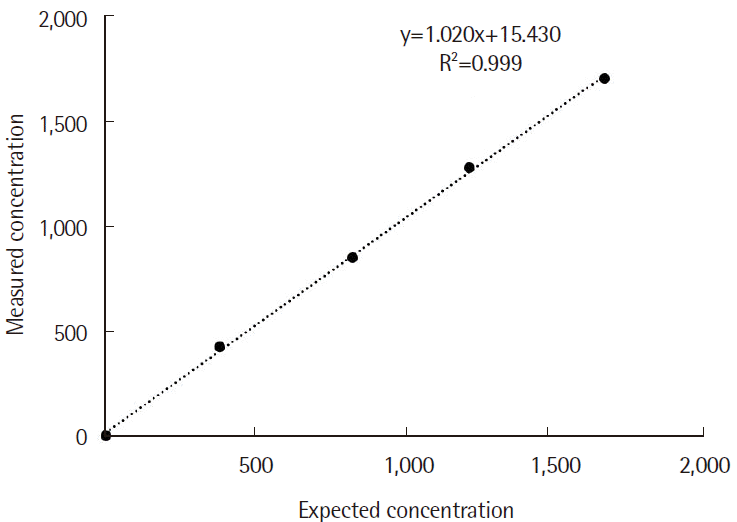 | Fig. 1
Linearity of the Siemens ADVIA Centaur XP immunoassay system for iPTH quantification. Good linearity is observed in the range from 5.1 to 1,670.0 pg/mL (R2 =0.999).
Abbreviation: iPTH, intact parathyroid hormone.

|
3) 참고범위 검증(Reference range validation)
건강한 성인의 혈장 검체 20개를 사용해 iPTH를 측정한 결과 모두 시약 제조사의 참고범위(18.4-80.1 pg/mL) 안에 들어 제조사가 권장하는 참고범위가 검증되었다.
3. 혈장과 혈청의 iPTH 농도 비교
혈청과 혈장 iPTH 농도의 중앙값은 각각 35.1 pg/mL, 41.1 pg/mL이고, 혈장에서의 측정값이 유의하게 높았으며(
P <0.001) (
Fig. 2), 상관분석에서 상관계수가 0.925로 강한 양의 상관관계를 보였다(
Fig. 3).
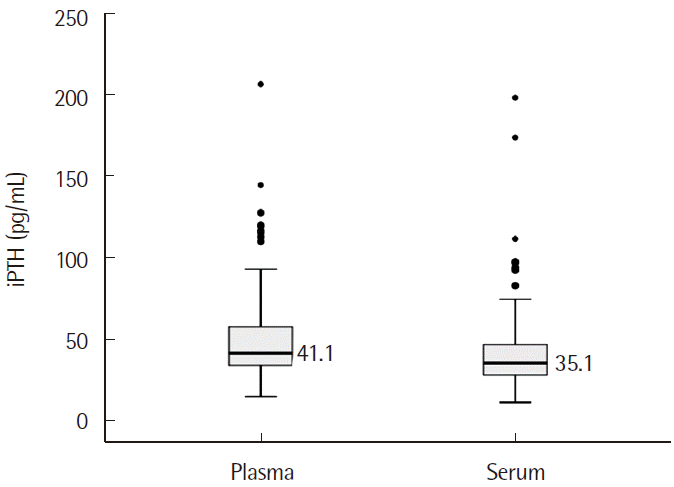 | Fig. 2
Box plot of plasma and serum iPTH measurements. Plasma sam-ples show significantly higher iPTH levels compared with serum samples (median value of 41.1 vs 35.1 pg/mL, P <0.001).
Abbreviation: iPTH, intact parathyroid hormone.

|
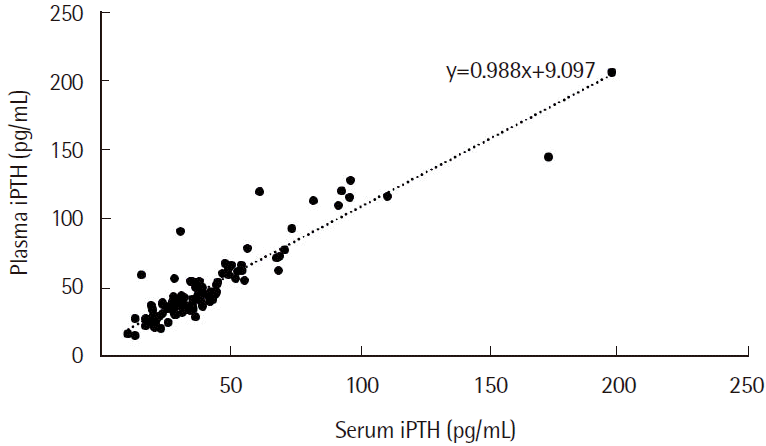 | Fig. 3Scatter plot of plasma and serum iPTH measurements. Plasma and serum iPTH levels show a strong positive correlation (r=0.925). Abbreviation: iPTH, intact parathyroid hormone. 
|
Go to :

고 찰
이 연구에서는 혈장 iPTH 검사의 유용성을 평가하였다. 혈장과혈청 iPTH의 검사소요시간 비교에서는 혈장이 혈청에 비해 유의하게 짧은 검사소요시간을 보였다. 혈장과 혈청의 검사소요시간의 평균이 각각 45.5분과 89.7분으로 42.2분의 차이를 보였다. 이는 혈액응고에 소요되는 시간인 30분 보다도 더욱 큰 차이인데 혈액응고 과정이 없어 검사자가 혈액응고가 끝난 검체를 확인하고 다음 단계로 진행하는 과정이 생략되어 이와 같은 차이가 발생한 것으로 보인다.
반복정밀도와 검사실 내 정밀도는 제조사의 기준을 만족하였고, 직선성 평가에서 우수한 직선성을 보였으며, 참고범위 검증에서도 CLSI EP28-A3의 참고치 검증 기준을 만족하여 혈장 iPTH 검사의 분석능이 검증되었다.
혈청 iPTH와 혈장 iPTH의 농도값은 높은 상관관계를 보였고, 혈장 농도가 높았고, 유의한 차이를 보였다. 그러므로 혈청과 혈장검체에 제시된 각각의 참고범위를 검증하여 사용하는 것이 권장된다. 검체 별로 국가방사선혈액자원은행에서 냉동보관(-80°C) 시 보관 기간(최대 1,266일, 최소 502일, 중앙값 693.5일)의 차이가 있었고, 냉동보관(-80°C) 시에는 혈청이 혈장보다 안정적이라는 연구 결과[
18]가 있어 보관 기간의 차이가 측정값에 영향을 미쳤을 가능성도 있다.
혈청 iPTH의 경우 검사 전 응고과정이 필요하여 수술 중 부갑상선호르몬 측정과 같이 부갑상선호르몬 농도 측정이 빠르게 필요한 경우 원심분리 후 바로 검사가 가능한 혈장 iPTH 검사를 활용할 수 있다.
본 연구에서 사용한 각 검체의 냉동보관 기간이 상이하여 보관 중 iPTH 농도가 바뀔 수 있어 제한점이 될 수 있다. 또한 대부분의 환자의 검사결과가 참고범위 안에 포함되어 있어 참고범위를 벗어나는 고농도와 저농도에서의 혈장과 혈청 검사결과 비교가 충분히 이루어지지 못한 점도 본 연구의 제한점이다. 차후 고농도와 저농도에서의 검체 간 비교가 필요할 것으로 보인다. 또 다른 제한점은 수술 중 혈장 검체로 iPTH 검사를 하고 혈청 검체로 iPTH 농도를 경과관찰할 때 혈장과 혈청 iPTH 검사를 혼용하게 되는 경우이다. 혈장과 혈청 iPTH는 참고범위가 다르며, 본 연구에서도 같은 환자에서 채혈한 혈장과 혈청의 iPTH 농도가 유의한 차이를 보였다. 따라서 iPTH 농도의 증감을 임상에서 오인하거나 경과관찰 중 검사결과 확인을 할 때 검체의 종류가 다르므로 연속적인 결과로 조회되지 않아 불편할 수 있다. 그러므로 iPTH 측정 목적과 검체 구분에 따른 결과보고 방식 등에 대한 검사실 내 체계 설립이 필요하다.
결론적으로 혈장 iPTH 농도는 혈청 iPTH 농도보다 높게 측정되었고, 각각의 평균 농도값은 강한 양의 상관관계를 보였다. 또한, 혈장 검체는 혈청 검체와 비교했을 때 혈액응고에 소요되는 시간인 30분 보다 더 검사소요시간을 단축시킬 수 있으므로, 수술 중 iPTH 농도 측정과 같이 신속한 검사결과 확인이 필요한 경우 유용하게 사용할 수 있다.
Go to :

감사의 글
이 연구는 과학기술정보통신부 한국원자력의학원 연구운영비지원사업(No.50544-2019)의 지원을 받아 수행하였습니다. 본 연구에사용된 인체자원은 한국원자력의학원 국가방사선혈액자원은행에서 제공받았습니다.
Go to :

Notes
Go to :

REFERENCES
3. Goettsch C, Iwata H, Aikawa E. 2014; Parathyroid hormone: Critical bridge between bone metabolism and cardiovascular disease. Arterioscler Thromb Vasc Biol. 34:1333–5. DOI:
10.1161/ATVBAHA.114.303637. PMID:
24951650. PMCID:
PMC4094346.

4. Bilezikian JP, Khan A, Potts JT Jr, Brandi ML, Clarke BL, Shoback D, et al. 2011; Hypoparathyroidism in the adult: epidemiology, diagnosis, pathophysiology, target-organ involvement, treatment, and challenges for future research. J Bone Miner Res. 26:2317–37. DOI:
10.1002/jbmr.483. PMID:
21812031. PMCID:
PMC3405491.

6. Adhikary LP, Yadava SK, Pokharel A, Khadka D, Thakur R. 2015; Relation between calcium, phosphorus, calcium-phosphorus index and iPTH in chronic kidney disease patients. J Nepal Health Res Counc. 13:50–3. PMID:
26411713.
8. Naik AH, Wani MA, Wani KA, Laway BA, Malik AA, Shah ZA. 2018; Intraoperative parathyroid hormone monitoring in guiding adequate parathyroidectomy. Indian J Endocrinol Metab. 22:410–6. DOI:
10.4103/ijem.IJEM_678_17. PMID:
30090736. PMCID:
PMC6063190.

9. Carr AA, Yen TW, Wilson SD, Evans DB, Wang TS. 2017; Using parathyroid hormone spikes during parathyroidectomy to guide intraoperative decision-making. J Surg Res. 209:162–7. DOI:
10.1016/j.jss.2016.10.006. PMID:
28032553.

11. Lindblom P, Westerdahl J, Bergenfelz A. 2002; Low parathyroid hormone levels after thyroid surgery: a feasible predictor of hypocalcemia. Sur-gery. 131:515–20. DOI:
10.1067/msy.2002.123005. PMID:
12019404.

12. Lombardi CP, Raffaelli M, Princi P, Santini S, Boscherini M, De Crea C, et al. 2004; Early prediction of post thyroidectomy hypocalcemia by one single iPTH measurement. Surgery. 136:1236–41. DOI:
10.1016/j.surg.2004.06.053. PMID:
15657581.
13. Lee DR, Hinson AM, Siegel ER, Steelman SC, Bodenner DL, Stack BC Jr. 2015; Comparison of intraoperative versus postoperative parathyroid hormone levels to predict hypocalcemia earlier after total thyroidectomy. Otolaryngol Head Neck Surg. 153:343–9. DOI:
10.1177/0194599815596341. PMID:
26209077.

14. Souberbielle JC, Brazier F, Piketty ML, Cormier C, Minisola S, Cavalier E. 2017; How the reference values for serum parathyroid hormone concentration are (or should be) established? J Endocrinol Invest. 40:241–56. DOI:
10.1007/s40618-016-0553-2. PMID:
27696297.

15. Clinical and Laboratory Standards Institute. 2014; User verification of precision and estimation of bias; Approved guideline-third edition. CLSI document EP15-A3. Clinical and Laboratory Standards Institute;Wayne, PA:
16. Clinical and Laboratory Standards Institute. 2003; Evaluation of the linearity of quantitative measurement procedures: A statistical approach; Approved guideline. CLSI document EP06-A. Clinical and Laboratory Standards Institute;Wayne, PA:
17. Clinical and Laboratory Standards Institute. 2008; Defining, establishing, and verifying reference intervals in the clinical laboratory; Approved guideline-third edition. CLSI document EP28-A3. Clinical and Laboratory Standards Institute;Wayne, PA:
18. Cavalier E, Delanaye P, Hubert P, Krzesinski JM, Chapelle JP, Rozet E. 2009; Estimation of the stability of parathyroid hormone when stored at -80 degrees C for a long period. Clin J Am Soc Nephrol. 4:1988–92. DOI:
10.2215/CJN.03970609. PMID:
19820128. PMCID:
PMC2798870.
Go to :





 PDF
PDF Citation
Citation Print
Print





 XML Download
XML Download