Abstract
Neuropathic pain is associated with primary lesion or dysfunction of the peripheral and central nerve systems, affecting up to 10% of the general population. Although both nociceptive pain and neuropathic pain utilize the same nervous system pathways, physiologic differences exist in the pathologic mechanism, clinical presentation, and treatments. Ectopic activity in primary afferent fibers, excitatory and inhibitory somatosensory signaling, nociceptive neuron alterations, and central pain modulation have been implicated in neuropathic pain. These neuropathic mechanisms are associated with the complexity of symptoms, difficult treatment decisions, and challenging poor outcomes. Treatment options include pharmacologic (e.g., anticonvulsants, antidepressants, lidocaine, N-methyl-D-aspartate antagonist, opioids), physical, psychological (e.g., cognitive behavioral therapy), or interventional management (e.g., peripheral or neuro-axial nerve blockade, spinal cord stimulators, intrathecal medications). Medication selection should be individualized, considering patients’ symptoms and potential beneficial or deleterious effects (side effects) on comorbidities. The interventional management of chronic neuropathic pain should be considered for patients who have not responded to pharmacologic and non-interventional treatments, as an integral component of a more comprehensive approach. This article presents an overview of physiological mechanisms, clinical presentation, and assessment of neuropathic pain, and discusses treatment options for neuropathic pain.
Go to : 
신경성 통증은 말초 및 중추 신경계의 병변이나 기능 이상으로 발생하는데, 말초 신경근병증이나 신경압박증후군과 같은 전형적인 신경 손상에 기인한 신경병증 통증 이외에 외상과염, 아킬레스건염, 족저근막염 혹은 급성 염좌 등 다양한 근골격계 질환에서도 확인된다[1,2]. 이들 통증의 강도는 반드시 조직의 손상 정도에 비례하지 않고, 손상이 치유된 이후에도 지속되는 경우가 흔하다[2]. 비슷한 정도의 손상에서도 개인에 따라 서로 다른 양상과 강도의 통증이 발생한다[3]. 통증의 신경생리학적 발생 기전에 따라 통각수용 통증(nociceptive pain), 말초 신경성 통증(peripheral neuropathic pain) 및 중추 신경성 통증(central neuropathic pain)으로 분류하기도 하는데 이들은 각각 통증 수용체, 말초신경, 중추 신경이 매개하는 신경생리학적 통증 분류에 해당한다[4]. 대부분의 통증들이 이들 기전의 복합적인 상호 작용으로 발생하지만, 상대적으로 주된 역할을 하는 우세한 기전이 존재한다. 대부분의 만성 통증 환자들은 부분적으로 신경성 통증을 호소하는데, 신경성 통증이 주된 통증 양상인 경우 통증 강도가 심하고 기능 상실이나 삶의 질 저하 정도가 두드러진다[5]. 체성감각의 신호 전달과정에서 흥분과 억제 및 중추 신경계에서 통증 신호 조절 등 복잡한 신경성 통증 기전이 신경성 통증의 치료를 어렵게 하기 때문에[6], 조기에 신경성 통증을 식별하고 포괄적으로 관리하는 접근이 중요하다.
Go to : 
신경성 통증은 체성각감 신경 자체의 손상이나 기능 이상을 포함하기 때문에 감각 이상을 흔히 동반하고 통증에 대한 과민화 등의 특이 증상이 수반된다[7]. 신경 자체의 손상은 기계적, 화학적 손상 및 감염 등 다양한 원인으로 발생할 수 있으며, 환자들은 칼로 베이는 듯한 혹은 타는 듯한 양상의 통증을 주로 호소한다[5]. 말초 신경 손상과 관련된 통증 지각은 신경간 통증(nerve trunk pain)과 지각부전 통증(dysesthetic pain)으로 구성되는데, 신경간(신경원 줄기) 통증은 감작된 통각 수용체의 활동 증가로 발생하여 깊고 쑤시는 양상으로 느껴지는 반해, 지각 부전 통증은 불타는, 저린, 찢기는, 혹은 전기가 통하는 양상의 친숙하지 않은 이상 감각 양상이며 손상된 구심성 신경 섬유가 과하게 흥분되면서 발생한다. 이질통(allodynia)과 통각과민(hyperalgesia)은 전형적인 신경성 통증의 양상에 해당한다. 이들 공통적인 임상 양상은 신경성 통증이 일련의 병태생리학적 기전을 공유하는 것을 시사한다. 신경성 통증 자체는 급성기에 손상이 치유될 때까지 손상 부위를 보호하는 역할을 하지만, 만성 신경성 통증의 경우 신경계가 부적절하게 반응하여 감각 신호를 잘못 받아들이고 불균형을 초래하여 지속적인 통증 상태를 유발한다. 신경성 통증은 양성 증상과 음성 증상으로도 분류하는데, 양성 증상은 근육의 경련이나 이상 감각 (paresthesia or dysesthesia) 등 신경계의 비정상적인 흥분과 관련되며, 음성 증상은 감각 소실(hypoesthesia or anesthesia)이나 근력약화 등 신경 전도 감소와 관련된다[8].
말초 신경성 통증이 피부 분절(dermatomal)이나 피부 신경의 분포 양상(cutaneous distribution)을 따라 발생하고 신경 조직을 자극하는 특정 부하 동작으로 증상이 악화되는데 반해, 중추 신경성 통증의 경우 증상의 범위가 특정 신경의 연관 부위를 벗어나 널리 분산되고 다양한 비특이적 자극에 의해 과도한 통증과 신경 증상을 나타내는 경향이 있다(Table 1).
Mechanism-based classification for musculoskeletal pain
Go to : 
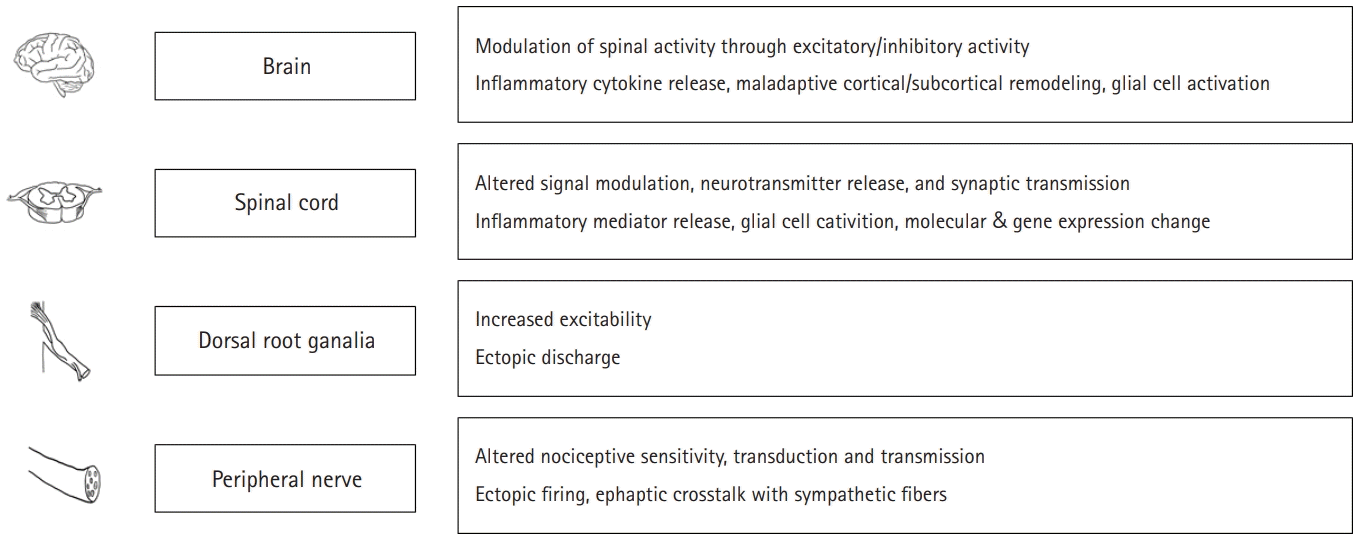
신경성 통증은 대개 구심성 통각 섬유의 손상에서 시작된다. 신경계의 손상이 국소적으로 시작된 경우에도 만성 통증으로 진행하는 과정에서 신경계 전반으로 반응 범위가 넓어진다(Fig. 1). 통각 수용과 관련된 신경 섬유(Aδ and C fibers) 말단에서 대사성 손상, 독소, 약물, 염증 물질 등에 의해 통증이 시작되면, 해당 신경 섬유가 보다 치밀해지고 과흥분 상태가 초래된다[5]. 축색을 따라 과한 자극, 압박, 염증, 외상, 저산소증 등이 원인이 되어 섬유가 변성되거나 channel 발현이 달라지면서 신호 전달 오류나 이소성 발화가 초래되고, 위성 교세포(satellite glial cell)나 자율신경세포의 분포 및 발현 양상의 변화로 통증 반응을 일으키기 쉬운 흥분 상태가 된다. 배근 신경절(dorsal root ganglia)에서 구심성 신경세포체(afferent neuron)가 손상되면 세포막과 신경 접합부(synapse)의 성상이 변하면서 말초 신경의 부적절한 신호 자극이 통증 전달 체계에 다양한 오류를 초래하게 된다[5].
반복적이거나 강한 자극이 상위 중추로 전달되면 척추 및 뇌의 중추성 통각 수용 전달체계는 뒤이어 오는 통증 자극에 매우 민감해지는데, 말초 신경병증에서 지속되는 통각 입력으로 중추성 통증 감작이 발생한다. 중추성 감작은 역치 이하의 구심성 자극에 대해 중추 신경계의 통각 관련 반응이 증가한 상태로 정의할 수 있는데, 신경 세포 접합부에서 칼슘 투과성 변화나 수용체 발현 양상과 관련된다. 중추 신경계에서 하향성 촉진 및 억제 조절 불균형도 만성 통증의 주요 요인이다. 대뇌 피질 및 피질하 기질의 가소성(plasticity)의 부적응도 통증 신호 해석과 관련되어 통증 상태를 지속시킨다[9].
말초성 신경병증 환자에서 통증에 대한 감작은 손상 인접부의 통각과민으로 나타나는데, 중추 신경계의 통증 유도 조절(conditioned pain modulation)을 통한 하향성 통증 억제 실패와 관련된다[5]. 말초 신경병증 환자들의 신경 영상 분석에서 피질 혹은 피질하 부위 뇌활성도 및 기능적 연결이 달라지며 뇌척수액 내의 다양한 사이토카인 증가가 관찰되는데, 이들 변화는 신경성 통증의 중추 신경 기전을 설명하는 데 도움이 된다[10].
Go to : 
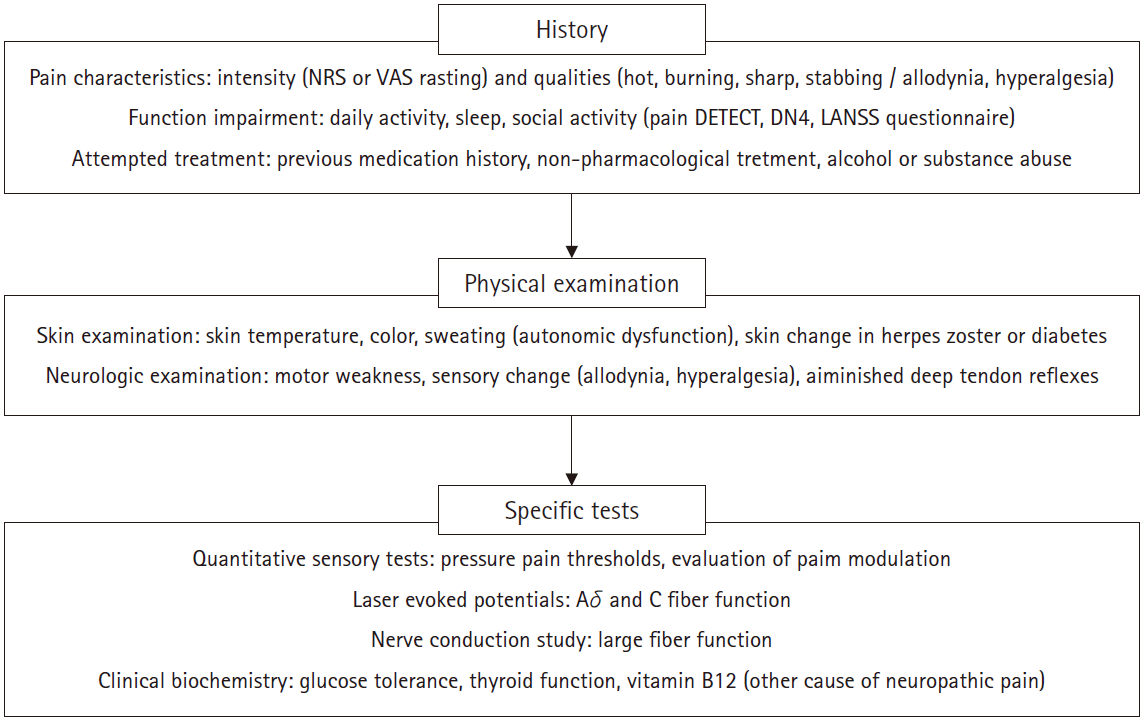
신경성 통증의 진단에 있어 표준화된 기준이 없기 때문에, 환자의 병력, 증상, 신경학적 검진 등을 포괄하여 신경성 통증의 양상을 평가하는 접근이 바람직하다(Fig. 2). 통증 자체의 평가에 있어 흔히 사용되는 척도로 시각통증척도(visual analog scale) 및 수치평가척도(numeral rating scale)나 Short Form McGill pain Questionnaire (SF-MPQ) [11]가 있으며, 통증 양상이나 기전을 고려하여 통증파국화척도(Pain Catastrophizing Scale) [12]나 Neuropathic Pain Scale [13] 등이 사용되기도 한다. 신경성 통증에 보다 특화된 평가 도구로 painDETECT [14], Doleur Neuropathic 4 (DN4) [15], Leeds Assessment of Neuropathic Symptom and Signs Pain Scale (LANSS) [16] 등은 신경성 통증의 양성(타는 느낌, 저린감, 접촉 자극에 대한 과민, 전기 오는 듯한 느낌, 온도 변화에 따른 통증) 혹은 음성(무딘감 등의 감각 소실) 증상들로 이루어진 구체적인 설문들로 신경성 통증 양상을 살펴볼 수 있다. 이들 설문들은 기존 통증 평가 척도에서 나아가 통각역치 감소 등의 정량적 감각측정검사(quantitative sensory testing)와 유의한 관련성을 보이며 타당도 및 신뢰도를 입증받았다[17].
Gursoy 등[18]은 124명의 수근관 증후근 환자에서 LANSS 설문을 이용하여 신경성 통증 정도와 신경생리학적 검사 결과를 비교하였다. 12점 이상의 LANSS 점수를 갖는 환자들을 신경성 통증군으로 분류하였을 때, 운동활동전위(compound muscle action potential amplitude)가 해당 군에서 유의하게 낮게 측정되었으나 수근관 증후군의 전기생리학적 중증도와 관련되지 않았다. 설문 내용 중 이질통과 유발통을 호소하는 환자들은 전기생리학적 중증도가 높았으나, 신경성 통증군 환자들에서 전기생리학적 중증도가 높게 관찰되지는 않았다.
Ceceli 등[19]은 90명의 수근관 증후군 환자에서 LANSS와 painDETECT 설문을 이용하여 신경성 통증을 비교하였는데, LANSS가 통증 지수와만 상관성을 보인 데 반해 painDETECT는 Semmes Weinstein Monofilaments Test 및 Duruoz Hand Index와 상관성을 보여 신경성 통증 환자를 분별하는 능력이 보다 뛰어나다고 보고하였다.
정량적 감각측정검사는 통각 체계의 예민도를 측정하기 위해 Aβ, Aδ 및 C fiber의 기능을 기계적 혹은 온도 자극을 이용해 평가한다[20]. 압력통각역치(pressure pain thresholds)의 감소, 통증의 시간적 가중(temporal summation of pain) 증가, 통증 유도 조절의 저하 등은 관절염 등의 근골격계 만성 통증 환자에서도 흔히 관찰되는 소견이다. 일반 대중에서 정상 범위 값들이 보고되면서 신경성 통증 환자의 감별에 도움이 되고 있다. 신경성 통증에 특징적인 양성 증상인 이질통과 통각과민 등의 감각 이상을 환자의 병력이나 신체검사를 통해 직접 평가하는 방법도 유용하다.
Laser-evoked potentials는 통각(유해)수용 기능을 평가하는 가장 유용한 신경생리학적 검사이다. 체성감각신경의 자극으로 통각수용 체계를 파악하기 어렵지만, 통각수용 통로의 손상 여부를 확인할 수 있다. 레이저 자극은 피부에 있는 Aδ와 C 통각 수용체를 선택적으로 자극한다[21]. 통각 자극 중 열에 의한 자극(heat-evoked potential)이 신경성 통증의 평가에 주로 사용되지만, 말단부 자극 과정에서 통각과 무관한 Aβ fiber의 활성화로 인해 결과 해석에 주의가 필요하다[22].
Go to : 
국제통증의학회(International Association for the Study of Pain)는 수술 전 없었거나, 양상이 다르거나, 강도가 보다 심해진 통증이 수술 부위나 수술과 연관된 부위에 3개월 이상 지속되는 경우를 수술 후 만성 통증으로 정의하고 있다. 외과 수술 영역의 30% 정도에서 수술 후 3개월 이상 지속되는 만성 통증이 발생하는 것으로 보고되고 있으며, 신경성 통증이 이들 만성 통증의 주된 원인으로 여겨지고 있다[2]. Fuzier 등[23]은 2,100명의 정형외과 수술 환자들을 대상으로 수술 후 3개월까지 지속되는 수술 후 통증 척도와 DN4 설문을 이용해 신경성 통증 유무를 확인하였는데, 48% 환자가 지속되는 수술 후 통증을 호소하였고 이들 중 43%가 신경성 통증 양상을 보였다. 특히, 외상과염 등의 주관절 수술과 사지 절단술을 받은 환자에서 신경성 통증 양상이 두드러졌고, 여성과 젊은 연령에서 수술 후 만성 통증이 보다 흔했다. 신경성 통증은 환자들의 수면 장애와 약물 과다 복용과 관련되었다. 관절염 환자들의 34%에서 작열통(burning pain)이나 이질통과 같은 신경성 통증 양상을 보였다[24]. Sadler 등[25]은 슬관절 치환술 환자에서 수술 전 전반적인 통증 및 신경성 통증 정도를 painDETECT 설문을 이용하여 평가하였는데, painDetect 점수가 19점 이상인 경우를 신경성 통증군으로 분류했을 때 30% 정도가 이에 해당되었다. 수술 전 신경성 통증군 환자들이 수술 후 6개월째에 더 심한 통증을 호소하였고 통각역치도 낮아져 있었다. 저자들은 술 전 painDETECT를 이용한 신경성 통증 감별이 술 후 만성 통증의 조기 진단에 도움이 된다고 보고하였다. Phillips 등[26]은 96명의 슬관절 치환술 환자에서 술 전 통증 정도와 신경성 통증 정도를 painDETECT 설문을 이용하여 평가하고 수술 후 슬관절 기능 평가와 비교하였다. 수술 전 신경성 통증은 수술 후 통증과 중증도의 상관관계를 보였으나 기능 평가와 관련성은 보이지 않았다.
Roh 등[27]은 수근관 증후군으로 수근관유리술을 시행받은 환자들에서 압력통각역치 및 중추성 통증과민 설문(Central Sensitization Index)을 이용하여 환자들의 수술 전 신경성 통증을 살펴보았다. 수술 전 신경성 통증은 수술 후 3개월까지의 수근관 수술 후 기능 평가에 유의한 영향을 미쳤으나, 그 효과는 감소하여 12개월째는 영향이 관찰되지 않았다. 수근관증후군 환자에서 수술 전 통증에 대한 감작(신경성 통증 양상)은 수술 후 6개월까지 지속되는 수장부 기둥통(pillar pain)의 유의한 위험요인이었다[28]. 대부분의 수근관 증후군 환자들에서 기둥통이 수술 6개월 이후 특별한 치료없이 호전되는 현상을 고려할 때, 통증 감작에 대한 적극적인 치료도 중요하지만 환자들에게 상기 증상에 대해 충분히 설명하고 안심시키는 접근이 중요해 보인다.
수부 골절 환자들에서 환자들의 부적절한 통증 극복 기전이나 신경성 통증 양상은 환자들의 수술 후 관절 운동을 지연시켜 술 후 6개월까지 수부 강직과 파악력 감소를 초래하였다[29]. Roh 등[29]은 수부 골절 후 환자들의 통증파국화척도와 통증불안증후척도(Pain Anxiety Symptom Scale)가 골절 수술 이후 3개월까지의 수부 강직과 전반적인 기능 상태에 뚜렷한 영향을 미친다고 보고하면서, 해당 시기에 환자들의 통증 극복 기전에 대한 관심이 필요하다고 보고하였다.
신경성 통증의 주요 양성 증상인 통증에 대한 감작은 주관절 외상과염 환자들에서 흔하게 관찰된다. 외상과염 환자들에서 압력통각역치와 통증과민 설문(Pain Sensitization Questionnaire)을 측정한 결과, 신경성 통증 양상이 환자들의 상지 기능 저하 및 1년 이상 지속되는 불응성 외상과염의 진행과 관련이 있었다[30]. 저자의 임상 경험으로 초음파나 MRI를 통해 확인되는 외상과염 병변의 손상 정도와 실제 환자들이 호소하는 증상 정도에는 상당한 차이가 있는데, 이러한 차이는 통증에 대한 감작, 즉 신경성 통증의 동반으로 해석될 수 있다. 불응성 외상과염 환자에서 수술적 치료를 고려하기 이전에 신경성 통증에 대한 임상 평가와 치료가 선행되어야 한다.
Roh 등[31]은 원위요골 골절 수술 후 복합통증증후군(complex regional pain syndrome, CRPS) 1형 양상을 보이는 환자군에서 압력통각역치와 통증과민설문을 측정하고 대조군과 비교하였다. 고에너지손상과 심한 골절 유형에서 복합통증증후군이 높은 빈도로 발생하였고, 1년째 추시에서 절반 정도의 환자들에서 증상 호전이 관찰되었다. 초기에 압력통각 수치가 낮고 통증과민화 점수가 높은 환자들에서 1년 이상 지속되는 불응성 복합통증증후군이 보다 흔하게 발생하였다. 원위 요골 골절 환자들에서 신경성 통증 양상을 조기에 확인하고 다학제적 접근으로 적극적으로 관리함으로써 복합통증증후군을 예방하고 예후를 호전시킬 수 있을지 추가적인 확인이 필요하다.
Go to : 
신경성 통증은 기존의 진통제에 잘 반응하지 않으며, 완벽한 치료 방법을 찾기 어렵다[32]. 신경계의 외부 자극에 대한 민감도를 낮추어 통증을 완화하고, 운동 능력을 유지하며, 삶의 질을 높이는 것이 치료의 주된 목적이 된다. 환자와 의료진 모두 충분한 시간을 갖고 치료에 적극적으로 참여하는 것이 필요하다. 근골격계 전문의, 통증의학 전문의, 신경과 전문의, 재활의학 전문의, 전문 간호사 등의 다양한 인력이 참여하는 다학제적 접근이 효과적이다. 약물 치료로 소염제의 효과는 제한적이며 진통제, 항경련제, 항우울제, 국소마취제, 마약성 진통제, 부정맥 치료제 등을 신경성 통증을 야기하는 다양한 병태생리 기전과 증상에 맞추어 사용한다(Table 2). 통증의 신경성 요소와 비신경성 요소를 평가하고 함께 관리하는 것이 중요하다[33]. 당뇨성 말초 신경병증이나 herpetic neuralgia의 경우 근육의 경련과 타는 듯하거나 저린 양상의 신경 과흥분 양상을 흔하게 보이기 때문에 항경련제 약물을 선택해서 사용해 볼 수 있다. 약제 합병증을 줄이기 위해 하나의 단독 약제 투여보다 상승효과가 있는 다른 약제들을 함께 사용하는 것이 바람직한데[33], 마약성 진통제의 합병증을 줄이기 위해 삼환계 항우울제나 케타민을 같이 사용하는 방법이 예가 될 수 있다.
Pharmacologic therapy for neuropathic pain
말초 신경 손상, 당뇨성 신경병증, herpetic neuralgia, 통증성 신경종(painful neuroma), CRPS 등 다양한 만성 신경병증 환자에서 국소마취제를 통해 말초 신경의 활동을 차단함으로써 상당한 통증의 감소 효과를 기대할 수 있다. 국소 마취제 패치가 통증의 범위가 국소적인 경우 효과적일 수 있다[34]. Lidocaine이나 capsaicin 크림이 herpetic neuralgia에 효과적인 것으로 보고되고 있으나, 피부 자극 증상에 유의하여야 한다.
Gabapentin은 통증조절 신경전달물질인 GABA (gamma-aminobutyric acid)와 관련된 약물로 혈관-뇌 장벽을 통과하며 삼환계 항우울제와 비슷한 통증 억제 효과를 나타내나 보다 빠르게 작용하는 특성이 있다[35]. 고용량을 사용하는 경우 졸음이나 어지러움이 흔하게 발생하며, 오심이나 복통, 체중 증가 등을 호소하기도 한다. 또 다른 항경련제로 삼차신경통에 사용되는 carbamazepine이나 herpetic neuralgia에 사용되는 divalproex sodium 등이 있다[33].
삼환계 항우울제는 오랜 기간 당뇨성 신경병증 등 말초 신경병증의 통증 관리에 효과적으로 사용되어 왔으나 수일 이상의 효과 발현시간이 필요한 단점이 있다[36]. 입이 마르고 처지며 잔뇨를 호소하는 항콜린성 부작용을 초래할 수 있고, 잠재적으로 심독성을 가지고 있다. Amitriptyline은 삼환계 항우울제로 가장 흔하게 사용되지만 진정작용이 강해 노령층에서 주의가 필요하며, desipramine이나 nortriptyline이 진정 작용을 줄이면서 통증을 조절하는 목적으로 사용되고 있다. Selective serotonin reuptake inhibitors (SSRIs)는 삼환계 항우울제의 항콜린 부작용이나 심독성은 없지만 신경병증 통증에 효과적이지 못해, duloxetine hydrochloride 등 일부만 herpetic neuralgia 등에 사용되고 있다[7]. 세로토닌(serotonin)은 중추 및 자율신경계의 monoamine 신경전달물질로, monoamine의 재흡수를 막는 항우울제들의 과도한 사용이나 병합으로 일반적인 용량을 벗어나면 빈맥, 동공확장 등의 자율 신경 이상, 강직과 반사 항진 등의 운동 신경 이상, 그리고 불안과 환각 등의 중추 신경 이상을 야기하는 세로토닌 증후군을 유발할 수 있어 주의가 필요하다.
배면 각(dorsal horn)의 개재 뉴런에서 분비되는 endorphins이나 enkephalins 등의 내인성 진통 물질이 통증 신호의 상위 중추 전달을 막아 통증을 감소시키는 역할을 하는데, 외인성 opioid들도 이들과 유사하게 뇌와 척수에서 작용한다. 말초 신경병증 환자들의 통증 정도와 신체 활동 측면에서 opioid의 효과가 입증된 바 있으나, 약물 특성상 남용과 중독의 문제가 있을 수 있다[37].
신경 손상은 말초의 구심성 신경섬유를 과도하게 흥분시켜 N-methyl-D-aspartate (NMDA) receptor를 상향 조절한다. 케타민 등의 NMDA-receptor 차단 물질은 해당 과정을 차단해 신경성 통증에 대한 치료 효과를 보이는데, 케타민 사용이 마약성 진통제 사용을 줄이면서 신경성 통증을 조절하는 데 효과적이다[10].
만성 신경성 통증은 발생 기전이 복잡해 단일 약물 치료에 잘 반응하지 않고 부분적인 통증의 완화에 그치거나 심한 부작용이 발생하는 경우가 빈번하다[38]. 비약물적, 비중재적 치료로 경피적 전기 자극 등의 물리치료 및 운동치료, 인지 행동 치료들이 신경성 통증의 조절을 위해 사용되고 있지만 아직까지 해당 치료의 역할에 대해 추가적인 연구가 필요하다. 거울 요법(mirror therapy)이나 운동 표상(motor imaginary) 등은 통증이 발생되지 않는 동작을 관찰하거나 상상하는 방식으로 진행한다. 이러한 재활 치료는 복합통증증후군에서 통증과 기능 장해를 조절하는 데 효과적이나, 아직까지 해당 치료가 다른 신경성 통증에 미치는 효과에 대해서는 이견이 있다[39,40]. 심리학적 중재는 약물 및 물리치료 등의 중재 이후 진행해 볼 수 있는데 인지행동 치료가 대표적이다[41]. 사고나 신념 등의 인지적 측면과 구체적인 신체 행동의 측면을 체계적으로 통합하여 통증에 대한 부적절한 행동 양식을 치료하는 방식으로, 환자들의 통증과 함께 감정, 기능, 사회 활동 등에 포괄적으로 접근한다[42,43].
경막외 주사의 경우 herpes zoster로 인한 신경성 통증에 상당한 효과를 보이는 것으로 보고되고 있다[44]. 신경계에 전기장을 투과시켜 신경 연합의 신호 전달 과정을 조절하는 박동성 고주파(pulsed radiofrequency)가 장기 효과 측면에서 경막외 주사 치료보다 우수한 것으로 보고되고 있으나, 반복적인 치료가 필요하고 아직까지 치료 효과에 대한 근거가 부족해 침습적인 치료가 필요한 환자들을 대상으로 고려해 볼 수 있다. 복합통증증후군 환자에서 국소 마취제를 이용한 교감신경 차단술로 위성 신경절을 차단한 경우 6개월 추시에서 40% 환자에서 대부분의 통증 소실, 36%에서 부분적인 통증 소실이 보고되었으나, 장기 치료 효과는 확인되지 않았다. 배근신경절에 lidocaine을 주입함으로써 전반적인 감각을 유지하면서 특정 위치의 환각지 통증을 조절할 수 있다[45]. 교감신경 차단술의 효과를 지속시키기 위해 화학적, 고주파, 혹은 외과적 제거술로 교감신경계를 차단하는 시도가 있으나, 통증 악화 등 심각한 합병증으로 아직까지 치료법의 사용이 제한적이다[46].
척수신경 자극술(spinal neurostimulation)의 경우 물리치료군과의 무작위비교연구에서 통증 감소 효과가 2년까지 지속되고 이후 점차 감소하는 양상을 보였다[47]. 만성 통증 환자에서 절반 이상의 통증 감소가 확인되면 영구적인 자극기 삽입이 고려될 수 있다. 척수 바깥의 구심성 신경 섬유나 말초 피하의 신경 자극이 occipital neuralgia나 postherpetic neuralgia 등 일부 만성 신경성 통증에 효과적으로 사용된다[48,49]. Epidural motor cortex stimulation나 repetitive transcranial magnetic stimulation 등 두개골을 통해 반복적으로 전기나 자기 자극을 전중심부 운동피질에 가하는 신경 자극법도 만성 신경성 통증에 시도되고 있다[44,50].
Go to : 
신경성 통증은 기존의 진통제에 대개 잘 반응하지 않고 완벽한 치료 방법이 없기 때문에, 신경성 통증을 정확히 평가하고 증상을 조절하여 기능 상태를 유지하는 것이 중요하다. 신경계의 흥분과 관련된 양성 증상과 신경 전도 감소에 따른 음성 증상을 살펴봐야 하는데, 이질통과 통각과민 등 전형적인 임상 양상은 신경성 통증의 진단에 도움이 된다. 약물치료로 진통제, 항경련제, 항우울제, 국소마취제, 마약성 진통제 등을 환자 상태를 맞추어 사용하는데, 약제 합병증을 줄이기 위해 하나의 단독 약제 투여보다 상승효과가 있는 다른 약제들을 복합해서 사용하는 것이 바람직하다. 비약물적, 비중재적 치료로 경피적 전기 자극 등의 물리치료 및 운동치료, 인지 행동 치료들이 신경성 통증의 조절을 위한 다학제적 접근으로 도움이 된다. 비중재적 치료에 반응하지 않는 환자의 경우, 경막외 주사, 교감신경차단술, 척수신경 자극술 등의 보다 침습적 시술이 고려될 수 있다. 신경성 통증이 만성화된 경우 통증의 강도가 심하고 기능 상실 및 삶의 질 저하 정도가 두드러지기 때문에, 조기에 신경성 통증을 식별하고 적극적으로 관리하는 접근이 필요하다.
Go to : 
REFERENCES
1. Jensen TS, Baron R, Haanpaa M, et al. A new definition of neuropathic pain. Pain. 2011; 152:2204–5.

2. Giske L, Bautz-Holter E, Sandvik L, Roe C. Relationship between pain and neuropathic symptoms in chronic musculoskeletal pain. Pain Med. 2009; 10:910–7.

3. Nakamura M, Nishiwaki Y, Sumitani M, et al. Investigation of chronic musculoskeletal pain (third report): with special reference to the importance of neuropathic pain and psychogenic pain. J Orthop Sci. 2014; 19:667–75.

4. Smart KM, Blake C, Staines A, Thacker M, Doody C. Mechanisms-based classifications of musculoskeletal pain: part 1 of 3: symptoms and signs of central sensitisation in patients with low back (+/- leg) pain. Man Ther. 2012; 17:336–44.
6. Smart KM, Blake C, Staines A, Doody C. The discriminative validity of "nociceptive," "peripheral neuropathic," and "central sensitization" as mechanisms-based classifications of musculoskeletal pain. Clin J Pain. 2011; 27:655–63.

7. Dworkin RH, O'Connor AB, Backonja M, et al. Pharmacologic management of neuropathic pain: evidence-based recommendations. Pain. 2007; 132:237–51.

8. Zusman M. Mechanisms of peripheral neuropathic pain: implications for musculoskeletal physiotherapy. Physical Therapy Reviews. 2008; 13:313–23.

9. Meacham K, Shepherd A, Mohapatra DP, Haroutounian S. Neuropathic pain: central vs. peripheral mechanisms. Curr Pain Headache Rep. 2017; 21:28.

10. Gilron I, Watson CP, Cahill CM, Moulin DE. Neuropathic pain: a practical guide for the clinician. CMAJ. 2006; 175:265–75.

12. Osman A, Barrios FX, Gutierrez PM, Kopper BA, Merrifield T, Grittmann L. The Pain Catastrophizing Scale: further psychometric evaluation with adult samples. J Behav Med. 2000; 23:351–65.
13. Galer BS, Jensen MP. Development and preliminary validation of a pain measure specific to neuropathic pain: the Neuropathic Pain Scale. Neurology. 1997; 48:332–8.

14. Freynhagen R, Baron R, Gockel U, Tolle TR. painDETECT: a new screening questionnaire to identify neuropathic components in patients with back pain. Curr Med Res Opin. 2006; 22:1911–20.

15. Chatila N, Pereira B, Maarrawi J, Dallel R. Validation of a new Arabic version of the Neuropathic Pain Diagnostic Questionnaire (DN4). Pain Pract. 2017; 17:78–87.

16. Bennett M. The LANSS Pain Scale: the Leeds assessment of neuropathic symptoms and signs. Pain. 2001; 92:147–57.

17. Tampin B, Briffa NK, Goucke R, Slater H. Identification of neuropathic pain in patients with neck/upper limb pain: application of a grading system and screening tools. Pain. 2013; 154:2813–22.

18. Gursoy AE, Kolukisa M, Yildiz GB, Kocaman G, Celebi A, Kocer A. Relationship between electrodiagnostic severity and neuropathic pain assessed by the LANSS pain scale in carpal tunnel syndrome. Neuropsychiatr Dis Treat. 2013; 9:65–71.
19. Ceceli E, Gumruk S, Okumus M, Kocaoglu S, Goksu H, Karagoz A. Comparison of 2 methods of neuropathic pain assessment in carpal tunnel syndrome and hand functions. Neurosciences (Riyadh). 2018; 23:23–8.

20. Rolke R, Baron R, Maier C, et al. Quantitative sensory testing in the German Research Network on Neuropathic Pain (DFNS): standardized protocol and reference values. Pain. 2006; 123:231–43.

21. Garcia-Larrea L. Objective pain diagnostics: clinical neurophysiology. Neurophysiol Clin. 2012; 42:187–97.

22. Haanpaa M, Attal N, Backonja M, et al. NeuPSIG guidelines on neuropathic pain assessment. Pain. 2011; 152:14–27.
23. Fuzier R, Rousset J, Bataille B, Salces-y-Nedeo A, Magues JP. One half of patients reports persistent pain three months after orthopaedic surgery. Anaesth Crit Care Pain Med. 2015; 34:159–64.

24. Kurien T, Arendt-Nielsen L, Petersen KK, Graven-Nielsen T, Scammell BE. Preoperative neuropathic pain-like symptoms and central pain mechanisms in knee osteoarthritis predicts poor outcome 6 months after total knee replacement surgery. J Pain. 2018; 19:1329–41.

25. Sadler A, Wilson J, Colvin L. Acute and chronic neuropathic pain in the hospital setting: use of screening tools. Clin J Pain. 2013; 29:507–11.
26. Phillips JR, Hopwood B, Arthur C, Stroud R, Toms AD. The natural history of pain and neuropathic pain after knee replacement: a prospective cohort study of the point prevalence of pain and neuropathic pain to a minimum three-year follow-up. Bone Joint J. 2014; 96:1227–33.
27. Roh YH, Kim S, Gong HS, Baek GH. Influence of centrally mediated symptoms on functional outcomes after carpal tunnel release. Sci Rep. 2018; 8:11134.

28. Roh YH, Koh YD, Kim JO, Lee KH, Gong HS, Baek GH. Preoperative pain sensitization is associated with postoperative pillar pain after open carpal tunnel release. Clin Orthop Relat Res. 2018; 476:734–40.

29. Roh YH, Noh JH, Oh JH, Gong HS, Baek GH. To what degree do pain-coping strategies affect joint stiffness and functional outcomes in patients with hand fractures? Clin Orthop Relat Res. 2015; 473:3484–90.

30. Roh YH, Gong HS, Baek GH. The prognostic value of pain sensitization in patients with lateral epicondylitis. J Hand Surg Am. 2019; 44:250. e1-7.

31. Roh YH, Gong HS, Baek GH. Prognostic value of pain sensitization during early recovery after distal radius fracture in complex regional pain syndrome. Pain Med. 2019; 20:1066–71.

32. Namaka M, Gramlich CR, Ruhlen D, Melanson M, Sutton I, Major J. A treatment algorithm for neuropathic pain. Clin Ther. 2004; 26:951–79.

33. Galluzzi KE. Management of neuropathic pain. J Am Osteopath Assoc. 2005; 105(9 Suppl 4):S12–9.
34. Katz NP, Gammaitoni AR, Davis MW, Dworkin RH; Lidoderm Patch Study Group. Lidocaine patch 5% reduces pain intensity and interference with quality of life in patients with postherpetic neuralgia: an effectiveness trial. Pain Med. 2002; 3:324–32.

35. Backonja M, Beydoun A, Edwards KR, et al. Gabapentin for the symptomatic treatment of painful neuropathy in patients with diabetes mellitus: a randomized controlled trial. JAMA. 1998; 280:1831–6.

36. Raja SN, Haythornthwaite JA, Pappagallo M, et al. Opioids versus antidepressants in postherpetic neuralgia: a randomized, placebo-controlled trial. Neurology. 2002; 59:1015–21.

37. Rowbotham MC, Twilling L, Davies PS, Reisner L, Taylor K, Mohr D. Oral opioid therapy for chronic peripheral and central neuropathic pain. N Engl J Med. 2003; 348:1223–32.

38. Bates D, Schultheis BC, Hanes MC, et al. A comprehensive algorithm for management of neuropathic pain. Pain Med. 2019; 20:S2–S12.

39. Thieme H, Morkisch N, Rietz C, Dohle C, Borgetto B. The efficacy of movement representation techniques for treatment of limb pain--a systematic review and meta-analysis. J Pain. 2016; 17:167–80.

40. Dobson JL, McMillan J, Li L. Benefits of exercise intervention in reducing neuropathic pain. Front Cell Neurosci. 2014; 8:102.

41. Eccleston C, Hearn L, Williams AC. Psychological therapies for the management of chronic neuropathic pain in adults. Cochrane Database Syst Rev. 2015; 2015:CD011259.

42. Hurley RW, Adams MC, Benzon HT. Neuropathic pain: treatment guidelines and updates. Curr Opin Anaesthesiol. 2013; 26:580–7.
43. Otis JD, Sanderson K, Hardway C, Pincus M, Tun C, Soumekh S. A randomized controlled pilot study of a cognitive-behavioral therapy approach for painful diabetic peripheral neuropathy. J Pain. 2013; 14:475–82.

44. Dworkin RH, O'Connor AB, Kent J, et al. Interventional management of neuropathic pain: NeuPSIG recommendations. Pain. 2013; 154:2249–61.

45. Nee RJ, Butler D. Management of peripheral neuropathic pain: integrating neurobiology, neurodynamics, and clinical evidence. Physical Therapy in sport. 2006; 7:36–49.

46. Stacey BR. Management of peripheral neuropathic pain. Am J Phys Med Rehabil. 2005; 84(3 Suppl):S4–16.

47. North RB, Kumar K, Wallace MS, et al. Spinal cord stimulation versus re-operation in patients with failed back surgery syndrome: an international multicenter randomized controlled trial (EVIDENCE study). Neuromodulation. 2011; 14:330–5.

48. Kumar K, Rizvi S. Cost-effectiveness of spinal cord stimulation therapy in management of chronic pain. Pain Med. 2013; 14:1631–49.

49. Lefaucheur JP. Cortical neurostimulation for neuropathic pain: state of the art and perspectives. Pain. 2016; 157 Suppl 1:S81–9.
50. Sukul VV, Slavin KV. Deep brain and motor cortex stimulation. Curr Pain Headache Rep. 2014; 18:427.

51. Stearns L, Boortz-Marx R, Du Pen S, et al. Intrathecal drug delivery for the management of cancer pain: a multidisciplinary consensus of best clinical practices. J Support Oncol. 2005; 3:399–408.
Go to : 




 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download