Abstract
Objective
To evaluate the risk factors and effect of early hypocarbia for the development of cystic periventricular leukomalacia (CPVL) in very low birth weight infants.
Methods
We reviewed medical records of 187 infants with weighting less than 1,500 g who were admitted to the neonatal intensive care unit at Wonkwang University Hospital from January 2012 to December 2016 retrospectively. Twenty five infants died within 28 days of birth. Of the remaining 162 infants, we compared 21 with CPVL group who were detected by cranial ultrasonography and randomly selected 105 infants as 5 times of CPVL were matched for gestational age were enrolled in this study. For statistical analysis, univariate and multivariate analysis of perinatal, maternal, neonatal risk factors and effect of variable early hypocarbia level on development of CPVL were performed.
Results
Incidence of CPVL was 12.96% (21/162). On univariate analysis, intraventricular hemorrhage (≥grade III) (23.8% vs. 6.7%, P=0.0289), culture proven sepsis (19.1% vs. 4.8%, P=0.0417), and hospitalization (days) (73.1±42.1 vs. 57.8±22.4, P=0.0175) and PaCO2 <25 mmHg within 72 hours after birth (66.7% vs. 29.5%, P=0.0022) were associated with CPVL. And multivariate analysis showed culture proven sepsis (odds ratio [OR], 12.399; 95% confidence interval [CI] 1.563–98.348; P=0.017) and PaCO2 <25 mmHg within 72 hours after birth (OR, 8.468; 95% CI 2.150-33.358, P=0.002) were found to be independent risk factors.
뇌실주위백질연화증은 주로 미숙아에서 출생 전후 여러 원인에 의한 동맥혈의 저산소증과 허혈로 뇌실외후방 주변(dorsal and lateral to external angles of lateral ventricle) 백질부의 괴사가 발생하는 비출혈성 신경 병태 이상이 주요인인 것으로 알려져 있다.1 최근 신생아 집중 치료의 발전으로 극소 저체중 출생아, 초미숙아에 이르기까지 생존율의 향상과 더불어 낭종성 백질연화증(cystic periventricular leukomalacia, CPVL)의 진단율도 높아졌으나 뇌실주위백질연화증이 미숙아에서 유발되는 신경학적 장애의 주원인으로 밝혀지면서 발생 요인이나 예방에 더욱 관심이 증가하고 있다.
뇌실주위백질연화증 발생의 병리기전은 미숙아에서 뇌혈관의 자율조절 기능의 불안정과 측뇌실 주위 혈관의 발달 미숙으로 저산소나 허혈에 취약한 점과 재관류에 의한 자유산소기의 손상, 감염과 관련된 시토카인(cytokine) 등이 관여하는 것으로 알려져 있다.23 그리고 뇌실주위백질연화증의 발생과 관련되는 위험요인으로는 출생 전으로는 산모의 조기 양막 파열, 융모양막염, 태아곤란증, 산전 출혈 등이 있고, 출생 후 요인으로는 신생아 가사, 저혈량증, 패혈증, 저탄산혈증, 동맥관 개존증, 신생아 감염, 잦은 무호흡 등이 보고되고 있다.2 이 중 탄산혈증과 관련하여 적절한 농도의 이산화탄소는 손상 뇌에 다소 보호 작용이 있으나,4 저탄산혈증은 대뇌 혈관 주변의 pH를 증가시켜 혈관 수축에 따른 대뇌 혈류량 감소로 허혈성 뇌손상을 일으킨다고 알려져 있다.56 특히 미숙아에서 출생 초기 심한 저탄산혈증은 뇌실주위백질연화증의 위험요인으로 이미 보고된 바 있다.789 한 연구에 의하면 초기 과도한 기계 호흡으로 인한 의인성 저탄산혈증이 뇌실주위백질연화증을 일으켜 뇌성마비가 발생하는 것으로 보고하고 있으나8 어느 수준의 저탄산혈증이 뇌실주위백질연화증 발생에 관여하는지에 대한 주장은 다소 차이를 보이고 있다. 이에 저자들은 극소 저체중 출생아를 대상으로 뇌실주위백질연화증 발생의 위험인자를 분석하고, 특히 어느 수준의 저탄산혈증이 낭종성 뇌실주위백질연화증 발생과 관련 있는지를 알아보고자 본 연구를 시행하였다.
2012년 1월부터 2016년 12월까지 본원 신생아 중환자실에 입원한 극소 저체중 출생아 202명 중 출생 시 염색체 이상, 다발성 선천 기형, 의미 있는 심기형을 보인 환아 15명을 제외한 187명을 대상으로 의무기록지를 분석하여 후향적으로 연구를 시행하였다. 이 중 생후 28일 이전에 25명이 사망하여 1차 대상 환아는 162명이었다. 모든 환아는 뇌 초음파검사를 시행하였고 뇌실주위 백질부에 낭종성 변화를 보인 21명을 CPVL군으로 분류하고, 이들의 재태 연령, 출생 체중을 기준으로 5배수에 해당하는 105명만을 무작위 선택하여 대조군으로 하여 총 126명을 비교하였다.
대상 환아들은 의무기록지를 바탕으로 주산기 요인과 관련하여 재태 연령, 출생 체중, 성별, 아프가(Apgar) 점수, 출생 장소, 제왕절개 분만, 조기 양막 파열, 태아곤란, 임신성 고혈압, 산모의 당뇨, 다태아 임신, 인공수정, 양수과소증, 분만전 스테로이드 투여, 산모의 황산마그네슘 투여, 부당 경량아(small for gestational age, SGA)를 조사하였다. 그리고 신생아 요인으로 저혈당(생후 24시간 내 혈장 당 <40 mg/dL, 생후 24시간 이후 <50 mg/dL), 폐출혈, 심장 초음파로 확인된 혈역학적으로 의미가 있는 동맥관 단락이 있는 동맥관 개존, 수술적 결찰이 시행된 동맥관 개존, 무호흡, 저혈압(생후 첫 72시간 이내에 평균 동맥압 <30 mmHg이면서 치료가 필요한 경우, 이후 시기에는 평균 동맥압이 5th percentile 미만이면서 치료가 필요한 경우), 신생아 호흡곤란 증후군, modified Bell's staging criteria10 2단계 이상의 괴사성 장염, 덱사메사손 투여, Papile 등11의 분류에 의한 3단계 이상의 뇌실 내 출혈, 세균이 배양으로 확인된 패혈증, 배꼽 동정맥 카테터 사용, 인공호흡기 사용 및 사용 기간, 산소 투여 기간, 총 정맥내 영양 기간, 수혈 횟수, 입원 기간, 경련 유무 등을 조사하였다. 또한 CPVL의 발생에 어느 수준의 저탄산혈증이 관련하는가를 알아보기 위하여 신생아 생후 첫 72시간 이내의 동맥혈이산화탄소분압(PaCO2) 값이 1회라도 35 mmHg 미만인 경우와 30 mmHg 미만인 경우 그리고 25 mmHg 미만인 경우를 조사하였고, 동맥혈이산화탄소분압 값의 평균, 최고치, 최저치도 조사하여 두 군 간에 비교하였다. 배꼽 동맥 카테터가 없는 모든 환아에서 말초 동맥혈 천자를 통하여 채혈을 시행하였고, 생후 24시간 이내에는 4시간에서 6시간 간격으로, 이후에는 필요에 따라 동맥혈 가스분석을 시행하였다. 산소를 투여받는 모든 환아에서는 최소 1일 1회의 동맥혈 가스분석을 시행하였다.
호흡곤란 증후군 환아의 경우 출생 2시간 이내에 폐표면활성제를 기관 내 투여한 후 동시성 간헐적 강제환기(synchronized intermittent mandatory ventilation)를 공급하였고, 가능하면 6시간에서 72시간 이내에 이탈하도록 하였다. 간헐적 강제환기 시 최대 흡기압 14–20 cmH2O, 최대 호기말 양압 4–5 cmH2O, 호흡수 20–40회/분, 흡기 시간 0.3–0.4초를 기본으로 하였다. 동맥혈 가스분석에서 저탄산혈증이 있을 때 호흡수 또는 최대 흡기압을 줄였고, 지속시 지속성 기도 양압 또는 고유량법 인공호흡기로 변경하였다.
뇌 초음파검사는 생후 3일과 1주에 각각 시행하고 정상인 경우는 2주 간격으로, 이상이 있는 경우는 1주 간격으로 추적검사를 시행하였다. 모든 뇌 초음파검사는 신생아 전문의에 의하여 시행 및 판독되었으며, 뇌실주위 백질의 음영 증가와 함께 낭종성 변화가 보인 경우 CPVL로 진단하였고, 이러한 변화가 일시적인 경우는 제외하였다. 퇴원 전 뇌 초음파검사에서 CPVL이 확인된 모든 환아에서 뇌 자기공명영상(magnetic resonance imaging)을 시행하여 CPVL 존재 및 다른 뇌 이상 여부도 확인하였다.
통계학적 분석은 SPSS for Windows version 21.0 (IBM Corp., Armonk, NY, USA)을 사용하였고, 범주형 변수는 Chi-square 또는 Fisher's exact test로, 연속변수는 Student's t-test로 분석하였다. 그리고 P<0.05의 의의를 보인 요인을 대상으로 이들이 독립적인 위험요인으로 작용할 수 있는가를 보기 위하여 다중 로지스틱 회귀분석도 진행하였다.
연구 대상은 염색체 이상, 다발성 선천 기형 등을 제외한 극소 저체중 출생아 총 187명 중 생후 28일 이내 사망한 환아 25명을 제외한 162명 중에서 CPVL 발생 극소 저체중 출생아 21명과 재태 연령, 출생 체중을 기준하여 5배수에 해당하는 105명만을 대조군으로 하여 분석하였다. CPVL 발생은 총 162명 중 21명으로 12.96%의 빈도를 보였다. CPVL로 진단된 21명의 평균 재태 연령과 평균 출생 체중은 27.5±2.2주, 1,092.9±269.4 g이었다.
CPVL군과 대조군의 평균 재태 연령과 평균 출생 체중은 두 군 간에 유의한 차이를 보이지 않았으며, 주산기 요인으로 성별, 아프가 점수, 출생 장소, 제왕절개 분만, 조기 양막 파열, 태아곤란, 임신성 고혈압, 산모의 당뇨, 다태아 임신, 인공수정, 양수과소증, 분만전 스테로이드 투여, 산모의 황산마그네슘 투여 그리고 SGA의 비교에서도 유의성을 보이지 않았다(Table 1).
신생아 요인으로 3단계 이상의 뇌실 내 출혈(23.8% vs. 6.7%,
P=0.0289), 세균 배양이 확인된 패혈증(19.1% vs. 4.8%, P=0.0417), 입원 기간(73.1±42.1일 vs. 57.8±22.4일, P=0.0175)에서 유의성을 보여주었으나 저혈당, 폐출혈, 심장초음파로 확인된 혈역학적으로 의미가 있는 동맥관 단락이 있는 동맥관 개존, 수술적 결찰이 시행된 동맥관 개존, 무호흡, 저혈압, 신생아 호흡곤란 증후군, 2단계 이상의 괴사성 장염, 덱사메사손 투여, 배꼽 동정맥 카테터 사용, 인공호흡기 사용 및 사용 기간, 산소 투여 기간, 총 정맥내 영양 기간, 수혈 횟수, 경련 유무는 유의성을 보이지 않았다(Table 2).
CPVL의 발생에 어느 수준의 저탄산혈증이 관련 있는가를 알아보기 위한 조사에서는 신생아 생후 첫 72시간 이내의 동맥혈이산화탄소분압 값이 <25 mmHg인 경우에서 두 군 간의 유의성(66.7% vs. 29.5%, P=0.0022)을 보였으나 <30 mmHg과 <35 mmHg인 경우에서는 두 군 간의 차이가 없었으며, 동맥혈이산화탄소분압 값의 평균, 최고치, 최저치의 조사에서도 두 군 간의 의의는 없었다(Table 3).
CPVL 발생에 독립적으로 관여하는 위험요인을 알아보기 위하여 주산기 시기와 신생아 시기의 관련 요인 및 동맥혈이산화탄소분압 정도와의 관련성 조사에서 의의를 보인 요인들을 대상으로 다중 로지스틱 회귀분석을 시행하였다. 이 중 세균 배양이 확인된 패혈증(odds ratio [OR], 12.399; 95% confidence interval [CI] 1.563-98.348; P=0.017)과 생후 첫 72시간 이내의 동맥혈이산화탄소분압 <25 mmHg (OR, 8.468; 95% CI 2.150-33.358; P=0.002)만이 독립적인 위험요인으로 조사되었다(Table 4).
뇌실주위백질연화증은 미숙아에서 뇌백질 부위의 비출혈성 신경병리학적 이상을 보이는 주요인이다. 주로 극소 저체중 출생아, 특히 재태 연령 23–30주 또는 24–32주에서 가장 많이 나타나는데 대부분 1,500 g 미만이고 여러 인자들의 상호작용으로 뇌실주위 뇌백질의 저산소성 허혈과 손상을 유발하여 신경학적 장애를 일으켜 뇌성마비, 인지장애를 일으키게 된다.1213 Virchow14가 1867년 미숙아에서 처음으로 뇌실주위 백질부 손상을 발표하고, 1962년 Banker와 Larroche15는 사망한 미숙아에서 병리학적 관점에서 뇌실주위 백질 부위의 응고 괴사를 보고하면서 처음으로 이를 백질부위연화증이라 명명하였다.
뇌실주위백질연화증의 발생 호발 부위는 측내실 삼각부(trigone) 근처의 시방선(optic radiation) 부위와 몬로공(foramen of Monro) 주위의 심부 백질이며,16 발생 빈도는 해외 문헌에 의하면 주로 3–20%이나171819 최근 중국에서는 19.8–34.1%이고, 이 중 낭종성을 2.5–23%로 보고하고 있으며,20 국내에서는 극소 저체중 출생아에서 5.9–15.1%2122232425 그리고 본 연구에서 낭종성은 12.96%의 발생률을 보였다.
Volpe26는 최근 뇌실주위백질연화증을 손상 정도에 따라 낭종의 크기가 5 mm 이상을 보이는 국소 낭종성 괴사, 2–3 mm로 낭종의 크기가 적은 국소 비낭종성 괴사 그리고 미만성 괴사의 세 영역으로 분류하였으며, 미만성은 백질부의 감소로 뇌실 확장을 보이는 형태이다. 본 연구에서는 낭종성 괴사인 경우를 조사하고 분석하였다.
뇌실주위백질연화증의 발생 병리기전은 미숙아의 뇌실주위 혈관의 해부학적, 생리학적 인자, 뇌혈류 자동조절 기능의 장애, 미숙아 뇌백질의 선천적인 취약성 등이 중요한 인자이다.316 해부학적으로 미숙아의 뇌실주위 혈관은 대뇌동맥으로부터 분지되는 장투과 동맥(long penetrating artery)의 분지가 미약하고 단투과 동맥(short penetrating artery)과의 문합이 거의 없어 혈관 분포의 경계 및 말단 지역이 잘 나뉘어져 있어 저산소성 허혈성 손상에 노출되기 쉽다.316 이들 혈관은 임신 3기에 이르러 잘 이루어지면서 백질의 손상은 감소하게 된다.13 또한 뇌혈관 자동조절 기능의 장애로 인하여 주산기 가사, 심부전증, 무호흡 등에 따르는 저산소증, 과탄산혈증, 산혈증이 동반될 때 전신 혈압 변동에 따른 혈압 조절 기능이 잘 이루어지지 않아 전신 혈압이 감소할 때 뇌혈류도 감소하는 허혈성 뇌손상을 가져오게 되어 뇌실주위백질연화증 발생의 위험도가 높다.27
병리학적 변화를 보면 뇌손상 후 3–6시간 내에 응고 괴사, 6–8시간이 지나면 미세아교세포(microglial cell)의 활성화 및 별아교세포(astrocyte)의 증식, 이후 수일이 지나면 대식세포 증식과 더불어 핵 파괴(karyorrhexis)와 별아교세포의 변성, 이어서 8–12일 사이 조직의 액화 괴사에 따른 소낭종의 형성이 시작되어 2주 정도면 완전히 소낭종이 이루어지나 경증인 경우에는 뇌수초의 감소와 뇌실 확장 소견만 나타날 수 있다.13 이러한 병변은 초음파, 자기공명영상술 등으로 출생 초기부터 진단 가능하며 이후에도 추적관찰이 용이해졌다.
병태생리학적 면에서 보면 재태 24–32주에 뇌실주위에 주로 보이는 예비희소돌기아교세포(pre-oligodendrocyte)는 저산소성 허혈성 등 독성 반응에 매우 민감하고, 재태 22주부터 나타나 활성화된 미세아교세포는 독성 매개물질, 유리기(free radical), 산소 반응 매개물질을 생산할 수 있게 된다. 따라서 저산소성 허혈에 민감한 뇌실주위 신경세포는 세포자멸사의 증가와 피질과 시상부위의 용량 감소를 보이게 된다. 예비희소돌기아교세포는 32주 이후에는 희소돌기아교세포로 성숙되며 유리기의 손상에 잘 견딜 수 있게 된다.1328 그 외 발생에 관여하는 인자로는 감염, 염증, 시토카인, 유리기, 글루타메이트 등의 흥분성 아미노산 등이 있으며 출생 전으로는 산모의 조기 양막 파열, 융모양막염 및 산전 출혈 등이며, 출생 후로는 주산기 가사, 뇌실 내 출혈, 무호흡, 경련, 기계적 환기요법, 저혈당, 산혈증, 패혈증 등이 영향을 미치는 것으로 알려져 있다.293031
본 저자들의 조사에서는 3단계 이상의 뇌실 내 출혈(P=0.0289), 세균 배양으로 확인된 패혈증(P=0.0417), 입원 기간(P=0.0175) 그리고 출생 후 첫 72시간 이내의 동맥혈이산화탄소분압 <25 mmHg에서 유의성을 보여주었다. 그러나 이들 요인에서 독립적인 위험요인으로 확인된 경우는 세균 배양으로 확인된 패혈증과 생후 첫 72시간 이내의 동맥혈이산화탄소분압 <25 mmHg인 경우였다. 입원 기간의 증가도 대조군과 비교에서 의의(P=0.0175)를 보였으나 다중 회귀분석을 통한 독립적 요인으로 관여하는지는 의의를 보이지 않았다. 뇌실주위백질연화증 발생에 독립적 요인으로 분석된 패혈증은 태아나 신생아 시기에 어느 경우든 전신에 시토카인을 증가시키고 미숙한 뇌 백질부위에 미세아교세포의 활성화를 가져오게 하여 손상을 가져온다.32 패혈증은 염증 반응 촉진인자인 시토카인 인터루킨-1 (interleukin-1), 인터루킨-6 (interleukin-6) 및 종양 괴사인자-알파(tumor necrosis factor-α)의 농도를 급격히 상승시키고 대뇌혈류의 자율조절 기능의 장애로 혈류의 감소를 가져와 미숙아에서 낭종성 뇌실주위백질연화증이 발생하는데 중요한 역할을 한다고 하며, 혈장응고효소-음성 포도알균(coagulase-negative Staphylococcus) 감염은 Toll-유사 수용체(Toll-like receptor 2)의 활성화로 희소돌기아교세포에 중대한 손상을 일으킨다고 하였다.323334 재태 주령 28–32주는 뇌 발달 과정 중 희소돌기아교세포의 활발한 분화와 신경섬유의 수초발생(myelinogenesis)이 일어나는 시기로 이 시기의 패혈증은 저산소성 허혈성 손상의 발생을 더욱 증가시킨다.35 Chau 등36은 자기공명영상 분석을 통하여 패혈증 환자에서 광범위한 구조적 또는 대사적 이상 소견을 보였다고 보고하였다.
그리고 생후 초기의 저탄산혈증이 낭종성 뇌실주위백질연화증 발생과 관계하며, 이는 대뇌혈관 주변의 pH를 증가시킴으로써 혈관의 수축에 따른 대뇌 혈류량 감소를 가져와 허혈성 뇌손상을 일으키는 것으로 알려져 있으나 어느 수준의 저탄산혈증이 낭종성 뇌실주위백질연화증 발생에 관여하는지에 대해서는 다소 차이를 보이고 있다. Calvert 등37은 뇌실주위백질연화증을 보인 미숙아군에서 대조군에 비하여 동맥혈이산화탄소분압 <25 mmHg의 지속 기간이 더 길다고 보고하였으며, Fujimoto 등7동맥혈이산화탄소분압 <20 mmHg의 저탄산성 알칼리혈증을 보인 극소 저출생 체중아에서 뇌실주위백질연화증 발생 빈도가 높았고, 기계 호흡기 치료를 받지 않은 극소 저출생 체중아에서는 뇌실주위백질연화증이 발생하지 않아 이는 과잉 호흡기 치료가 저탄산혈증 발생과 관련이 있다고 보고하였다. Liao 등38도 출생 후 첫 72시간 최저 동맥혈이산화탄소분압 값이 대조군에 비하여 유의하게 낮았으며 동맥혈이산화탄소분압 <25 mmHg이었을 때 뇌실주위백질연화증 발생이 높았음을 보고하였다. 그러나 Okumura 등8은 뇌실주위백질연화증을 보인 환아에서 저탄산혈증은 호흡기 치료 시 지표와 관련이 없음을 보고하고 이는 선행된 뇌손상에 의한 과호흡의 결과인 것으로 해석하였으며, Park 등39도 첫 72시간 동안의 동맥혈이산화탄소분압은 뇌실주위백질연화증 발생과 관련이 없는 것으로 보인다고 보고하였다. 본 연구에서는 저탄산혈증이 동맥혈이산화탄소분압 <35 mmHg과 <30 mmHg에서는 뇌실주위백질연화증 발생에 의의를 보이지 않았으나 동맥혈이산화탄소분압 <25 mmHg의 저탄산혈증에서는 의의를 보이고 또한 독립적으로도 발생에 관여하였다. 본 연구에서 호흡기 치료의 유무나 기간은 뇌실주위백질연화증 발생의 위험 요소에 의의를 보이지 않았으나 출생 초기 호흡기 치료의 지표 분석을 이용하여 기계호흡에 따른 의인성 저탄산혈증과의 관련 여부에 대한 분석이 더 필요할 것으로 보인다.
그리고 본 연구에서 뇌실 내 출혈이 낭종성 뇌실주위백질연화증 발생에 의의(P=0.0145)를 보였지만 독립적 요인으로는 의의를 보이지 않았다. 그 기전은 출혈로 인하여 유발된 철이온이 산소유리기의 증가 및 활성화를 초래하여 뇌실 주변에 손상을 일으켜 발생하는 것으로 생각되며, Hatzidaki 등40이나 Shim과 Chey25의 보고에서도 같은 결과를 보여주었다. 그러나 독립적 요인의 분석에 P=0.067을 보여 더 많은 대상 환아가 분석 대상이었으면 의의를 보였을 가능성도 있어 추후 더 많은 자료를 모아 분석할 필요가 있는 것으로 생각되었다.
본 연구의 한계점으로는 먼저 대상 환아들의 주산기 요인 중의 하나인 산모의 융모양막염에 대한 분석을 시행할 수 없었다는 점이다. 본원 산부인과에서는 태막에 대한 조직학적 검사를 시행하지 않아 병리학적 융모양막염 진단이 불가능하였다. 또한 본 연구에서는 어느 수준의 저탄산혈증이 CPVL 발생에 관련이 있는지 만을 조사하였으며, 저탄산혈증의 지속 기간과 CPVL 발생 연관성에 대해서는 알 수 없었다. 또한 동맥혈 가스 분석에서 이산화탄소분압 외에도 중요한 인자인 수소이온농도(pH), 염기과잉(base excess), 중탄산염(bicarbonate) 등에 대해서는 분석하지 않았다. 추후 이에 대한 추가적인 연구가 필요할 것으로 사료된다. 결과적으로 본 연구를 통하여 세균 배양이 확인된 패혈증과 생후 초기 첫 72시간 이내의 동맥혈이산화탄소분압 <25 mmHg의 저탄산혈증이 낭종성 백질연화증 발생에 독립적인 위험요인으로 관계가 있는 것으로 조사되었다.
Figures and Tables
Table 1
Comparison of Perinatal and Maternal Risk Factors between CPVL and Control Group in Very Low Birth Weight Infants
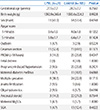
Table 2
Comparison of Neonatal Risk Factors between CPVL and Control Group in Very Low Birth Weight Infants

감사의 글
본 연구는 2018년도 원광대학교 교내 학술연구비 지원을 받아 진행되었으며, 본 연구 제안서는 원광대학교병원 기관윤리위원회(IRB)에서 승인되었다(WKUH 2019-04-036).
References
2. Resch B, Vollaard E, Maurer U, Haas J, Rosegger H, Müller W. Risk factors and determinants of neurodevelopmental outcome in cystic periventricular leucomalacia. Eur J Pediatr. 2000; 159:663–670.

3. Khwaja O, Volpe JJ. Pathogenesis of cerebral white matter injury of prematurity. Arch Dis Child Fetal Neonatal Ed. 2008; 93:F153–F161.

4. Vannucci RC, Towfighi J, Heitjan DF, Brucklacher RM. Carbon dioxide protects the perinatal brain from hypoxic-ischemic damage: an experimental study in the immature rat. Pediatrics. 1995; 95:868–874.

5. Dammann O, Allred EN, Kuban KC, Van Marter LJ, Stewart JE, Pagano M, et al. Hypocarbia during the first 24 postnatal hours and white matter echolucencies in newborns ≤28 weeks gestation. Pediatr Res. 2001; 49:388–393.

6. Leahy FA, Cates D, Maccallum M, Rigatto H. Effect of CO2 and 100% O2 on cerebral blood flow in preterm infants. J Appl Physiol Respir Environ Exerc Physiol. 1980; 48:468–472.

7. Fujimoto S, Togari H, Yamaguchi N, Mizutani F, Suzuki S, Sobajima H. Hypocarbia and cystic periventricular leukomalacia in premature infants. Arch Dis Child Fetal Neonatal Ed. 1994; 71:F107–F110.

8. Okumura A, Hayakawa F, Kato T, Itomi K, Maruyama K, Ishihara N, et al. Hypocarbia in preterm infants with periventricular leukomalacia: the relation between hypocarbia and mechanical ventilation. Pediatrics. 2001; 107:469–475.
9. Giannakopoulou C, Korakaki E, Manoura A, Bikouvarakis S, Papageorgiou M, Gourgiotis D, et al. Significance of hypocarbia in the development of periventricular leukomalacia in preterm infants. Pediatr int. 2004; 46:268–273.

10. Kamitsuka MD, Horton MK, Williams MA. The incidence of necrotizing enterocolitis after introducing standardized feeding schedules for infants between 1250 and 2500 grams and less than 35 weeks of gestation. Pediatrics. 2000; 105:379–384.

11. Papile LA, Burstein J, Burstein R, Koffler H. Incidence and evolution of subependymal and intraventricular hemorrhage: a study of infants with birth weights less than 1,500 gm. J Pediatr. 1978; 92:529–534.

12. Zaghloul N, Ahmed M. Pathophysiology of periventricular leukomalacia: what we learned from animal models. Neural Regen Res. 2017; 12:1795–1796.

13. Ahya KP, Suryawanshi P. Neonatal periventricular leukomalacia: current perspectives. Res Rep Neonatol. 2018; 8:1–8.

15. Banker BQ, Larroche JC. Periventricular leukomalacia of infancy. A form of neonatal anoxic encephalopathy. Arch Neurol. 1962; 7:386–410.
16. Volpe JJ. Hypoxic-ischemic encephalopathy: neuropathology and pathogenesis. In : Volpe JJ, editor. Neurology of the newborn. 3rd ed. Philadelphia: WB Saunders Co.;1995. p. 291–299.
17. Perlman JM. White matter injury in the preterm infant: an important determination of abnormal neurodevelopment outcome. Early Hum Dev. 1998; 53:99–120.

18. Sakamoto S, Terao T. How to lower perinatal mortality? Perinatal care in Japan. Croat Med J. 1998; 39:197–207.
19. Hagberg B, Hagberg G, Beckung E, Uvebrant P. Changing panorama of cerebral palsy in Sweden. VIII. Prevalence and origin in the birth year period 1991–94. Acta Paediatr. 2001; 90:271–277.

20. Chen HJ, Wei KL, Zhou CL, Yao YJ, Yang YJ, Fan XF, et al. Iincidence of brain injuries in premature infants with gestational age ≤ 34 weeks in ten urban hospitals in China. World J Pediatr. 2013; 9:17–24.
21. Lee SH, Kim SH, Lee KH, You DK, Choi SJ, Hwang JH, et al. A study on the incidence and risk factors of cystic periventricular leukomalacia in very low birth weight infants. J Korean Soc Neonatol. 2003; 10:61–66.
22. Lee HS, Lee SK, Kim YJ, Lee SG. Development of periventricular leukomalacia and severe intraventricular hemorrhage in very low birth weight newborns and relationship with ventilator care (study of ventilator care as a risk factor of PVL and PV-IVH). Korean J Pediatr. 2005; 48:1330–1336.
23. Kim MJ, Kim AS, Choi SM, Kim DK, Lee DS, Cho SM, et al. Incidence and risk factors for cystic periventricular leukomalacia in premature low birth weight infants. J Korean Soc Neonatol. 2007; 14:22–29.
24. Park JM, Choi BS, Sohn IA, Seol IJ, Kim CR, Park HK, et al. Risk factors for cystic periventricular leukomalacia in very low birth weight infants. Neonatal Med. 2014; 21:172–178.

25. Shim GH, Chey MJ. Risk factors of cystic periventricular leukomalacia in preterm infants with gestational ages of less than 32 weeks according to gestational age group. Korean J Perinatol. 2016; 27:36–44.

26. Volpe JJ. Confusions in nomenclature: “periventricular leukomalacia” and “white matter injury”-identical, distinct, or overlapping? Pediatr Neurol. 2017; 73:3–6.

27. Lou HC, Lassen NA, Friis-Hansen B. Impaired autoregulation of cerebral blood flow in the distressed newborn infant. J Pediatr. 1979; 94:118–121.

28. Back SA, Luo NL, Borenstein NS, Levine JM, Volpe JJ, Kinney HC. Late oligodendrocyte progenitors coincide with the developmental window of vulnerability for human perinatal white matter injury. J Neurosci. 2001; 21:1302–1312.

29. Volpe JJ. Neurobiology of periventricular leukomalacia in the premature infant. Pediatr Res. 2001; 50:553–562.

30. Rezaie P, Dean A. Periventricular leukomalacia, inflammation and white matter lesions within the developing nervous system. Neuropathology. 2002; 22:106–132.

31. Perlman JM, Risser R, Broyles RS. Bilateral cystic periventricular leukomalacia in the premature infant: associated risk factors. Pediatrics. 1996; 97(6 Pt 1):822–827.

32. Volpe JJ. Postnatal sepsis, necrotizing entercolitis, and the critical role of systemic inflammation in white matter injury in premature infants. J Pediatr. 2008; 153:160–163.

33. Chakravarty S, Herkenham M. Toll-like receptor 4 on nonhematopoietic cells sustains CNS inflammation during endotoxemia, independent of systemic cytokines. J Neurosci. 2005; 25:1788–1796.

34. Sharma R, Tepas JJ 3rd, Hudak ML, Mollitt DL, Wludyka PS, Teng RJ, et al. Neonatal gut barrier and multiple organ failure: role of endotoxin and proinflammatory cytokines in sepsis and necrotizing enterocolitis. J Pediatr Surg. 2007; 42:454–461.

35. Leviton A, Paneth N. White matter damage in preterm newborns--an epidemiologic perspective. Early Hum Dev. 1990; 24:1–22.
36. Chau V, Brant R, Poskitt KJ, Tam EW, Synnes A, Miller SP. Postnatal infection is associated with widespread abnormalities of brain development in premature newborns. Pediatr Res. 2012; 71:274–279.

37. Calvert SA, Hoskins EM, Fong KW, Forsyth SC. Etiological factors associated with the development of periventricular leukomalacia. Acta Paediatr Scand. 1987; 76:254–259.

38. Liao SL, Lai SH, Chou YH, Kuo CY. Effect of hypocapnia in the first three days of life on the subsequent development of periventricular leukomalacia in premature infants. Acta Paediatr Taiwan. 2001; 42:90–93.
39. Park EH, Namgung R, Park MS, Park KI, Kim MJ, Lee C. The relation between hypocarbia and periventricular leukomalacia in preterm infants with mechanical ventilation. J Korean Soc Neonatol. 2002; 2:150–158.




 PDF
PDF ePub
ePub Citation
Citation Print
Print




 XML Download
XML Download