Abstract
목적
슬관절 주위 악성 골연부 종양 치료 시 종양의 도약전이나 슬관절 내 침범, 종양인공관절 치환술 후 반복적 감염 치료를 위한 인접골 절제, 국소재발 및 기계적 파괴가 발생한 경우 슬관절 상하부 전치환술은 하지와 슬관절 기능을 보존하는 한 방법이다. 이 중 반복된 감염 치료를 위해 슬관절면 반대측 골까지 절제 후 한시적 슬관절 고정술을 한 환자에서 가동관절로 재치환술 시 적응증, 합병증, 치환물의 생존율에 대하여 알아보고자 하였다
대상 및 방법
본 연구는 슬관절 상하부 전치환술 환자 34예 중 슬관절 주위 종양인공관절 치환술 후 반복적인 감염으로 슬관절면 반대측 골까지 절제한 후 한시적 슬관절 고정술이 불가피했던 13예를 대상으로 하였다. 진단, 원발병소의 위치, 슬관절 상하부 전치환술을 받기 전까지 수술 횟수 및 기간, 재 재건술 후 치환물의 생존율, 합병증, 기능적 결과를 분석하였
결과
슬관절 상하부 종양인공관절 치환물의 Kaplan-Meier 법에 의한 5, 10년 생존율은 각각 69.0%±12.8%, 46.0%±20.7%였다. 총 13예 중 6예(46.2%)에서 주 합병증이 발생하여 3예는 내고정물을 제거 후 슬관절 고정술을, 2예는 내고정물의 부분교체를, 나머지 1예는 감염된 육아조직만 제거하였다. 최종 추시상 가동관절을 유지한 10예의 Musculoskeletal Tumor Society 기능평가 점수는 평균 24.6점(21–27점)이었다. 슬관절 상하부 종양인공관절 치환술이 실패하여 슬관절 고정술로 재치환 한 3예의 기능평가 평균 점수는 12.3점(12–13점)이었다. 가동관절을 유지한 10예의 슬관절 가동 범위는 평균 67°였다(0°–100°). 슬관절 능동적 신전제한은 평균 48° (20°–80°)였다.
초록
Purpose
Tumor infiltration around the knee joint or skip metastasis, repeated infection sequelae after tumor prosthesis implantation, regional recurrence, and mechanical failure of the megaprosthesis might require combined distal femur and proximal tibia replacement (CFTR). Among the aforementioned situations, there are few reports on the indication, complications, and implant survival of CFTR in temporarily arthrodesed patients who had a massive bony defect on either side of the knee joint to control infection.
Materials and Methods
Thirty-four CFTR patients were reviewed retrospectively and 13 temporary arthrodesed cases switched to CFTR were extracted. All 13 cases had undergone a massive bony resection on either side of the knee joint and temporary arthrodesis state to control the repeated infection. This paper describes the diagnosis, tumor location, number of operations until CFTR, duration from the index operation to CFTR, survival of CFTR, complications, and Musculoskeletal Tumor Society (MSTS) score.
Results
According to Kaplan-Meier plot, the 5- and 10-year survival of CFTR was 69.0%±12.8%, 46.0%±20.7%, respectively. Six (46.2%) of the 13 cases had major complications. Three cases underwent removal of the prosthesis and were converted to arthrodesis due to infection. Two cases underwent partial change of the implant due to loosening and periprosthetic fracture. The remaining case with a deep infection was resolved after extensive debridement. At the final follow-up, the average MSTS score of 10 cases with CFTR was 24.6 (21–27). In contrast, the MSTS score of 3 arthrodesis cases with failed CFTR was 12.3 (12–13). The average range of motion of the 10 CFTR cases was 67° (0°–100°). The mean extension lag of 10 cases was 48° (20°–80°).
Conclusion
Although the complication rates is substantial, conversion of an arthrodesed knee to a mobile joint using CFTR in a patient who had a massive bony defect on either side of the knee joint to control infection should be considered. The patient's functional outcome was different from the arthrodesed one. For successful conversion to a mobile joint, thorough the eradication of scar tissue and creating sufficient space for the tumor prosthesis to flex the knee joint up to 60° to 70° without soft tissue tension.
슬관절 주위는 악성 골종양이 가장 호발하는 부위이다.123) 절제 후 종양인공관절을 이용한 재건술은 가장 널리 사용되나 슬관절 전치환술에 비해 단기 및 장기 합병증 빈도가 상당히 높으며 근위 경골 재건술은 감염이, 원위 대퇴골 치환술은 해리가 주된 합병증이다.4567891011) 이와 같이 슬관절 주위 골 중 한 부위만 종양인공관절로 치환하여도 지속적 합병증의 위험이 따르게 되는데 일부 환자는 해당 하지를 보존하기 위해 슬관절 상하부 전체를 종양인공관절로 치환할 수밖에 없는 상황이 발생한다. 슬관절 양측을 종양인공관절로 치환한 환자의 치료성적은 편측만 치환받은 경우보다 불량한 것으로 보고되며 환자의 생존율이 높아짐에 따라 이런 수술이 필요한 환자가 점점 많아질 것으로 예측되므로 합병증 및 궁극적인 결과를 알고 적응증이 되는 환자에게 선택적으로 시행하는 것이 중요하다.812)
슬관절 상하부 전체를 종양인공관절로 치환이 필요한 경우는 네 가지로 생각된다. 첫째, 드물게 진단 시에 종양이 슬관절을 침범하거나 인접 골로 도약전이가 확인되면 관절 외 절제 혹은 슬관절 상하부 전체를 포함한 절제가 불가피하다. 둘째, 근위 경골이나 원위 대퇴골 종양인공관절 치환술 후 생긴 감염이 광범위하여 해당 인공 관절만 제거하는 것으로 감염이 소실되지 않을 때는 인접골까지 절제 후 한시적 슬관절 고정술이 필요하다. 이런 환자에서 감염 소실 후 가동관절로 재치환하는 경우 슬관절 상하부 전치환술이 적용된다. 셋째, 종양인공관절 치환술 후 기계적 파괴가 발생하여 인접골을 포함한 절제만이 안정된 재건을 얻을 수 있는 경우이다. 넷째, 종양인공관절 치환술 후 인접 골에 국소재발이 발생한 경우이다. 위 네 가지 상황에 처한 환자의 하지를 보존하려면 슬관절 상하부 전치환술이 필요하고 이 술식을 받은 환자가 편측만 종양인공관절 치환술을 받은 환자에 비해 합병증 발생의 빈도가 높다는 것은 알려져 있으나 재건술식상 문제점과 재건술 후 합병증의 양상이 다르며 이런 문제에 대하여 상세히 분석한 보고는 매우 드물다.8)
본 연구는 슬관절 상하부 전치환술이 필요한 네 가지 경우 중 종양인공관절 치환술 후 감염 치료를 위해 슬관절면 반대측 골까지 절제가 불가피하였던 환자 13예의 수술 전 경과, 재 재건술 후 치환물의 생존율, 합병증, 기능적 결과를 분석하였다.
본 연구는 1999년부터 2016년까지 원자력병원 정형외과에서 슬관절 상하부 전치환술을 받은 환자 34명 중 13명을 대상으로 후향적 연구로 진행되었다. 슬관절 상하부 전치환술을 받은 34예의 이유는 1) 근위 경골이나 원위 대퇴골 종양인공관절 치환술 후 감염 치료를 위해 인접골까지 절제가 불가피하였던 환자가 13예, 2) 종양절제 후 인접골에 발생한 국소재발이 12예, 3) 종양인공관절의 기계적 파괴가 5예, 4) 진단 시 종양에 의한 슬관절 침범 혹은 도약전이가 4예였다. 남자가 9예, 여자가 4예였으며 초진 시 평균연령은 23세(9–63세)였다. 진단은 골육종이 10예, 거대세포종, 골의 림프종, 연부조직의 악성 섬유성 조직구종이 각각 1예였다. 원발 병소의 위치는 근위 경골이 12예, 원위 대퇴골이 1예였다. 종양절제 후 일차 재건 술식은 종양인공관절 치환술이 3예, 골수강내 금속정과 골시멘트를 이용한 슬관절 고정술이 3예, 열처리한 자가골과 종양인공관절 조합술이 3예, 피질골 부분절제술이 2예, 소파술 및 단순 절제술이 각각 1예였다(Table 1). 진단일부터 최종 추시까지 기간은 평균 153개월(56–300개월)이었다. 최종 추시상 환자의 생존 상태는 지속적 무병생존이 11예, 질병의 증거가 없는 상태가 2예였다.
최초 수술 후 감염으로 내고정물을 제거하고 반복적인 감염치료 수술 후 슬관절 상하부 전치환술을 시행하기까지 기간은 평균 87개월(24–189개월)이었으며 평균 감염 치료수술 횟수는 6회(2–13회)였다. 슬관절 상하부 전치환술을 시행하기 전 재건 상태는 전부 골수강내 금속정과 골시멘트를 이용한 슬관절 고정술이었다. 감염치료를 위해 한시적 슬관절 고정술을 시행한 환자의 가동관절로의 전환 조건은 슬관절 고정술 후 최소 6개월이 경과하고 C 반응성 단백(C-reactive protein, CRP)이 연속적으로 3회 이상 정상(0.5 mg/L 이하)인 경우로 하였다. 마지막 슬관절 고정술 후 가동관절로 치환하기까지 기간은 평균 25개월(6–84개월)이었다(Table 1).
감염 치료를 위해 한시적으로 고정하였던 슬관절을 가동관절로 치환하기 위한 절개선은 마지막 수술시 사용하였던 반흔 조직으로 접근하였다. 골시멘트와 골수강내 금속정을 전부 제거한 후 연부조직에 생긴 반흔 조직을 건강한 근육층이 확인되는 깊이까지 제거하였다. 특히 근위 비골이 남아 있는 경우 비골신경이 손상되지 않도록 주의하면서 근위 비골을 가능한 한 많이 절제하였다. 근위 비골이 이미 제거된 경우에도 슬관절 후방과 비골이 있던 부위의 반흔 조직을 철저히 제거하여 종양인공관절을 재삽입 후 피부 및 연부조직의 봉합 시 조직의 장력을 최소화하였다. 남아 있는 근위 대퇴골과 원위 경골의 피질골을 종양인공관절의 골수강내 고정물이 잘 삽입될 수 있도록 확공하고 골수강 내 스템 안착에 적합하도록 단단부를 수평으로 처리하였다. 슬관절 상하부 종양인공관절 전치환술에 사용된 기구의 종류는 MUTARS형이 12예 KOTZ형이 1예였다. 종양인공관절의 고정 방법은 11예는 골시멘트를 사용하지 않았으며 나머지 2예는 골시멘트를 이용하여 고정하였다(Table 1). 슬관절 상하부 종양인공관절 치환술 시 슬개골 및 슬개건의 상태는 7예는 슬관절면 상방전위가 있었으며 6예는 감염 치료를 위한 반복적 수술 시 감염치료를 위하여 절제된 상태였다. 슬관절 신전 기능을 회복하기 위하여 남아있는 슬개건의 재건이나 상방 전위된 슬개골을 경골 부위 종양인공관절에 재부착하기 위한 추가 술식은 시행하지 않았다
수술 후 배액관은 하루에 배액이 50 ml 이하가 되는 2주경에 제거하고 수동적 및 능동적 운동은 수술 후 3주경에 시작하였다. 추시는 단순 방사선 검사 및 전체혈구 수 측정(complete blood count), CRP를 포함한 혈액검사를 첫 2년 동안은 3개월 간격으로 일년에 4회 시행하였고 그 후는 일년에 2회 시행하였다. 합병증은 감염이나 기계적 파괴 혹은 골절로 재수술 및 종양인공관절의 제거가 필요한 경우를 주 합병증으로, 그 외의 균이 동정되지 않는 지속적 배액, 표재성 감염, 창상 괴사 등은 부 합병증으로 기술하였다. 슬관절 상하부 종양인공관절의 생존율은 Kaplan-Meier 법을 이용하였다. 수술 전 후 기능적 평가는 Musculoskeletal Tumor Society (MSTS) 평가 방법을 이용하였다.13)
슬관절 상하부 종양인공관절 치환물의 Kaplan-Meier 법에 의한 5년, 10년 생존율은 각각 69.0%±12.8%, 46.0%±20.7%였다. 총 13예의 슬관절 상하부 종양인공관절 대치물 중 6예(46.2%)에서 주 합병증이 발생하였다(Table 2). 그 중 3예는 내고정물을 전부 제거하였고, 2예는 내고정물의 부분교체, 나머지 1예는 감염된 육아조직만을 제거하였다. 종양인공관절을 제거한 3예는 감염이 가동관절 치환술 후 각각 2개월, 14개월, 77개월에 재발하여 골수강 내 금속정과 골시멘트를 이용한 슬관절 고정술로 치환하였다. 부분제거한 2예는 각각 19개월, 29개월에 발생한 대퇴부 골수강내 스템 해리와 대퇴쪽 종양인공관절 주위의 골절로 더 긴 골수강내 스템으로 교체하였다(Fig. 1). 나머지 1예는 술 후 180개월에 비화농성 감염으로 관절주위에 광범위하게 생긴 감염성 육아조직을 철저히 제거하고 종양인공관절은 분해하여 가압 소독하여 재삽입 후 더 이상 감염이 재발하지 않았다(증례 9). 보존적 요법만으로 치료되었던 부 합병증은 3예였다. 저 등급 감염된 2예는 창상세척과 경구 항생제 투여로, 종양인공관절 주위로 약 200 ml 정도 크기의 삼출액낭이 형성된 1예는 반복적인 천자 및 압박 고정 후 소실되었다(Table 2).
최종 추시상 10예(76.9%)는 종양인공관절에 의한 가동관절을 유지하였고 나머지 3예(23.1%)는 슬관절 고정 상태였다. 가동관절을 유지한 10예의 MSTS 기능평가 점수는 평가항목 6개 총 점수 30점 중 평균 24.6점(21–27점)이었다. 슬관절 상하부 종양인공관절 치환술이 실패하여 슬관절 고정술로 재치환한 3예의 기능평가 평균 점수는 12.3점(12–13점)이었다. 가동관절을 유지한 10예의 슬관절 가동 범위는 평균 67° (0°–100°)였다. 슬관절 굴곡 구축은 3예가 10° 정도의 경한 구축을 보였으며 나머지 7예는 정상이었다. 슬관절 후속 굴곡은 평균 70° (20°–100°)였다. 슬관절 능동적 신전제한은 평균 48° (20°–80°)였다.
슬관절 주위 악성 골연부 종양으로 전 절제가 필요한 경우 재건 술식으로 가장 흔하게 적용되는 방법은 종양인공관절이다.1415) 이 술식은 종양의 침범 상태에 따라 절제 범위를 임의로 조절할 수 있으며, 술식이 표준화되어 있고, 언제든지 시용가능하며, 수술 후에 즉각적인 안정성을 얻을 수 있어 환자의 재활에도 이점이 크다.16) 그러나 골조직의 대량 절제 후 감염, 해리, 기계적 파괴 등의 문제점이 상존한다. 슬관절 주위골 중 원위 대퇴골이나 근위 경골 한쪽만 종양인공관절로 치환해도 슬관절 전치환술에 비해 매우 높은 합병증의 빈도를 보이는데 종양의 침범 양상이나 종양 인공관절 치환술 후 생긴 합병증에 따라서는 하지보존과 동시에 슬관절 기능을 유지하기 위해 슬관절 양측 종양인공관절 치환술이 불가피한 경우가 있다. 환자가 진단 당시부터 본 술식이 필요한 경우는 제한적이나 악성 골연부 종양 환자의 생존율이 높아짐에 따라 합병증도 증가하고 사지 보존을 위해 슬관절 상하부 전치환술이 필요한 경우도 늘어나게 되므로 이런 술식의 적용기준과 합병증 및 기능적 결과에 대한 이해가 중요하다.
저자들은 이런 수술이 필요하다고 판단되는 네 종류의 환자들 중 종양인공 치환술 후 감염으로 내고정물 제거술을 하였으나 증상이 지속되어 인접골까지 절제 후 한시적 슬관절 고정술로 치료한 13예의 환자를 다시 가동관절로 치환한 후 결과를 분석하였다. 총 13예 중 6예가 주 종양인공관절을 부분적 혹은 영구적으로 제거해야 하는 비교적 높은 합병증 발생률을 보였으며 결국 3예는 가동관절을 유지하지 못하고 슬관절 고정술로 재치환하였다. 그러나 가동관절을 얻었던 10예의 MSTS 기능평가 점수는 슬관절 고정술을 한 환자의 두 배에 달하므로 시도할 가치가 있는 술식이라고 생각한다. 반복적인 감염으로 슬관절 고정술을 시행한 환자를 가동관절로 치환하기 위해 염두에 두어야 할 점은 반흔 조직의 철저한 제거와 종양인공관절을 삽입한 후 굴곡 및 신전이 가능할 정도의 피부 및 연부조직이 남아있는지의 여부 확인으로 생각된다. 종양인공관절을 삽입한 후 가동이 가능한 공간이 확보되지 않으면 이 술식을 적용하지 않거나 유리 피판술 등으로 종양인공관절을 충분히 덮을 수 있는 연부조직을 확보한 후 수술을 시행하는 것이 합리적이라고 생각된다
본 연구의 제한점은 비교적 적은 증례 수에 있다. 그러나 종양인골관절 치환술이 적용되는 환자 숫자가 적고 그 중 감염으로 인접골까지 절제하는 수술이 필요한 환자 수는 더욱 적으므로 이는 환자군의 특성상 불가피하다. 비록 적은 증례이나 슬관절 상하부 치환술 후 평균 추시기간이 70개월로 비교적 길기 때문에 본 술식 후 생기는 합병증 및 기능적 결과를 알아보는 데는 무리가 없다고 생각된다
진단 당시 종양의 도약전이나 슬관절내 침범, 종양인공관절 치환술 후 생기는 감염, 국소재발 및 기계적 파괴가 발생한 환자는 슬관절 상하부 전치환술이 하지와 슬관절 기능을 유지하는 최선의 방법 중 하나이다. 슬관절 상하부 전치환술의 적응증이 되는 환자는 매우 적으므로 이런 술식 후 재건물의 생존율과 합병증을 보고한 문헌은 3개 정도로 매우 제한적이다. 위 세 가지 논문 중 Gosheger 등6)과 Henderson 등8)의 연구는 통상적인 종양인공관절 치환술의 결과와 함께 분석한 것으로 5년 생존율이 각각 63%, 34%로 원위 대퇴골만 치환한 것에 비해 낮은 생존율 결과를 보였다. 나머지 Sevelda 등12)의 보고는 슬관절 상하부 전치환술 39예만 따로 분석한 것으로서, 진단 시 종양의 침범 정도가 심하여 일차적 수술로 상하부 전치환술을 한 21예와 추시 도중 종양인공관절의 기계적 파괴로 이차적으로 본 술식을 한 18예의 5년 생존율이 생존율이 각각 52%, 29%로 이차적 치환술을 한 경우의 생존율이 현저히 낮다고 보고하였다. 이에 반해 본 연구의 13예는 전부 감염 후유증에 의한 이차적 치환술임에도 불구하고 종양인공관절의 5년, 10년 생존율이 각각 69%, 49%로 타 연구에 비해 상당히 높은 결과를 보였다. 본 연구의 증례가 13예로 작아서 우연히 높은 생존율을 보였다고 생각할 수 있으나 Sevelda 등12)의 연구에서 이차적 치환술을 시행한 18예와 큰 차이가 없으며 기계적 파괴로 슬관절 상하부 전치환술을 받은 환자의 연부조직 상태는 감염치료를 위해 반복적인 수술을 받은 본 연구의 증례에 비해 상당히 좋았을 것이라고 가정할 때 왜 재건물의 생존율이 현저히 낮았는지는 알 수 없다.
종양인공관절 치환술 후 감염이 가장 호발하는 위치는 근위 경골이다.1718) 근위 경골 절제술 후 재건술 시 비복근 국소 피판술이 도입된 이래 빈도가 현저히 감소하였으나 아직도 25%에 이르는 감염률이 보고되고 있다.10) 본 연구에서도 13예 중 1예를 제외하고는 전부 원발병소가 근위 경골이었다. 근위 경골 종양인공치환술 후 심부 감염이 발생하면 종양인공관절을 제거하고 한시적으로 골수강 내 고정물과 골시멘트를 이용하여 슬관절 고정술을 시행한 후 최소한 6개월 이상 감염이 재발하지 않는 것을 확인한 다음 종양인공관절을 재삽입하는 것을 고려하는 것이 저자들의 감염 치료 원칙이다. 그러나 슬관절을 고정한 상태에서도 감염이 재발하는 경우가 있으며, 이런 경우 반복적인 변연절제술과 슬관절 고정술이 필요하며 일부 환자는 원위 대퇴골 골간단까지 감염이 확산되어 슬관절 상방 부위까지 골 절제를 한 후에야 감염 치료가 가능할 수 있다. 이렇게 반복적인 감염이 있었던 환자를 다시 가동관절로 치환할 때 가장 큰 문제점은 종양인공관절을 재삽입할 수 있는 공간의 확보와 슬관절의 굴신이 가능할 정도의 피부 및 연부조직이 남아있는가 하는 것이다. 종양인공관절을 재삽입하고 슬관절을 60° 이상 굴곡한 상태에서 과도한 장력이 없이 피부 봉합이 가능해야 슬관절 고정상태에서 가동관절로 치환술이 적응이 된다고 생각한다. 이 목표를 달성하기 위해서 철저한 반흔조직 제거가 필수적이며 특히 슬관절 후방과 하퇴의 정상 근육이 노출될 정도로 반흔조직 유리술을 시행하여야 한다. 근위 비골이 남아 있는 경우는 근위 비골 제거술을 시행하면 인공관절을 삽입하기에 적절한 공간을 추가로 확보할 수 있다. 철저한 반흔 제거술 후에도 연부조직이 종양인공관절을 적절하게 피복하기 불충분하다면 무리하게 가동관절로 치환하지 않고 먼저 유리 피판술을 시행하여 충분한 연부조직을 확보한 후 가동관절로 치환하는 것이 합리적일 것으로 보인다. 본 연구에서 증례 5와 10은 유리 피판술을 먼저 시행하고 가동관절로 전환을 시도했다면 환자가 슬관절 고정술로 재치환술 시행을 피할 수 있었을 것으로 생각한다.
능동적 슬관절 신전을 위해서는 슬개골을 포함한 신전 기전이 남아 있어야 하나 반복적인 감염 수술을 받은 환자는 슬개골 및 건의 손상이 심하여 슬개골이 없거나 상방전위가 심한 경우가 대부분이다. 이런 환자에서 신전기전 재건까지 도모하는 것은 무리이며 상당한 정도의 능동적 신전제한은 받아들여야 할 것으로 보인다. 신전기전 손상과 내고정물의 해리 혹은 종양인공관절 주위 골절빈도 증가와 관련이 있을 것으로 보이나 현재로서는 적절한 해결책은 없다고 생각한다
마지막으로, 감염된 종양인공관절 치료를 위해 인접골 절제 및 슬관절 고정술까지 필요하였던 환자를 수술 기법상 어려움과 재감염의 위험이 있는 데도 불구하고 가동관절로 치환하는 것이 정말로 노력에 비해 효과가 있는가에 관한 근거가 필요하다. 슬관절 고정술 상태인 환자는 슬관절 기능적 소실로 인한 사회적 비용과 슬관절 고정물 자체의 문제로 인한 의학적 비용이 발생한다. 슬관절 고정술 상태의 환자는 대중교통 이용 및 자가운전을 하기 힘든 상태이므로 거의 모든 사회적 활동에 보호자가 필요하고 이에 따른 사회적 경제적 부담이 상당하다. 의학적 면으로도 슬관절 고정상태로 지내는 동안 시행한 수술의 상당부분이 골수강 내고정물의 피로 골절로 인한 것으로 재수술에 따르는 육체적 경제적 문제가 결코 적다고 할 수 없는 수준이다
Figures and Tables
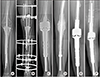 | Figure 1(A) A 9-year-old girl with an osteosarcoma of the proximal tibia underwent a resection of the proximal tibia and was reconstructed with temporary arthrodesis using an intramedullary nail and bone cement (case No. 1). (B, C) At three years after surgery, she showed limb shortening of 5 cm. Limb lengthening using an Ilizarov apparatus was done and the tumor prosthesis was implanted. (D) Despite this, she developed repeated infection. Therefore, resection up to the distal femur and re-arthrodesis was performed. (E) At 9 months after re-arthrodesis, there were no signs of infection and she was switched to combined distal femur and proximal tibia replacement (CFTR). (F) At 29 months after CFTR, loosening of the distal femoral stem was evident. The loosened stem was replaced with a longer stem and massive onlay allograft was performed to supplement the osteoporotic host bone. |
Table 1
Patients' Characteristic

CFTR, combined femur tibia replacement; F, female; M, male; OS, osteosarcoma; GCT, giant cell tumor; MFH, malignant fibrous histiocytoma; RA, resection arthrodesis; Hemicortical, hemicortical excision; PPC, pasteurized autograft-prosthesis composite; TP, tumor prosthesis; c, cemented; nc, non-cemented; CDF, continous disease free; NED, no evidence of disease.
References
2. Niu X, Xu H, Inwards CY, et al. Primary bone tumors: epidemiologic comparison of 9200 patients treated at Beijing Ji Shui Tan Hospi tal, Beijing, China, with 10 165 patients at Mayo Clinic, Rochester, Minnesota. Arch Pathol Lab Med. 2015; 139:1149–1155.

3. Carter SR, Grimer RJ, Sneath RS. A review of 13-years experience of osteosarcoma. Clin Orthop Relat Res. 1991; (270):45–51.

4. Myers GJ, Abudu AT, Carter SR, Tillman RM, Grimer RJ. The long-term results of endoprosthetic replacement of the proximal tibia for bone tumours. J Bone Joint Surg Br. 2007; 89:1632–1637.


5. Myers GJ, Abudu AT, Carter SR, Tillman RM, Grimer RJ. Endoprosthetic replacement of the distal femur for bone tumours: long-term results. J Bone Joint Surg Br. 2007; 89:521–526.

6. Gosheger G, Gebert C, Ahrens H, Streitbuerger A, Winkelmann W, Hardes J. Endoprosthetic reconstruction in 250 patients with sarcoma. Clin Orthop Relat Res. 2006; 450:164–171.

7. Biau D, Faure F, Katsahian S, Jeanrot C, Tomeno B, Anract P. Survival of total knee replacement with a megaprosthesis after bone tumor resection. J Bone Joint Surg Am. 2006; 88:1285–1293.


8. Henderson ER, Groundland JS, Pala E, et al. Failure mode classification for tumor endoprostheses: retrospective review of five institutions and a literature review. J Bone Joint Surg Am. 2011; 93:418–429.


9. Flint MN, Griffin AM, Bell RS, Ferguson PC, Wunder JS. Aseptic loosening is uncommon with uncemented proximal tibia tumor prostheses. Clin Orthop Relat Res. 2006; 450:52–59.


10. Cho WH, Song WS, Jeon DG, Kong CB, Kim JI, Lee SY. Cause of infection in proximal tibial endoprosthetic reconstructions. Arch Orthop Trauma Surg. 2012; 132:163–169.


11. Capanna R, Scoccianti G, Frenos F, Vilardi A, Beltrami G, Campanacci DA. What was the survival of megaprostheses in lower limb reconstructions after tumor resections? Clin Orthop Relat Res. 2015; 473:820–830.


12. Sevelda F, Waldstein W, Panotopoulos J, et al. Survival, failure modes and function of combined distal femur and proximal tibia reconstruction following tumor resection. Eur J Surg Oncol. 2017; 43:416–422.


13. Enneking WF, Dunham W, Gebhardt MC, Malawar M, Pritchard DJ. A system for the functional evaluation of reconstructive procedures after surgical treatment of tumors of the musculoskeletal system. Clin Orthop Relat Res. 1993; (286):241–246.

14. Pala E, Trovarelli G, Calabrò T, Angelini A, Abati CN, Ruggieri P. Survival of modern knee tumor megaprostheses: failures, functional results, and a comparative statistical analysis. Clin Orthop Relat Res. 2015; 473:891–899.


15. Jeys LM, Kulkarni A, Grimer RJ, Carter SR, Tillman RM, Abudu A. Endoprosthetic reconstruction for the treatment of musculoskeletal tumors of the appendicular skeleton and pelvis. J Bone Joint Surg Am. 2008; 90:1265–1271.


16. Ahlmann ER, Menendez LR, Kermani C, Gotha H. Survivorship and clinical outcome of modular endoprosthetic reconstruction for neoplastic disease of the lower limb. J Bone Joint Surg Br. 2006; 88:790–795.






 PDF
PDF ePub
ePub Citation
Citation Print
Print




 XML Download
XML Download