Abstract
Purpose
To evaluate the safety and clinical efficacy of percutaneous intraductal radiofrequency ablation (RFA) followed by dual stent placement in advanced malignant biliary hilar duct obstruction.
Materials and Methods
Between September 2013 and August 2015, ten patients with malignant biliary hilar duct obstruction who underwent percutaneous intraductal RFA followed by dual stent placement were included in this retrospective study. Technical success, clinical success, procedure-related complications, stent patency, and patient's survival durations after treatment were investigated.
Results
Percutaneous intraductal RFA followed by dual stent placement was successful in all patients; the technical success rate was 100%. No major complications were identified. After the procedure, serum total bilirubin levels were notably normalized, and therefore, percutaneous transhepatic biliary drainage (PTBD) catheter was successfully removed in 8 patients; the clinical success rate was 80%. Four patients with stent dysfunction associated with tumor ingrowth/overgrowth underwent a repeat PTBD procedure or secondary stent insertion. Mean stent patency and survival durations were 233.8 ± 35.6 days [95% confidence interval (CI), 164.0–303.5 days] and 387.2 ± 114.6 days (95% CI, 162.6–611.8 days), respectively.
Conclusion
Percutaneous intraductal RFA combined with dual stent placement in advanced malignant biliary hilar duct obstruction is a safe and feasible palliative treatment option.
대상과 방법
2013년 9월부터 2015년 8월까지 2년 동안 악성 간문부 담관 폐쇄에 대해 경피적 담관 내 고주파 소작술 후 양측성 스텐트 삽입술을 시행 받은 11명의 환자 중 10명의 환자가 이 후향적 연구에 포함되었다. 기술적 성공률, 임상적 성공률, 시술 관련한 합병증, 스텐트 개존기간, 그리고 시술 후 생존기간을 평가하였다.
결과
경피적 담관 내 고주파 소작술 후 양측성 스텐트 삽입술을 10명(100%)의 모든 환자에서 시술 관련한 주요 합병증없이 기술적으로 성공하였다. 8명의 환자에서 시술 후 재원 기간 안에(5~18일, 중간값 7일) 경피적 배액관을 제거하는 데 성공하여 임상적 성공률은 80%였다. 4명의 환자에서는 경피적 배액관을 제거한 후 경과관찰 도중(130~287일, 중간값 259일) 담관염이 재발하였고, 영상학적 검사에서 모두 종양 내성장, 과증식으로 인한 스텐트의 기능 부전이 유발된 것을 확인하였다. 평균 스텐트 개존기간과 평균 시술 후 생존기간은 233.8 ± 35.6일(95% 신뢰구간 164.0~303.5일)과 387.2 ± 114.6일(95% 신뢰구간 162.6~611.8일)이었다.
악성 간문부 담관 폐쇄는 간문부암, 담낭암, 간외담관암, 간내담관암, 다른 부위 암의 담관계 인근의 림프선 전이 등에 의해 생기며, 이 중 담관계암은 2002년 한국중앙암등록사업 연례보고서에 의하면 전체 암의 약 4.7%를 차지하고 연간 3000여명 이상의 환자가 발병하는 것으로 알려져 있다(12). 그러나 담관계암의 치료에서 가장 효과적인 치료인 수술적 절제를 받을 수 있는 환자는 25%에 불과하며, 다른 부위의 암에서 담관계 인근의 림프선 전이가 있어 담관 폐쇄가 발생한 환자도 원칙적으로 수술이 불가능한 경우가 대부분이다. 이러한 환자들은 임상적으로 담관 폐쇄에 따른 담관염의 위험성이 높고, 실제 대부분이 이로 인한 패혈증으로 사망하는 경우가 많기에 담관의 개존성을 높이고 담관염을 예방하는 것이 환자의 삶의 질을 향상시킬 수 있는 중요한 방법이라고 하겠다. 그중 담관 배액술은 방법에 따라 경피경간 배액술, 내시경적 배액술 및 수술적 배액술로 나눌 수 있다. 배액관의 종류에 따라서는 플라스틱 스텐트와 자가팽창형 금속 스텐트로 구분할 수 있는데, 환자의 기대 여명이 6개월 이상이 된다면 접근 경로에 관계 없이 자가팽창형 금속 스텐트를 사용하는 것이 바람직하다(3). 이론적으로 금속 스텐트는 망사구조에 의해 담관의 곁가지를 막지 않고 직경이 커 스텐트의 개존율이 우수하여, 연구 결과마다 차이는 있으나 대부분 플라스틱 스텐트보다 직경이 큰 금속 스텐트에서 5~10개월로 우수한 장기 개존율을 보여주었다(456).
경피적 경로를 통한 담관 내 고주파 소작술(radiofrequency ablation)은 최근에 연구되기 시작하였으며 고주파 전기를 특수제작한 카테터를 통하여 조직에 침투시켜 괴사를 일으키는 방식이다. 17명의 담관암 환자, 11명의 췌장암 환자, 4명의 담낭암 환자 및 5명의 전이성 암 환자를 대상으로 시행한 한 연구에서 성공적인 시술 경과를 보고한 바 있다(7). 또한 악성 담관폐쇄 환자에 대해 스텐트 설치술만 시행한 군과 고주파 소작술 후 스텐트 설치술을 시행한 군을 비교한 2015년의 연구(8)에서는 고주파 소작술 후 스텐트 설치술을 시행한 군에서 6개월 스텐트 개존률이 통계적으로 유의하게 높았음을 보고하여 고주파 소작술이 장기적으로 스텐트의 개존기간을 유지할 수 있는 유용한 방법임을 보고하였다.
본 연구에서는 수술적 절제가 어려운 진행성 악성 간문부 담관 폐쇄 환자에서 관내 고주파 소작술 후 양측성 스텐트 삽입술의 유효성을 스텐트 개존기간으로 평가하고, 합병증을 포함한 임상효과, 시술 후 생존기간을 분석함으로써 시술의 안정성을 포함한 임상적 의의에 대해 평가하고자 한다.
본 연구는 원내 연구윤리위원회(Institutional Review Board)의 승인을 받아 시행되었으며 후향적 연구로 모든 연구대상자로부터 시술 전 사전동의(informed consent)를 획득하였다. 2013년 9월부터 2015년 8월까지 2년 동안 Bismuth type III 이상의 악성 간문부 담관 폐쇄에 대해 경피적 담관 내 고주파 소작술과 양측성 스텐트 삽입술을 시행 받은 11명의 환자를 대상으로 하였으며 환자들의 인터벤션 영상기록과 시술판독지를 분석하고, 진료기록과 검체 검사를 포함한 전자의무기록을 후향적으로 확인하였다. 그중에서 시술 후 2주 이내에 자의에 의한 퇴원으로 경과 관찰에서 중도 탈락된 1명은 이번 연구에서 배제하여 총 10명의 환자가 이 연구에 포함되었으며 연구 대상 연령의 중간값은 70세(57~84세)로 남자 7명, 여자 3명이었다.
담관 내 고주파 소작술에 ELRA RF catheter (STARmed, Goyang, Korea)를 사용하였다(Fig. 1). 이 카테터는 온도 조절가능한 양극성 전극 형태(temperature controlled bipolar type electrode)로 총 길이는 40 cm 또는 175 cm, 직경은 7 Fr(2.31 mm)이며 22 mm 또는 33 mm의 두 가지 길이 전극을 가지고 있다. 0.035 inch 유도철사를 따라 담관 내부에 삽입되어 열을 발생시킴으로써 2.5 mm 직경의 관상으로 종양 조직을 손상 및 괴사시킨다. 이 과정에서 고주파 소작술로 인해 나타나는 온도를 조절할 수 있어, 과도한 조직의 손상을 예방할 수 있다.
2016년에는 이 온도 조절 고주파 카테터를 이용한 돼지 실험을 통해 내시경적 고주파 색전술을 합병증 없이 시행한 연구가 발표되어(9) 임상적 적용의 기초가 되었다.
경피적 담관 내 고주파 소작술과 스텐트 삽입술은 18년의 경험을 가진 인터벤션 전문의에 의해 시행되었다. 환자는 먼저 앙와위 자세에서 투시조영 기기 유도 하에 경피적 담관 배액술을 시행하고 병실에서 경과 관찰하였다. 담관염이 임상적으로 호전되고 생체징후가 안정되면 경피적 배액관의 경로를 통하여 담관 조영술을 확인하여 간문부 담관 내 협착 병변의 위치와 범위를 평가하였다. 그 후 유도철사와 5 Fr Kumpe angled-tip cath-eter (Cook, Bloomington, IN, USA)를 이용하여 간문부 협착 부위를 지나게 하고 미리 유도철사를 거치한 상태에서 투시조영 하에 고주파 카테터의 전극 부위가 종양으로 인한 협착부위에 위치하도록 하였다. 이 과정에서 연구에 포함된 모든 환자가 양측 간내담관을 포함한 간문부에 병변이 있었기 때문에 이전에 시행하였던 경피적 담관 배액술의 배액관이 하나인 경우에는 우담관-좌담관, 우담관-총담관 또는 좌담관-우담관, 좌담관-총담관의 T-자 형태로 유도철사를 거치하였고(Fig. 2), 배액관이 양측 담관으로 두개인 경우에는 우담관-총담관, 좌담관-총담관의 Y-자 형태로 유도철사를 거치하였다(Fig. 3). 양극성 전극 카테터를 고주파 발전기(radiofrequency generator)에 연결하고 고주파 소작술을 시행하였다. 간문부를 포함한 좌우담관 모두의 협착 부위에 시행하였으며, 만약 병변이 2.5 cm 이상인 경우에는 구획을 순차적으로 소작하였다. 모든 환자에서 소작술에 관련한 출력은 이전 논문들(8910)을 참고하여 10 Watts로 고정하여 2분간 적용하였고 발생되는 온도는 최고 80℃ 이하로 조절하였다. 소작술 이후에 즉시 이전 거치되어 있던 유도철사의 경피적 경로를 통하여 표준화된 방법으로 T-자 또는 Y-자 모양으로 양측성 스텐트를 삽입하였는데, T-자 스텐트 삽입술은 Niti-S biliary stent (Taewoong, Gimpo, Korea)를 이용하여 ‘stent-in-stent’ 방식으로 설치하였으며 (11), Y-자 스텐트 삽입술은 Epic stent (Boston Scientific, Marlborough, MA, USA) 또는 E·Luminexx stent (Bard, Tempe, AZ, USA)를 이용하여 ‘stent-by-stent’ 방식으로 설치하였다(12). 설치된 자가팽창형 스텐트가 원래 직경의 50% 미만으로만 확장되면 스텐트보다 2~3 mm 직경이 작은 Mustang balloon dilatation catheter (Boston Scientific)로 확장술을 추가적으로 시행하였고, 스텐트 삽입술이 끝나면 경피적 담관 배액관을 거치한 후 시술을 종료하였다. 수일 후에 담관염과 관련된 증상 재발 없이 생체징후가 안정된 환자에서는 담관조영술을 시행하고, 스텐트를 통한 조영제의 내부 배액이 원활한 경우 경피적 배액관을 제거하였다.
연구의 종점(endpoint)은 기술적 성공률, 임상적 성공률, 합병증 발생 유무, 스텐트 개존기간, 시술 후 생존기간의 측정에 두었다. 기술적 성공은 고주파 소작술 뒤 스텐트 설치를 계획한 대로 완료하고 얻은 담관조영술에서 간문부 담관 폐쇄가 재개통 되었는지 여부로 정의하였다. 임상적 성공은 스텐트 설치 후 담관 배액관을 막고(clamping) 1~2주일 안에 시행한 담관조영술에서 스텐트를 통한 조영제의 배액이 원활하여 배액관을 제거하고 난 뒤에도 생체징후가 안정화 상태를 유지하면서, 혈청 총빌리루빈이 정상 범위에 있는 것으로 정의하였다. 시술과 관련된 모든 합병증은 the Society of Interventional Radiology의 보고 기준에 따라 주요 합병증(major complications)과 경증 합병증(minor complications)으로 구분하였다(13). 주요 합병증은 발생 시 해결을 위한 수술적 치료 또는 주요 시술이 필요했거나, 입원 기간이 예상치 않게 48시간을 초과하여 증가하거나, 영구적인 후유증이나 사망을 초래할 수 있는 합병증으로 정의하였고, 그 외 합병증은 경증의 것으로 간주하였다.
각각의 환자에 대한 추적 관찰은 퇴원 후 1개월, 3개월, 그리고 그 후 3개월마다의 외래 방문을 격려하고, 혈액 검사와 영상학적 검사를 통해 시행하였다. 추적기간 동안에 황달이나 복통, 발열 등의 증상이 생겨 담관염이 다시 발생한 것으로 생각되면 전산화단층촬영 또는 자기공명 췌담관조영술로 폐쇄성 황달 여부를 확인하였다. 영상학적 검사상 스텐트 기능 부전이 의심되면 경피적 담관 배액술이나 내시경 담관 배액술을 시행하였고, 담관조영술을 통해 스텐트 기능 부전의 원인을 확인하고 필요한 경우 추가적인 스텐트 삽입술을 시행하였다. 일차 스텐트 개존기간은 스텐트 설치술 후 성공적으로 경피적 배액관을 제거한 시점으로부터 다시 협착에 의한 담관염의 증상이 나타나 영상학적 검사에서 확인되었을 시점까지로 정의하고 만약 환자의 여명 동안 스텐트 기능 부전이 발생하지 않으면 환자의 생존기간과 스텐트 개존기간을 같은 것으로 간주하였다. 시술 후 생존기간은 스텐트 설치술 후 성공적으로 경피적 배액관을 제거한 시점부터 환자의 사망 날짜까지로 정의하였다.
정량적 변수는 평균 ± 표준편차로 표현하였다. 연속변수에 대해서는 대응표본 비모수 검정법인 Wilcoxon 부호 순위 검정을 시행하였다. 환자마다 추적 조사기간이 다른 점을 고려하여 적절한 분석을 위해 스텐트의 개존기간과 환자의 생존기간은 Kaplan-Meier method를 이용하여 계산하였다. 환자의 사망시점까지 스텐트의 기능 부전에 따른 증상이 없었으면 사망시점을 끝점으로 개통기간을 간주하고, 이러한 경우의 자료는 중도탈락 처리하였다. 통계분석은 PASW Statistics for Windows, Version 18.0 (SPSS Inc., Chicago, IL, USA) 프로그램을 이용하였다. p값이 0.05 미만인 경우 통계적 유의성이 있는 것으로 판단하였다.
악성 간문부 담관 폐쇄의 원인으로는 간담관암이 9명(90%), 담낭암의 간문부 침습이 1명(10%)이었으며, 환자 모두 시술 이전에 위의 원인과 관련된 수술력은 없었으나, 6명(60%)에서는 이전에 항암화학치료를 받았다. 10명(100%) 모두 임상적으로 발열, 우상복부통증, 황달, 소양감 등의 징후가 있어, 임상적으로 담낭염 혹은 담관염 의심하에 시행한 전산화단층촬영 또는 자기공명영상에서 Bismuth type III 이상의 악성 간문부 담관폐쇄가 확인되었고(Bismuth classification: Type IIIA, 2; Type IIIB, 0; Type IV, 8), 경피적 담관 배액술을 시행받았다. 환자의 혈청 총빌리루빈을 정상 범위 내로 감소시키고 담관염 증상의 완화를 위한 경피적 담관 배액술은 4명(40%)에서 편측 간엽에 단일 배액관으로 소기의 목적을 달성하였으며(Right, 2; Left, 2), 다른 6명(60%)에서는 양측 간엽에 각각 한 개씩, 총 두 개의 배액관이 필요하였다(Table 1).
모든 환자에서 시술 관련한 주요 합병증 없이 고주파 소작술과 스텐트 삽입술을 시행하고 얻은 담관조영술에서 간문부 담관폐쇄의 재개통을 확인하여 기술적인 성공률은 100%였다. 우측간엽에 단일 배액관으로 담관 배액술을 시행한 2명(20%)의 환자에서는 우담관-좌담관으로의 수평 방향과 우담관-총담관으로의 수직방향으로 고주파 소작술을 시행한 뒤 같은 방향순서대로 ‘stent-in-stent’의 기법으로 스텐트 설치를 연이어 시행하였다. 좌측 간엽에 단일 배액관으로 담관 배액술을 시행한 2명(20%)의 환자에서는 좌담관-우담관, 좌담관-총담관 순으로 위와 같은 방법으로 시술하였다. 그중 한 명의 환자에서는 우담관에서 좌담관으로 카테터를 넘기는데 실패하여 좌담관을 21 gauge needle로 천자한 후 Amplatz GooseNeck Microsnare kit (Covidien, Mansfield, MA, USA)를 사용하여 ‘through-and-through’ 기법으로 유도철사를 잡아 폐쇄 고리(closed loop)를 만든 뒤 풍선카테터로 담관 확장술을 시행하고 카테터를 넘겨 수평 방향의 시술을 성공하였다. 양측 간엽에 두 개의 배액관으로 담관 배액술을 시행한 6명(50%)의 환자에서는 우담관-총담관, 좌담관-총담관으로 유도철사를 거치한 후 고주파 소작술과 ‘stent-by-stent’ 기법으로 스텐트 설치를 시행하였다. 9명(90%)에서는 시술 직후 투시조영 영상에서 스텐트가 담즙 배액이 자연적으로 가능할 만큼 자가로 펴지지 못한 경우로 판단하여 추가적으로 풍선확장술을 시행하였다(Table 2). 모든 환자에서 시술 중 스텐트 전위(migration) 또는 스텐트위치 이상(mal-positioning) 등의 결함은 발생하지 않았다. 2명(20%)의 환자에서 시술 후 심한 복통과 발열을 호소하였으나, 혈중 아밀라아제(amylase)나 지질분해효소(lipase) 수치가 증가하지는 않았고, 진통제, 해열제를 포함한 보존적 치료 후 증상이 호전되었다. 그 외 담관염의 재발, 담관 천공, 담즙유출로 인한 복막염, 또는 간내 혈종 등의 시술과 관련된 조기 합병증은 재원기간 동안 발생하지 않았다.
평균 혈중 빌리루빈 수치의 변화는 Wilcoxon 부호 순위 검정을 통하여 분석하였다. 경피적 담관 배액술 전 11.1 mg/dL (range 9.4~20.2)에서 고주파 소작술과 스텐트 삽입술 시술전 1.2 mg/dL(0.4~4.8)로 감소하였고(p < 0.05), 시술 후 배액관을 제거하기 직전 검사에서는 1.5 mg/dL(0.2~5.4)로 여전히 정상 범위를 유지하였다(p = 0.09), 따라서, 경피적 담관배액술을 통해 통계학적으로 의미 있는 담관 내 감압을 이루었고, 고주파 소작술과 스텐트 삽입술을 통하여 배액관을 제거하고도 담관 폐쇄와 이로 인한 담관염이 호전된 상태를 유지하였음을 판단할 수 있었다. 8명의 환자에서는 시술 후 재원 기간안에(5~18일, 중간값 7일) 혈청 총빌리루빈 수치가 위와 같이 정상 범위로 감소 또는 유지되는 한편, 추적 담관 조영 검사에서 스텐트의 위치와 팽창 정도가 적절함을 확인하고, 스텐트를 통한 십이지장으로의 효과적인 조영제의 배액을 관찰한 후 경피적 배액관을 제거하는 데 성공하여 8명(80%)의 환자에서 임상적 성공을 이루었다. 2명의 환자에서는 시술 후 재원 기간에 반복되는 폐렴과 섬망 및 전신 약화로 호스피스 치료를 위해 전원되었고 각각 시술 후 20일, 24일만에 배액관을 유지한 채로 사망하였다.
고주파 소작술을 시행하고 스텐트를 설치한 후 경피적 배액관을 제거하여 임상적 성공을 거둔 환자들을 대상으로 연구 종료시점까지 스텐트 개존기간과 시술 후 생존기간을 조사하였다. 이 기간에 사망한 6명은 사망시점을 추적 종료시점으로 간주하여, 총 8명에서 중간값 228일(15~775일) 동안 경과 관찰하였다(Table 3). Patient 3과 7은 연구 종료시점이 되지 않은 각각 39일과 15일 동안만 추적 관찰되었다. 이 기간 동안 스텐트의 기능 부전은 없었고, 이 경우는 스텐트의 개존기간과 생존기간의 분석에서 중도 탈락 처리하였다. Patient 4와 6은 경과관찰 기간 도중 스텐트의 기능 부전으로 인한 담관염의 재발 없이 각각 뇌 전이암에서 생긴 출혈과 폐렴에 동반된 패혈증으로 인해 임상적 성공을 거둔 후 20일, 76일째에 사망하였고, 이 경우는 스텐트의 개존기간 분석에서만 중도 탈락 처리하였다. 그중 patient 6은 배액관을 제거한 뒤 12일째에 지속적인 발열의 평가를 위해 시행한 전산화단층촬영에서 Y-자 스텐트가 배액하는 간 우측 후구역과 좌엽의 담관 확장 소견은 없었으나 스텐트가 배액하지 못했던 구획인 우측 간천정(liver dome) 부위에 간농양이 확인되었다. 이에 대해 경피적 농양 배액술을 추가로 시행받고 발열은 호전되었으며 그 후 사망시점까지 스텐트의 기능 부전은 발생하지 않았다. Patient 1, 2, 5, 8, 총 4명의 환자에서는 경과관찰 도중(130~287일, 중간값 259일) 담관염이 재발하였고, 전산화단층촬영 검사에서 모두 종양의 내성장(tumoringrowth) 또는 과증식(overgrowth)으로 인한 스텐트의 기능 부전이 유발된 것을 확인하였다. 이 4명의 환자들에 대해서는 각각 경피적 담관 배액술(3명) 또는 내시경 담관 배액술(1명)과 추가 스텐트 삽입(3명) 시술이 시행되었으며 임상적으로 담관염은 모두 호전되었다. Kaplan-Meier method를 이용한 평균스텐트 개존기간(mean stent patency duration)과 평균 시술 후 생존기간(mean survival duration)은 각각 233.8 ± 35.6일 (95% 신뢰구간 164.0~303.5일)과 387.2 ± 114.6일(95% 신뢰구간 162.6~611.8일)이었다(Fig. 4).
자가팽창성 금속 스텐트 삽입술은 수술적 절제가 불가능한 악성 담관 폐쇄 환자에게 시행하여 삶의 질을 향상시킬 수 있는 효과적인 고식적 치료법으로 인정되고 있다(14). 그러나 스텐트 기능 부전이 시술 6개월 이내에 50% 정도의 높은 빈도로 발생함이 보고되었으며(3), 특히 간문부 담관 폐쇄 환자에서 시행된 경우에서는 스텐트 기능 부전의 발생 비율이 더욱 높은 것으로 알려져 있다(15). 커버된 스텐트의 삽입을 제안하는 연구들도 있으나(1617) 간문부 부위의 악성 담관 폐쇄 환자에서는 커버된 스텐트를 사용하는 것이 간내담관 주요 분지들 혹은 췌담관의 배액을 막아버려서 담낭염 및 췌장염의 발생률을 증가시키고 사망률을 높일 수 있기 때문에 이는 스텐트 설치술의 보완책으로 고려하기 어렵다(1819).
양극성 고주파 카테터의 도입 이후 여러 연구에서 고주파 소작술을 악성 담관 폐쇄의 치료에 스텐트 삽입술과 병합하여 사용한 결과를 보고하고 있다. 먼저 Khorsandi 등(20)은 돼지에서 담관 내부에 고주파 소작술을 실시하여 5~10 Watts의 출력과 2분의 시술 시간이 안전하고 효과적이라는 것을 보고하여 임상적 적용의 기틀을 마련하였다. Steel 등(21)은 악성 폐쇄성 황달 환자 22명을 대상으로 내시경을 이용한 담관 내 고주파 소작술을 시행하였으며, 단기 및 장기 스텐트 기능 부전의 발생률이 낮고 심각한 합병증은 발생하지 않았다고 보고하였다.
이후로 내시경을 이용한 담관 내 고주파 소작술이 널리 사용됨에 따라, Mizandari 등(7)은 2013년에 악성 담관 폐쇄 환자 39명을 대상으로 투시 검사 유도하에 경피적 배액술 경로를 통한 담관 내 고주파 소작술을 시행했음을 발표하였다. 이 보고에서는 모든 환자에서 시술을 성공적으로 완료한 가운데, 추적관찰 도중 39명 중 한 명의 환자에서만 시술 후 42일 만에 스텐트 기능 부전이 발견되었음을 서술하여 경피적 경로를 통한 고주파 소작술의 실현 가능성, 안전성 및 효율성을 입증하였다. 그러나 이 연구에서는 Bismuth type III 이상의 진행된 간문부 담관 폐쇄의 경우가 단지 11예(28.2%)만 포함되었음에도 불구하고, 스텐트 개존기간의 중간값은 84.5일로 상대적으로 짧았다. 그 후 2015년에 악성 담관 폐쇄 환자 26명을 대상으로 경피적 배액술과 스텐트 삽입술만을 받은 대조군과 경피적 배액술 후 고주파 소작술과 스텐트 삽입술을 같이 시행받은 환자군을 비교한 Li 등(8)의 연구에 따르면, 1주 황달 호전 정도 및 3개월 스텐트 개존율은 두 군 간에 비슷한 것으로 나타났으나, 6개월 스텐트 개존율은 고주파 소작술을 같이 시행받은 환자군이 스텐트 삽입술 단독의 대조군보다 통계적으로 유의하게 높았다. 이 비교 연구로 고주파 소작술이 악성 담관 폐쇄 환자의 스텐트 삽입술에 있어 장기적인 임상적 이점을 줄 수 있음이 증명되었다. 그러나 이 연구에 포함된 26명 중 21명은 총담관폐쇄가 있는 증례였고, 다른 5명의 환자만이 간문부 간담관암(hilar cholangiocarcinoma)으로 인한 간문부 담관 폐쇄가 있었다. 그중 오직 2명의 간문부 담관 폐쇄 환자에서만 고주파 소작술과 Y-자 스텐트 설치술을 시행하였기 때문에, 간문부 담관폐쇄 환자에서 고주파 소작술이 가지는 임상적 의의를 밝히는 데는 여전히 한계점이 남아 있다. 최근에 들어서는 Bismuth type III 이상의 진행된 간문부 담관 폐쇄 환자 9명에서의 고주
파 소작술과 병합한 스텐트 설치술에 관한 문헌(10)이 발표되었으며, 이전 연구들에 비해 상대적으로 긴 중간값 100일의 스텐트 개존기간을 보고하였다. 그러나 연구에 포함되었던 9명 모두가 간문부 담관 폐쇄 환자인데도, 그중 4명에서만 양측성 고주파 소작술과 Y-자의 양측성 스텐트를 설치하였고, 다른 5명에서는 단측성으로만 고주파 소작술과 스텐트 설치술을 시행하였기에 간문부 담관 폐쇄 환자에 대한 고주파 소작술과 양측성 스텐트에 관한 연구로서는 역시 한계점이 있다.
본 연구는 모든 환자에서 간문부를 포함한 양측 간내담관과 총담관에 대한 소작술이 모두 시행되었으며 그 후에 양측성 스텐트가 설치되었다. 시술 전 양측성 경피적 배액관이 있던 환자에서는 우담관-총담관, 좌담관-총담관으로 소작술이 시행되었고 총담관에서는 최소 2회 이상, 협착 부위가 넓은 경우는 그 이상의 횟수로 소작술이 시행되었다. 한편 일측성 경피적 배액관만 거치되어 있는 환자에서는 우담관-좌담관, 우담관-총담관 또는 좌담관-우담관, 좌담관-총담관의 순으로 소작술이 시행되었기 때문에 총담관이 아닌 우담관 또는 좌담관에서 최소 2회 이상의 반복되는 소작술이 시행되었다(Table 2). 이전의 두 연구(810)에서 Y-자 스텐트가 설치되었던 2명, 4명의 경우에도 총담관에서 소작술이 반복되어 시행되었고, 시술과 관련된 합병증 없이 안전하였음은 이미 보고되었다. 총담관보다 직경이 상대적으로 작은 양측 간내담관의 경우는 소작술에 의해 담관의 조직이 받는 열손상의 가능성이 높을 것으로 생각되지만, 이와 관련된 내용은 이전 문헌에서 보고되지 않았다. 또한, 이번연구에 포함된 10명의 모든 환자 중 간내담관의 소작술과 관련된 담관 출혈, 담관 천공과 그로 인한 담즙 누출과 같은 합병증은 전혀 없었다. 현재까지 담관 내 고주파 소작술 시술이 비교적 안전한 것으로 알려지고 있어도, 일부에서 혈담증이나 담관천공 등과 같은 심각한 합병증을 보고하였던(22) 것을 감안할 때, 이 결과는 본 연구에서 사용된 고주파 소작술의 출력 변수(10 Watts, 2분)로 총담관 및 좌우 간내담관에 대해 반복해서 시술하여도 안전함을 시사한다. 이러한 사항은 T-자 스텐트가 Y-자 스텐트에 비해 적은 수의 경피적 배액관을 필요로 하기 때문에 경피적 배액관을 시술하는 데 관련된 이환율(morbidity)이 낮다는 장점과 이어져, 만약 초기 담관염을 조절하는 데 한개의 경피적 배액관으로 충분했다면, 그 후 고주파 소작술을 병행하는 스텐트 설치술을 계획할 때 T-자 스텐트 설치술을 안전하게 적극적으로 고려할 수 있을 것이다. 같은 흐름에서 만약 심한 간문부 협착으로 반대쪽 담관으로 카테터나 스텐트를 넘기기가 어렵다면 본 연구에서와 같은 올가미 카테터를 이용한 ‘through-and-through’ 기법도 하나의 경피적 배액관만을 이용하여 고주파 소작술과 T-자 스텐트 설치술을 완료하는 데 도움이 된다.
이 연구에 포함된 환자들에서는 임상적 성공을 거둔 후 담관염이 재발할 때까지 233.8 ± 35.6일(95% 신뢰구간 164.0~303.5일)의 평균 스텐트 개존기간으로 2016년 Wang 등(10)의 연구에서 보고한 중간값 100일(95% 신뢰구간, 85~115일)과 2013년 Mizandari 등(7)이 보고한 중간값 84.5일(95% 신뢰구 간 14~260일)보다 긴 개존기간을 보였다. 또한 고주파 소작술과 스텐트 설치술 후 경피적 배액관을 제거하기 위한 추적 담관 조영 검사에서 고주파 소작술로 인해 초래될 것으로 예상할 수 있는 괴사 조직의 파편들과 그로 인한 스텐트 일시 폐쇄로 인한 기능 부전은 확인되지 않았고, 문제 없이 배액관을 제거할 수 있어 임상적 성공을 거두었다. 그러나 고주파 소작술과 스텐트 설치술 후 수일의 시간이 지난 상황에서 혈청 총빌리루빈 감소가 더딘 원인을 확인하기 위해 시행한 한 환자의 담관경 (choledochoscopy) 사진에서 볼 때(Fig. 2), 종양 조직이 소작되어 담관 내경이 커지게 된 소견으로 유추할 수 있듯이 소작술시행 시에는 파편화된 괴사 조직이 상당량 발생할 것이므로 스텐트 설치술 전후에는 충분한 양의 생리식염수 관류(irrigation)를 통해 이를 제거해 주는 것이 초기 스텐트 기능 부전을 막는데 도움이 될 것으로 생각되며, 이는 Monga 등(23)이 발표한 소작술 후의 담관 내 영상 소견과도 일치한다.
본 연구는 단일 기관 내에서 적은 수의 환자군을 대상으로 한 후향적 연구여서 선택 바이어스는 피할 수 없었고, 따라서 이 결과를 다른 환자에게 완전히 일반화할 수는 없다. 그러나 각각 2명과 4명의 간문부 담관 폐쇄 환자에서 고주파 소작술과 병합한 Y-자 스텐트 설치술을 보고하였던 이전 연구들(810)과 달리 본 연구에서는 Y-자 스텐트 설치술(4명) 외에 T-자 스텐트 설치술(4명)에서도 임상적 성공을 거두고 이전 연구에 비해 긴 스텐트 개존기간을 확인할 수 있었다는 점에서 의의가 있다. 그러나 악성 간문부 담관 폐쇄는 비교적 드문 질환으로 대규모, 다기관 연구를 통해 진행하기가 어려운 점이 있었다. 또한 고주파 소작술이 스텐트의 개존기간 및 환자의 생존기간에 미치는 영향이 있는지를 판단하기 위해서는 스텐트 설치술 단독군과 고주파 소작술 및 스텐트 설치술의 동시 시행군에 대한 비교 연구와 함께 환자 여명 기간 동안의 장기 추적 관찰이 필요하다.
결론적으로, 경피적 담관 내 고주파 소작술과 양측성 스텐트 삽입술은 진행된 악성 간문부 담관 폐쇄 환자에 대해 시행할 수 있는 안전하고 유용한 보존적 치료 방법이다. 스텐트 개존기간 면에서 기존 스텐트 삽입술 단일 시술보다 장점이 있을 것으로 기대되나, 장기간 스텐트 개통성 및 환자 생존율에서의 이점을 확인하기 위해서는 향후 이에 대한 공감대 형성을 통한 후속 비교 연구 및 다기관 전향적 연구, 바람직하게는 무작위 연구가 필요할 것으로 생각한다.
Figures and Tables
 | Fig. 1The ELRA™ is a bipolar radiofrequency catheter with four radiologically marked electrodes (between the arrowheads) at the tip and temperature sensor inside. |
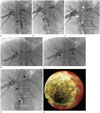 | Fig. 262-year-old man with Bismuth type IV hilar cholangiocarcinoma confirmed by diagnostic biopsy.
A. A catheter-directed percutaneous transhepatic cholangiography demonstrates the stricture (arrows).
B-D. Radiofrequency ablation for proximal CBD (arrows), LMD (white arrows), and RMD (arrowheads), respectively.
E. A transverse stent deployment to cover stenosis at LMD-RMD (arrows).
F. A vertical stent deployment at LMD-CBD in a stent-in-stent manner as T-configuration dual stents placement (arrows).
G. Choledochoscopy shows maintenance of ductal luminal patency by ablation of intraductal tumor followed by metallic stent deployment.
CBD = common bile duct, LMD = left main duct, RMD = right main duct
|
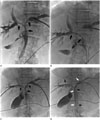 | Fig. 373-year-old woman with Bismuth type IV hilar cholangiocarcinoma underwent fluoroscopy-guided biliary drainage catheter placement bilaterally.
A. A catheter-directed percutaneous transhepatic cholangiography demonstrates the stricture (arrows).
B. Radiofrequency ablation (arrows) for RMD-proximal CBD. Ablation for LMD was done, additionally (not shown).
C. Post-ablation cholangiography shows residual partial hilar stenosis (arrows).
D. Y-configuration dual stents placement to cover stenoses at RMD-CBD (arrows), LMD-CBD (white arrows) in a stent-by-stent manner.
CBD = common bile duct, LMD = left main duct, RMD = right main duct
|
 | Fig. 4Stent patency and patient survival duration.
A. Kaplan-Meier curve of stent patency. The calculation starts on the day of PTBD catheter removal after percutaneous intraductal RFA followed by stent deployment procedure and extends to the time of proven stent dysfunction.
B. Kaplan-Meier curve of patient survival duration. The calculation starts on the date of day of PTBD catheter removal after percutaneous intraductal RFA followed by stent deployment procedure and extends to the date of death.
PTBD = percutaneous transhepatic biliary drainage, RFA = radiofrequency ablation
|
Table 3
Clinical Outcomes of All Patients

*The calculation starts on the day of percutaneous intraductal RFA followed by stent deployment procedure.
†The calculation starts on the day of PTBD catheter removal after percutaneous intraductal RFA followed by stent deployment procedure.
ERCP = endoscopic retrograde cholangio-pancreatography, FU = follow-up, PTBD = percutaneous transhepatic biliary drainage, RFA = radiofrequency ablation
References
1. Alexander F, Rossi RL, O'Bryan M, Khettry U, Braasch JW, Watkins E Jr. Biliary carcinoma. A review of 109 cases. Am J Surg. 1984; 147:503–550.
2. Wade TP, Prasad CN, Virgo KS, Johnson FE. Experience with distal bile duct cancers in U.S. Veterans Affairs hospitals: 1987-1991. J Surg Oncol. 1997; 64:242–245.
3. Loew BJ, Howell DA, Sanders MK, Desilets DJ, Kortan PP, May GR, et al. Comparative performance of uncoated, self-expanding metal biliary stents of different designs in 2 diameters: final results of an international multicenter, randomized, controlled trial. Gastrointest Endosc. 2009; 70:445–453.
4. Davids PH, Groen AK, Rauws EA, Tytgat GN, Huibregtse K. Randomised trial of self-expanding metal stents versus polyethylene stents for distal malignant biliary obstruction. Lancet. 1992; 340:1488–1492.
5. Kaassis M, Boyer J, Dumas R, Ponchon T, Coumaros D, Delcenserie R, et al. Plastic or metal stents for malignant stricture of the common bile duct? Results of a randomized prospective study. Gastrointest Endosc. 2003; 57:178–118.
6. Schmassmann A, von Gunten E, Knuchel J, Scheurer U, Fehr HF, Halter F. Wallstents versus plastic stents in malignant biliary obstruction: effects of stent patency of the first and second stent on patient compliance and survival. Am J Gastroenterol. 1996; 91:654–659.
7. Mizandari M, Pai M, Xi F, Valek V, Tomas A, Quaretti P, et al. Percutaneous intraductal radiofrequency ablation is a safe treatment for malignant biliary obstruction: feasibility and early results. Cardiovasc Intervent Radiol. 2013; 36:814–819.
8. Li TF, Huang GH, Li Z, Hao CF, Ren JZ, Duan XH, et al. Percutaneous transhepatic cholangiography and intraductal radiofrequency ablation combined with biliary stent placement for malignant biliary obstruction. J Vasc Interv Radiol. 2015; 26:715–721.
9. Cho JH, Lee KH, Kim JM, Kim YS, Lee DH, Jeong S. Safety and effectiveness of endobiliary radiofrequency ablation according to the different power and target temperature in a swine model. J Gastroenterol Hepatol. 2017; 32:521–526.
10. Wang Y, Cui W, Fan W, Zhang Y, Yao W, Huang K, et al. Percutaneous intraductal radiofrequency ablation in the management of unresectable Bismuth types III and IV hilar cholangiocarcinoma. Oncotarget. 2016; 7:53911–53920.
11. Kim CW, Park AW, Won JW, Kim S, Lee JW, Lee SH. T-configured dual stent placement in malignant biliary hilar duct obstructions with a newly designed stent. J Vasc Interv Radiol. 2004; 15:713–717.
12. Gwon DI, Ko GY, Yoon HK, Kim YJ, Kim TH, Lee WH, et al. Safety and efficacy of percutaneous Y-configured covered stent placement for malignant hilar biliary obstruction: a prospective, pilot study. J Vasc Interv Radiol. 2012; 23:528–534.
13. Sacks D, McClenny TE, Cardella JF, Lewis CA. Society of Interventional Radiology clinical practice guidelines. J Vasc Interv Radiol. 2003; 14(9 Pt 2):S199–S202.
14. Shepherd HA, Royle G, Ross AP, Diba A, Arthur M, Colin-Jones D. Endoscopic biliary endoprosthesis in the palliation of malignant obstruction of the distal common bile duct: a randomized trial. Br J Surg. 1988; 75:1166–1168.
15. Dahlstrand U, Sandblom G, Eriksson LG, Nyman R, Rasmussen IC. Primary patency of percutaneously inserted self-expanding metallic stents in patients with malignant biliary obstruction. HPB (Oxford). 2009; 11:358–336.
16. Lee SJ, Kim MD, Lee MS, Kim IJ, Park SI, Won JY, et al. Comparison of the efficacy of covered versus uncovered metallic stents in treating inoperable malignant common bile duct obstruction: a randomized trial. J Vasc Interv Radiol. 2014; 25:1912–1920.
17. Yoon WJ, Lee JK, Lee KH, Lee WJ, Ryu JK, Kim YT, et al. A comparison of covered and uncovered Wallstents for the management of distal malignant biliary obstruction. Gastrointest Endosc. 2006; 63:996–1000.
18. Bezzi M, Zolovkins A, Cantisani V, Salvatori FM, Rossi M, Fanelli F, et al. New ePTFE/FEP-covered stent in the palliative treatment of malignant biliary obstruction. J Vasc Interv Radiol. 2002; 13:581–589.
19. Coté GA, Kumar N, Ansstas M, Edmundowicz SA, Jonnalagadda S, Mullady DK, et al. Risk of post-ERCP pancreatitis with placement of self-expandable metallic stents. Gastrointest Endosc. 2010; 72:748–754.
20. Khorsandi SE, Zacharoulis D, Vavra P, Navarra G, Kysela P, Habib N. The modern use of radiofrequency energy in surgery, endoscopy and interventional radiology. Eur Surg. 2008; 40:204–210.
21. Steel AW, Postgate AJ, Khorsandi S, Nicholls J, Jiao L, Vlavianos P, et al. Endoscopically applied radiofrequency ablation appears to be safe in the treatment of malignant biliary obstruction. Gastrointest Endosc. 2011; 73:149–153.
22. Dolak W, Schreiber F, Schwaighofer H, Gschwantler M, Plieschnegger W, Ziachehabi A, et al. Endoscopic radiofrequency ablation for malignant biliary obstruction: a nationwide retrospective study of 84 consecutive applications. Surg Endosc. 2014; 28:854–860.
23. Monga A, Gupta R, Ramchandani M, Rao GV, Santosh D, Reddy DN. Endoscopic radiofrequency ablation of cholangiocarcinoma: new palliative treatment modality (with videos). Gastrointest Endosc. 2011; 74:935–937.




 PDF
PDF ePub
ePub Citation
Citation Print
Print




 XML Download
XML Download