Abstract
Acute coronary syndrome (ACS) is characterized by the rapid progression of coronary thrombosis and myocardial ischemia associated with the erosion or rupture of vulnerable atherosclerotic plaques. High-sensitivity cardiac troponin assay-based diagnostic algorithms enable rapid diagnosis within a few hours for patients in whom ACS is suspected. Prompt restoration of blood flow in the occluded artery is the top priority in patients with ST-elevation myocardial infarction, and the recommended first medical contact-to-percutaneous coronary intervention time is within 120 minutes. Since patients with non-ST elevation ACS are heterogeneous in their clinical profiles and severity of myocardial ischemia, the treatment strategy for non-ST elevation ACS is based on risk stratification at presentation. An early invasive strategy is indicated for patient at high risk of cardiac events, whereas an ischemia-guided approach is indicated for stabilized patient with lower risk score. Appropriate antithrombotic medication is critically important in the management of ACS. Dual antiplatelet treatment (DAPT) including aspirin and newer P2Y12 inhibitors should be maintained. Generally, at least 12 months of DAPT is recommended in ACS patients; however, the optimal duration of DAPT depends on weighing the benefits of preventing ischemic events versus the risk of bleeding in individual patient.
급성 관상동맥증후군(acute coronary syndrome, ACS)은 전 세계적으로 주요한 사망 원인이며 한국에서도 증가하는 추세이다[1]. 취약한 죽상반의 파열 또는 미란에 의해 혈전이 생기며 그 결과 혈관 내강이 급격히 폐쇄되어 심근허혈 또는 괴사가 발생하는 질환으로서, 심전도 소견에 따라 ST분절상승 ACS (ST elevation ACS)와 비ST분절상승 ACS (non-ST elevation ACS, NSTE-ACS)로 분류한다. NSTE-ACS는 심근표지자가 상승하면 비ST분절상승 심근경색증(non-ST elevation myocardial infarction, NSTEMI), 정상 범위이면 불안정형협심증(unstable angina, UA)으로 분류한다. ACS의 공통적인 치료원칙은 1) 발병 초기 급사 예방, 2) 항혈전제(항혈소판제, 항응고제), 3) 적절한 관상동맥중재술, 4) 위험인자 조절을 통한 이차예방 및 재활요법이다. 본고에서는 최근 개정된 미국과 유럽 심장학회의 진료지침을 중심으로 ACS의 진단과 치료과정을 요약하고자 한다[23456].
흉통으로 응급실에 내원한 환자 중에는 ACS 외에도 대동맥박리, 심막염, 근골격계 통증이나 역류성식도염 등 다양한 심장성 또는 비심장성 원인이 섞여 있으므로 이들 환자에서 신속한 ACS 진단을 위한 rule-in/rule-out 전략이 필요하다. 흉통의 특성, 관상동맥 위험인자 해당 여부, 진찰소견 등은 중요한 단서이지만 ACS 진단을 확정하기에는 불충분하다. STEMI (ST elevation myocardial infarction)에서는 대부분 전형적인 흉통과 심전도에서 ST분절상승이 나타나므로 임상증상과 심전도 소견으로 재관류 치료 여부를 결정할 수 있다. 그러나 NSTE-ACS에서는 임상증상이나 심전도만으로는 진단이 어려운 경우가 많으므로 심근표지자를 바탕으로 진단한다.
ACS의 심근표지자로 과거에는 myoglobin, CK-MB를 사용하였으나 현재는 심근세포 손상을 진단하는 민감도와 특이도가 높은 심장 트로포닌(troponin)-I 또는 트로포닌-T를 사용한다. CK-MB가 정상 범위임에도 불구하고 미량의 트로포닌이 검출될 수 있으며 이에 따라 과거에는 UA로 진단된 ACS가 현재는 NSTEMI로 분류되므로 최근에는 UA/NSTEMI를 구별하지 않고 NSTE-ACS로 통칭하는 경향이다. 트로포닌은 심근경색증 외에도 심부전, 신부전, 패혈증, 폐질환, 폐색전증, 뇌졸중 등 다양한 원인에 의한 심근손상에서 상승할 수 있다[6]. 트로포닌은 정상적으로 혈액에서 검출되지 않으며 가양성이 없으므로 혈중 트로포닌이 상승한 환자는 상승하지 않은 환자에 비해 예후가 나쁘며 이는 심근경색증뿐 아니라 다양한 심장 및 심장 외 원인에 의한 상승에서도 마찬가지이다. ACS에서 트로포닌 농도는 급격히 상승하여 수일간 높은 상태가 유지되므로 트로포닌 상승이 있더라도 시간에 따른 변화가 없다면 ACS 외의 다른 원인일 가능성이 높다. 최근 사용되는 고감도 트로포닌 검사는 과거에 비해 민감도가 향상되어 발병 초기에 신속한 진단이 가능하고 경미한 농도 변화도 감지할 수 있어서 짧은 시간 간격으로 반복 측정할 수 있다. 2015년 유럽심장학회는 급성 흉통 환자에서 심근경색증을 신속하게 진단할 수 있는 “rule-in/rule-out” 알고리즘을 제안하였는데, 내원 시, 1시간 후, 3시간 후에 각각 고감도 심장 트로포닌을 측정하여 절대값의 변화를 비교하는 것으로 상승 폭이 클수록 심근경색증일 가능성이 높다[6]. 이를 요약하면 첫째, 0-3시간 rule-in/rule-out으로서, 내원 직후와 3시간 후에 각각 측정한 고감도 트로포닌 농도가 모두 정상 범위이고 흉통이 없으며 Global Registry of Acute Coronary Events (GRACE) 점수 140점 미만으로 원내 사망위험이 낮으면 급성 심근경색증을 배제할 수 있다(rule-out). 흉통 발생 후 6시간 이상 경과한 환자에서 고감도 트로포닌 1회 검사로 심근경색증 여부를 진단할 수 있으며 정상 범위이면 심근경색증을 배제할 수 있다(rule-out). 내원 시 고감도 트로포닌이 뚜렷하게 높거나, 또는 3시간 후 측정값이 유의하게 상승한 경우에는 급성 심근경색증으로 진단할 수 있다(rule-in). 둘째, 0-1시간 rule-in/rule-out으로서, 내원 직후와 1시간 후 고감도 트로포닌 값의 변화에 따라 급성 심근경색증을 진단한다. 변화의 정도가 중간 범위여서 rule-in 또는 rule-out하기 어려운 경우에는 고감도 트로포닌 검사를 반복하고 영상 검사, 관상동맥조영술 등을 시행하여 ACS 여부를 판정한다. 셋째, 0-1시간 rule-out으로서 흉통 발생 후 2-3시간 이후에 내원한 환자에서 고감도 트로포닌 수치가 매우 낮다면 급성 심근경색증 진단을 배제할 수 있다(rule-out).
0-1시간 rule-in 알고리즘은 진단 특이도가 높으며 급성 심근경색증의 약 60%를 rule-in 할 수 있고, 심근경색증 외의 원인으로 포함되었더라도 대부분 스트레스 심근증, 급성 심근염, 대동맥박리, 폐색전증 등으로 입원이나 관상동맥 검사가 필요한 경우에 해당한다. 그러나 rule-out에 사용하기에는 민감도가 낮으므로 몇가지 주의가 필요하다. 즉, 1) 흉통, 심전도 등 임상 정보와 함께 사용한다, 2) 심근손상 후 트로포닌이 상승하기까지 시간이 걸리므로 흉통 발생 후 일찍(1시간 이내에) 내원한 경우에는 두번째 트로포닌 검사를 3시간 후에 시행한다, 3) 드물게 트로포닌이 늦게 상승할 수 있으므로 임상적으로 심근경색증의 가능성이 높다면 추가 검사가 필요하다.
아스피린은 항혈소판제로서 ACS 치료에 처음 사용된 항혈전제이다. 혈소판 활성화 경로 중 cyclooxygenase-1을 비가역적으로 불활성화시켜 thromboxane A2 생성을 억제한다. 아스피린 장기 복용은 안정형 협심증과 ACS 환자에서 심혈관 사건을 줄일 수 있다. 처음 ACS 진단 시에 비코팅 아스피린을 162-325 mg 경구투여하고, 이후 특별한 금기증이 없다면 매일 75-100 mg을 투여한다. 용량을 높이더라도 항혈소판 효과에는 큰 차이가 없으며 출혈 위험성이 증가한다. 심혈관질환 환자의 약 28%에서 아스피린 저항성이 있는 것으로 보고되었다[7].
혈소판의 P2Y12 수용체를 불활성화시켜 adenosine diphosphate 유도성 혈소판 응집을 억제하며 clopidogrel, prasugrel, ticagrelor가 있다. ACS 또는 관상동맥중재술 후 아스피린과 P2Y12 수용체 억제제를 병용 투여하여 아스피린 저항성을 보완하고 혈전에 의한 심혈관 사건 발생율을 낮출 수 있다. Clopidogrel은 전구약물로서 장에서 흡수된 후 85%는 효소작용에 의해 불활성화되고 나머지가 간에서 cytochrome P450 시스템에 의해 두 단계의 산화과정을 거쳐 활성 대사물로 전환되므로 복용 후 약효가 나타날 때까지 2-4시간이 걸린다. 또한 clopidogrel의 대사는 유전자 다형성에 의해 개인간 변동성이 커서 항혈소판 효과의 개인차가 있고 일부 환자에서는 현저히 감소되어 있다. Prasugrel, ticagrelor는 이러한 단점을 보완한 약제로 보다 빠르고 안정된 항혈소판 효과를 나타내며 스텐트 혈전증을 포함한 심혈관 사건 재발을 줄일 수 있다[89]. Prasugrel은 clopidogrel과 같은 thienopyridine계 전구약물이나 간에서 산화과정을 한번만 거쳐 활성화되므로 clopidogrel에 비해 빠르고 강력한 항혈소판 효과를 나타낸다. 그만큼 출혈 위험성도 높으므로 뇌졸중 과거력 등 출혈 위험이 높은 환자에서는 피하고 고령, 저체중 환자에서 감량이 필요하다. Ticagrelor는 cyclopentyltriazolopyrimidine 계열의 약제로 전구약물이 아니어서 체내에서 대사 과정을 거치지 않고 직접 혈소판의 P2Y12 수용체에 작용한다. Clopidogrel에 비하여 항혈소판 효과가 빠르고 강력하며 thienopyridine계 약물과 달리 가역적인 항혈소판 효과를 나타낸다. 그러나 출혈 경향이 심하거나 과민반응이 있으면 금기이며 반감기가 짧아 하루 2회 복용이 필요하다. 최근 유럽심장학회의 지침에 의하면 ACS에서 P2Y12 수용체 억제제를 사용할 때 우선적으로 prasugrel이나 ticagrelor가 권고되며 이들 약제를 사용하기 어려운 경우에만 clopidogrel을 사용한다[6]. Prasugrel은 관상동맥중재술이 결정된 경우에 한하여 사용할 수 있다. Ticagrelor는 ACS에서 관상동맥중재술 시행 여부에 관련 없이 이차예방 목적으로 사용할 수 있고 이전의 clopidogrel 복용과 관계 없이 투여할 수 있으며 고령 또는 저체중 환자에서도 별도의 용량조절이 필요하지 않다.
혈소판 응집의 마지막 단계에 작용하여 피브리노젠 및 von Willebrand 인자와 당단백 IIb/IIIa 수용체의 결합을 억제하여 빠르고 강력한 항혈소판 효과를 나타낸다. 임상연구에서 당단백 IIb/IIIa 억제제는 관상동맥중재술을 받는 NSTE-ACS의 임상경과를 개선시키는 효과가 있었으나 이는 대부분 P2Y12 수용체 억제제가 도입되기 전에 진행된 것으로, 최근에 사용되는 prasugrel이나 ticagrelor 등과 같은 강력한 P2Y12 수용체 억제제를 복용하는 환자에서 당단백 IIb/IIIa 억제제 추가 투여에 따른 이득은 없다. 따라서 NSTE-ACS에서 당단백 IIb/IIIa 억제제는 관상동맥중재술이 예정된 고위험 환자에서 시술 전 P2Y12 수용체 억제제를 복용하지 않았거나 또는 관상동맥중재술 중 다량의 혈전이나 혈류 장애가 관찰될 때에 한하여 제한적으로 사용된다[6].
NSTE-ACS 발병 초기에 항혈소판제와 함께 비경구적 항응고제를 투여한다. 비분획헤파린은 응고시간 모니터링이 필요하고 일부 환자에서 헤파린유발성 혈소판감소증이 발생하는 단점이 있다. 저분자량헤파린은 비분획헤파린에 비해 출혈 위험성은 비슷하거나 낮고 임상경과 개선효과가 약간 우월한 것으로 알려져 있다. Fondaparinux는 응고인자-Xa 선택적 억제제로 저분자량헤파린과 유사한 효과가 있으나 카테터 혈전 발행 위험이 있으므로 관상동맥중재술 중에 단독으로 투여할 수 없다. Bivalirudin은 혈액과 혈전의 thrombin을 직접 억제하나 아직 우리나라에 도입되지 않았다. 중재시술 전후에 단독으로 사용할 수 있으므로 헤파린유발성 혈소판감소증 환자에서 헤파린 대체약물로 투여할 수 있으나 STEMI에서 효과에 대한 근거가 부족하여 사용이 제한적이다[101112].
STEMI는 대부분 단일 혈관의 완전폐쇄에 의해 심근손상이 급속히 진행하므로 심근손상을 최소화하고 임상경과를 개선하기 위하여 즉각적인 재관류 치료가 원칙이다. STEMI에서 증상 발생 2-3시간 이내에 재관류가 매우 중요한데, 일차적 관상동맥중재술이 가장 효과적이다. 따라서 STEMI 환자는 최대한 신속하게 중재시술이 가능한 병원으로 이송되어야 한다(Figure 1) [2]. 최근 일차의료기관 또는 응급의료기관과 중재시술병원 사이의 관계를 나타내는 ‘first medical contact to-balloon (FMCTB) time’ 이라는 용어를 사용하며 중재시술병원에서 FMCTB는 90분 이내, 응급실 방문부터 중재시술 시작까지 door-to-balloon time은 60분 이내가 권고된다[23]. 중재시술을 할 수 없는 병원에서는 30분 이내에 중재시술병원으로 환자를 이송하여 총 FMCTB 시간 120분 이내가 권고된다. 유럽심장학회 지침에서 심근경색 범위가 넓거나 발병 2시간 이내에 내원한 경우에는 FMCTB를 30분 더 단축하도록 권고하고 있다[6]. 이 시간 내에 전원이 불가하고 증상 발생 후 2시간 이내인 경우에는 응급실 방문 30분 이내에 혈전용해제를 투여한다.
일차적 관상동맥중재시술에서 심근경색을 일으킨 경색관련 병변은 당연히 치료해야 하지만 경색관련 병변이 아닌 나머지 혈관 병변에 대한 예방목적의 중재시술에 대해서는 논란이 있다. 전통적으로 STEMI에서 경색관련 병변을 우선 치료하고 추후에 나머지 병변을 치료하는 단계적 관상동맥중재술을 권고하고, 심인성 쇼크나 매우 불안정한 병변에 대해서만 동시 치료를 권고하였다. 그러나 최근 연구결과에 따르면 일부 환자에서 경색 관련 병변 이외의 병변까지 동시에 관상동맥중재술을 시행한 경우에 임상경과 개선효과가 더 나을 수 있으므로[131415], 2015년 미국심장학회는 과거의 지침을 변경하여 혈역학적으로 안정된 경우라도 병변의 중증도에 따라 경색 관련 이외의 병변에 동시 관상동맥중재술을 시행할 수 있다고 하였다[16]. 혈전흡인술은 이론적으로는 관상동맥중재시술 중 부서진 혈전과 죽상경화반 조각들이 원위부 색전을 일으키는 것을 방지하여 심근재관류 효과를 높인다. 과거 연구에서는 STEMI에서 심근경색의 크기를 줄이는 효과가 보고되었으나[17], 최근 연구에서는 30일, 180일, 1년째 사망률 및 주요 심장사건 발생률이 비슷하며 임상적인 이득이 확인되지 않았다[181920]. 따라서 현재 STEMI에서 일상적인 혈전흡인술은 권고되지 않는다[16]. 최근 연구에 따르면 STEMI에서 요골동맥 접근 중재술은 대퇴동맥 접근 중재술에 비해 유의한 출혈 사건과 사망률을 낮추므로[21] 요골동맥 접근이 우선적으로 추천된다. 그러나 동맥 접근은 환자의 혈역학적 상태와 시술자의 경험 등에 따라 장단점이 다를 수 있으므로 개별적으로 결정해야 한다.
NSTE-ACS는 심근손상이 없는 경증 UA부터 광범위한 심근괴사와 심인성 쇼크를 일으키는 중증 NSTEMI까지 혈관 폐쇄의 정도나 진행 속도가 매우 다양하고 고령, 다수의 동반질환, 다혈관질환, 좌심실부전 등 다양한 환자군을 포함하는 복잡한 스펙트럼의 질환이다. 따라서 심근허혈의 중증도와 환자의 상태를 고려한 위험도 평가에 따라 적절한 약물치료 선택, 관상동맥중재술 여부와 적절한 시기 결정, 적극적인 동반질환 관리 등 차별화된 치료전략이 필요하다[46]. 허혈 혹은 경색 유발병변의 혈전을 억제하기 위하여 항혈소판제와 항응고제를 투여하고 재관류가 필요한 경우에는 관상동맥중재술을 시행한다(Figure 2) [4]. 현재까지 NSTE-ACS에서는 재관류 목적으로 혈전용해제를 사용할 수 없는데, 이는 임상적 이득이 없고 출혈 합병증 위험만 증가하기 때문이다.
ACS 환자의 초기 위험도 평가도구로서 TIMI (Thrombolysis in Myocardial Infarction) risk score, GRACE risk score 등이 이용된다. NSTE-ACS에서 이들 평가도구와 활력징후, 증상, 심근표지자, 과거병력, 동반질환, 심전도 등의 초기 임상정보를 참고하여 환자의 위험도를 계층화하고 이에 따른 치료전략을 세우도록 권장된다[46] (Table 1). 위험도가 높을수록 관상동맥중재술 시기를 더 앞당기는 치료전략을 선택한다. 고위험군에서는 침습적 전략을 선택하여 조기에 관상동맥중재술을 시행하는 것이 허혈이나 심근경색 재발, 재입원, 사망 감소효과를 기대할 수 있다. 위험도가 낮고 안정된 환자에서는 허혈 상태에 따른 전략을 적용하여 단독 약물치료가 가능하다. 약물치료에 반응하지 않는 경우에는 관상동맥조영술 결과에 따라 관상동맥중재술 또는 동맥우회로 이식술을 포함한 침습적 전략으로 전환할 수 있다.
ACS에서 관상동맥중재술은 혈전생성 위험이 매우 높은 취약한 죽상반에 스텐트를 삽입하는 과정으로 안정형협심증에 비해 스텐트혈전증이 발생할 위험이 높다. 스텐트혈전증이 관상동맥중재술 후 1% 내외로 드물게 발생함에도 불구하고 많은 관심과 논란이 되고 있는 이유는 사망률이 7-45%로 치명적이기 때문이며[22] 환자 요인, 병변의 특성, 중재시술 요인 등 많은 요인이 복합적으로 관여하여 발생하는 것으로 알려져 있다. 관상동맥중재술 후에는 스텐트혈전증 예방을 위해 저용량 아스피린에 P2Y12 수용체 억제제를 추가하는 이중 항혈소판제 요법(dual antiplatelet treatment, DAPT)이 필수적이다[523].
혈전용해제 치료를 받은 STEMI를 제외한 ACS에서 최소 12개월 이상 DAPT를 유지하는 것이 권장된다. 각 환자의 허혈위험과 출혈위험에 따라 기간을 일부 조정할 수 있으며 항응고제 복용, 뇌 병변 등으로 출혈 위험이 높거나 중대한 출혈이 있는 경우에는 DAPT 기간을 12개월 이내로 단축할 수 있다[456] (Figure 3). ACS에서 스텐트혈전증 및 주요 심뇌혈관사건의 발생 위험은 수년간 지속되므로 임상적으로 안정된 환자에서 DAPT 기간을 1년 이상 연장하여 심뇌혈관사건을 줄일 수 있으나 동시에 출혈위험도 증가한다. 혈전증 위험이 높은 환자일수록 출혈위험 역시 높은 경향이 있어서 각 환자에서 DAPT의 득실을 정확히 예측하기 어렵다. 이러한 배경으로 DAPT 점수가 고안되었으며 DAPT 점수가 2점 이상인 경우에는 출혈위험이 낮으므로 DAPT의 기간을 늘릴 수 있다[6] (Table 2).
ACS 환자 중 심방세동 등의 이유로 장기간 항응고제 복용이 필요한 경우가 있다. 아스피린, clopidogrel, 경구용 항응고제를 모두 복용하는 삼중 약물요법은 DAPT에 비해 출혈위험을 유의하게 증가시킨다[24]. 관상동맥중재술 후 초기에는 스텐트혈전증 예방을 위해 DAPT가 필수적이므로 출혈위험이 낮은 환자에서는 관상동맥중재술 후 6개월 동안 삼중 약물요법으로 치료한 후 경구용 항응고제에 아스피린이나 clopidogrel을 추가하는 이중 약물요법을 6개월간 유지하도록 권장된다[4]. 출혈위험이 높은 환자에서는 1개월 동안 삼중 약물요법, 이후 11개월 동안 이중 약물요법, 1년 이후에는 항응고제 단독 요법이 권장된다. 삼중 약물요법이 필요한 경우에는 항혈소판 효과가 강한 ticagrelor나 prasugrel을 피하고 clopidogrel을 사용한다.
ACS의 공통적인 병태생리는 동맥 내의 혈전 형성으로 인한 심근허혈이 발생하는 것이므로 적절한 항혈전제와 관상동맥중재술이 치료의 근간이 된다. ACS 중 STEMI에서는 가능한 빠른 시간 내에 관상동맥중재술을 시행하여 재관류 시간을 단축해야 하고, NSTE-ACS에서는 환자의 위험도에 따라 관상동맥중재술 여부 및 시기를 결정하는 것이 중요하다. 항혈전제는 급성기 허혈의 치료와 이차예방에 필수적이지만 출혈위험을 증가시키므로 적절한 병합투여가 중요하다. 환자의 출혈위험이 높지 않으면 ACS 발병 후 1년까지 아스피린과 P2Y12 수용체 억제제를 병합 투여하는 DAPT가 원칙이고, 스텐트를 삽입한 경우는 더욱 강력한 P2Y12 수용체 억제제인 ticagrelor 또는 prasugrel 사용이 권장된다. 발병 1년 이후에는 허혈위험과 출혈위험에 따라 DAPT를 계속할지를 결정한다.
본 원고는 급성 관상동맥증후군의 병태생리학적 기전에 따른 분류, 진단방법, 약물치료, 중재술의 적응증 및 치료법, 중재술 이후의 항혈소판제 투약방침, 퇴원 후 관리 등을 체계적으로 잘 정리 소개하고 있다. 급성 관상동맥증후군의 진단에 있어 최근 관심이 높아진 고감도 심장 트로포닌 검사의 의의와 판독법에 대해 자세히 설명하고 있어 이 검사법을 막 도입하고 있는 의료진에게 도움이 되는 지식을 포함하고 있다. 약물치료에 있어서는 특히 항혈소판제 및 항응고제의 특성 및 적용법에 대해 적절히 소개하였다. 중재술 여부의 선택 및 시행 방침에 대해서는 ST분절상승 및 비상승 심근경색증 각각을 구분하여 시술의 적응증 및 치료 전략, 시술 후 퇴원 시 약물투약 및 예방관리에 대해서 잘 정리하였다. 따라서 우리나라의 급성 관상동맥증후군의 진단 및 치료를 시행하는 데 있어 좋은 지침이 될 수 있는 논문이라 판단된다.
[정리: 편집위원회]
Figures and Tables
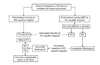 | Figure 1Treatment algorithm in ST elevation myocardial infarction. PCI, percutaneous coronary intervention; FMCTB, first medical contact to balloon time (Modified from Task Force on the Management of ST-segment Elevation Acute Myocardial Infarction of the European Society of Cardiology, et al. Eur Heart J 2012;33:2569– 2619) [2]. |
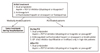 | Figure 2Treatment algorithm in non-ST elevation acute coronary syndrome. PCI, percutaneous coronary intervention; GP, glycoprotein. a)The more potent P2Y12 inhibitors (ticagrelor and prasugrel) are preferred over clopidogrel in 2015 European Society of Cardiology guideline (Modified from Amsterdam EA, et al. Circulation 2014;130:e344-e426) [4]. |
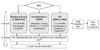 | Figure 3Treatment algorithm for duration of P2Y12 inhibitor therapy in acute coronary syndrome (ACS). NSTE-ACS, non-ST elevation myocardial infarction acute coronary syndrome; STEMI, ST elevation myocardial infarction; PCI, percutaneous coronary intervention; BMS, bare metal stent; DES, drug-eluting stent; DAPT, dual antiplatelet treatment. a)The more potent P2Y12 inhibitors (ticagrelor and prasugrel) are preferred over clopidogrel in 2015 European Society of Cardiology guideline (Modified from Levine GN, et al. Circulation 2016;134:e123-e155) [5]. |
Table 1
Factors associated with appropriate selection of immediate invasive or ischemia-guided strategy in patients with non-ST elevation myocardial infarction acute coronary syndrome

Modified from Roffi M, et al. Eur Heart J 2016;37:267– 315 [6].
TIMI, Thrombolysis in Myocardial Infarction; GRACE, Global Registry of Acute Coronary Events.
References
1. Hong JS, Kang HC, Lee SH, Kim J. Long-term trend in the incidence of acute myocardial infarction in Korea: 1997-2007. Korean Circ J. 2009; 39:467–476.

2. Task Force on the Management of ST-segment Elevation Acute Myocardial Infarction of the European Society of Cardiology (ESC). Steg PG, James SK, Atar D, Badano LP, Blomstrom-Lundqvist C, Borger MA, Di Mario C, Dickstein K, Ducrocq G, Fernandez-Aviles F, Gershlick AH, Giannuzzi P, Halvorsen S, Huber K, Juni P, Kastrati A, Knuuti J, Lenzen MJ, Mahaffey KW, Valgimigli M, van't Hof A, Widimsky P, Zahger D. ESC guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur Heart J. 2012; 33:2569–2619.
3. O'Gara PT, Kushner FG, Ascheim DD, Casey DE Jr, Chung MK, de Lemos JA, Ettinger SM, Fang JC, Fesmire FM, Franklin BA, Granger CB, Krumholz HM, Linderbaum JA, Morrow DA, Newby LK, Ornato JP, Ou N, Radford MJ, Tamis-Holland JE, Tommaso CL, Tracy CM, Woo YJ, Zhao DX, Anderson JL, Jacobs AK, Halperin JL, Albert NM, Brindis RG, Creager MA, DeMets D, Guyton RA, Hochman JS, Kovacs RJ, Kushner FG, Ohman EM, Stevenson WG, Yancy CW. American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2013; 127:e362–e425.
4. Amsterdam EA, Wenger NK, Brindis RG, Casey DE Jr, Ganiats TG, Holmes DR Jr, Jaffe AS, Jneid H, Kelly RF, Kontos MC, Levine GN, Liebson PR, Mukherjee D, Peterson ED, Sabatine MS, Smalling RW, Zieman SJ. ACC/AHA Task Force Members. 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation. 2014; 130:e344–e426.
5. Levine GN, Bates ER, Bittl JA, Brindis RG, Fihn SD, Fleisher LA, Granger CB, Lange RA, Mack MJ, Mauri L, Mehran R, Mukherjee D, Newby LK, O'Gara PT, Sabatine MS, Smith PK, Smith SC Jr. 2016 ACC/AHA guideline focused update on duration of dual antiplatelet therapy in patients with coronary artery disease: a report of the American College of Cardiology/American Heart Association Task Force on clinical practice guidelines: an update of the 2011 ACCF/AHA/SCAI guideline for percutaneous coronary intervention, 2011 ACCF/AHA guideline for coronary artery bypass graft surgery, 2012 ACC/AHA/ACP/AATS/PCNA/SCAI/STS guideline for the diagnosis and management of patients with stable ischemic heart disease, 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction, 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes, and 2014 ACC/AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery. Circulation. 2016; 134:e123–e155.

6. Roffi M, Patrono C, Collet JP, Mueller C, Valgimigli M, Andreotti F, Bax JJ, Borger MA, Brotons C, Chew DP, Gencer B, Hasenfuss G, Kjeldsen K, Lancellotti P, Landmesser U, Mehilli J, Mukherjee D, Storey RF, Windecker S, Baumgartner H, Gaemperli O, Achenbach S, Agewall S, Badimon L, Baigent C, Bueno H, Bugiardini R, Carerj S, Casselman F, Cuisset T, Erol C, Fitzsimons D, Halle M, Hamm C, Hildick-Smith D, Huber K, Iliodromitis E, James S, Lewis BS, Lip GY, Piepoli MF, Richter D, Rosemann T, Sechtem U, Steg PG, Vrints C, Luis Zamorano J. 2015 ESC guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: Task force for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J. 2016; 37:267–315.

7. Krasopoulos G, Brister SJ, Beattie WS, Buchanan MR. Aspirin “resistance” and risk of cardiovascular morbidity: systematic review and meta-analysis. BMJ. 2008; 336:195–198.

8. Wiviott SD, Braunwald E, McCabe CH, Montalescot G, Ruzyllo W, Gottlieb S, Neumann FJ, Ardissino D, De Servi S, Murphy SA, Riesmeyer J, Weerakkody G, Gibson CM, Antman EM. TRITON-TIMI 38 Investigators. Prasugrel versus clopidogrel in patients with acute coronary syndromes. N Engl J Med. 2007; 357:2001–2015.

9. Wallentin L, Becker RC, Budaj A, Cannon CP, Emanuelsson H, Held C, Horrow J, Husted S, James S, Katus H, Mahaffey KW, Scirica BM, Skene A, Steg PG, Storey RF, Harrington RA, Freij A, Thorsen M. PLATO Investigators. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med. 2009; 361:1045–1057.

10. Stone GW, Witzenbichler B, Guagliumi G, Peruga JZ, Brodie BR, Dudek D, Kornowski R, Hartmann F, Gersh BJ, Pocock SJ, Dangas G, Wong SC, Kirtane AJ, Parise H, Mehran R. HORIZONS-AMI Trial Investigators. Bivalirudin during primary PCI in acute myocardial infarction. N Engl J Med. 2008; 358:2218–2230.

11. Shahzad A, Kemp I, Mars C, Wilson K, Roome C, Cooper R, Andron M, Appleby C, Fisher M, Khand A, Kunadian B, Mills JD, Morris JL, Morrison WL, Munir S, Palmer ND, Perry RA, Ramsdale DR, Velavan P, Stables RH. HEAT-PPCI trial investigators. Unfractionated heparin versus bivalirudin in primary percutaneous coronary intervention (HEAT-PPCI): an open-label, single centre, randomised controlled trial. Lancet. 2014; 384:1849–1858.

12. Valgimigli M, Frigoli E, Leonardi S, Rothenbuhler M, Gagnor A, Calabro P, Garducci S, Rubartelli P, Briguori C, Ando G, Repetto A, Limbruno U, Garbo R, Sganzerla P, Russo F, Lupi A, Cortese B, Ausiello A, Ierna S, Esposito G, Presbitero P, Santarelli A, Sardella G, Varbella F, Tresoldi S, de Cesare N, Rigattieri S, Zingarelli A, Tosi P, van't Hof A, Boccuzzi G, Omerovic E, Sabate M, Heg D, Juni P, Vranckx P. MATRIX Investigators. Bivalirudin or unfractionated heparin in acute coronary syndromes. N Engl J Med. 2015; 373:997–1009.

13. Engstrom T, Kelbaek H, Helqvist S, Hofsten DE, Klovgaard L, Holmvang L, Jorgensen E, Pedersen F, Saunamaki K, Clemmensen P, De Backer O, Ravkilde J, Tilsted HH, Villadsen AB, Aaroe J, Jensen SE, Raungaard B, Kober L. DANAMI-3—PRIMULTI Investigators. Complete revascularisation versus treatment of the culprit lesion only in patients with ST-segment elevation myocardial infarction and multivessel disease (DANAMI-3—PRIMULTI): an open-label, randomised controlled trial. Lancet. 2015; 386:665–671.

14. Gershlick AH, Khan JN, Kelly DJ, Greenwood JP, Sasikaran T, Curzen N, Blackman DJ, Dalby M, Fairbrother KL, Banya W, Wang D, Flather M, Hetherington SL, Kelion AD, Talwar S, Gunning M, Hall R, Swanton H, McCann GP. Randomized trial of complete versus lesion-only revascularization in patients undergoing primary percutaneous coronary intervention for STEMI and multivessel disease: the CvLPRIT trial. J Am Coll Cardiol. 2015; 65:963–972.

15. Kim I, Kim MC, Jeong HC, Park KH, Sim DS, Hong YJ, Kim JH, Jeong MH, Cho JG, Park JC, Seung KB, Chang K, Ahn Y. Optimal timing of percutaneous coronary intervention for nonculprit vessel in patients with ST-segment elevation myocardial infarction and multivessel disease. Korean Circ J. 2017; 47:36–43.

16. Levine GN, Bates ER, Blankenship JC, Bailey SR, Bittl JA, Cercek B, ChambersCE , Ellis SG, Guyton RA, Hollenberg SM, Khot UN, Lange RA, Mauri L, Mehran R, Moussa ID, Mukherjee D, Ting HH, O'Gara PT, Kushner FG, Ascheim DD, Brindis RG, Casey DE Jr, Chung MK, de Lemos JA, Diercks DB, Fang JC, Franklin BA, Granger CB, Krumholz HM, Linderbaum JA, Morrow DA, Newby LK, Ornato JP, Ou N, Radford MJ, Tamis-Holland JE, Tommaso CL, Tracy CM, Woo YJ, Zhao DX. 2015 ACC/AHA/SCAI focused update on primary percutaneous coronary intervention for patients with ST-elevation myocardial infarction: an update of the 2011 ACCF/AHA/SCAI guideline for percutaneous coronary intervention and the 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction. J Am Coll Cardiol. 2016; 67:1235–1250.

17. Vlaar PJ, Svilaas T, van der Horst IC, Diercks GF, Fokkema ML, de Smet BJ, van den Heuvel AF, Anthonio RL, Jessurun GA, Tan ES, Suurmeijer AJ, Zijlstra F. Cardiac death and reinfarction after 1 year in the Thrombus Aspiration during Percutaneous coronary intervention in Acute myocardial infarction Study (TAPAS): a 1-year follow-up study. Lancet. 2008; 371:1915–1920.

18. Frobert O, Lagerqvist B, Olivecrona GK, Omerovic E, Gudnason T, Maeng M, Aasa M, Angerås O, Calais F, Danielewicz M, Erlinge D, Hellsten L, Jensen U, Johansson AC, Karegren A, Nilsson J, Robertson L, Sandhall L, Sjogren I, Ostlund O, Harnek J, James SK. TASTE Trial. Thrombus aspiration during ST-segment elevation myocardial infarction. N Engl J Med. 2013; 369:1587–1597.

19. Lagerqvist B, Frobert O, Olivecrona GK, Gudnason T, Maeng M, Alstrom P, Andersson J, Calais F, Carlsson J, Collste O, Gotberg M, Hardhammar P, Ioanes D, Kallryd A, Linder R, Lundin A, Odenstedt J, Omerovic E, Puskar V, Todt T, Zelleroth E, Ostlund O, James SK. Outcomes 1 year after thrombus aspiration for myocardial infarction. N Engl J Med. 2014; 371:1111–1120.

20. Jolly SS, Cairns JA, Yusuf S, Meeks B, Pogue J, Rokoss MJ, Kedev S, Thabane L, Stankovic G, Moreno R, Gershlick A, Chowdhary S, Lavi S, Niemela K, Steg PG, Bernat I, Xu Y, Cantor WJ, Overgaard CB, Naber CK, Cheema AN, Welsh RC, Bertrand OF, Avezum A, Bhindi R, Pancholy S, Rao SV, Natarajan MK, ten Berg JM, Shestakovska O, Gao P, Widimsky P, Dzavik V. TOTAL Investigators. Randomized trial of primary PCI with or without routine manual thrombectomy. N Engl J Med. 2015; 372:1389–1398.

21. Youn YJ, Lee JW, Ahn SG, Lee SH, Yoon J, Cho BR, Cheong SS, Kim HY, Lee JH, Bae JH, Lee JB, Suh J, Park KS, Han KR, Jeong MH, Rha SW, Her SH, Cho YH, Kim SW. Current practice of transradial coronary angiography and intervention: results from the Korean Transradial Intervention Prospective Registry. Korean Circ J. 2015; 45:457–468.

22. Wenaweser P, Rey C, Eberli FR, Togni M, Tuller D, Locher S, Remondino A, Seiler C, Hess OM, Meier B, Windecker S. Stent thrombosis following bare-metal stent implantation: success of emergency percutaneous coronary intervention and predictors of adverse outcome. Eur Heart J. 2005; 26:1180–1187.

23. Levine GN, Bates ER, Blankenship JC, Bailey SR, Bittl JA, Cercek B, Chambers CE, Ellis SG, Guyton RA, Hollenberg SM, Khot UN, Lange RA, Mauri L, Mehran R, Moussa ID, Mukherjee D, Ting HH, O'Gara PT, Kushner FG, Ascheim DD, Brindis RG, Casey DE Jr, Chung MK, de Lemos JA, Diercks DB, Fang JC, Franklin BA, Granger CB, Krumholz HM, Linderbaum JA, Morrow DA, Newby LK, Ornato JP, Ou N, Radford MJ, Tamis-Holland JE, Tommaso CL, Tracy CM, Woo YJ, Zhao DX. 2015 ACC/AHA/SCAI focused update on primary percutaneous coronary intervention for patients with ST-elevation myocardial infarction: an update of the 2011 ACCF/AHA/SCAI guideline for percutaneous coronary intervention and the 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Society for Cardiovascular Angiography and Interventions. Circulation. 2016; 133:1135–1147.





 PDF
PDF ePub
ePub Citation
Citation Print
Print




 XML Download
XML Download