Abstract
Dry eye disease (also known as keratoconjunctivitis sicca) is a multifactorial disease of the tear film and ocular surface. It results in various symptoms of discomfort such as pain, tearing, fatigue, and headache. Visual function can also deteriorate, and quality of life is negatively affected. Tear film instability which may lead to damage to the ocular surface with an inflammatory reaction is key to the pathogenesis of dry eye disease. This review discussed the classification, pathogenesis, diagnostic approaches, and treatment options of dry eye disease.
안구건조증이란 2007년 DEWS (International Dry Eye Workshop)에서 정의된 바와 같이, 눈물과 안구표면의 다인성 질환으로서, 안구의 다양한 불편감을 유발함은 물론 시력의 장애, 더 나아가 안구표면에 손상을 유발하는 눈물층의 불안정성을 일으킨다고 알려져 있다[1]. 안구건조증 환자는 정상군에 비하여 시기능이 저하되어 있는데 대비감도가 현저히 떨어진다고 보고되었을 뿐만 아니라[2], 시력의 질에 영향을 주는 고위수차가 유의하게 증가되어있다고 밝힌 연구결과도 있다[3]. 더불어 다양한 설문양식을 통한 연구에서 안구건조증은 삶의 질을 유의하게 저하시킨다고 밝혀져 있다[456]. 이처럼 안구건조증은 질환 자체의 중증도 여부를 떠나 의료재정에 대한 부담을 점차적으로 증가시키고 있기 때문에 본 질환에 대한 이해도를 높임으로써 환자를 체계적으로 치료하고 관리하는데 도움이 될 것이다. 이에 본 논문에서는 최신 문헌을 통하여 안구건조증의 진단과 치료동향을 고찰해보고자 한다.
안구건조증의 정의를 알기에 앞서, 눈물층에 대하여 먼저 이해하여야만 한다. 눈물층은 안구표면, 즉 각막과 결막을 덮고 있으며 3개의 층으로 구성되어 있다. 가장 아래층인 점액질층은 각결막 상피 표면을 덮고 있으며, 그 위에 수성층이 존재하고, 지질층이 수성층을 덮음으로써 눈물의 증발을 막는 역할을 한다[7]. 서론에서 언급하였듯이 안구건조증은 안구표면과 눈물층에 발생하는 다인성 질환으로서, 시력 장애, 불편감을 야기하고 안구표면의 손상을 일으킨다. 눈물층의 삼투도를 증가시켜 안구표면의 염증을 유발하는 것이 주요 병인으로 알려져 있다[8]. 안구건조증은 병인에 따라 크게 두 가지로 분류된다. 첫 번째는 눈물샘에서 수성 성분의 눈물 분비가 감소되어 발생하는 경우인데 다시 쇼그렌증후군과 연관된 건성안과 그렇지 않은 건성안, 즉 주로 전신 약제와 관련된 경우의 두 가지로 나뉜다[9]. 두 번째는 지질층의 장애로 눈물의 증발이 증가되어 발생하는 경우로서 마이봄샘 기능부전과 관련이 있다[8]. 안구건조증의 위험인자로는 다양한 것이 알려져 있는데 고령, 여성, 눈 수술의 과거력, 갑상선질환, 높은 학력 등이 그것이며, 비타민 A나 오메가 3 지방산 부족 등의 영양소 결핍과의 연관성도 연구되어 있다[10]. 2011년도에 우리나라에서 시행된 국민건강영양조사에 따르면 전체 이환율이 약 16%로 조사되어 있다[11].
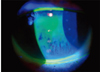
임상현장에서 안구건조증을 진단하는데 있어 가장 흔하게 사용되는 방법은 쉬르머 검사(Schirmer's test), 눈물막 파괴시간 검사(tear break up time), 각결막 염색 검사법 등이 대표적이다. 쉬르머 검사는 아래 눈꺼풀 결막낭 안쪽에 검사용지를 삽입하여 눈물의 분비량을 측정하는 검사이며, 진료실에 세극등 현미경이 구비되어 있지 않아도 손쉽게 시행할 수 있는 검사이다(Figure 1). Norn [12]에 의하여 고안된 눈물막 파괴시간 검사법은 안구건조증을 진단하는데 있어 간단하면서도 가장 흔하게 시행되는 대표적인 검사법이다(Figure 2). 검사 전 형광 염색액을 안구에 점안하여 세극등 현미경의 청색광 필터를 선택한 후 환자의 눈을 깜빡이게 하여 처음으로 눈물막이 갈라지는 시간을 초 단위로 측정한다. 안구건조증의 핵심적인 병인이 눈물층의 불균형이라는 점을 감안할 때 눈물막 파괴시간 검사법은 이를 감지해낼 수 있는 매우 효과적인 검사법이라고 할 수 있겠다. 이외에도 앞서 언급하였듯이 마이봄샘의 이상 여부를 관찰하거나 각막 및 결막의 미란 상태를 관찰하여 안구건조증의 중증도를 판단하고 치료계획을 수립할 수 있다[13]. 최근에는 각종 진단 장비의 눈부신 발전으로 눈물의 삼투도를 측정하는 TearLab system (TearLab Inc., San Diego, CA, USA)과 눈물 지질층을 분석하여 영상으로 관찰할 수 있는 LipiView interferometry system (TearScience Inc., Morrisville, NC, USA)이 개발되어 일부 임상현장과 연구에 유용하게 활용되고 있으나, 고가의 장비로서 일반 진료에 적용하기에는 그 한계가 있다.
안구건조증의 치료목표는 환자의 증상을 경감시키고 동반된 안구표면의 손상을 개선시킴으로써 환자의 삶의 질을 향상시키는데 있다. 치료에 앞서 쇼그렌증후군 등의 류마티스 질환 등의 전신질환 동반 여부를 확인하는 것이 필요하고, 항히스타민제, 베타차단제, 삼환계항우울제, 에스트로겐요법 등의 각종 전신 약제 등이 안구건조증을 악화시킨다고 알려져 있으므로 이에 대한 문진도 반드시 필요할 것이다[14]. 또한 안구건조증 이외에 동반된 안과적 염증질환을 확인하여야만 성공적인 치료효과를 거둘 수 있다.
점안치료제 중 가장 흔하게 사용되어 쉽게 처방할 수 있는 약제는 소위 인공눈물이라고 불리우는 안구표면 윤활제이다. 국내에서 가장 흔하게 처방하는 인공눈물은 히알루론산 나트륨(sodium hyaluronate) 제제와 카복시메틸셀룰로스 나트륨(sodium carboxymethylcellulose) 제제의 두 가지가 대표적이다. 인공눈물은 안구표면의 눈물을 보충해 줄 뿐만 아니라, 저삼투 성분으로 구성되어 있어 안구건조증에서 동반되는 고삼투 성분의 눈물층 삼투 농도를 낮추어 주고, 이로 인하여 안구표면 염증을 감소시키는 효과를 가져다 줄 수 있다[15].
안구건조증의 병리에서 언급하였듯이, 눈물층 불균형은 눈물의 삼투 농도 상승으로 인하여 안구표면의 염증반응이 유발되고 다시 이러한 염증반응이 눈물 분비 이상과 눈물층의 불균형을 야기하는 악순환을 가져오기 때문에[16] 항염증 치료는 안구건조증 치료의 매우 중요한 부분을 차지하고 있다. 대표적으로 스테로이드 점안 제제는 안구건조증의 모든 단계에서 증상과 병리 소견 개선에 효과적이라고 알려져 있고[17], 우리나라에서는 0.02% 혹은 0.1%의 플루오로메톨론(fluorometholone) 제제가 흔하게 쓰이지만 경우에 따라 이보다 약리 효능이 강한 로테프레드놀(loteprednol) 및 프레드니솔론(prednisolone) 제제가 쓰이기도 한다. 물론 이러한 스테로이드 제제의 사용에 있어 안압 상승, 백내장 촉발, 그리고 안구표면의 기회 감염 등의 부작용 발생을 유의하여야만 할 것이다. 또 다른 항염증 치료로서 2006년 이후로는 국내에 점안용 0.05% 싸이클로스포린(cyclosporine) 제제가 출시되어 스테로이드 제제의 부작용을 획기적으로 줄일 수 있으므로 안구건조증 치료에 널리 사용되고 있다. 싸이클로스포린 점안 치료는 각결막 상피의 면역 활성 마커(예, human leukocyte antigen - antigen D related), 세포자멸사 마커(예, Fas), 및 염증성 싸이토카인 (예, interleukin-6) 등을 감소시키는 등 안구표면의 염증반응을 감소시켜 안구건조증의 증상개선은 물론 눈물막 파괴시간의 증가 및 눈물 분비량 증가 등 객관적 소견의 개선효과도 있음이 밝혀졌다. 또한 일부 연구에서는 싸이클로스포린의 점안 치료가 눈물층의 점액 분비를 담당하는 결막 술잔 세포의 밀도를 증가시킬 뿐만 아니라[18] 마이봄샘 기능부전 치료에도 효과가 있어[19] 안구건조증의 다양한 병인을 해결해 줄 약물로 주목받고 있다.
또 다른 약제로 최근 등장하여 각광을 받고 있는 디쿠아포솔(diquafosol tetrasodium)은 P2Y2 수용체에 작용하는 길항체로서 눈물의 수성 성분은 물론 점액 성분의 분비를 촉진하는 것으로 알려져 있다[20]. 여러 무작위, 이중 맹검 시험에서 3% 디쿠아포솔 점안치료는 안구표면의 미란을 감소시킴으로써 눈물층을 안정화시키고 안구건조증을 완화시키는 효과가 입증되었다[2122]. 디쿠아포솔은 결막의 술잔 세포를 자극하여 눈물의 수성 및 점액 성분 분비를 촉진시키고 각막 상피의 장벽 기능을 강화시키는 효과가 동물 실험에서 증명이 되었다[2324]. Yamaguchi 등[25]은 안구건조증을 치료하는데 있어 각각의 눈물층에 따른 개별적인 접근이 필요하다고 강조하였는데 디쿠아포솔은 모든 눈물층의 안정화에 효과가 있다고 주장한다.
안과 영역, 특히 안구건조증의 치료에서 경구 약제의 역할은 제한되어 있으며 효과가 입증된 약제 또한 많지 않다. 첫 번째 약제는 테트라싸이클린(tetracycline)과 독시싸이클린(doxycycline)으로서 주사성 좌창이나, 만성적인 눈꺼풀 염증 및 마이봄샘 기능부전과 함께 동반되는 건성안의 치료에 효과적이라고 알려져 있다. 주사성 좌창에서는 항염증 작용과 함께, 신생혈관의 형성을 억제하여 안구건조증을 완화시킨다[2627]. 눈꺼풀 염증 및 마이봄샘 기능부전에서는 지방 분해효소의 형성을 억제하여 안구건조증 완화에 도움을 준다[28]. 지방 분해효소는 안구표면에서 다이글리세리드(diglyceride) 및 자유지방산의 생산을 증가시켜 눈물의 지질층에 불균형을 가져오고 안구표면의 염증을 증가시킴으로서 안구건조증을 악화시킨다. 지방 분해효소는 안구표면의 미생물인 포도상구균(Staphylococcus)에 의해서 생성이 증가되는 것으로도 알려져 있어, 테트라싸이클린과 독시싸이클린은 지방 분해효소의 생성을 직접 억제하기도 하고, 포도상구균에 항생효과를 가짐으로써 간접적으로 효소의 생성을 억제하기도 한다[2930]. 추천하는 용법으로는 50 mg을 하루에 한번 복용하여 이를 2주 기간으로 시작하고, 이후에는 약 2-3달에 걸쳐 100 mg을 하루에 한번 복용하여 유지하는 용법을 권장한다. 이보다 장기간 사용하는 경우에는 보다 저용량(20 mg)을 하루에 한번 사용하는 방법이 있다. 이들 약제는 12세 미만의 어린이나, 임부에서는 복용을 피하는 것이 좋고, 신장과 간장에 독성이 있을 수 있으므로 사용에 유의하여야 할 것이다.
앞서 언급한 점안 안약이나 경구 약제 치료에 반응하지 않는 건성안일 경우 눈물점 마개를 삽입하기도 한다. 필자의 의견으로는 눈물점 마개 치료가 안구표면에 동반된 염증을 악화시키는 경우도 있기 때문에 사용에 유의하여야 하지만 아직은 논란이 있다. 안구표면의 손상이 심한 경우에는 자가혈청 치료가 많은 도움이 된다[34]. 어떤 환자들은 안구건조증의 중증도에 비하여 심각한 통증을 호소하기도 하는데 이럴 경우 자가혈청 치료가 통증을 완화하는데 도움이 되기도 한다. 이러한 환자들은 각막 신경의 독특한 구조 변성을 동반하는 경우가 많은데 아마도 자가혈청 치료가 이를 개선하는 것으로 생각되지만 그 기전은 명확하지 않다[35]. 우울증 등의 정신과적인 문제를 가진 환자의 경우도 안구건조증의 중증도에 비하여 큰 불편감을 호소하는 경우가 많으므로 이런 경우 정신과적인 지지요법이 동반되어야 할 것이다[36]. 그 밖에 실내 습도를 적절히 유지하거나 독서 및 영상 시청 시 정기적인 휴식 등 생활습관 변화가 도움이 됨은 물론이다.
안구건조증은 치료가 쉽지 않고, 질환으로 인한 불편감으로 인하여 환자의 삶의 질까지 영향을 미친다. 치료가 잘 되지 않는 이유는 환자의 치료 순응도가 전반적으로 떨어지기 때문이다. 오랜 기간 동안, 하루에도 수 차례씩 치료 약제를 점안하여야 하므로 환자의 순응도가 떨어지고, 증상이 일부 호전되면 약제를 중단하는 경우도 흔하다. 환자의 생활습관 변화가 반드시 동반되어야 하는 것도 또 다른 이유이다. 더불어 안구건조증이란 다양한 원인에 따라 발생하는 다요인성 질환이므로 반드시 원인에 따른 접근과 진단 및 치료가 필요하므로 진료 시 세심한 주의가 요구될 것이다. 이러한 점을 바탕으로 환자에게 꾸준하고 적절한 치료를 받을 경우 안구건조증은 호전될 수 있는 질환임을 인지시키는 것이 매우 중요할 것이다.
본 논문에서는 2007년 Dry eye workshop (DEWS)에서 제안된 안구건조증의 새로운 정의를 바탕으로 다양한 병인 및 증상을 가지는 복잡한 질환에 대한 병인을 체계적으로 분류하기 위한 진단적 접근방법 및 이에 따른 최신지견을 포함한 여러 가지 치료방법을 소개하고 있다. 눈물층의 해부학적인 구조에 대한 이해를 바탕으로 한 다양하고 복잡한 안구건조증의 병인의 분류 및 임상적 진단방법에 대한 이론적인 설명은 안과에서 유병률이 가장 높은 질환인 안구건조증을 체계적으로 이해하는데 중요하며, 특히 다양한 병인 및 질환의 단계에 따른 치료방법의 소개는 실제 임상의 및 연구자들에게 다양한 치료방법을 이해하고 선택하는데 좋은 지침이 될 수 있는 논문이며, 병태 및 여러 가지 치료약제의 기전에 대한 이해를 체계적으로 기술함으로써 관련 질환의 연구방향을 제시했다는 점에서 중요한 의의가 있다고 판단된다.
[정리: 편집위원회]
Figures and Tables
References
1. Management and therapy of dry eye disease: report of the Management and Therapy Subcommittee of the International Dry Eye WorkShop (2007). Ocul Surf. 2007; 5:163–178.
2. Rolando M, Iester M, Macri A, Calabria G. Low spatial-contrast sensitivity in dry eyes. Cornea. 1998; 17:376–379.

3. Denoyer A, Rabut G, Baudouin C. Tear film aberration dyna-mics and vision-related quality of life in patients with dry eye disease. Ophthalmology. 2012; 119:1811–1818.

4. Mertzanis P, Abetz L, Rajagopalan K, Espindle D, Chalmers R, Snyder C, Caffery B, Edrington T, Simpson T, Nelson JD, Begley C. The relative burden of dry eye in patients' lives: com-parisons to a U.S. normative sample. Invest Ophthalmol Vis Sci. 2005; 46:46–50.

5. Abetz L, Rajagopalan K, Mertzanis P, Begley C, Barnes R, Chalmers R. Impact of Dry Eye on Everyday Life (IDEEL) Study Group. Development and validation of the impact of dry eye on everyday life (IDEEL) questionnaire, a patient-reported outcomes (PRO) measure for the assessment of the burden of dry eye on patients. Health Qual Life Outcomes. 2011; 9:111.

6. Baudouin C, Creuzot-Garcher C, Hoang-Xuan T, Rigeade MC, Brouquet Y, Bassols A, Guillemin I, Benmedjahed K, Arnould B. Severe impairment of health-related quality of life in patients suffering from ocular surface diseases. J Fr Ophtalmol. 2008; 31:369–378.

7. Bron AJ, Tomlinson A, Foulks GN, Pepose JS, Baudouin C, Geerling G, Nichols KK, Lemp MA. Rethinking dry eye disease: a perspective on clinical implications. Ocul Surf. 2014; 12:2 Suppl. S1–S31.

8. The definition and classification of dry eye disease: report of the Definition and Classification Subcommittee of the Inter-national Dry Eye WorkShop (2007). Ocul Surf. 2007; 5:75–92.
9. Akpek EK, Lindsley KB, Adyanthaya RS, Swamy R, Baer AN, McDonnell PJ. Treatment of Sjogren's syndrome-associated dry eye an evidence-based review. Ophthalmology. 2011; 118:1242–1252.
10. Kastelan S, Tomic M, Salopek-Rabatic J, Novak B. Diagnostic procedures and management of dry eye. Biomed Res Int. 2013; 2013:309723.
11. Ahn JM, Lee SH, Rim TH, Park RJ, Yang HS, Kim TI, Yoon KC, Seo KY. Epidemiologic Survey Committee of the Korean Ophthalmological Society. Prevalence of and risk factors asso-ciated with dry eye: the Korea National Health and Nutrition Examination Survey 2010-2011. Am J Ophthalmol. 2014; 158:1205–1214.e7.

12. Norn MS. Desiccation of the precorneal film. I. Corneal wet-ting-time. Acta Ophthalmol (Copenh). 1969; 47:865–880.
13. Paugh JR, Kwan J, Christensen M, Nguyen AL, Senchyna M, Meadows D. Development of a Meibomian Gland Dys-function-Specific Symptom Questionnaire. Eye Contact Lens. 2016; 07. 27. [Epub]. DOI: 10.1097/ICL.0000000000000294.

14. Barabino S, Labetoulle M, Rolando M, Messmer EM. Under-standing Symptoms and Quality of Life in Patients With Dry Eye Syndrome. Ocul Surf. 2016; 14:365–376.

15. Herrero-Vanrell R, Peral A. International Dry Eye Workshop (DEWS): update of the disease. Arch Soc Esp Oftalmol. 2007; 82:733–734.
16. Luo L, Li DQ, Doshi A, Farley W, Corrales RM, Pflugfelder SC. Experimental dry eye stimulates production of inflammatory cytokines and MMP-9 and activates MAPK signaling pathways on the ocular surface. Invest Ophthalmol Vis Sci. 2004; 45:4293–4301.

17. Avunduk AM, Avunduk MC, Varnell ED, Kaufman HE. The comparison of efficacies of topical corticosteroids and nonsteroidal anti-inflammatory drops on dry eye patients: a clinical and immunocytochemical study. Am J Ophthalmol. 2003; 136:593–602.

18. Kunert KS, Tisdale AS, Gipson IK. Goblet cell numbers and epithelial proliferation in the conjunctiva of patients with dry eye syndrome treated with cyclosporine. Arch Ophthalmol. 2002; 120:330–337.

19. Prabhasawat P, Tesavibul N, Mahawong W. A randomized double-masked study of 0.05% cyclosporine ophthalmic emul-sion in the treatment of meibomian gland dysfunction. Cornea. 2012; 31:1386–1393.

20. Tauber J, Davitt WF, Bokosky JE, Nichols KK, Yerxa BR, Schaberg AE, LaVange LM, Mills-Wilson MC, Kellerman DJ. Double-masked, placebo-controlled safety and efficacy trial of diquafosol tetrasodium (INS365) ophthalmic solution for the treatment of dry eye. Cornea. 2004; 23:784–792.

21. Matsumoto Y, Ohashi Y, Watanabe H, Tsubota K. Diquafosol Ophthalmic Solution Phase 2 Study Group. Efficacy and safety of diquafosol ophthalmic solution in patients with dry eye syndrome: a Japanese phase 2 clinical trial. Ophthalmology. 2012; 119:1954–1960.

22. Takamura E, Tsubota K, Watanabe H, Ohashi Y. Diquafosol Ophthalmic Solution Phase 3 Study Group. A randomised, double-masked comparison study of diquafosol versus sodium hyaluronate ophthalmic solutions in dry eye patients. Br J Ophthalmol. 2012; 96:1310–1315.

23. Kojima T, Dogru M, Ibrahim OM, Nagata T, Higa K, Shimizu T, Shirasawa T, Satake Y, Shimazaki S, Shimazaki J, Tsubota K. The effects of 3% diquafosol sodium application on the tear functions and ocular surface of the Cu,Zn-superoxide dis-mutase-1 (Sod1)-knockout mice. Mol Vis. 2014; 20:929–938.
24. Terakado K, Yogo T, Kohara Y, Soeta S, Nezu Y, Harada Y, Hara Y, Amasaki H, Tagawa M. Conjunctival expression of the P2Y2 receptor and the effects of 3% diquafosol ophthalmic solution in dogs. Vet J. 2014; 202:48–52.

25. Yamaguchi M, Nishijima T, Shimazaki J, Takamura E, Yokoi N, Watanabe H, Ohashi Y. Clinical usefulness of diquafosol for real-world dry eye patients: a prospective, open-label, non-interventional, observational study. Adv Ther. 2014; 31:1169–1181.

26. Frucht-Pery J, Chayet AS, Feldman ST, Lin S, Brown SI. The effect of doxycycline on ocular rosacea. Am J Ophthalmol. 1989; 107:434–435.

27. Maatta M, Kari O, Tervahartiala T, Peltonen S, Kari M, Saari M, Sorsa T. Tear fluid levels of MMP-8 are elevated in ocular rosacea: treatment effect of oral doxycycline. Graefes Arch Clin Exp Ophthalmol. 2006; 244:957–962.
28. Dougherty JM, McCulley JP, Silvany RE, Meyer DR. The role of tetracycline in chronic blepharitis: inhibition of lipase production in staphylococci. Invest Ophthalmol Vis Sci. 1991; 32:2970–2975.




 PDF
PDF ePub
ePub Citation
Citation Print
Print




 XML Download
XML Download