Abstract
Rheumatic diseases are associated various extra-articular manifestations, such as eye, nerve, pericardium, and pleura. The anterior part of the eye has distinguished anatomic structure resembling synovial joints, thus it is a common site of ocular manifestation in rheumatic disease. These changes include sicca syndrome, peripheral ulcerative keratitis, episcleritis, scleritis, and iritis. Some of these findings may be the clues for the diagnosis of the rheumatic diseases, and some ocular manifestations may represent the activity or prognosis of the rheumatic diseases. These ocular complications may leads to severe visual loss. It is crucial to rule out underlying systemic diagnosis in rheumatic disease associated ocular diseases, and when diagnosed, the coordination of the rheumatologist with the ophthalmologist in the treatment is imperative.
류마티스질환은 환경적, 유전적 요인으로 인한 자가면역으로 관절과 결합조직의 만성적인 염증 및 조직손상을 초래하는 질환을 일컫는 광범위한 용어로 류마티스관절염, 결절다발동맥염, 전신홍반루프스, 쇼그렌증후근, 재발성다발연골염, 베세트병, 피부경화증 등을 포함한다. 류마티스질환에서는 여러 가지 증상 중 하나로 안구증상이 나타날 수 있으며 질환의 활동성을 반영하는 경우도 있다. 또한 질환의 진단기준을 충족하기 위해 특정 안구소견이 요구되는 경우도 있으며 다양한 안질환이 류마티스질환과 연관성을 보이기도 한다. 눈의 해부학적 구조를 보면 결막, 각막, 공막과 같은 조직은 결합조직과 같이 콜라겐을 주성분으로 하고 있으며, 포도막, 망막은 풍부한 혈관구조를 갖는 반면, 각막은 투명성을 유지하기 위하여 무혈관구조를 지니고 있다. 또한 각막과 수정체 사이의 전방에는 전방관련면역편위 (anterior chamber associated immune deviation)라고 하는 면역관용이 유지되고 있다[1]. 이와 같은 구조적 특징으로 류마티스질환에서 나타나는 자가면역이 안구에도 영향을 미치는 경우가 많은데 주로 건성안, 각막염, 공막염 및 상공막염, 포도막염, 망막혈관염, 시신경병증의 형태로 나타나게 된다.
건성안은 류마티스질환에서 가장 흔하게 나타나는 안구증상의 하나이며, 건성안은 일차쇼그렌증후군을 비롯하여 다양한 류마티스질환과 연관되어 나타난다[23]. 건성안은 크게 증발형(evaporative type)과 눈물분비결핍형(aqueous deficiency type)으로 분류하는데 쇼그렌증후군에서는 자가면역에 의한 눈물샘의 염증으로 인한 손상으로 눈물분비가 저하되어 눈물분비결핍형의 건성안이 나타나게 되는데(Figure 1), 눈물샘의 손상뿐만 아니라 안구표면의 염증으로 인한 각결막 상피세포 손상 및 술잔세포의 소실로 눈물막이 불안정해지기도 한다[45].
건성안은 환자가 만성적인 안구건조증상이나 시력의 기복과 같은 시각증상을 보이고 눈물막이 불안정한 소견을 보이는 경우 진단하게 되는데, 류마티스질환과 연관된 건성안에서는 특징적으로 각결막의 미만성미란이 관찰되거나 눈물분비가 감소되어 나타나는 경우가 많다. 안구건조증상의 정량적인 평가를 위해서 Ocular Surface Disease Index [6], Standard Patient Evaluation of Eye Dryness와 같은 설문이 이용되며[7], 눈물분비량은 쉬르머검사(Schirmer test)를 통하여 검사하며 5분 동안 검사용지가 5 mm 이내로 젖을 때 비정상으로 판독한다. 또한 눈물막의 안정성은 안구표면을 플루레신염색하여 세극등으로 관찰하였을 때 눈물막의 파괴가 10초 미만에 관찰되는 경우 비정상으로 본다[89]. 한편 쇼그렌증후군에서는 각막지각이 감소되는 것으로 보고되는데[10], 이로 인해 심한 안구소견에 비해 주관적인 증상은 비교적 가벼운 경우도 많기 때문에 환자가 안구건조증상을 호소하지 않더라도 건성안으로 인한 각결막 손상이 있는지 반드시 확인하는 것이 필요하다. 최근 건성안의 발병기전에 안구표면의 염증이 주요한 역할을 하는 것으로 밝혀지고 있는데, 건성안 환자의 눈물에서 TNF, IL-6, IL-1b, IFN-r과 같은 염증성 사이토카인이 증가되며[1112], 건조자극에 의해 T세포가 Th17 세포로 분화하여 IL-17의 분비가 증가하는 것으로 보고되고 있다[1314]. 건성안의 치료는 질환의 중증도에 따라 단계적으로 진행하게 되는데 안구표면의 손상이 적고 눈물막의 불안정성만 관찰되는 경우에는 인공눈물안약을 점안하지만, 류마티스질환과 연관되어 나타나는 건성안에서는 대부분 중등도 이상의 각결막의 손상과 함께 눈물분비의 감소가 동반되어 나타나는 경우가 많으므로 스테로이드 점안제나 사이클로스포린 점안제와 같은 항염증치료를 병행하게 된다[15]. 안구표면손상의 치유를 위해 자가혈청안약이나 치료용 콘택트렌즈를 사용하기도 하며 쇼그렌증후군과 같이 눈물분비가 심하게 감소된 환자에서는 안구표면에서 비강으로 눈물이 배출되는 눈물소관을 폴리머 마개를 이용하여 임시 혹은 영구적으로 폐쇄하여 효과를 보기도 한다.
공막주변의 혈관구조는 표층에 비교적 직선으로 경선방향으로 위치하는 모세혈관얼기와 공막과 가깝게 유착되어 서로 자유롭게 연결되는 형태를 보이는 심부 상공막 모세혈관얼기로 이루어져있는데, 표층 모세혈관얼기의 염증을 상공막염이라고 하며, 심부 모세혈관얼기와 공막의 염증을 공막염이라고 한다.
상공막염은 비교적 갑자기 나타나는 안구충혈, 안구불편감 혹은 통증을 증상으로 하며 시력이 이환되는 경우는 드물다. 대부분 1-2주 이내에 저절로 호전되나 1-3개월 간격으로 수년 동안 재발을 반복하는 경우도 있다. 최근에는 기존에 알려진 것보다는 류마티스질환과의 연관성이 높은 것으로 생각되고 있으며, 치료에는 인공눈물 혹은 비스테로이드항염제 안약이 주로 사용되며 경구약제의 투여가 필요한 경우는 드물다.
이에 비해 공막염은 충혈과 안구통증이 심하게 나타나게 되는데, 형태에 따라 미만성, 결절성, 괴사성으로 분류하며 괴사성은 염증을 동반한 경우와 염증을 동반하지 않고 공막연화가 진행되는 경우로 분류한다. 또한 안구의 후방에 있는 공막을 침범한 경우 후부공막염으로 따로 분류하여 치료하기도 한다.
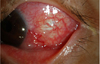
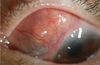
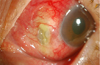
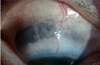
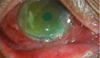
미만성공막염은 가장 흔하고 비교적 가벼운 경과를 보이는 질환으로 25-45%에서 류마티스질환과의 연관성을 보이는 것으로 알려지고 있으며(Figure 2), 결절성공막염은 각막윤부에 연하여 심부충혈을 동반한 공막결절이 나타나며 류마티스질환과의 연관성이 44-50% 정도로 더 높게 나타난다 (Figure 3). 미만성공막염이나 결절성공막염은 괴사성공막염에 비해 진행이 빠르지 않고 영구적인 시력손실의 위험은 그다지 크지 않다. 반면 염증을 동반한 괴사성공막염은 가장 심한 형태의 공막염으로 공막의 무혈관괴사를 동반하고 안구천공이나 실명을 초래할 수도 있는 질환으로 기존 문헌에서는 류마티스질환과의 연관성이 50-81%로 높게 보고되고 있으나[16], 국내 증례의 경우 류마티스질환과의 연관성보다는 이전의 안구수술, 특히 익상편수술과 연관되어 발생하는 경우가 더 많으며[17], 녹농균이나 진균에 의한 감염성공막염이 합병되는 경우도 흔한 것으로 최근 보고를 통해 알려졌다[18] (Figure 4). 염증을 동반하지 않은 괴사성공막염은 천공공막연화증(scleromalacia perforans)이라고도 하며 류마티스관절염에 장기간 이환된 환자에서 광범위하고 심한 공막연화로 인해 공막부위가 푸르게 혹은 검게 관찰되며 연화된 부위의 돌출로 인해 난시가 심하게 발생하여 시력이 저하되기도 한다(Figure 5).
공막염의 치료는 1차적으로 경구 비스테로이드항염제를 사용하는데 인도메타신 25 mg을 1일 4회 투여하는 것으로 시작하여 공막염이 호전되고 최소 1달이 경과된 후 약제를 중단해야 재발을 예방할 수 있다. 비스테로이드항염제에 반응이 없는 미만성 혹은 결절성공막염이나 괴사성공막염의 경우 경구 스테로이드를 체중(kg)당 1 mg을 투여하고 마찬가지로 공막염이 관해되고 1달이 경과된 후부터 용량을 줄여나가기 시작한다. 경구 스테로이드에 반응이 없는 경우나 스테로이드와 연관된 건강을 위협하는 부작용이 있는 경우 cyclophosphamide, cyclosporine A, methotrexate, azathioprine, mycophenolate mofetil 등의 면역억제제를 투여하는데, 심한 괴사성공막염, 면역억제제 치료가 필요한 자가면역질환이 동반된 공막염에서는 면역억제제를 1차약으로 투여한다. 최근에는 항종양괴사인자[19], 항CD-20단일클론항체[20], IL-2 혹은 IL-1 수용체 길항제 등을 투여하여 공막염의 치료에 효과가 있었다는 보고들이 발표되고 있다. 공막천공이 임박하였거나 천공이 발생한 경우 안구보존을 위해 공막이식, 양막이식, 결막판이식과 같은 수술이 필요하다[21].
공막염은 류마티스질환 중 류마티스관절염과의 연관성이 가장 높게 나타나며, 베게너육아종증이나 재발성다발연골염 등이 연관성이 높은 질환으로 알려져 있다. 공막염이 연관되어 발생한 류마티스관절염 환자는 면역억제제를 이용한 적극적인 치료를 시행하지 않는 경우 3년 사망률이 36-45%에 달하는 것으로 알려져 있다[22]. 류마티스질환과 연관되어 발생하는 공막염은 공막염 이환 시 기왕에 류마티스질환을 진단받았던 경우가 흔하지만, 보고에 따라 15-59%의 환자에서는 공막염이 류마티스질환의 첫 소견으로 나타나는 경우도 있으므로 류마티스질환의 병력이 없는 환자에서는 반드시 감별진단을 위한 검사를 시행해야 한다. 베게너육아종증과 동반된 경우 심한 공막염으로 영구적인 시력손실을 일으킬 위험이 높은 반면 전신홍반루프스나 강직척추염과 동반된 공막염은 비교적 가벼운 경과를 거치고 저절로 호전되는 경우도 있다.
각막주변부는 윤부혈관연속활과 인접해있으면서 이에 의한 혈액공급에 대사를 의존하고 있으며 혈관염이나 자가면역반응에서 흔히 안구변화를 보이는 구조이다. 또한 인근 상공막이나 공막의 염증이 각막주변부로 이환하기도 한다. 각막주변에 둘레를 따라 발생하는 상피결손과 기질궤양을 동반하는 주변궤양각막염은 그 크기가 각막주변둘레의 2시간 범위 이상일 때 대궤양(macroulcerative) 병변이라고 한다. 각막주변둘레의 2시간 범위 이내인 소궤양(microulcerative) 병변이 주로 포도상구균 항원에 대한 면역반응으로 발생하여 비교적 가벼운 경과를 거치는 반면에 대궤양 병변은 류마티스질환과의 연관성이 높고 각막천공으로 까지 진행하는 경우도 있으므로 유의해야 한다[23] (Figure 6). 주변궤양각막염은 주위의 공막염과 동반하여 나타나는 경우도 있으나 단독으로 발생하는 예도 흔하며 통증, 충혈, 시력저하와 함께 각막주변부의 궤양과 함께 기질융해가 일어나 각막이 얇아지기도 한다. 대개 각막궤양은 깊이가 깊고 윤부를 따라 고랑형태로 진행하지만 각막중심부를 향해 진행하기도 한다.
주변궤양각막염은 류마티스관절염과의 연관성이 가장 높게 나타나며 베게너육아종증이나 결절다발동맥염과 연관되어 나타나기도 한다. 각막주변의 국소적인 혈관염에 의해 면역복합체가 침착하게 되고 염증세포들이 동원되어 각막궤양을 일으키는 것으로 알려져 있는데, 치료를 위해서는 연관된 류마티스질환을 조절하는 것이 중요하며 스테로이드 경구투여나 사이클로스포린과 같은 면역억제제의 국소투여가 치료의 근간이 되는데, 국소 스테로이드 투여는 각막융해를 촉진하여 각막천공을 일으킬 수 있으므로 주의해야 한다. 약물치료에 반응하지 않고 진행하는 주변궤양각막염은 결막절제술이나 얇아진 주변각막의 보강을 위한 층판각공막편이식술, 양막이식술 혹은 조직접착제를 이용한 치료가 필요할 수 있다.
포도막염은 공막과 망막 사이의 포도막에 발생하는 염증을 가리키는 용어이지만, 일반적으로 안내에 발생하는 염증을 통칭하여 포도막염이라고 하기도 한다. 포도막염은 모양체 앞쪽의 홍채와 전방에 발생하는 전부포도막염(anterior uveitis), 모양체 뒤쪽에서부터 망막 주변부까지에 발생하는 주변포도막염(intermediate uveitis), 유리체기저부의 뒤쪽을 침범하는 후포도막염(posterior uveitis)과 포도막 전체에 발생하는 범포도막염(panuveitis)으로 분류할 수 있다. 전부포도막염은 모양체충혈, 통증, 시력저하 및 광과민성 등의 증상이 나타나며 만성포도막염에서는 염증의 정도에 비해 증상이 가볍게 나타날 수 있다. 세극등현미경으로 관찰하면 각막내피세포에 각막후면침착물(keratic precipitate)이 나타나며 전방에 염증세포와 방수흐림이 나타난다. 그 외에 홍채결절이나 홍채후유착이 보일 수 있다. 주변포도막염은 비문증이나 시력저하를 증상으로 하며 망막주변부의 세포침윤이 관찰되고 전방 내의 염증세포는 비교적 심하지 않게 보인다. 후포도막염은 이환되는 위치에 따라 비문증 혹은 중심시력손실이 나타나며, 유리체강내의 염증세포, 흐림, 유리체박리, 맥락막염, 망막염, 혹은 혈관염의 소견이 관찰될 수 있다.
강직척추염, 라이터증후군, 건선관절염, 연소기만성관절염, 재발성다발연골염, 베세트병 등에서 포도막염이 동반되어 나타날 수 있는데 HLA-B27은 강직척추염 및 포도막염과 강한 연관성을 가지는 것으로 알려져 있다[24]. 연소기만성관절염은 4개 이하의 관절에 이환되는 소수관절발현(pauciarticular onset) 연소기만성관절염의 경우 78-91%에서 포도막염이 발생하며 5개 이상의 관절을 침범하는 다관절발현(polyarticular onset) 연소기만성관절염은 비교적 적은 7-14%의 포도막염 이환율을 보인고, 전신발현(systemic onset) 연소기만성관절염은 1-6% 정도에서 포도막염이 보고되고 있다.
포도막염의 치료는 시력을 위협하는 합병증을 예방하고, 환자의 증상을 완화하며, 기저질환을 치료하는 방향으로 이루어지는데, 환자의 증상완화를 위해 조절마비제를 투여하고, 스테로이드의 점안이나 안구 주변 혹은 안구 내 주사, 전신면역억제제가 사용될 수 있다.
류마티스질환의 치료에 사용되는 약제들은 때로 안구합병증을 일으키기도 한다. 비스테로이드항염제는 회오리각막병증(vortex keratopathy), 독성시신경병증 등이 보고되었으며, 스테로이드는 장기간 투여 시 수정체의 후낭하혼탁과 같은 백내장의 발생 위험을 증가시키는 것으로 알려져 있다. 클로로퀸 제재는 독성 황반병증 혹은 망막병증[25], 회오리각막염, 독성시신경병증을 일으킬 수 있으며[26], methotrexate의 사용과 연관된 점상각막병증이 보고되고 있다.
이와 같이 류마티스질환과 연관되어 각결막, 공막, 포도막에 다양한 염증성질환이 나타날 수 있으며, 이러한 안구소견은 류마티스질환의 진단의 단서가 되고, 때로는 류마티스질환의 첫 발현으로 나타나기도 하며 환자의 예후를 시사하는 경우도 있다. 위에 서술된 여러 가지 안질환은 자세한 병력청취를 통해 기왕력을 파악하여 류마티스질환과의 연관성을 감별하는 것이 중요하며, 안구소견뿐만 아니라 기저질환을 함께 치료하기 위한 협진체계를 구축하는 것이 필요할 것이다.
본 논문은 류마티스 질환에서 나타날 수 있는 건성안, 상공막염 및 공막염, 주변궤양각막염, 포도막염 등의 전안부 질환의 원인, 진단, 그리고 치료에 대해 체계적으로 정리한 논문이다. 특히 쇼그렌증후군을 포함한 대부분의 류마티스 질환에서 흔히 발생하는 건성안 등의 염증성 및 면역성 안구소견은 각결막의 손상과 시력장애를 유발하므로, 치료를 위해 항염증제나 면역억제제의 투여가 필요함을 기술하였다. 이러한 안구소견을 통해 류마티스 질환을 이차적으로 진단하거나 중등도와 예후를 판단할 수 있으므로, 향후 류마티스내과 의사와 안과 의사의 협진체계 구축이 중요함을 기술한 의미있는 논문이라고 판단된다
[정리: 편집위원회]
Figures and Tables
References
1. Treacy O, Fahy G, Ritter T, O'Flynn L. Corneal immunosuppressive mechanisms, anterior chamber-associated immune deviation (ACAID) and their role in allograft rejection. Methods Mol Biol. 2016; 1371:205–214.

2. Hamideh F, Prete PE. Ophthalmologic manifestations of rheumatic diseases. Semin Arthritis Rheum. 2001; 30:217–241.

3. Widdifield J, Paterson JM, Bernatsky S, Tu K, Tomlinson G, Kuriya B, Thorne JC, Bombardier C. The epidemiology of rheumatoid arthritis in Ontario, Canada. Arthritis Rheumatol. 2014; 66:786–793.

4. The definition and classification of dry eye disease: report of the Definition and Classification Subcommittee of the International Dry Eye Workshop (2007). Ocul Surf. 2007; 5:75–92.
5. Shiboski SC, Shiboski CH, Criswell L, Baer A, Challacombe S, Lanfranchi H, Schiodt M, Umehara H, Vivino F, Zhao Y, Dong Y, Greenspan D, Heidenreich AM, Helin P, Kirkham B, Kitagawa K, Larkin G, Li M, Lietman T, Lindegaard J, McNamara N, Sack K, Shirlaw P, Sugai S, Vollenweider C, Whitcher J, Wu A, Zhang S, Zhang W, Greenspan J, Daniels T. Sjogren's International Collaborative Clinical Alliance (SICCA) Research Groups. American College of Rheumatology classification criteria for Sjogren's syndrome: a data-driven, expert consensus approach in the Sjogren's International Collaborative Clinical Alliance cohort. Arthritis Care Res (Hoboken). 2012; 64:475–487.

6. Schiffman RM, Christianson MD, Jacobsen G, Hirsch JD, Reis BL. Reliability and validity of the Ocular Surface Disease Index. Arch Ophthalmol. 2000; 118:615–621.

7. Ngo W, Situ P, Keir N, Korb D, Blackie C, Simpson T. Psychometric properties and validation of the Standard Patient Evaluation of Eye Dryness questionnaire. Cornea. 2013; 32:1204–1210.

8. Han SB, Hyon JY, Woo SJ, Lee JJ, Kim TH, Kim KW. Prevalence of dry eye disease in an elderly Korean population. Arch Ophthalmol. 2011; 129:633–638.

9. Hyon JY, Kim HM, Lee D, Chung ES, Song JS, Choi CY, Lee J. Korean Corneal Disease Study Group. Korean guidelines for the diagnosis and management of dry eye: development and validation of clinical efficacy. Korean J Ophthalmol. 2014; 28:197–206.

10. Han SB, Hyon JY, Wee WR, Lee JH, Lee YJ, Yun PY. Reduced corneal sensitivity in patients with primary Sjogren's syndrome. Acta Ophthalmol. 2010; 88:e277–e278.
11. Hagan S, Tomlinson A. Tear fluid biomarker profiling: a review of multiplex bead analysis. Ocul Surf. 2013; 11:219–235.

12. Tong L, Thumboo J, Tan YK, Wong TY, Albani S. The eye: a window of opportunity in rheumatoid arthritis? Nat Rev Rheumatol. 2014; 10:552–560.

13. Zheng X, de Paiva CS, Li DQ, Farley WJ, Pflugfelder SC. Desiccating stress promotion of Th17 differentiation by ocular surface tissues through a dendritic cell-mediated pathway. Invest Ophthalmol Vis Sci. 2010; 51:3083–3091.

14. Tan X, Sun S, Liu Y, Zhu T, Wang K, Ren T, Wu Z, Xu H, Zhu L. Analysis of Th17-associated cytokines in tears of patients with dry eye syndrome. Eye (Lond). 2014; 28:608–613.

15. Hyon JY, Lee YJ, Yun PY. Management of ocular surface inflammation in Sjogren syndrome. Cornea. 2007; 26:9 Suppl 1. S13–S15.
16. Markovitz E, Perry ZH, Tsumi E, Abu-Shakra M. Ocular involvement and its' manifestations in rheumatoid arthritis patients. Harefuah. 2011; 150:713–718. 751
17. Jeon HS, Hyon JY, Kim MK, Chung TY, Yoon KC, Kim JY, Na KS, Kim HJ, Kim TI, Lee JS, Lee HK, Song JS. Efficacy and safety of immunosuppressive agents in the treatment of necrotising scleritis: a retrospective, multicentre study in Korea. Br J Ophthalmol. 2015; [Epub]http://dx.doi.org/10.1136/bjophthalmol-2015-307462.

18. Ahn SJ, Oh JY, Kim MK, Lee JH, Wee WR. Clinical features, predisposing factors, and treatment outcomes of scleritis in the Korean population. Korean J Ophthalmol. 2010; 24:331–335.

19. Murphy CC, Ayliffe WH, Booth A, Makanjuola D, Andrews PA, Jayne D. Tumor necrosis factor alpha blockade with infliximab for refractory uveitis and scleritis. Ophthalmology. 2004; 111:352–356.

20. Suhler EB, Lim LL, Beardsley RM, Giles TR, Pasadhika S, Lee ST, de Saint Sardos A, Butler NJ, Smith JR, Rosenbaum JT. Rituximab therapy for refractory scleritis: results of a phase I/II dose-ranging, randomized, clinical trial. Ophthalmology. 2014; 121:1885–1891.
21. Yokogawa H, Kobayashi A, Yamazaki N, Masaki T, Sugiyama K. Surgical therapies for corneal perforations: 10 years of cases in a tertiary referral hospital. Clin Ophthalmol. 2014; 8:2165–2170.
22. Foster CS, Forstot SL, Wilson LA. Mortality rate in rheumatoid arthritis patients developing necrotizing scleritis or peripheral ulcerative keratitis: effects of systemic immunosuppression. Ophthalmology. 1984; 91:1253–1263.

23. Artifoni M, Rothschild PR, Brezin A, Guillevin L, Puechal X. Ocular inflammatory diseases associated with rheumatoid arthritis. Nat Rev Rheumatol. 2014; 10:108–116.

24. Llorenc V, Mesquida M, Sainz de la Maza M, Keller J, Molins B, Espinosa G, Hernandez MV, Gonzalez-Martin J, Adan A. Epidemiology of uveitis in a Western urban multiethnic population: the challenge of globalization. Acta Ophthalmol. 2015; 93:561–567.





 PDF
PDF ePub
ePub Citation
Citation Print
Print




 XML Download
XML Download