Abstract
Current pharmacological therapies for allergic diseases can improve clinical symptoms but cannot change their long-term clinical course. There is an unmet need for a curative treatment for allergic diseases. Allergen immunotherapy (AIT) is the practice of administering increasing doses of clinically relevant allergens to an allergic subject to reduce the clinical symptoms associated with subsequent exposure to the allergen. AIT is clinically effective for allergic asthma, allergic rhinitis, venom-induced anaphylaxis, and atopic dermatitis. AIT can change the natural course of allergic diseases and induce allergen-specific immune tolerance. In current clinical practice, AIT is delivered either subcutaneously or sublingually. Both subcutaneous and sublingual AIT have long-term therapeutic efficacy after of 3-5 years of treatment. The development of safer and more effective AIT strategies is needed. Conclusion: AIT is a disease-modifying therapy for allergic diseases. Future development of AIT should be directed toward achieving long-term clinical remission in patients with allergic diseases by the safe and effective induction of immune tolerance.
외부 물질에 대한 과민한 반응(알레르기)과 연관되어 발생한다고 알려진 알레르기질환은 기관지천식, 알레르기비염, 알레르기결막염, 아토피피부염, 음식물 알레르기 등을 포함하며, 현재 전 세계적으로 가장 흔한 만성질환의 하나로 알려져 있다[1]. 최근 약 50년 동안 전 세계적으로 알레르기질환의 유병률이 급격하게 증가하고 있으며, 환경적 요인이 이러한 변화의 원인인 것으로 판단된다[2].
전통적으로 알레르기질환의 치료에는 알레르기 유발물질(알레르겐)에 대한 회피요법, 약물요법, 그리고 알레르겐 면역요법(이하 면역요법)의 3 가지 치료가 주된 치료법으로 알려져 있다[34]. 실제적으로 알레르기질환의 치료를 위해서 현재 임상에서 가장 흔하게 적용되고 있는 약물요법의 경우 알레르기 반응에 관여하는 화학 매개체(히스타민, 류코트리엔 등)들에 대한 억제약물(항히스타민제, 항류코트리엔제 등)혹은 알레르기 반응으로 인한 조직의 염증을 억제하는 항염증약물(스테로이드제, 면역억제제 등)들이 주로 사용되고 있다[5]. 하지만 이러한 약물요법은 지속적으로 약물을 투여할 경우에만 임상증상을 호전된 상태로 유지시킬 수 있다는 단점이 있다. 따라서 약물치료 없이 알레르기질환을 근본적으로 호전시킬 수 있는 치료, 즉 완치요법을 희망하는 환자들의 요구가 불충족되어, 알레르기질환에 대한 대체요법이나 민간요법들이 세계적으로 성행하고 있는 상황이다[67].
일반적으로 면역요법은 면역반응을 조절(항진시키거나 혹은 억제)함으로써 질병을 호전시키는 치료법으로 정의된다[8]. 역사적으로 면역요법은 알레르기질환뿐만 아니라 악성질환, 자가면역질환 등에서도 치료목적으로 시도되어 왔으며, 최근 들어서 악성질환에서 단클론 항체를 이용한 비특이적인 면역항진 치료법의 현저한 임상효과(생존기간의 유의한 연장)가 보고됨에 따라서 악성질환의 치료에서 면역요법의 실제 임상적용의 새로운 전기가 마련되고 있는 상황이다[9].
알레르기질환의 치료에서의 면역요법은 "알레르기질환을 앓고 있는 환자에게 알레르기 반응을 유발하는 원인물질을 소량으로부터 증량하면서 반복적으로 투여하여 그 물질에 노출되었을 경우에 발생하는 알레르기 증상을 감소시켜서 알레르기질환을 호전시키는 치료법"으로 정의된다[10]. 1998년 World Health Organization position paper와 더불어 최근 발간된 국내외 지침서들에서, 면역요법은 알레르기질환의 임상증상의 호전과 더불어 질병의 자연경과를 바꿀 수 있는 치료법으로 기술되고 있다[10111213]. 한편 국내임상의사들 사이에서 알레르기질환에서 면역요법은 "알레르겐-특이 면역요법" 혹은 "알레르기 면역치료" 등과 같이 다른 이름으로 불려지기도 한다. 하지만 최근 들어 국내외적으로 알레르기질환의 치료를 위한 면역요법은 “알레르겐 면역요법(allergen immunotherapy)"으로 통일되어 명명되고 있는 상황이다. 역사적으로 면역요법은 1911년 영국의 의사 Noon[14]에 의해서 꽃가루 알레르기를 가진 계절성 알레르기비염과 알레르기성 결막염 환자들에게 수용성 꽃가루 추출물을 소량에서부터 조금씩 증량하여 피하로 주사한 경우 꽃가루에 대한 알레르기 반응이 감소함을 보고한 이후부터 시작되었다. 그 이후 약 104년이 지난 현재 면역요법은 알레르기성 천식, 알레르기비염, 벌독 알레르기와 아토피피부염에서 임상적으로 효과적인 치료법으로 인정받게 되었다[15161718192021]. 본 종설에서는 알레르기질환의 근본적인 호전과 자연경과를 호전시킬 수 있는 치료법으로 알려진 면역요법에 대하여 최근에 발표된 국내외 지침서들의 내용을 중심으로 간략하게 살펴보고자 한다[10111213].
최근까지 시행된 전향적, 이중맹검, 무작위 연구들을 종합분석한 결과, 면역요법은 알레르기성 천식, 알레르기비염, 곤충독 아나필락시스에 있어서 명확한 임상적 근거(근거등급 A)를 가진 것으로 입증된 치료방법이다. 또한 최근 발표된 종합분석 결과 흡입 항원에 감작된 아토피피부염 환자에서 면역요법의 치료효과가 중등도의 임상적 근거(근거등급 B)가 있음이 보고된 바 있다.
알레르기질환에서 면역요법은 알레르기 검사(알레르기 피부시험 또는 혈청 알레르겐-특이 IgE 항체 검사) 양성 결과에 근거하여 알레르겐에 대한 감작이 명확하게 확인된 환자들에서 시행되어야 한다. 또한 감작된 원인 알레르겐에 노출 시 알레르기 증상이 발생되며, 원인 알레르겐에 대한 충분한 회피가 어려운 환자들이 면역요법의 대상이 된다. 표준적인 약물치료만으로 알레르기질환의 증상이 잘 조절되지 않거나, 약물치료에 부작용이 있는 경우 혹은 환자가 장기적인 약물요법을 거부하는 경우에도 면역요법이 시도될 수 있다(Table 1).
한편 심한 면역질환(자가면역질환 등)을 앓고 있거나 악성종양을 앓고 있는 환자, 면역요법 도중 심한 알레르기 반응(아나필락시스)이 발생될 경우 응급처치 목적으로 사용되는 epinephrine 주사의 사용이 불가능한 환자(심한 고혈압이나 관상동맥 질환을 앓고 있는 경우, 베타 차단제 혹은 안지오텐신 전환효소 억제제를 장기간 복용하고 있는 환자)에서는 면역요법을 시행하지 않는다. 또한 5세 미만의 소아나 중증환자, 임산부의 경우에는 면역요법을 시작하는 것이 금기이다. 하지만 이미 면역요법을 시행 중인 임산부에서는 임신기간 동안 면역요법을 지속할 수 있다(Table 2).
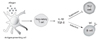
면역요법이 알레르기질환을 호전시키는 기전은 아직까지 완전하게 밝혀져 있지 않다. 과거에는 면역요법 후 혈청 알레르겐-특이 IgE 항체는 감소하는 반면, 알레르겐-특이 IgG 혹은 IgG4 항체의 증가가 관찰되어 알레르겐에 대한 IgG 항체(특히 IgG4 항체)가 알레르겐과 IgE 항체간의 반응을 차단하는 차단 항체로 작용될 가능성에 대해서 강조되어왔다[22]. 그러나 최근 연구들에서 면역요법의 치료효과 기전은 피하 혹은 설하 경로로 투여된 고농도의 알레르겐이 항원제시 세포(antigen-presenting cell)인 수지상세포(dendritic cell)를 통해서 알레르겐-특이 조절 T세포(regulatory T cell를 활성화시켜 IL-10과 TGF-β 분비를 유도하고, 분비된 IL-10과 TGF-β에 의해서 알레르겐 특이 Th2 세포의 활성화가 억제되고, 알레르겐 특이 B 세포에서 차단항체인 IgG 항체 생산이 증가되어 알레르기 반응을 억제하는 것으로 추측되고 있다[23] (Figure 1, Table 3).
면역요법을 시행 받은 환자들에서 위약 치료 환자들에 비해서 임상증상이 호전되고, 약물 요구량이 감소되며, 알레르겐에 대한 특이적 알레르기 반응이 감소되고, 코 또는 기관지 등의 표적기관의 비특이적인 과민반응 또한 감소된다. 또한 면역요법을 받은 환자들에서 치료 받은 알레르겐에 대한 알레르기 반응의 정도(피부반응, 혈청 특이 IgE 항체)가 감소된다. 면역요법을 충분한 기간(3-5년) 동안 시행받은 환자들 중 일부는 면역요법을 중단한 이후에도 약물요법을 실시하지 않아도 장기적으로 알레르기 증상이 발생되지 않는 장기간의 임상적 관해상태에 도달할 수 있다. 면역요법은 새로운 알레르겐에 대한 감작을 예방하고, 비염을 앓고 있는 환자들에서 천식의 발병을 예방한다(Table 3). 면역요법은 치료시약에 포함된 알레르겐의 종류가 적을수록, 그리고 치료 시작 연령이 낮을수록 치료효과가 좋다고 알려져 있다. 하지만 만성 기관지염, 폐기종 혹은 기도의 고정폐쇄, 등의 구조적인 합병증을 동반한 중증 천식에서는 치료효과가 적다.
최근까지 이중맹검 대조연구(double blind placebocontrolled study)를 통하여 면역요법의 임상효과가 명확하게 입증된 알레르겐 종류는 꽃가루(잔디, 자작나무, Parietaria, 돼지풀)와 집먼지진드기, 그리고 곰팡이의 경우 Alternaria와 Cladosporium, 그리고 개와 고양이가 있다. 면역요법의 임상효과는 치료시약에 포함된 알레르겐에 한정되어 나타난다. 따라서 면역요법 시에 적절한 임상효과를 얻기 위해서는 면역요법 치료시약에 포함될 알레르겐의 선정이 매우 중요하다. 면역요법 시에 치료시약에 포함될 알레르겐의 종류를 선정할 때에는 알레르기 피부단자 시험 또는 혈청 알레르겐 특이 IgE 항체가 양성을 보이고, 의심되는 알레르겐에 대해서 잦은 빈도로 실생활에서 노출되며, 알레르겐에 대한 노출과 임상증상간의 연관성이 병력이나 유발 검사결과로 확인된 알레르겐으로 한정하는 것이 바람직하다. 우리나라의 경우 집먼지진드기가 알레르기질환과 연관된 가장 흔한 중요 알레르겐으로 알려져 있으며, 실제적으로 면역요법 치료시약으로 임상에서 가장 많이 사용되고 있다.
면역요법은 알레르겐의 투여 경로에 따라 피하, 설하, 비강/기관지 내 흡입과 경구로 투여하는 방법들이 있다. 전통적으로 알레르겐을 피하주사로 투여하는 피하면역요법이 가장 널리 사용되어 왔으나 최근에는 설하면역요법의 임상효과가 명확하게 입증되어 유럽을 중심으로 점차 사용이 증가되고 있다. 피하면역요법과 비교할 때 설하면역요법의 장점은 심한 전신 부작용의 발생이 매우 드물다는 안전성에 있다. 반면에 현재까지 발표된 소수의 비교 연구들에 따르면 피하면역요법이 설하면역요법보다 더 높은 치료효과를 보인다는 보고가 이루어 지고 있다.
알레르겐을 피하주사로 투여하는 피하면역요법은 현재까지 면역요법의 표준적인 시행방법으로 여겨지고 있다. 피하면역요법의 진행방법은 주사 투여의 횟수나 치료 간격을 기준으로 용량 증량 기간인 초기 치료기간과 유지 치료기간으로 나누어진다.
초기 치료는 용량을 증량하는 방법에 따라 전통적 방법, 집중면역요법, 급속면역요법, 초급속면역요법으로 나뉜다. 일반적으로 면역요법의 초기 치료는 낮은 농도의 항원을 이용하여 매회 약 2배의 농도로 증가시키며 1주 간격으로 1일 1회씩 주사하는 전통적 초기 치료방법이 가장 흔하게 사용되고 있으며, 초기 치료기간이 약 3-4개월이 소요된다. 그러나 초기 치료기간을 단축시키기 원하는 환자들에게는 1회 방문 시 30분 간격으로 2-3회 주사하여 1-2개월 안에 최대 유지용량에 도달시키는 집중면역요법(cluster immunotherapy) 또한 적용이 가능하다. 환자의 사정에 따라 초기 치료기간 동안의 잦은 병원 방문이 매우 힘든 환자(직장, 학생), 거주지와 병원간의 거리가 먼 경우, 빠른 면역요법 임상효과의 발현을 희망하는 경우에는 초기치료를 약 3-5일 안에 마치는 급속면역요법(rush immunotherapy) 혹은 하루 안에 초기치료를 마치는 초급속면역요법(ultrarush immunotherapy)이 시도될 수 있다. 단, 급속면역요법 혹은 초급속면역요법을 시행 받은 환자들의 경우 전통적인 면역요법 초기치료 방법에 비해서 전신적인 알레르기 반응에 의한 부작용 발생의 위험이 높아지므로, 전신 부작용의 발생여부를 주의 깊게 관찰하고 부작용에 대해서 적절히 대처할 수 있는 환경에서 실시되어야 한다.
면역요법의 유지 치료기간은 초기치료가 끝난 후 최대유지용량의 알레르겐 추출물을 1개월 간격으로 3-5년 간 주사가 진행된다. 유지 치료기간 동안 주사하는 알레르겐 용량이 높을수록 치료의 효과가 높다. 하지만 1회 주사 시 투여되는 알레르겐의 용량이 너무 높을 경우 전신적 부작용의 발생 가능성 또한 높아지기 때문에 환자 개개인마다 부작용이 없이 투여가 가능한 충분한 알레르겐 용량을 주사하는 것이 필요하다.
피하주사 면역요법의 부작용으로는 주사 맞은 부위에 국한되어 발생되는 국소 부작용과 전신적 부작용이 있다. 따라서 환자에게 면역요법 치료 시작 전 발생 가능한 부작용과 대처방법에 대하여 미리 설명하고 교육하는 것이 중요하다. 피하주사 면역요법 시행 후 발생되는 주된 국소 부작용은 주로 주사 직후 혹은 주사 후 수 시간이 지난 이후 주사부위가 가려우면서 붓는 경우로 대부분 자연적으로 소실된다. 심한 국소부종이 발생한 경우와 주사 후 30분 이내에 주사 부위의 경결의 직경이 지나치게 큰 경우는 전신적 부작용의 발생 위험성이 있으므로 면밀하게 전신 부작용 발생 여부를 관찰하며, 다음 면역요법 시 주사용량의 감량을 고려해봐야 한다. 전신 부작용으로는 전신 두드러기, 천식 증상의 발생, 혹은 드물지만 기도부종으로 인한 심한 호흡곤란이나 혈압강하 및 의식 저하 등을 동반한 생명이 위급할 수 있는 급성 전신성 알레르기반응인 아나필락시스가 발생할 가능성이 있다. 이러한 심한 전신 부작용은 대부분 주사 후 30분 이내에 발생되므로, 피하주사 면역요법 후 환자가 병원에서 최소한 30분 이상을 대기한 후 부작용 발생여부를 확인 받고, 귀가하도록 하여야 한다. 전신 부작용이 발생할 경우 증상에 따라 항히스타민제 및 전신 스테로이드제 투여, 기관지 확장제 흡입, epinephrine 근육주사 등을 시행한다. 지난 번 접종 시 상기한 부작용이 발생되거나, 천식 중상의 악화, 발열성 질환이 발생된 경우, 예정된 주사 간격을 환자가 장기간 지연시킨 경우에는 피하면역요법 주사 용량을 줄여야 된다. 피하주사 면역요법 주사 전에 경구 항히스타민제를 미리 복용할 경우 부작용 발생빈도를 줄일 수 있다.
설하면역요법 시에 발생하는 흔한 부작용으로는 국소 자극증상(구강 내 소양증, 부종 등)이나, 위장관계 부작용(구역, 구토, 설사, 복통 등)등이 있으나, 심한 전신적 부작용이 발생한 경우는 매우 드물며 현재까지 보고된 심한 부작용은 주로 천식 증상의 악화이다.
현재까지 면역요법의 치료효과와 안전성을 높이려는 다양한 시도들이 이루어지고 있지만 아직까지 다음과 같은 몇 가지 한계점들이 존재한다. 1) 면역요법의 치료효과가 높은 환자를 미리 예측할 수 있는 임상지표 혹은 검사지표가 명확하게 확립되어 있지 않다. 2) 면역요법에 사용되고 있는 치료시약들에 포함된 알레르겐의 질과 양이 표준화되지 못하여 여러 회사들에서 생산된 치료시약들 중에서 환자들 개개인에 맞는 최적의 치료시약을 선정하는 데에 어려움이 따른다. 3) 환자 개개인마다의 치료효과와 치료의 편이성 측면에서 피하주사 면역요법과 설하면역요법 중 어떤 치료를 선택하는 것이 좋을지 판정하기 어려운 경우가 있다. 4) 면역요법의 충분한 치료효과를 위한 유지치료기간이 3-5년으로 장기간이 필요하다. 이로 인하여 면역요법을 시행 받은 환자들 중 일부에서 중간에 치료를 중단하는 경우가 발생된다. 5) 면역요법이 알레르기질환 환자들에게 치료효과를 나타내는 기전이 명확하게 밝혀지지 못하여, 현재의 면역요법을 더욱 발전시키는데 어려움이 존재한다. 6) 일부 환자들 중에서 만족스러운 치료효과를 경험하지 못하는 단점이 있다. 7) 매우 드물지만 생명이 위급한 전신적 부작용의 발생 가능성이 있으며, 8) 주사 치료로 인한 통증, 9) 초기 치료를 위해 자주 병원을 방문하기 위해서 상당한 정도의 시간과 노력이 필요한 문제점이 있다.
면역요법을 기술적으로 발전시키기 위해 유전자 재조합 알레르겐, 주요 알레르겐의 펩타이드, 면역증강제와 결합시킨 알레르겐을 이용한 면역요법 등의 새로운 시도들이 이루어지고 있다[22425]. 최근 알레르기비염 환자에서 유전자 재조합 자작나무 꽃가루 알레르겐을 이용한 면역요법이 임상적으로 효과적임이 보고되었다[26]. 또한 알레르겐을 화학물질로 처리하여 변형시키고, 다량체로 만들어 수산화 알루미늄과 결합시켜, 치료효과는 유지하면서 부작용을 낮추어 초기 치료기간을 단축시킬 수 있도록 고안된 면역요법 치료 시약이 개발되었다[25].
최근 알레르기비염 환자에서 피하면역요법을 단독으로 시행할 경우와 비교하여 항-IgE 단일클론항체(omalizumab)을 주사치료를 피하면역요법과 함께 병합하여 시행할 경우에 더 우수한 치료효과를 보임이 보고된 바 있다[25]. 또한 알레르기비염 환자들에서 꽃가루 알레르겐으로 급속면역요법 시작 전에 항-IgE 단클론항체 주사치료를 시행한 치료군이 꽃가루 알레르겐으로 급속면역치료요법만을 시행한 대조군에 비하여 부작용의 발생빈도가 더 낮음이 보고되었다[25].
미래의 면역요법은 현재의 면역요법이 가지는 단점들을 보완하여, 치료 중 발생할 수 있는 부작용의 가능성을 최소화하고, 치료 효과가 극대화되어, 현재의 약물요법과 동등한 정도의 안전성과 효능을 지닌 통상적인 치료법으로 발전될 것으로 기대된다[232425]. 면역요법의 발전을 위한 현재의 시도는 1) 알레르겐 자체를 발전시키는 방향(peptide, recombinant allergen, chemically modified allergen), 2) 면역보강제를 첨가 혹은 알레르겐과 부착하거나 다른 약물치료를 병합하는 방향, 3) 알레르겐의 투여 경로를 변화시키려는 방향(sublingual, intralymphatic, epicutaneous 경로 등), 4)알레르기질환의 고위험군 유아나 소아에게 발병 이전에 미리 실시하여 질환의 발생을 예방하기 위한 예방백신의 형태로 발전시키려는 방향으로 다양하게 이루어지고 있다[232425].
면역요법은 알레르기질환의 주요 발병기전인 알레르기 반응을 근본적으로 개선시킬 수 있는 유일한 치료법이다[11]. 면역요법은 임상증상을 호전시킬 뿐만 아니라, 약물요법의 필요성을 감소시키고, 새로운 알레르기질환의 발생을 예방하며, 치료 종료 후에도 장기적으로 임상증상의 호전을 유지시킬 수 있고, 궁극적으로 질병의 자연경과를 바꿀 수 있는 임상적으로 유용한 치료법이다[11]. 최근 들어 기초 면역학 지식이 발전함에 따라서 면역요법의 작용기전에서 조절 T 세포의 활성화를 통한 면역관용기전이 주된 역할을 함이 밝혀지고 있다[2223]. 특히 최근에 개발된 anti-IgE 또는 anti-IL-4 receptor antibody와 같은 생물학적 제제들이 천식, 알레르기성 비염, 아토피피부염에서 치료효과가 있음이 입증되어 알레르기질환에 대한 면역조절치료 방법의 새로운 발전 가능성을 제시하고 있다[272829]. 따라서 향후에는 이러한 생물학적 면역조절 치료제들과 면역요법의 병합치료가 시행될 경우, 치료에 따른 임상효과는 증가시키고 부작용을 감소시킬 수 있을 것으로 판단된다. 따라서 알레르기 환자들에게 감작된 알레르기 유발물질의 종류와 환자들의 상황에 맞추어, 기존의 약물치료, 면역요법, 생물학적 제제를 적절하게 선택하고 조합하여 치료에 적용시킬 경우 알레르기질환에 대한 최적의 환자-맞춤형 치료를 구현할 수 있을 것으로 판단된다[30]. 미래에는 면역요법이 알레르기질환 환자들에서 질환을 근본적으로 호전시켜, 질병의 자연경과를 바꿀 수 있는 좀 더 안전하고 효과적인 치료법으로 발전될 것으로 기대된다.
Figures and Tables
Acknowledgement
This work was supported by National Research Foundation of Korea (NRF) grant funded by the Korea government (MSIP) (no. 2014R1A2A1A11049386).
References
1. Asher MI, Montefort S, Bjorksten B, Lai CK, Strachan DP, Weiland SK, Williams H. ISAAC Phase Three Study Group. Worldwide time trends in the prevalence of symptoms of asthma, allergic rhinoconjunctivitis, and eczema in childhood: ISAAC phases one and three repeat multicountry cross-sectional surveys. Lancet. 2006; 368:733–743.

2. Akdis CA. Therapies for allergic inflammation: refining strategies to induce tolerance. Nat Med. 2012; 18:736–749.

3. Global Initiative for Asthma. 2012 Update: global strategy for asthma management and prevention [Internet]. [place unknown]: Global Initiative for Asthma;2012. 2015 Apr 21. Available from: http://www.ginasthma.org/documents/5/documents_variants/37.
5. Akdis CA, Akdis M, Bieber T, Bindslev-Jensen C, Boguniewicz M, Eigenmann P, Hamid Q, Kapp A, Leung DY, Lipozencic J, Luger TA, Muraro A, Novak N, Platts-Mills TA, Rosenwasser L, Scheynius A, Simons FE, Spergel J, Turjanmaa K, Wahn U, Weidinger S, Werfel T, Zuberbier T. European Academy of Allergology and Clinical Immunology/American Academy of Allergy, Asthma and Immunology. Diagnosis and treatment of atopic dermatitis in children and adults: European Academy of Allergology and Clinical Immunology/American Academy of Allergy, Asthma and Immunology/PRACTALL Consensus Report. J Allergy Clin Immunol. 2006; 118:152–169.

6. Schafer T. Epidemiology of complementary alternative medicine for asthma and allergy in Europe and Germany. Ann Allergy Asthma Immunol. 2004; 93:2 Suppl 1. S5–S10.
7. Jung JH, Lee JH, Kang IG, Cha HE, Kim ST. The present state of Korean traditional medicine and alternative medicine in nasal disease. Korean J Otorhinolaryngol-Head Neck Surg. 2010; 53:12–19.

10. Bousquet J, Lockey R, Malling HJ. Allergen immunotherapy: therapeutic vaccines for allergic diseases: a WHO position paper. J Allergy Clin Immunol. 1998; 102(4 Pt 1):558–562.

11. Burks AW, Calderon MA, Casale T, Cox L, Demoly P, Jutel M, Nelson H, Akdis CA. Update on allergy immunotherapy: American Academy of Allergy, Asthma & Immunology/European Academy of Allergy and Clinical Immunology/PRACTALL consensus report. J Allergy Clin Immunol. 2013; 131:1288–1296.

12. Cox L, Nelson H, Lockey R, Calabria C, Chacko T, Finegold I, Nelson M, Weber R, Bernstein DI, Blessing-Moore J, Khan DA, Lang DM, Nicklas RA, Oppenheimer J, Portnoy JM, Randolph C, Schuller DE, Spector SL, Tilles S, Wallace D. Allergen immunotherapy: a practice parameter third update. J Allergy Clin Immunol. 2011; 127:1 Suppl. S1–S55.
13. Hur GY, Kim TB, Kim ST, Han MY, Nahm DH, Lee YW, Sohn SW, Lee HH, Kim WK, Song TW, Kim S, Kim SH, Park JW. Allergy immunotherapy. Korean J Asthma Allergy Clin Immunol. 2010; 30:153–183.
15. Abramson MJ, Puy RM, Weiner JM. Injection allergen immunotherapy for asthma. Cochrane Database Syst Rev. 2010; (8):CD001186.

16. Calderon MA, Alves B, Jacobson M, Hurwitz B, Sheikh A, Durham S. Allergen injection immunotherapy for seasonal allergic rhinitis. Cochrane Database Syst Rev. 2007; (1):CD001936.

17. Boyle RJ, Elremeli M, Hockenhull J, Cherry MG, Bulsara MK, Daniels M, Oude Elberink JN. Venom immunotherapy for preventing allergic reactions to insect stings. Cochrane Database Syst Rev. 2012; 10:CD008838.

18. Bae JM, Choi YY, Park CO, Chung KY, Lee KH. Efficacy of allergen-specific immunotherapy for atopic dermatitis: a systematic review and meta-analysis of randomized controlled trials. J Allergy Clin Immunol. 2013; 132:110–117.

19. Pipet A, Botturi K, Pinot D, Vervloet D, Magnan A. Allergenspecific immunotherapy in allergic rhinitis and asthma: mechanisms and proof of efficacy. Respir Med. 2009; 103:800–812.

20. Radulovic S, Calderon MA, Wilson D, Durham S. Sublingual immunotherapy for allergic rhinitis. Cochrane Database Syst Rev. 2010; (12):CD002893.

21. Calderon MA, Penagos M, Sheikh A, Canonica GW, Durham S. Sublingual immunotherapy for treating allergic conjunctivitis. Cochrane Database Syst Rev. 2011; (7):CD007685.

22. Shakir EM, Cheung DS, Grayson MH. Mechanisms of immunotherapy: a historical perspective. Ann Allergy Asthma Immunol. 2010; 105:340–347.

23. Jutel M, Van de Veen W, Agache I, Azkur KA, Akdis M, Akdis CA. Mechanisms of allergen-specific immunotherapy and novel ways for vaccine development. Allergol Int. 2013; 62:425–433.

24. Passalacqua G, Compalati E, Canonica GW. Advances in allergen-specific immunotherapy. Curr Drug Targets. 2009; 10:1255–1262.

26. Pauli G, Larsen TH, Rak S, Horak F, Pastorello E, Valenta R, Purohit A, Arvidsson M, Kavina A, Schroeder JW, Mothes N, Spitzauer S, Montagut A, Galvain S, Melac M, Andre C, Poulsen LK, Malling HJ. Efficacy of recombinant birch pollen vaccine for the treatment of birch-allergic rhinoconjunctivitis. J Allergy Clin Immunol. 2008; 122:951–960.

27. Holgate ST, Djukanovic R, Casale T, Bousquet J. Anti-immunoglobulin E treatment with omalizumab in allergic diseases: an update on anti-inflammatory activity and clinical efficacy. Clin Exp Allergy. 2005; 35:408–416.

28. Beck LA, Thaci D, Hamilton JD, Graham NM, Bieber T, Rocklin R, Ming JE, Ren H, Kao R, Simpson E, Ardeleanu M, Weinstein SP, Pirozzi G, Guttman-Yassky E, Suarez-Farinas M, Hager MD, Stahl N, Yancopoulos GD, Radin AR. Dupilumab treatment in adults with moderate-to-severe atopic dermatitis. N Engl J Med. 2014; 371:130–139.





 PDF
PDF ePub
ePub Citation
Citation Print
Print






 XML Download
XML Download