Abstract
Spinal pain is a common symptom that motivates visiting a physician. However, the natural course is usually benign and few patients need invasive treatment. Even though history taking, neurological examination, and imaging studies provide useful information for understanding the etiology of spinal pain, the pain chart is the most important tool for decision making regarding spinal interventions. Invasive treatments for chronic spinal pain refractory to conservative management include surgery as well as established interventions such as medial branch blocks, nerve root blocks, the sacroiliac joint block, and radiofrequency neurotomy, as well as emerging procedures such as pressure-controlled discography and percutaneous epidural adhesiolysis. Surgery should be considered for patients with a progressive neurologic deficit including significant radiculopathy, failure of spinal interventions, or an uncertain or serious diagnosis.
척추 통증(spinal pain)은 흔한 증상이나 만성화되면 암성 통증(cancer pain)보다 그 정도가 더 심한 경우도 있어 환자가 수술을 고려하는 경우가 보편적이나 수술은 척추통증의 많은 원인 질환 중 일부만 해결할 수 있을 뿐이다[1]. 척추통증은 그 기전이 복잡하여 자기공명영상검사(magnetic resonance imaging, MRI)나 전산화단층촬영(computed tomography, CT)과 같은 영상검사만으로 진단할 수 없고, 신경학적 검사와 전기생리학적 검사와 같은 기능검사를 하더라도 확진할 수 없는 경우가 많다[23456]. 특히 후관절통(facet joint pain)이나 천장관절통(sacroiliac joint pain)은 수술로 해결될 수 없어 척추통증을 제어할 좀더 보편적 방법으로 신경차단술(pain block) 또는 척추중재시술(spinal intervention)이 제시되었다. 신경해부학이 밝혀낸 척추신경의 분포를 기초로 구축된 신경중재시술은 척추통증을 치료할 뿐만 아니라 진단하는 중요한 수단으로 부각되고 있다.
신경중재시술은 추간판 자극검사(disc stimulation test)처럼 통증을 유발시키거나, 내측신경지차단술(medial branch block)처럼 통증을 감소시켜 확진하는 목(diagnostic purpose)과 고주파내측신경절리술(radiofrequency [RF] medial branch neurotomy)처럼 통증을 영구 제어할 목적(the-rapeutic purpose)으로 사용된다[78]. 신경중재시술을 바르게 이해하고 적절히 적용한다면 치료할 수 있는 치료 대상군을 넓히고, 과도하게 성행하고 있는 척추수술을 줄일 수 있으며, 척추통증에 대한 이해를 깊게할 수 있을 것이다. 또한 환자에게 불필요한 침습적 치료나 근거 없는 보존적 치료를 받지 않도록하여 환자의 치료결과를 높이고 과도한 의료비 상승을 억제할 수 있을 것이다. 본 종설에서 저자는 척추통증의 진단 및 치료 목적으로 사용되는 척추중재시술 방법을 중심으로 소개하고자 한다.
성공적 척추중재시술의 첫단계는 척추통증에 대한 정확한 가설을 수립하는 것이다. 가설은 병력 청취, 신경학적 검사, 통증 차트(pain chart) 작성을 통해 수립할 수 있다[9]. 통증 차트에는 환자의 통증 양상, 통증 정도, 유발 요인 및 해소 요인, 통증 분포에 대한 정보를 담고 있다. 이런 정보를 가지고 환자의 통증이 체성통증(somatic pain)인지 신경근성통증(radicular pain)인지를 분류한다[9]. 일반적으로 체성통증은 광범위하고(diffuse), 깊으며(deep), 쑤시는(throbbing) 양상이고, 신경근성 통증은 좁고(localized), 칼로 에이는 듯한(lancinating), 전기가 오는(electrical) 양상을 보인다[910]. 통증의 정도는 0부터 10까지의 시각화척도(visual analog scale, VAS)점수로 기술하며, 보편적으로 VAS 점수가 5 이하인 경우에는 환자교육, 약물치료, 운동치료를 포함하는 보존적 치료를 시행하고, 5-7인 경우 척추중재시술을 시행한다[9]. VAS 점수가 7 이상인 경우에는 여러 가지를 종합적으로 고려해 수술을 우선 고려해야 하며 수술 전 정밀검사를 시행해야 할 것이다[9].
척추통증 환자에 대한 병력은 일반적 차트보다는 통증을 전문적으로 기술할 수 있는 통증 차트를 사용하는 것이 바람직하다[9]. 통증 차트에 기록된 통증 양상, 통증 정도, 통증 분포, 유발요인, 해소요인 등을 분석함으로써 환자마다 맞춤형의 치료를 계획할 수 있다[9]. 통증 차트를 분석해보면 체성통증인 후관절통, 천장관절통, 추간판인성통증(discogenic pain)과 신경근성통증의 특징이 서로 달라 척추 통증의 진단에 MRI나 CT에 버금가는 도움을 주고 있다[69]. 신경학적 검사를 시행하여 통증 뿐만 아니라 신경근병증(radiculopathy)유무를 확인할 필요가 있다. 신경근병증이 있으면 근육 약화, 감각 둔화, 건반사 감소를 보이며, 신경근병증이 뚜렷한 환자에게 척추중재시술을 우선적으로 고려하는 것은 바람직하지 않으며 원인을 찾고 근본적 치료를 시행하는 것이 바람직하다. MRI나 CT와 같은 정밀영상검사를 시행하였다면 종양, 골절, 감염 등의 위험징후(red flag conditions)가 있는지를 살펴보아야 한다. 위험 징후가 확인되는 경우에는 그 징후에 해당 하는 검사와 치료를 해야 한다.
이러한 정보를 바탕으로 통증 가설을 수립하였다면 두번째 단계로 그 가설을 입증할 진단 목적의 신경차단술(diagnostic pain block)을 시행하여 확진한다. 예를 들어, 후관절통은 내측지신경차단술, 천장관절통은 천장관절차단술(sacroiliac joint block), 추간판인성통증은 추간판자극술로 확진할 수 있다[8]. 통증 가설이 수립되었다면 다양한 방법으로 통증을 제어할 수 있다. 후관절통은 치료 목적의 내측지신경차단술 또는 내측지에 대한 고주파신경절리술(RF neurotomy), 천장관절통은 치료 목적의 천장관절차단술 또는 외측천골신경(lateral sacral nerve)에 대한 고주파신경절리술, 추간판인성통증은 추간판내스테로이드주사(intradiscal steroid injection), 고주파수핵성형술(RF nucleoplasty) 또는 고주파섬유륜성형술(RF annuloplasty)을 시술할 수 있다[11121314].
시술 전 날 샤워를 하여 감염을 예방한다. 시술 6시간 전에 가급적 금식하며, 진통제는 가급적 수술 5일전, 아스피린 및 혈소판응고억제제 사용 환자는 가급적 수술 7일전 사용을 중단해야 한다[15]. 와파린(wafarin) 같은 강한 혈액응고억제제 복용 환자는 금기이나 꼭 시술이 필요한 경우라면 주치의와 상의하여 수술 5일전 사용을 금지하여야 한다[15]. 위험 약물을 복용하고 있거나, 전신질환이 있는 경우에는 득과 실을 따져 시술 여부를 신중하게 결정해야 할 것이다. 시술방에서 환자는 혈압, 심박동, 산소포화도, 심전도 감시가 이루어 져야 한다. 주사침(spinal needle)은 일반적으로 직경 25G에 길이 10 cm의 주사침이 사용된다. 25G는 매우 가늘어 삽입통(needling pain)이 적은 반면 잘 휘어져 목표지점으로 진입이 어려워 좀더 굵은 주사침이 사용되기도 한다. 목표지점으로 주사침을 진입시킬 때는 주사침의 탄성을 이용하거나 끝을 구부리고 주사침을 회전시켜 방향을 바꾸는 기술이 이용된다. 불필요한 염증반응을 줄이기 위해 방부제가 없는 국소마취제(preservative-free anesthetic)가 선호되며 척추중재시술에는 리도카인(lidocaine), 부피바카인(bupivacaine), 로비피바카인(ropivacaine) 등이 주로 사용된다. 위약 효과(placebo effect)를 방지하고자 작용이 빠른 마취제와 느린 마취제를 각각 사용하여 그 결과를 비교(double comparative block)하여야 한다[8]. 일반적으로 첫 번째 시술은 작용이 느린 부피바카인 또는 로피바카인으로 하고, 두 번째는 작용이 빠른 리도카인으로 시술한 다음 VAS 점수를 시간대 별로 만 하루 동안 기록하여 통증 감소 양상을 분석하면 위약 효과를 배제할 수 있다[16]. 진단 특이도(specificity)를 높이기 위해서는 국소마취제를 각 분절마다 0.5 mL만 사용하여야 한다[16]. 국소마취제의 양을 증가시키면 진단의 민감도(sensitivity)는 증가시킬 수 있지만 특이도가 떨어져 진단적 가치가 저하된다.
C-형 방사선투시기(C-arm fluoroscope)는 척추중재시술의 필수 장비로 안전하고 효과적 시술을 가능하게 한다. 그러나 방사선은 확인된 발암요인으로 척추중재시술 시에는 환자와 의사 모두 최소한 노출되어야 하며 중요 장기는 최대한 보호되어야 한다. 치료 과정에서 하루에도 여러 번 방사선에 노출되는 의사는 특히 보호안경, 보호의복, 보호장갑을 착용하여야 한다. 수술용겸자(surgical forcep)를 이용한 주사침 삽입술을 익힌다면 손을 보호할 수 있다. 또한 방사선이 잘 통과되어 영상의 질이 높아지고, 쉽게 환자 위치를 변화시킬 수 있는 방사선투시침대(radiolucent table)가 구비되어 있다면 더욱 편리하다. 과거의 요오드화 조영제(iodinated contrast dye)와는 달리 현재 사용되는 조영제(non-iodinated contrast dye)는 수용성이며, 신경 자극 효과가 적고, 신장으로 신속히 배출되어 안전해졌지만, 신장질환이 있는 환자나 과민반응이 있는 환자에서는 신중히 사용되어야한다. 환자의 시술이 끝나면 간단한 소독을 하고 부작용이 발생하지 않는지 관찰한 다음 귀가 한다. 시술 후 환자에게 통증기록지를 주어 만 하루 동안 통증 감소 양상을 기록하게 하여 다음 외래 방문에서 반응을 평가한다[1516].
내측지신경은 신경근(nerve root)에서 갈라진 후지신경(dorsal ramus)이 상관절돌기(superior articular process)와 횡돌기(transverse process)사이의 Burton점을 통과하면서 내측으로 뻗어 나온 신경가지이다[17]. 주로 후관절의 관절낭 표면에 분포하며 감각신경으로 후관절통을 척수로 실어나르는 역할을 한다. 특징적으로 요추 후관절은 내측지신경의 삼중 지배를 받고 있다. 각 관절은 인접한 두 상부요추 내측지신경의 하행분지(descending branch)와 바로 아래 하부요추의 상행분지(ascending branch)가 공동으로 관절에 신경분포를 하고 있다[18]. 효과적인 신경차단을 위해서는 세 분지를 모두 차단해야 한다[16]. 예를 들어 가장 흔한 후관절통의 원인인 L4-5 후관절을 차단하기 위해서는 L3, 4, 5 신경근에서 나오는 내측지신경을 모두 차단해야 한다. 명심해야할 것은 요추 신경근은 추간공(neural foramen)에서 나와 하행하다가 후지신경을 분지하며, 이 후지신경은 아래 요추의 횡돌기를 넘어 해당 요추-아래 요추가 이루는 후관절에 분포하는 내측지신경을 내게된다. 예를 들면, L4 횡돌기를 넘어가는 내측지신경은 L3 내측지신경인 것이다. 이러한 위치 차이를 정확하게 인지하여야 시술 시에 혼돈이 없다. L5는 내측지신경이 없고 후지신경(doral primary ramus)만이 있어 이것이 목표가 된다.
요추 신경공은 요추 척추강 내 구조물이 변형되어 신경근의 형태로 빠져나가는 경계 부위이다. 경막(dura)은 신경공으로 들어갈 때 신경근을 감싸는 신경외막이 되며 경막을 감싸던 경막외막은 신경공에서 신경근외막으로 된다. 척수에서 나오는 후근신경(dorsal root)과 전근신경(ventral root)은 추간공 근처에서 합쳐지게 되며, 다시 직경이 큰 전지신경(ventral ramus)과 직경이 작은 후지 신경(dorsal ramus)로 나뉘게 된다[18]. 후근신경은 신경의 직경이 확대되는 후근신경절(dorsal root ganglion)을 형성한다. 전지신경에서 신경공을 통해 역행하여 척추강내에 분포하는 회행성 분지를 루시카의 되돌이신경(recurrent nerve of Luschka)이라고 부른다. 경막은 지방조직으로 쌓여 있으나 추간공까지 연장되어 있지 않다. 신경근 주위에는 신경근 동맥과 정맥이 분포하고 있어 주사침 등에 쉽게 출혈을 일으킬 수 있다.
경추부 C3-4부터 C7-T1까지 후관절은 경추 내측지신경이 분포한다. 그러나 C2-3 후관절은 제3후두신경(third occipital nerve)과 C2의 교통분(communicating branch)에 의해 지배를 받고 있다. C3부터 C6까지의 내측지신경은 관절주(articular pillar)의 허리부분을 돌아 나오므로 이 부위가 신경차단술의 목표점이 된다[19]. 그러나 C7 내측지신경차단술의 경우 C7 횡돌기의 상측방이 목표점이 되고, C8 내측지 신경차단술의 경우 T1 횡돌기의 상측방이 목표점이 된다. 경추 후관절 역시 내측지신경의 삼중 지배를 받고 있다. 각 관절은 인접한 두 상부경추 내측지신경의 하행분지(descending branch)와 바로 아래 하부경추의 상행분지(ascending branch)가 공동으로 관절에 신경분포를 하고 있다. 효과적인 신경차단을 위해서는 세 분지를 모두 차단해야 한다[16]. 예를 들어 가장 흔한 후관절통의 원인인 C5-6 후관절을 차단하기 위해서는 C4, 5, 6 신경근에서 나오는 내측지신경을 모두 차단해야 한다. 명심해야할 것은 요추와 달리 경추 신경근은 추간공(neural foramen)에서 나오는 신경근이 아래 신경근이라는 것이며, 이것이 후방으로 후지신경을 분지하여 아래 경추의 관절주를 지나 해당 경추-아래 경추가 이루는 후관절에 분포하는 내측지신경을 내게 된다. 예를 들면, C4 관절주를 넘어가는 내측지신경은 C4 내측지신경인 것이다. 이러한 위치 차이를 정확하게 인지하여야 시술 시에 요추와 혼돈하는 일이 없다.
경추 신경공 역시 경추 척추강 내에서 시작한 신경근이 체간으로 빠져나가는 경계 부위이다.구상돌기(uncus)가 경추 추간반과 신경근을 경계지어주며 경추추간판전위가 신경공 방향으로 잘 일어나지 않도록 하는 점이 요추와 차별점이다. 또한 요추 횡돌기에 해당하는 외측과로 추골동맥이 지나가는 점이 특징적이다. 이 추골동맥과 신경근의 손상을 피하기 위해 경추 신경공 차단술은 신경근의 뒤부분으로 하게 된다. 요추4-5 신경공으로는 요추 4번 신경근이 빠져 나가지만, 경추 4-5 신경공으로는 경추 5번 신경근 빠져나가는 사실을 잘 주지하여 신경차단술을 시행하여야 할 것이다. 경추 신경공 주위에는 특히 신경근 동맥과 정맥이 분포하고 있어 주사침 등에 쉽게 출혈을 일으키거나, 주입한 약제에 의한 색전증으로 심각한 부작용이 초래될 수 있는 점 또한 주지하여야 한다.
과거에는 후관절의 관절강 내로 국소마취제를 직접 주입하였으나, 관절낭의 손상 여부에 따라 일정한 양을 주입할 수 없고, 후관절의 손상부위에 따라 약이 달리 누출되어 반응이 달라지는 점이 있고, 치료의 대상이 되는 신경이 직접 분포하는 곳이 아니라는 점에서 최근에는 내측지신경차단술이 보편적으로 사용된다[81516]. 내측지신경차단술로 척추성 통증이 확인된 환자는 내측지신경을 고주파로 신경을 절리함으로써 장기간의 치료 효과를 거둘 수 있다[89]. 복와위(prone)에서 시술부위를 소독하고 소독포로 덮는다. C형 방사선투시기를 15-20도 사위상(oblique view)을 잡아 상관절돌기, 횡돌기, 척추경이 모두 잘 보이도록 한다. C형 방사선투시기 하에 상관절돌기와 횡돌기가 서로 만나는 Burton점으로 주사침을 진입시킨다(Figure 1). L5는 천골익(sacral ala)과 L5상관절이 이루는 천골오목(sacral notch)이 목표지점이다. 측면상(lateral view)에서 주사침이 횡돌기를 넘어 들어가지 않은 것을 확인하고 0.5 mL의 0.75% 로피바카인 또는 0.5% 부피바카인 또는 4% 리도카인을 주입한다. 각 목표지점마다 동일한 시술을 시행하고 주사침을 제거한다.
관절강 내로 주사하지 않고 내측지차단술이 선호되는 것은 요추와 동일한다. C형 방사선투시기를 환자의 우전방에 위치시켜 경추부에 후전상(postero-anterior view), 측면상, 사위상(oblique view)을 쉽게 포착할 수 있게 한다. 복와위에서 시술부위를 소독하고 소독포로 덮는다. C형 방사선투시기를 후전상으로 하고 관절주의 허리부위를 목표지점으로 하여 주사침을 삽입한다(Figure 2). 일단 주사침이 뼈에 접촉하면 C형 방사선투시기를 5도 사위상으로 만들어 허리부위를 확실하게 드러내 탐침의 정확한 위치를 교정할 수 있다. 0.75% 로피바카인 또는 0.5% 부피바카인 또는 4% 리도카인 0.5 mL를 주입 후 주사침을 제거한다. 제3후두신경절 차단술도 원칙은 같으나 신경이 비교적 굵고 주행이 일정치 않아 세부위를 차단해야한다. 목표지점은 측방사진에서 경추2, 3번의 관절주의 중심을 지난 선을 긋고, 경추2-3번 신경공내에서 경추3번의 상관절의 위쪽 끝, 중심, 아래쪽 끝을 지나는 선을 그엇을 때 서로 교하차하는 세점이다(Figure 3).
선택적 경막외차단술은 후궁간 경막외차단술(translami-nar epidural block)에 비해 진단 및 치료에 있어 더 우수하다[20]. 선택적 경막외차단술은 병적 신경근에 직접 약물을 투입하므로 소량의 약물로도 더 나은 효과를 기대할 수 있다. 또한 약물을 적게 사용하며 주사침의 직경이 적어 합병증이 적게 유발된다. 환자를 복와위로 하고 C형 방사선투시기를 20-35도 사위상으로 하여 신경공이 잘 보이게 한다. 주사침을 신경공의 상부 방향으로 삽입시켜 척추경(pedicle)의 직하방에 위치하도록 한다(Figure 4). 0.2 mL 정도의 조영제를 주입하여 주사침의 위치와 신경근의 주행을 확인한다. 조영제는 신경근과 척추강에 걸쳐 고루 확산되는 소견을 보이는 것이 이상적이다. 주사침이 후근신경절의 근위부에 위치하면 척추마취가 될 수 있으므로 탐침은 후근신경절의 원위부에 위치하여야 한다. 0.2% 로피바키안 또는 0.25% 부피바카인 또는 2% 리도카인 1-2 mL를 주입한다. 치료 목적일 때는 스테로이드를 혼합하여 총 2-4 mL를 투여할 수 있다.
경추 선택적 경막외차단술은 드물지만 심각한 척수경색으로 인한 사지마비 및 사망을 초래할 수 있다[1516]. 따라서 이러한 합병증을 예방하기 위해서 입자가 큰 스테로이드는 금기이다. 입자가 작은 베타메타손이나 덱사메타손을 사용하는 것이 안전하다. 조영제가 혈관내로 삽입되어 근동맥이 조영되면 즉시 시술을 멈추어야 한다. 또한 감염이 국소적 진행하면 경막상농양을 형성할 수 있고 또 전신적으로 전파되면 패혈증이 생길 수 있다. 신경근 근처에 출혈을 초래하여 국소 혈종이 생기는 경우도 있다. 앙와위에서 C형 방사선투시기는 두부 상방에 위치시킨다. 경추성두통(cervicogenic headache)은 C3-4와 C4-5 신경공이 목표가 되도록 하고 신경근성 상완통이 있는 환자들은 피부분절에 따라 시술할 신경근을 정한다. C형 방사선투시기를 움직여 신경근과 평행하도록 위치한다. 주사침을 상관절돌기의 끝으로 삽입하여 일단 접촉하게 한다. 접촉된 지점이 전후상에서 관절주(facet column)의 중간을 넘어가지 않은 것이 확인되면(Figure 5), 1 mL의 0.2% 로피바카인 또는 0.25% 부피바카인 또는 2% 리도카인을 단독 또는 스테로이드와 혼합하여 서서히 주사한다.
천장관절에는 L5 후지신경과 S1, 2, 3 측방천골분지가 분포하지만 신경 경로가 다양하여 내측지차단술 처럼 직접 신경을 차단 하는 것이 어려워 아직까지 천장관절내 직접 주사가 기본이다. 그러나 고주파신경절리술 시에는 직접 L5 후지신경과 S1, 2, 3 측방천골가지가 목표지점이 되어야 한다[91415]. 복와위에서 시술부위를 소독하고 소독포를 덮는다. C형 방사선투시기를 후전상으로 하고 천장관절이 잘 보이도록 조정한다. 보통 두개의 관절면이 보이는데 내측 관절면이 후방에 있어 이것이 목표이다. 천장관절의 하방은 주로 활액관절이고 상방은 인대로 고정되어 있어 목표는 하방이다(Figure 4). 관절강의 하방을 목표로 탐침의 방향은 내측에서 외측으로 향하도록 한다. 조영제를 주입하여 탐침이 정확하게 관절강 내에 있는가를 확인하고 조영제를 계속 주입하여 관절강 전체에 조영제가 확산되도록 한다. 조영제누수가 없고 관절강이 조영이 우수하다면 0.75% 로피바카인 또는 0.5% 부피바카인 또는 4% 리도카인 1-2 mL를 주입 후 주사침을 제거한다.
천장관절차단술 중 조영제가 누수되는 경우에는 국소마취제를 투여할 지라도 누수가 되어 충분한 효과를 기대할 수 없다. 오히려 주위의 원하지 않는 신경이 차단되어 환자가 불편함을 겪을 수도 있다. 따라서 이런 경우에는 골간인대에 국소마취제를 투여하여 천장골관절 차단 효과를 기대할 수 있다[91415]. 복와위로 시술부위를 소독하고 소독포로 덮덮는다. C형 방사선투시기의 사위상에서 골간인대 부위를 확인한다. 입점은 대부분 천골의 정중부에 위치한다. C형 투시기의 각도와 평행하게 탐침을 진행시켜 골간 인대 내로 탐침을 삽입시킨다. 조영제를 투입하여 천장골 관절근처의 확산을 확인한 후 0.75% 로피바카인 또는 0.5% 부피바카인 또는 4% 리도카인 1-2 mL를 주입한다.
추간판자극술(disc stimulation test)은 영상검사일 뿐 아니라 통증을 유발시켜 환자의 통증과 추간판 변성을 연결시키는 검사라는 의미에서 최근에는 추간판자극술이라는 용어가 사용되고 있다. 추간판인성통증은 일반적으로 MRI만으로 진단하기 어려워 추간판자극술이 진단에 이용되고 있다. 추간판자극술의 하나인 압력조절식 추간판촬영(pressure-controlled discography)은 추간판내압을 정확하게 측정할 뿐 만아니라 과도한 압력 상승을 방지하여 과거 추간판조영술의 민감도 및 특이도를 향상 시켰다[72122232425]. 특히 과거의 단점으로 여겨졌던 조영제 주사 속도의 불규칙한 점이 컴퓨터로 조절되고, 다양한 정보 분석이 가능한 장비(APCD; Cybermedics, Iksan, Korea)가 개발되어 정확한 진단이 편리해졌다. 환자를 방사선 투과성 침대 위에 옮겨 복와위를 취하게 한다. 환자를 복와위로 두면 통증이 유발되어도 척추를 움직이는 범위가 제한되어 검사 및 촬영이 용이한 점이 있다. C형 방사선조영기를 사면상으로 하여 상관절돌기의 끝이 찌르고자 하는 추간판의 상하, 좌우의 가운데에 위치하도록 하고 22G 천자침을 방사선조영기 입사각으로 바로 찌르게 된다. 대조군을 포함하여 천자를 마친 뒤 압력계가 연결된 주사기에 조영제를 채워 대조군 부터 주입한다. 천천히 주입하면서 천자침 끝에 조영제가 나오는 순간 주입을 멈추고 압력이 평형을 이루는 상태에서 압력을 측정하여 이를 추간판 고유의 내부압으로 한다. 이 압력을 0으로 두고 이때부터 다시 조영제를 천천히 주입하면서 주입 용적과 압력을 정확히 기재한다. 통증이 VAS 6점 이상으로 유발되거나, 압력이 50 psi 이상이거나, 주입용적이 3 mL 이상이면 주입을 중단하여야 한다. 유발된 통증이 평소 통증과 동일하거나(concordant) 유사한(similar) 경우이면서 압력이 50 psi 미만, 용적이 3 mL 미만에서 유발된 경우 양성(positive disc)으로 판정한다[21]. 추간판인성통증이 확진된 경우 시행하는 추간판내시술은 추간판내로 스테로이드나 고장성 덱스트로스를 주입하는 방법과 고주파나 레이저를 이용하여 섬유륜 또는 수핵을 응고 또는 해리시키는 방법이 있다[1112132627].
경피적경막외강신경성형술(percutaneous epidural adhesiolysis)은 척추통증의 주된 원인을 유착으로 정의하고, 통증 생성 및 약물 전달을 막는 유착을 카테터 및 약물을 이용하여 박리함으로써 효과적으로 약물을 전달하고 통증을 감소시키는 것이 주된 기전이다[282930]. 경피적경막외강신경성형술 및 경피적경막외강유착박리술은 넓은 의미에서 같은 용어라고 할 것이다. 내시경을 이용하지 않는 방식과 내시경을 이용하는 방식으로 나누어지며, 내시경을 이용하는 방식에는 내시경만 이용하는 방식과 레이저를 이용하는 방식으로 나누어 진다. 경피적경막외강신경성형술은 유착박리 기능 뿐만 아니라 안전한 경막외강 확보를 통한 많은 양의 마취제 및 스테로이드를 안전하게 목표 지점에 주입할 수 있는 장점이 있다. 또한 여러 마디를 동시에 치료할 수도 있으며, 카테터를 거치시킨 상태로 여러 날 동안 치료제를 반복적으로 주입할 수도 있다.
시술 대상은 적절한 기간 동안 보존적 치료를 시행하였음에도 불구하고 지속되는 척추수술후증후군, 척추관협착증, 추간판탈출증과 만성요통에서 효과가 있다고 밝혀져 있다. 특히 척추수술후증후군과 척추관협착증에서의 효과가 잘 입증되어있는 편이다[28293031323334]. 경피적경막외강신경성형술이 최소침습치료이긴 하나 기존 신경차단술에 비해 위험성 높다고 알려져 있으므로 최소한 1회이상의 기존 신경차단술을 시행받아보는 것이 권장된다. 환자를 척추중재시술용 침대위에 복와위로 높이고, 환의를 벗겨 천골부위가 충분히 노출되도록한다. 항문 주변에 거즈를 두면 소독약이 흘러내려가는 것을 방지할 수 있다. 비교적 시간이 오래 걸리는 중재시술이므로 수술방 또는 시술방에서 천골부를 소독후 수술포를 덮고 수술가운을 입은채 시술하는 것이 바람직하다. 2% 리도카인을 이용해 천골구멍위 피부를 국소마취한다. 마취가 이루어지고 나면 17G 탐침으로 천골구멍위 피부에 약간의 구멍을 낸 다음 준비한 Tuohy 탐침을 천골구멍으로 찔러 넣는다. 탐침 끝이 경막외강 내로 2-3 cm 정도 전진한 뒤 조영제를 약 5 mL 정도 주입하여 경막외강조영술(epidurogram)을 시행한다. 첫 번째 경막외강조영술의 목적은 카테터를 경막의 복측으로 위치시켜 전진시키기 위해 천골신경근의 위치를 파악하기 위한 목적이다. 또한 경막외강조영술을 하면서 주사기의 플런저에 전해지는 압력을 느끼고, 환자의 통증 유발 양상을 보아 경막외강내의 화학적 자극 상태를 일부 파악할 수 있다. 카테터를 목표지점에 위치 시키기 위해서는 숙련된 손동작이 필요하다. 카테터의 끝을 0.5-1 인치 정도 길이로 30도 정도로 꺽어 돌려가며 방향전환을 하는 방법이 있으며, 처음부터 방향전환이 가능한 카테터시스템을 사용하는 방법도 있다. 목표지점에 카테터끝이 도달하고 나면 경막외강조영술을 다시 하여 유착정도를 파악한다. 유착부위에서 카테터의 움직임을 이용하여 물리적 유착박리를 시도한다. 또한 10% 고장성 식염수, 1500 U 정도의 hyaluronidase, 생리식염수 또는 조영제를 이용하여 유착박리를 시도한다. 다시 경막외강조영술을 시행하여 유착박리가 이루어졌는지 확인한 다음(Figure 6), 0.25% 부피바카인 또는 0.2% 로피바카인을 주입한다. 이때 스테로이드를 함께 사용할 수 있는데 베타메타손과 덱사메타손이 권장되며 트리암시놀론과 같은 particulate 스테로이드는 합병증 예방을 위해 금지되고 있다. 약제 주입이 끝나면 catheter를 환자의 몸에서 빼지않고 부착해놓은 상태로 회복실로 옮긴다. 시술 30분 후 10% 고정성식염수 6 mL를 서서히 주입하여 유착박리 및 신경부종 감소를 도모한다. 이 과정에서 통증을 심하게 호소하는 경우에는 신경학적 부작용을 방지하기 위해 주입을 중단해야한다. 경피적경막외강신경성형술의 어떤 단계에서도 통증이 심하게 유발되는 경우에는 시술을 멈추고 환자 상태를 면밀히 관찰한 다음 시술을 지속할지 여부를 결정하는 것이 합병증 방지를 위해 권장된다. 앞서 살펴본 바와 같이 경피적경막외강신경성형술은 경막외강조영술, 유착박리술 또는 신경성형술, 약제주입이라는 3가지 필수 단계를 거친다. 시술자는 이러한 3단계를 꼭 기록하고, 영상자료로 남겨놓는 것이 좋다. 또한 기존의 신경차단술에 비해 사용하는 약제의 용량이 많고 위험성을 내재하고 있는 유착박리라는 과정이 있는 만큼 합병증 발생가능성을 충분히 인지하고 있어야하며 환자에게도 고지되어야한다. 현재까지 임상 결과에 따르면 경피적경막외강신경성형술의 수술 후 1-3개월의 단기성적은 80-90% 정도이나 수술 후 1년의 장기성적은 약 70-80% 정도이다[28293031323334]. 지금까지 9개 정도의 무작위대조군시험에서 양호한 결과를 보이고 있어 분명히 효과가 있는 시술이라고 할 것이나, 척추통증의 양호한 임상 경과를 감안할 때 충분한 보존적 치료나 기존의 신경차단술 없이 행하는 것은 삼가하여야할 것이며 무엇보다도 정확한 적응증에 시행하여야 할 것이다. 적절한 적응증 및 비용-효과에 대한 추가 연구가 꼭 필요할 것으로 예상된다.
척추중재시술은 만성척추통증의 진단 및 치료에 중요한 역할을 하고 있다. 통증 차트 작성을 통한 신중한 환자 선택과 정확한 시술이 척추중재시술의 성공에 매우 중요하다. 신경근병증을 포함하여 신경학적 이상이 진행하거나, 척추중재시술에 반응하지 않는 심한 통증이 있거나, 감염이나 종양과 같이 심각한 상태가 확인되면 수술적 치료를 신중히 고려하여야 한다.
본 논문은 척추 통증의 치료에 대한 접근과 치료를 전반적으로 잘 서술하고 있으며 특히 비수술적 치료에 대한 설명을 각 시술별로 준비단계 부터 방법론을 포함해 서술함으로써 읽는 이로 하여금 체계적 접근이 가능하도록 하고 있다. 특히 주목할 점은 척추 통증의 치료적 접근 시 통증의 평가에 대해 통증 차트와 신경학적 검진 등을 모두 사용하여 가설을 세우고 진단을 구체화해야 함을 강조한 것이 현재 무분별하게 성행하는 척추 수술에 대해 돌아보는 기회를 제공한 의미 있는 논문이라 판단된다.
[정리: 편집위원회]
Figures and Tables
 | Figure 1Lumbar medial branch block. (A) Anterior-posterior view. The target points lie against the lateral surface of the superior articular process (SAP), at the most medial end of the transverse process (TP). (B) Lateral view. The target points rest on the superior surface of the transverse processes. (C) Oblique view. The target points lie on the bisecting regions of the superior articular processes and tranverse processes. SN, spinal nerve; P, pedicle. |
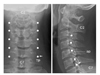 | Figure 2Cervical medial branch block. (A) An anterior-posterior radiograph shows the dots which rest on the concave lateral surface of the articular pillar (ap) of the each cervical vertebrae. (B) A lateral view of the cervical spine. The dot shown by the thin arrow indicated the target point for block of the C5 medial branch which rests on the intersection point of two crossing lines. (A,B) The target point of the C7 medial branch rests on upper border of the transverse process (TP) in the AP view and the superior articular process in the lateral view (the thick arrow). |
 | Figure 3Third occipital nerve block. A lateral view of the upper cervical spine showing the target points for third occipital nerve blocks. The three target points lie on an axial ine that bisects the C2 and C3 articular pillars. The three target points lie at the intersections of the axial ine and transverse lines through the apex of the C3 superior articular process, tangential to the bottom of the C2-3 intervertebral foramen, and midway between these first two lines. |
 | Figure 4Lumbar transforaminal epidural block. (A) Anterior-posterior (AP) view. The target point lies immediately below the pedicle and above the exit root (the safety triangle). (B) Lateral view. The targe point lies just posterior to the vertebra and below the pedicle. (C) Oblique view of the target zone. A needle should be inserted and directed towards the safety triangle which is bordered by the lower margin of the pedicle (P) and the upper margin of the exit root. Sacroiliac joint block. (A) An AP view of the sacroiliac joint in which the posterior margins of the joint are maximally crisp over the lower one-third of the joint (narrow arrow). The target point for an intra-articular injection is marked with a dot and a thick arrow. NF, neural foramen; SAP, superior articular process; TP, transverse process. |
 | Figure 5Cervical transforaminal epidural block. (A) Anterior-posterior view. The target point lies opposite the sagittal bisector of the articular pillar. (B) Oblique view. The target rests on the postserior wall of the cervical neural foramen (NF) at its middle third. |
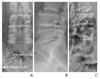
 | Figure 6Percutaneous epidural adhesiolysis. (A) A cervical epidurogram performed after the placement of the Racz cervical catheter. The tip of the catheter is indicated by the arrow. The C6 nerve root (NR) is not visualized before adhesiolysis. (B) After mechanical and hydrostatic adhesiolysis, the C6 nerve root is well visualized in the re-performed epidurogram. |
Acknowledgement
This study was supported by a grant from Korea Evaluation Institute of Industrial Technology (10043086) and a grant from Institute of Medical System Engineering in Gwangju Institute of Science & Technologies.
References
1. Robert R, Raoul S, Hamel O, Doe K, Lanoiselee JM, Berthelot JM, Caillon F, Bord E. Chronic lower back pain: a new therapeutic approach. Neurochirurgie. 2004; 50(2-3 Pt 1):117–122.
2. Boos N, Rieder R, Schade V, Spratt KF, Semmer N, Aebi M. 1995 Volvo Award in clinical sciences. The diagnostic accuracy of magnetic resonance imaging, work perception, and psychosocial factors in identifying symptomatic disc herniations. Spine (Phila Pa 1976). 1995; 20:2613–2625.

3. Kim SJ, Lee TH, Lim SM. Prevalence of disc degeneration in asymptomatic korean subjects. Part 1: lumbar spine. J Korean Neurosurg Soc. 2013; 53:31–38.

4. Kim SJ, Lee TH, Yi S. Prevalence of disc degeneration in asymp-tomatic korean subjects. Part 3: cervical and lumbar relationship. J Korean Neurosurg Soc. 2013; 53:167–173.

5. Lee TH, Kim SJ, Lim SM. Prevalence of disc degeneration in asymptomatic Korean subjects. Part 2: cervical spine. J Korean Neurosurg Soc. 2013; 53:89–95.

6. Schwarzer AC, Wang SC, O'Driscoll D, Harrington T, Bogduk N, Laurent R. The ability of computed tomography to identify a painful zygapophysial joint in patients with chronic low back pain. Spine (Phila Pa 1976). 1995; 20:907–912.

7. Shin DA, Kim HI, Jung JH, Shin DG, Lee JO. Diagnostic relevance of pressure-controlled discography. J Korean Med Sci. 2006; 21:911–916.

8. Slipman CW, Bhat AL, Gilchrist RV, Issac Z, Chou L, Lenrow DA. A critical review of the evidence for the use of zygapophysial injections and radiofrequency denervation in the treatment of low back pain. Spine J. 2003; 3:310–316.

9. Jung JH, Kim HI, Shin DA, Shin DG, Lee JO, Kim HJ, Chung JH. Usefulness of pain distribution pattern assessment in decision-making for the patients with lumbar zygapophyseal and sacroiliac joint arthropathy. J Korean Med Sci. 2007; 22:1048–1054.

10. Schwarzer AC, Wang SC, Bogduk N, McNaught PJ, Laurent R. Prevalence and clinical features of lumbar zygapophysial joint pain: a study in an Australian population with chronic low back pain. Ann Rheum Dis. 1995; 54:100–106.

11. Chou LH, Lew HL, Coelho PC, Slipman CW. Intradiscal electrothermal annuloplasty. Am J Phys Med Rehabil. 2005; 84:538–549.

12. Cohen SP, Williams S, Kurihara C, Griffith S, Larkin TM. Nucleoplasty with or without intradiscal electrothermal therapy (IDET) as a treatment for lumbar herniated disc. J Spinal Disord Tech. 2005; 18:Suppl. S119–S124.

13. Khot A, Bowditch M, Powell J, Sharp D. The use of intradiscal steroid therapy for lumbar spinal discogenic pain: a randomized controlled trial. Spine (Phila Pa 1976). 2004; 29:833–836.

14. Yin W, Willard F, Carreiro J, Dreyfuss P. Sensory stimulation-guided sacroiliac joint radiofrequency neurotomy: technique based on neuroanatomy of the dorsal sacral plexus. Spine (Phila Pa 1976). 2003; 28:2419–2425.

15. Korean Spinal Neurosurgery Society. The textbook of spine. Seoul: Koonja Publishing Company;2008.
16. Bogduk N. International Spine Intervention Society. Practice guidelines for spinal diagnostic and treatment procedures. 1st ed. San Francisco: International Spine Intervention Society;2004.
17. Masini M, Paiva WS, Araujo AS Jr. Anatomical description of the facet joint innervation and its implication in the treatment of recurrent back pain. J Neurosurg Sci. 2005; 49:143–146.
18. Higuchi K, Sato T. Anatomical study of lumbar spine innervation. Folia Morphol (Warsz). 2002; 61:71–79.
19. Shin WR, Kim HI, Shin DG, Shin DA. Radiofrequency neurotomy of cervical medial branches for chronic cervicobrachialgia. J Korean Med Sci. 2006; 21:119–125.

20. Vad VB, Bhat AL, Lutz GE, Cammisa F. Transforaminal epidural steroid injections in lumbosacral radiculopathy: a prospective randomized study. Spine (Phila Pa 1976). 2002; 27:11–16.
21. Derby R, Howard MW, Grant JM, Lettice JJ, Van Peteghem PK, Ryan DP. The ability of pressure-controlled discography to predict surgical and nonsurgical outcomes. Spine (Phila Pa 1976). 1999; 24:364–371.

22. Derby R, Kim BJ, Lee SH, Chen Y, Seo KS, Aprill C. Comparison of discographic findings in asymptomatic subject discs and the negative discs of chronic LBP patients: can discogra-phy distinguish asymptomatic discs among morphologically abnormal discs? Spine J. 2005; 5:389–394.

23. Choi WS, Shin DA, Kim HI, Lee SH, Derby R, Lee SH, Kim HJ. Toward more useful pressure-controlled discography: in vitro evaluation of injection speed, sensor location, and tube length. Pain Med. 2011; 12:36–44.

24. Kim HI, Shin DA. Automated pressure-controlled discography with constant injection speed and real-time pressure measurement. J Korean Neurosurg Soc. 2009; 46:16–22.

25. Shin DA, Kim SH, Han IB, Rhim SC, Kim HI. Factors influencing manometric pressure during pressure-controlled discography. Spine (Phila Pa 1976). 2009; 34:E790–E793.

26. Freedman BA, Cohen SP, Kuklo TR, Lehman RA, Larkin P, Giuliani JR. Intradiscal electrothermal therapy (IDET) for chronic low back pain in active-duty soldiers: 2-year follow-up. Spine J. 2003; 3:502–509.

27. Klein RG, Eek BC, O'Neill CW, Elin C, Mooney V, Derby RR. Biochemical injection treatment for discogenic low back pain: a pilot study. Spine J. 2003; 3:220–226.
28. Manchikanti L, Singh V, Cash KA, Pampati V. Assessment of effectiveness of percutaneous adhesiolysis and caudal epidural injections in managing post lumbar surgery syndrome: 2-year follow-up of a randomized, controlled trial. J Pain Res. 2012; 5:597–608.

29. Manchikanti L, Cash KA, McManus CD, Pampati V, Singh V, Benyamin R. The preliminary results of a comparative effectiveness evaluation of adhesiolysis and caudal epidural injections in managing chronic low back pain secondary to spinal stenosis: a randomized, equivalence controlled trial. Pain Physician. 2009; 12:E341–E354.
30. Manchikanti L, Rivera JJ, Pampati V, Damron KS, McManus CD, Brandon DE, Wilson SR. One day lumbar epidural adhesiolysis and hypertonic saline neurolysis in treatment of chronic low back pain: a randomized, double-blind trial. Pain Physician. 2004; 7:177–186.
31. Gerdesmeyer L, Wagenpfeil S, Birkenmaier C, Veihelmann A, Hauschild M, Wagner K, Muderis MA, Gollwitzer H, Diehl P, Toepfer A. Percutaneous epidural lysis of adhesions in chronic lumbar radicular pain: a randomized, double-blind, placebo-controlled trial. Pain Physician. 2013; 16:185–196.
32. Dashfield AK, Taylor MB, Cleaver JS, Farrow D. Comparison of caudal steroid epidural with targeted steroid placement during spinal endoscopy for chronic sciatica: a prospective, randomized, double-blind trial. Br J Anaesth. 2005; 94:514–519.

33. Manchikanti L, Boswell MV, Rivera JJ, Pampati VS, Damron KS, McManus CD, Brandon DE, Wilson SR. A randomized, controlled trial of spinal endoscopic adhesiolysis in chronic refractory low back and lower extremity pain. BMC Anesthesiol. 2005; 5:10.




 PDF
PDF ePub
ePub Citation
Citation Print
Print



 XML Download
XML Download