Abstract
As degenerative spinal disease among spinal diseases causing lumbar and cervical spinal pain is the endless repetition of "the biological healing of mechanical damage" occurring over a lifetime, spinal pain by degenerative spinal disease occurs as a series of successive changes through the repetitive damage-healing process of various spinal structures including the intervertebral disc rather than a temporary phenomenon of any given pathophysiologic change in one moment. Degenerative spinal disease generally begins with degeneration of the intervertebral disc. Then herniation of the intervertebral disc resulting in subsequent radicular pain occurs when the nucleus pulposus with degeneration located in the intervertebral disc tears and penetrates the annulus fibrosus. Subsequently, disc space narrowing occurs and alters the spinal biomechanics, followed by degenerative changes to the vertebral endplate, vertebra itself, and facet joint. Finally, these changes lead to spinal stenosis, which is the final destination of degenerative spine disease. Although the exact pathogenesis of spinal pain could be still unclear because of some inconsistencies between the degenerative changes in the spine and the clinical manifestations of spinal pain, an accurate understanding of the pathophysiology and future predictions for further mechanical injury as well as thorough history taking and careful attention to the long-term clinical courses and other associated risk factors including daily life posture and work posture are needed for successful treatment of spinal pain.
요추 혹은 경추통증을 유발하는 척추질환의 평생 유병률(life-time prevalence)은 65-80%에 이르는 것으로 알려져 있으며[12], 최근 6개월간 한 차례 이상의 요통을 호소하는 비율이 40%에 이르며[3], 경추부통증의 경우에는 이전에 통증이 없는 사람의 15-20%에서 새로운 통증이 발현된다[4]. 요통의 경우 20대부터 발생하기 시작하여 전체 유병률은 65세까지 지속적으로 증가하는 양상을 보이다가 그 이후부터는 서서히 감소한다[56].
급성요통의 경우, 특별한 치료 없이 시간이 경과함에 따라 호전되는 경우가 대부분인 것으로 알려져 있는데, 여러 가이드라인에서 급성 요통환자의 90%가 6주 내로 호전되며, 요통이 발생한지 1년이 지난 시점에서 통증이 호전된 비율은 54-90%에 달하는 것으로 보고되었다[78]. 이와 같이 요통의 자연 경과에 대해 낙관적인 통계수치는 요통을 포함한 척추통증을 아주 가벼운 증상으로 오해하게 만든다. 하지만, 요통은 재발이 매우 흔한데, 첫 증상 발생 후 1년 내로 재발할 확률이 50%, 2년 내로 재발할 확률이 60%, 5년 내로 재발할 확률은 70%에 달하며, 급성요통 환자의 상당수는 만성요통 또는 지속적인 통증으로 증상의 양상이 변화하게 된다[9]. 따라서, 요추 혹은 경추통증을 유발하는 척추질환은 일생을 걸쳐 일어나는 '기계적 손상에 대한 생물학적 치유'의 끝없는 반복의 과정이기에 척추통증은 어떤 한 순간에 갑자기 발생한 증상이 아니라 반복적인 손상, 치유 과정을 거쳐서 발현되는 증상임을 이해하고, 한 번의 시술 또는 수술로 요통을 완전히 해결할 수 있다는 잘못된 믿음을 버려야 한다.
요추 및 경추통증을 유발하는 척추질환들의 분류 혹은 감별진단들로는 통증의 발병원인 및 방사통 여부, 그리고 병태생리 등에 따라서 염좌와 긴장, 퇴행성 척추질환, 퇴행성 변형(전방전위증, 측만 및 후만 등), 골절을 포함한 외상성 병변, 척추 종양, 감염 그리고 강직성 척추염과 같은 염증성 질환 등으로 분류할 수 있다[1011]. 이 장에서는 일생을 걸쳐 일어나는 일련의 연속적인 변화 과정인 퇴행성 척추질환(추간판 변성, 신경근병증, 척추관 협착증 등)을 중심으로 병태생리를 살펴보고, 이에 따른 경막외 스테로이드 주사치료와 같은 비수술 중재적 치료의 적응 기전에 관해 정리해 보고자 한다.
척추는 20대부터 퇴행성 변화가 일어나기 시작하는데 추간판 변성부터 시작되어 변성된 수핵이 후방 섬유륜을 뚫고 추간판 탈출을 일으키며 결국에는 척추종판(endplate)과 척추뼈, 그리고 척추의 후방에 위치한 척추후관절까지 퇴행성 변화가 일어나게 된다. 이러한 퇴행성 변화가 중심 척추관이나 추간공(intervertebral foramen)을 침범하게 되면 중심성 혹은 외측성 척추관 협착증이 초래되는데, 척추관 협착증은 궁극적으로 척추의 퇴행성 변화의 종착역이라고 할 수 있다(Figure 1) [1112]. 이러한 일련의 과정으로 척추의 퇴행성 변화가 어떻게 일어나는지 잘 설명되지만, 척추의 퇴행성 변화와 실제 발현하는 척추통증 간에는 괴리가 있는 경우를 자주 보게 되며, 실제 발현된 통증의 정확한 발생 기전에 대해서 여전히 잘 설명되지 않는 경우도 흔하다[1314].
추간판은 무혈관 조직이고 수분을 다량 함유한 수핵에는 신경이 분포하지 않으나, 섬유륜의 바깥 부위는 혈관과 신경이 분포되어 있어 침해수용성 및 기계적 감각을 전달하는 신경섬유가 분포되어 있다. 이러한 감각수용체들은 추간판이 정상적인 기능을 하는 경우에는 일상적인 하중에 반응하지 않지만, 추간판에 변성, 염증, 손상 등이 있으면 일상적인 하중에도 통증을 전달하게 된다. 수핵의 내부는 아교질(gelatinous substance)로 차 있으며, 아교질은 수분, 프로테오글라이칸, 콜라겐으로 구성된다. 출생 당시에는 수핵의 성분 중 90%가 수분이지만, 시간이 지날수록 수분이 줄고 추간판의 퇴행이 진행하면서 수핵의 높이도 낮아 지게 된다. 수핵에 대사산물이 축척되고 조직 내의 산소 이용이 감소되면서 여러 염증성 효소작용에 의해 황산 케라탄과 같은 프로테오글라이칸 성분이 증가하고 aggrecan이 소실 및 분절화되고 이로 인해 수핵의 구조적 변형이 발생되어 사방으로 퍼지는 압력이 척추종판 및 섬유륜에 압력을 미치게 되어 섬유륜에 틈새가 생기기 시작하여 이들이 점차 연결되고 방사성으로 갈라져 수핵이 빠져나오게 된다. 척추종판도 두터워지거나 균열을 일으키고 척추뼈 몸통에 연결되는 추간판 가장자리에는 골증식체가 생기는 등의 퇴행성 변화를 보인다(Figure 2) [15].
이러한 추간판 내부의 손상과 퇴행으로 인하여 발생하는 통증을 추간판성(discogenic) 통증이라 지칭하며, 요통의 경우 39%가 이에 해당하는 것으로 알려져 있다[16]. 추간판의 탈출(팽윤과 돌출을 포함)로 인하여 신경근에 자극이 가해짐으로써 발생하는 소위 좌골신경통을 신경근 통증(radicular pain)으로 부르는데, 요통의 약 30% 정도를 차지한다[17]. 그러나 후방관절증이나 척추관협착증과 같은 척추통증의 다른 원인들도 결국 추간판의 손상과 퇴행에 의해 유발되므로[18], 추간판 손상과 퇴행이 척추통증의 가장 근본적인 문제로 볼 수 있다.
추간판성 요통은 추간판 탈출증(her-niated inter-vertebral disc)으로 인한 신경근 통증의 소견 없이 추간판의 손상과 퇴행으로 인하여 발생하는 요통을 뜻하며 추간판 내부의 퇴행과 척추종판(endplate)의 손상으로 발생된 염증이 추간판 내부의 감각신경을 자극하여 발생하는 것으로 알려져 있다. 특히, 수핵이 외측 섬유륜에 있는 신경과 접촉하게 되면, 신경이 손상되고 손상된 신경 말단이 추간판 내부인 내측 섬유륜, 수핵까지 침투하는 것으로 알려져 있다[19]. 이때 혈관과 골지 힘줄 기관(golgi tendon organ)과 같은 감각수용체와 교감신경도 새롭게 생성된다[20]. 즉, 추간판성 척추통증의 가장 중요한 요소는 다양한 손상과 퇴행에 의해 발생된 염증과 통각신경의 만남이다. 염증을 유발하는 퇴행과 손상의 원인으로는 나이, 비만, 흡연, 진동, 강한 기계적인 압박, 그리고 유전적인 소인을 들 수 있다. 기계적인 압박은 부하가 가해진 상태로 굴곡운동을 하거나[2122], 굴곡운동과 비틀림운동이 동시에 일어날 때 발생하는 것으로 알려져 있다[23].
이러한 추간판성 척추통증에 대한 치료로 경피적 추간판내감압술 및 경피적 수핵성형술(nucleoplasty) 등과 같은 추간판 내부 시술이 비수술 중재적 치료로 임상에서 사용되고 있다. 이러한 추간판 내부 시술은 추간판의 후방 섬유륜 부위에 고열을 가하여 추간판 내 감압 및 섬유륜 파열부위의 신경통증 완화, 그리고 탈출된 수핵을 감입시키는 목적으로 사용되지만, 아직 효과에 임상적 근거가 높은 상태가 아니며[24], 추간판 퇴행에 미치는 악영향 때문에 아직 논란의 여지가 많다[25]. 그 외 최근에는 인공추간판 치환술, 성장인자를 이용한 생물학적 치료, 추간판 내 세포치료 및 줄기세포치료 등을 추간판성 척추통증의 치료에 이용하고 있으나, 아직 많은 부분이 실험적 단계에 있다[26].
신경근 통증(radicular pain)은 신경근에 기계적 압박이 가해지거나 염증반응과 같은 화학적 반응에 의해 발생하며, 가장 흔히 발생하는 요천추 신경병증의 위치는 요추 5번과 천추 1번이며, 경추 신경병증의 위치는 경추 6번과 7번이다. 신경근 중 배측신경근 혹은 배측신경절에서 발산되는 이소성 방출(ectopic discharge)에 의한 통증이며 2-3인치 두께로 찌르는 듯한 통증이 하지로 방사되는 양상을 보인다[27]. 이러한 통증 양상은 말초신경에서는 보이지 않고 배측신경근이나 배측신경절을 자극했을 때만 보이는 것으로 알려져 있다. 배측신경과 신경절을 자극하는 가장 흔한 원인은 추간판 탈출증이다. 추간판 탈출증을 수핵 탈출증(herniated nucleus pulposus)로 부르는 경우도 있으나, 추간판 탈출증 수술에서 얻은 조직을 분석해 보면 수핵만 탈출되는 경우보다 수핵, 섬유륜, 종판 성분이 혼합되어 탈출되는 경우가 더 많으므로[28], 수핵 탈출증으로만 부르는 것은 옳지 않다. 앞서 추간판성 척추통증에서 설명된 것과 마찬가지로 추간판 탈출증의 원인도 나이, 비만, 흡연, 진동, 강한 기계적인 압박, 그리고 유전적인 소인을 들 수 있다[29]. Adams 등[21]은 사체 실험에서 요추가 중립위에서 압박을 받으면 척추종판의 손상이 오고 굴곡 상태에서 반복적인 압박을 받으면 처음에는 수핵이 섬유륜을 손상시키며 후방으로 열상을 만들다가 반복이 지속되면 섬유륜을 뚫고 탈출이 되는 소견을 기술하였다. 즉, 반복적인 굴곡부하가 추간판 탈출증의 기계적인 원인임을 밝힌 것이다. 오랜 기간 동안 추간판 탈출에 의한 기계적인 압박이 신경근 통증의 원인으로 간주되었으나 1990년대 말과 2000년대 초반이 되면서 동물실험에서 수핵의 내용물을 배측신경절에 접촉시키는 것만으로도 신경근 통증이 생기고 축삭의 손상을 동반한 신경전도속도의 감소를 일으키는 것이 보고된 후[3031], 탈출된 추간판의 구조물 중, 신경근에 염증을 일으키는 요소는 섬유륜보다는 수핵이라는 것도 실험적으로 증명되었으며[32], 수핵이 배측 신경근에 강력한 염증 반응을 일으키는 것은 수핵 속에 존재하는 수핵세포에 의한 것으로 실험적 연구에서 밝혀졌다[3334]. 이 후의 연구에서 수핵세포에 존재하는 종양괴사인자(tumor necrosis factor-α) [3536373839]와 아산화질소(nitrous oxide) 등에 의해 염증반응이 발생한다고 밝혀졌다[4041]. 실험적으로 수핵에 의해 발생된 신경근의 염증반응을 국소적인 스테로이드나[42], 항종양괴사인자 물질로[38394344] 감소시킬 수 있음이 밝혀져 실제 임상적으로 경막외 스테로이드 주사가 신경근 통증의 치료에 널리 사용되고 있는데 급성기 통증 혹은 일정 기간 보존적 치료를 하였음에도 증상의 호전이 없는 경우에 사용되어 3개월 이내에 자연경과보다 유의하게 높은 증상 완화 효과를 볼 수 있다[454647]. 하지만, 수핵에 의한 비기계적인 염증반응과 탈출된 추간판 물질에 의한 기계적인 압박이 동시에 작용하면 더 심한 신경근 병변을 일으키며, 해당 척추 분절의 불안정성 등으로 인한 동적인 압박까지 가중될 경우에는 경막외 스테로이드 주사치료만으로는 충분한 치료가 되지 않는 경우도 드물지 않다.
Kirkaldy-Willis 등[12]은 최종적으로는 척추관 협착증까지 이르게 되는 퇴행성 요추질환에서 일어나는 연쇄반응에 대한 이론을 제시하면서 비록 추간판과 후관절(facet joint)이 해부학적으로는 분리되어 있으나, 어느 한 구조물에 작용하는 외력과 병소는 다른 구조물에도 영향을 준다고 주장하였다. 만약 척추에 과도한 압축력이 가해지면 퇴행성 추간판 질환이 발생하고 이로 인해 후관절에 부하가 가해지면 후관절의 퇴행이 발생한다. 이러한 손상이 특정 레벨에서 발생하게 되면 위쪽과 아래쪽 구조물도 영향을 받게 되어 결과적으로 광범위한 척추증(spondylosis)의 형태로 진행하게 된다(Figure 1D,1E) [48].
후관절에 미세손상이 반복되면 연골이 파괴되고 활막이 두꺼워지는 퇴행성 변화가 일어난다. 후관절의 퇴행성 변화는 관절의 불안정성과 골관절 비대의 원인으로 작용한다. 비대해진 골관절로 인해 척추관 및 추간신경공이 좁아지고 신경근을 압박한다(Figure 1E). 이러한 연쇄반응은 추간판에서도 마찬가지로 일어나는데, 반복된 미세손상으로 섬유륜의 파열이 일어나게 된다. 섬유륜 파열 방향이 후외측으로 진행하게 되면 추간판 탈출이 발생하고 내부로 진행하면 추간판 내장증이 발생하며, 이 두 가지 문제는 추간판의 높이를 낮추고, 척추의 불안정성을 유발하여 결과적으로 외측 함요와 추간신경공의 협착이 일어난다.
경추부 척추증도 추간판 퇴행의 결과로 초래되는데 수핵 변성 및 섬유륜 팽윤에 의해 연골 종판에서의 기계적 부하가 증가되어 골막하 골형성이 촉진되어 골극들이 형성되며, 척수관의 앞쪽 혹은 추간신경공을 침범하게 된다[49]. 이러한 현상은 추간판이 소실된 경추 분절의 과운동성을 안정시키기 위해 추간판이 소실된 분절의 인접 경추 분절에서 흔히 시작된다. 또한, 구상돌기(uncinate process)의 비후로 인해 추간신경공의 협착이 발생하며, 아시아인에게 더 흔한 후종인대 골화증도 척추퇴행증과 함께 발생하여 심한 경수 압박을 유발할 수 있다. 유병률에 대한 여러 보고들에 의하면 남성의 경우 70세에 이르면 거의 100%에서, 여성의 경우에도 96%에서 척추퇴행증을 가진다고 하며, 사후생검을 통한 보고에서는 60세 남성의 1/2, 여성의 1/3에서 유의한 척추퇴행증이 관찰되었다고 보고되고 있다[50]. 1992년 방상선학적 검사를 통한 유병률 조사에서는 궁극적으로 남녀 모두 70% 이상에서 척추퇴행증을 가지며, 남성이 방사학적인 정도가 더 심하다고 보고하고 있다[51].
상기 기전들만으로도 척추관 협착증(spinal stenosis)에 의한 신경인성 파행을 설명할 수도 있으나 최근에는 척추주위 혈관의 역할이 중요하게 대두되고 있다. 요추부 척추관 협착증의 전형적인 증상인 신경인성 파행은 좁아진 척수관의 기계적 압박 외에 주위 혈관의 혈류문제에 의해서 유발되는 것으로 알려져 있다. 이는 척추협착증의 증상이 감압술만으로 호전되지 않는다는 사실에서도 확인할 수 있다. 척추관 협착증과 관련된 혈류 문제는 크게 두 가지로 구분되는데, 하나는 정맥확장(venous engorgement)이고 다른 하나는 동맥부전(arrterial insufficiency)이다. 정맥확장 이론은, 척추협착증 환자의 정맥이 확장되어 울혈과 혈류 정체를 일으키고 울혈과 정체된 부위가 경막 외 압력과 경막 내 압력을 증가시켜 미세순환 문제와 신경허혈 손상을 유발함으로써 전형적인 신경인성 파행 증상이 나타나게 된다는 것이다. 이와 반대로 동맥부전 이론에서는 정상적인 혈관 확장 반응이 척추협착증 환자에서는 나타나지 않는다는 것이다. 특히 척추관 협착증과 죽상동맥경화증은 모두 고령에서 호발하는 질환이므로 동맥부전이 동반될 가능성이 높다[52].
경추부 퇴행성 척수병증(cervical spondylotic myelo-pathy)은 척추관 협착을 기본으로 한 여러 병태생리학적 인자들의 합산물로서, 정적 기계적 인자, 동적 기계적 인자, 척수 허혈, 그리고 신장과 연관된 손상 등이 병발하여 발생하게 된다. 정적 기계적 인자들부터 살펴보면, 척추체의 후면 골극이 커지면서, 척추 중심관이 좁아지게 되며, 선천적으로 좁은 척추 중심관(10-13 mm)이 동반되어 있는 경우 더 잘 발생하게 된다. 연령과 관련된 황색인대 비후 및 척추뼈 자체의 비후, 그리고 퇴행성 후만증 및 아탈구 등도 경추부 퇴행성 척수병증의 발생에 일조를 하게 되며, 동적 기계적 인자로는 정상적인 경추부의 굴곡-신전이 기존의 척수 압박에 의해 기시된 척수 손상을 악화시키게 된다. 즉, 굴곡 동작에서는 척수가 길이가 늘어남으로써 척추체의 골극에 의해 척수가 신장되게 되며, 신전 동작에서는 황색인대가 접히면서 척수가 황색인대와 척추체 골극 사이에서 끼이게 된다[53].
요추 혹은 경추통증을 유발하는 척추질환들 중 퇴행성 척추질환은 일생을 걸쳐 일어나는 '기계적 손상에 대한 생물학적 치유'의 끝없는 반복의 과정이기에 퇴행성 척추질환으로 인해 발생하는 척추통증은 어떤 한 순간의 병태생리학적 변화에 의한 일시적 현상이라기 보다는 추간판을 포함한 여러 척추 구조물들의 반복적인 손상, 치유 과정을 통해 일련의 연속적인 변화 과정 속에서 발현하게 된다. 이러한 퇴행성 척추질환은 일반적으로 추간판 변성 및 퇴행으로 시작되며, 변성된 추간판 내의 수핵이 섬유륜을 뚫고 나오는 추간판 탈출증과 이로 인한 신경근병증이 발생하게 되며, 이어서 추간판 간격이 좁아짐으로써 척추종판, 척추뼈 및 척추후관절 등에 퇴행 변화가 발생하게 되어 궁극적으로는 퇴행성 척추질환의 종착역에 해당하는 척추관 협착증에 이르게 된다. 척추의 퇴행성 변화와 실제 발현하는 척추통증 간에는 괴리가 있어 실제 발현된 척추통증의 정확한 발생 기전에 대해서 여전히 잘 설명되지 않는 경우도 있지만, 성공적인 치료를 위해서는 환자의 기나긴 병력에 귀를 기울이고 일상생활 자세, 작업자세 등에 대해서도 관심을 가져야 하며, 향후 치유되어 나가는 자연경과와 이를 방해할 수 있는 기계적 손상의 가능성에 대해서도 정확히 예측할 수 있어야 할 것이다.
본 논문은 비외상성 경추 및 요추의 통증 접근에 있어서 가장 기본적인 병태생리를 잘 요약하여 일목요연하게 설명을 하였다. 근골격계 질환의 병태생리에 가장 흔하게 언급되는 것이 퇴행성 변화와 과사용인데, 이러한 퇴행성 변화는 단순 노화와 달리 반복적인 손상과 치유의 반복 과정에 의한 것을 잘 설명하였다. 이러한 퇴행성 변화와 실제 통증은 괴리가 있지만 저자가 결론에 제시하였던 퇴행성 변화에 의한 치료는 단순 통증 조절 외에 자세한 병력 청취, 자세와 작업 환경 개선 등 환자의 전반적인 부분에 대한 접근이 필요하다는 내용은 많은 일선에서 진료를 보는 의사들이 다시금 새겨봐야 할 중요한 언급이라고 할 수 있겠다.
[정리: 편집위원회]
Figures and Tables
Figure 1
The degenerative cascade of L4-5 spinal segment. (A) Normal disc, (B) degeneration of the intervertebral disc, (C) herniated intervertebral disc, (D) disc space narrowing and facet joint degeneration, and (E) spinal stenosis with discovertebral degeneration and spondylosis.
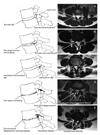
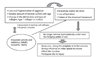
Figure 2
The spectrum of pathogenesis of the degenerative changes in the intervertebral disc. MMPS, matrix metalloproteinases; ADAMTS, a disintegrin and metalloproteinase with thrombospondin motifs, TIMPs, tissue inhibitors of metalloproteinases (From Choi YS. Asian Spine J 2009;3:39-44, according to the Creative Commons license) [15].
References
1. Bovim G, Schrader H, Sand T. Neck pain in the general population. Spine (Phila Pa 1976). 1994; 19:1307–1379.

2. Walker BF. The prevalence of low back pain: a systematic review of the literature from 1966 to 1998. J Spinal Disord. 2000; 13:205–217.

3. Von Korff M, Dworkin SF, Le Resche L, Kruger A. An epidemiologic comparison of pain complaints. Pain. 1988; 32:173–183.

4. Carroll LJ, Hogg-Johnson S, van der Velde G, Haldeman S, Holm LW, Carragee EJ, Hurwitz EL, Cote P, Nordin M, Peloso PM, Guzman J, Cassidy JD. Bone and Joint Decade 2000-2010 Task Force on Neck Pain and Its Associated Disorders. Course and prognostic factors for neck pain in the general population: results of the Bone and Joint Decade 2000-2010 Task Force on Neck Pain and Its Associated Disorders. Spine (Phila Pa 1976). 2008; 33:4 Suppl. S75–S82.
5. Lawrence RC, Helmick CG, Arnett FC, Deyo RA, Felson DT, Giannini EH, Heyse SP, Hirsch R, Hochberg MC, Hunder GG, Liang MH, Pillemer SR, Steen VD, Wolfe F. Estimates of the prevalence of arthritis and selected musculoskeletal disorders in the United States. Arthritis Rheum. 1998; 41:778–799.

6. Loney PL, Stratford PW. The prevalence of low back pain in adults: a methodological review of the literature. Phys Ther. 1999; 79:384–396.

7. Schiøttz-Christensen B, Nielsen GL, Hansen VK, Schodt T, Sorensen HT, Olesen F. Long-term prognosis of acute low back pain in patients seen in general practice: a 1-year prospective follow-up study. Fam Pract. 1999; 16:223–232.

8. Van den Hoogen HJ, Koes BW, Deville W, van Eijk JT, Bouter LM. The prognosis of low back pain in general practice. Spine (Phila Pa 1976). 1997; 22:1515–1521.

9. Stanton TR, Henschke N, Maher CG, Refshauge KM, Latimer J, McAuley JH. After an episode of acute low back pain, recurrence is unpredictable and not as common as previously thought. Spine (Phila Pa 1976). 2008; 33:2923–2928.

10. Jarvik JG, Deyo RA. Diagnostic evaluation of low back pain with emphasis on imaging. Ann Intern Med. 2002; 137:586–597.

11. Jeong GK, Bendo JA. Spinal disorders in the elderly. Clin Orthop Relat Res. 2004; (425):110–125.

12. Kirkaldy-Willis WH, Wedge JH, Yong-Hing K, Reilly J. Pathology and pathogenesis of lumbar spondylosis and stenosis. Spine (Phila Pa 1976). 1978; 3:319–328.

13. Boden SD, Davis DO, Dina TS, Patronas NJ, Wiesel SW. Abnormal magnetic-resonance scans of the lumbar spine in asymptomatic subjects: a prospective investigation. J Bone Joint Surg Am. 1990; 72:403–408.

14. Jensen MC, Brant-Zawadzki MN, Obuchowski N, Modic MT, Malkasian D, Ross JS. Magnetic resonance imaging of the lumbar spine in people without back pain. N Engl J Med. 1994; 331:69–73.

16. Schwarzer AC, Aprill CN, Derby R, Fortin J, Kine G, Bogduk N. The prevalence and clinical features of internal disc disruption in patients with chronic low back pain. Spine (Phila Pa 1976). 1995; 20:1878–1883.

17. Zhang YG, Guo TM, Guo X, Wu SX. Clinical diagnosis for discogenic low back pain. Int J Biol Sci. 2009; 5:647–658.

18. Hicks GE, Morone N, Weiner DK. Degenerative lumbar disc and facet disease in older adults: prevalence and clinical correlates. Spine (Phila Pa 1976). 2009; 34:1301–1306.
19. Takahashi K, Aoki Y, Ohtori S. Resolving discogenic pain. Eur Spine J. 2008; 17:Suppl 4. 428–431.

20. García-Cosamalón J, del Valle ME, Calavia MG, Garcia-Suarez O, Lopez-Muniz A, Otero J, Vega JA. Intervertebral disc, sensory nerves and neurotrophins: who is who in discogenic pain? J Anat. 2010; 217:1–15.

21. Adams MA, Freeman BJ, Morrison HP, Nelson IW, Dolan P. Mechanical initiation of intervertebral disc degeneration. Spine (Phila Pa 1976). 2000; 25:1625–1636.

22. Veres SP, Robertson PA, Broom ND. The morphology of acute disc herniation: a clinically relevant model defining the role of flexion. Spine (Phila Pa 1976). 2009; 34:2288–2296.
23. Veres SP, Robertson PA, Broom ND. The influence of torsion on disc herniation when combined with flexion. Eur Spine J. 2010; 19:1468–1478.

24. Manchikanti L, Falco FJ, Benyamin RM, Caraway DL, Deer TR, Singh V, Hameed H, Hirsch JA. An update of the syste-matic assessment of mechanical lumbar disc decompression with nucleoplasty. Pain Physician. 2013; 16:2 Suppl. SE25–SE54.
25. Carragee EJ, Don AS, Hurwitz EL, Cuellar JM, Carrino JA, Herzog R. 2009 ISSLS Prize Winner Does discography cause accelerated progression of degeneration changes in the lumbar disc: a ten-year matched cohort study. Spine (Phila Pa 1976). 2009; 34:2338–2345.

26. Hughes SP, Freemont AJ, Hukins DW, McGregor AH, Roberts S. The pathogenesis of degeneration of the intervertebral disc and emerging therapies in the management of back pain. J Bone Joint Surg Br. 2012; 94:1298–1304.

27. Bogduk N. On the definitions and physiology of back pain, referred pain, and radicular pain. Pain. 2009; 147:17–19.

28. Moore RJ, Vernon-Roberts B, Fraser RD, Osti OL, Schembri M. The origin and fate of herniated lumbar intervertebral disc tissue. Spine (Phila Pa 1976). 1996; 21:2149–2155.

29. Kalichman L, Hunter DJ. The genetics of intervertebral disc degeneration: familial predisposition and heritability estimation. Joint Bone Spine. 2008; 75:383–387.

30. Cornefjord M, Olmarker K, Rydevik R, Nordborg C. Mechanical and biochemical injury of spinal nerve roots: a morphological and neurophysiological study. Eur Spine J. 1996; 5:187–192.

31. Olmarker K, Rydevik B, Nordborg C. Autologous nucleus pulposus induces neurophysiologic and histologic changes in porcine cauda equina nerve roots. Spine (Phila Pa 1976). 1993; 18:1425–1432.

32. Iwabuchi M, Rydevik B, Kikuchi S, Olmarker K. Effects of anulus fibrosus and experimentally degenerated nucleus pulposus on nerve root conduction velocity: relevance of previous experimental investigations using normal nucleus pulposus. Spine (Phila Pa 1976). 2001; 26:1651–1655.

33. Kayama S, Olmarker K, Larsson K, Sjogren-Jansson E, Lindahl A, Rydevik B. Cultured, autologous nucleus pulposus cells induce functional changes in spinal nerve roots. Spine (Phila Pa 1976). 1998; 23:2155–2158.

34. Olmarker K, Brisby H, Yabuki S, Nordborg C, Rydevik B. The effects of normal, frozen, and hyaluronidase-digested nucleus pulposus on nerve root structure and function. Spine (Phila Pa 1976). 1997; 22:471–475.

35. Igarashi T, Kikuchi S, Shubayev V, Myers RR. 2000 Volvo Award winner in basic science studies: exogenous tumor necrosis factor-alpha mimics nucleus pulposus-induced neuropathology Molecular, histologic, and behavioral comparisons in rats. Spine (Phila Pa 1976). 2000; 25:2975–2980.

36. Aoki Y, Rydevik B, Kikuchi S, Olmarker K. Local application of disc-related cytokines on spinal nerve roots. Spine (Phila Pa 1976). 2002; 27:1614–1617.

37. Murata Y, Onda A, Rydevik B, Takahashi K, Olmarker K. Distribution and appearance of tumor necrosis factor-alpha in the dorsal root ganglion exposed to experimental disc herniation in rats. Spine (Phila Pa 1976). 2004; 29:2235–2241.

38. Olmarker K, Larsson K. Tumor necrosis factor alpha and nucleus-pulposus-induced nerve root injury. Spine (Phila Pa 1976). 1998; 23:2538–2544.
39. Olmarker K, Rydevik B. Selective inhibition of tumor necrosis factor-alpha prevents nucleus pulposus-induced thrombus formation, intraneural edema, and reduction of nerve conduction velocity: possible implications for future pharmacologic treatment strategies of sciatica. Spine (Phila Pa 1976). 2001; 26:863–869.

40. Kawakami M, Tamaki T, Hashizume H, Weinstein JN, Meller ST. The role of phospholipase A2 and nitric oxide in pain-related behavior produced by an allograft of intervertebral disc material to the sciatic nerve of the rat. Spine (Phila Pa 1976). 1997; 22:1074–1079.

41. Brisby H, Byrod G, Olmarker K, Miller VM, Aoki Y, Rydevik B. Nitric oxide as a mediator of nucleus pulposus-induced effects on spinal nerve roots. J Orthop Res. 2000; 18:815–820.

42. Olmarker K, Byrod G, Cornefjord M, Nordborg C, Rydevik B. Effects of methylprednisolone on nucleus pulposus-induced nerve root injury. Spine (Phila Pa 1976). 1994; 19:1803–1808.

43. Onda A, Yabuki S, Kikuchi S. Effects of neutralizing antibodies to tumor necrosis factor-alpha on nucleus pulposus-induced abnormal nociresponses in rat dorsal horn neurons. Spine (Phila Pa 1976). 2003; 28:967–972.

44. Karppinen J, Korhonen T, Malmivaara A, Paimela L, Kyllonen E, Lindgren KA, Rantanen P, Tervonen O, Niinimaki J, Seitsalo S, Hurri H. Tumor necrosis factor-alpha monoclonal antibody, infliximab, used to manage severe sciatica. Spine (Phila Pa 1976). 2003; 28:750–753.

45. Karppinen J, Malmivaara A, Kurunlahti M, Kyllonen E, Pieni-maki T, Nieminen P, Ohinmaa A, Tervonen O, Vanharanta H. Periradicular infiltration for sciatica: a randomized controlled trial. Spine (Phila Pa 1976). 2001; 26:1059–1067.
46. Carette S, Leclaire R, Marcoux S, Morin F, Blaise GA, St-Pierre A, Truchon R, Parent F, Levesque J, Bergeron V, Montminy P, Blanchette C. Epidural corticosteroid injections for sciatica due to herniated nucleus pulposus. N Engl J Med. 1997; 336:1634–1640.

47. Buttermann GR. Treatment of lumbar disc herniation: epidural steroid injection compared with discectomy: a prospective, randomized study. J Bone Joint Surg Am. 2004; 86:670–679.
48. Freemont AJ. The cellular pathobiology of the degenerate intervertebral disc and discogenic back pain. Rheumatology (Oxford). 2009; 48:5–10.

49. Parke WW. Correlative anatomy of cervical spondylotic myelopathy. Spine (Phila Pa 1976). 1988; 13:831–837.

50. Holt S, Yates PO. Cervical spondylosis and nerve root lesions: incidence at routine necropsy. J Bone Joint Surg Br. 1966; 48:407–423.
51. Rahim KA, Stambough JL. Radiographic evaluation of the degenerative cervical spine. Orthop Clin North Am. 1992; 23:395–403.

52. Jarvik JJ, Hollingworth W, Heagerty P, Haynor DR, Deyo RA. The longitudinal assessment of imaging and disability of the back (LAIDBack) study: baseline data. Spine (Phila Pa 1976). 2001; 26:1158–1166.

53. Fehlings MG, Skaf G. A review of the pathophysiology of cervical spondylotic myelopathy with insights for potential no-vel mechanisms drawn from traumatic spinal cord injury. Spine (Phila Pa 1976). 1998; 23:2730–2737.

54. Al-Mefty O, Harkey HL, Marawi I, Haines DE, Peeler DF, Wilner HI, Smith RR, Holaday HR, Haining JL, Russell WF, Harrison B, Middleton TH. Experimental chronic compressive cervical myelopathy. J Neurosurg. 1993; 79:550–561.

55. Henderson FC, Geddes JF, Vaccaro AR, Woodard E, Berry KJ, Benzel EC. Stretch-associated injury in cervical spondylotic myelopathy: new concept and review. Neurosurgery. 2005; 56:1101–1113.




 PDF
PDF ePub
ePub Citation
Citation Print
Print



 XML Download
XML Download