Abstract
Background and Objectives
Subjects and Method
Results
Conclusion
ACKNOWLEDGMENTS
Notes
Author Contribution
Conceptualization: Sang Chul Lim. Data curation: Hyung Chae Yang. Formal analysis: Hyung Chae Yang. Funding acquisition: Hyung Chae Yang. Investigation: Jong Yuap Seong. Methodology: Jong Min Park. Project administration: Hyung Chae Yang. Resources: Su Jeong Jeong. Software: Jisu Kim. Supervision: Sang Chul Lim. Validation: Chung Man Sung. Visualization: Su Jeong Jeong. Writing—original draft: Jong Yuap Seong. Writing—review & editing: Su Jeong Jeong.
REFERENCES
Fig. 1.
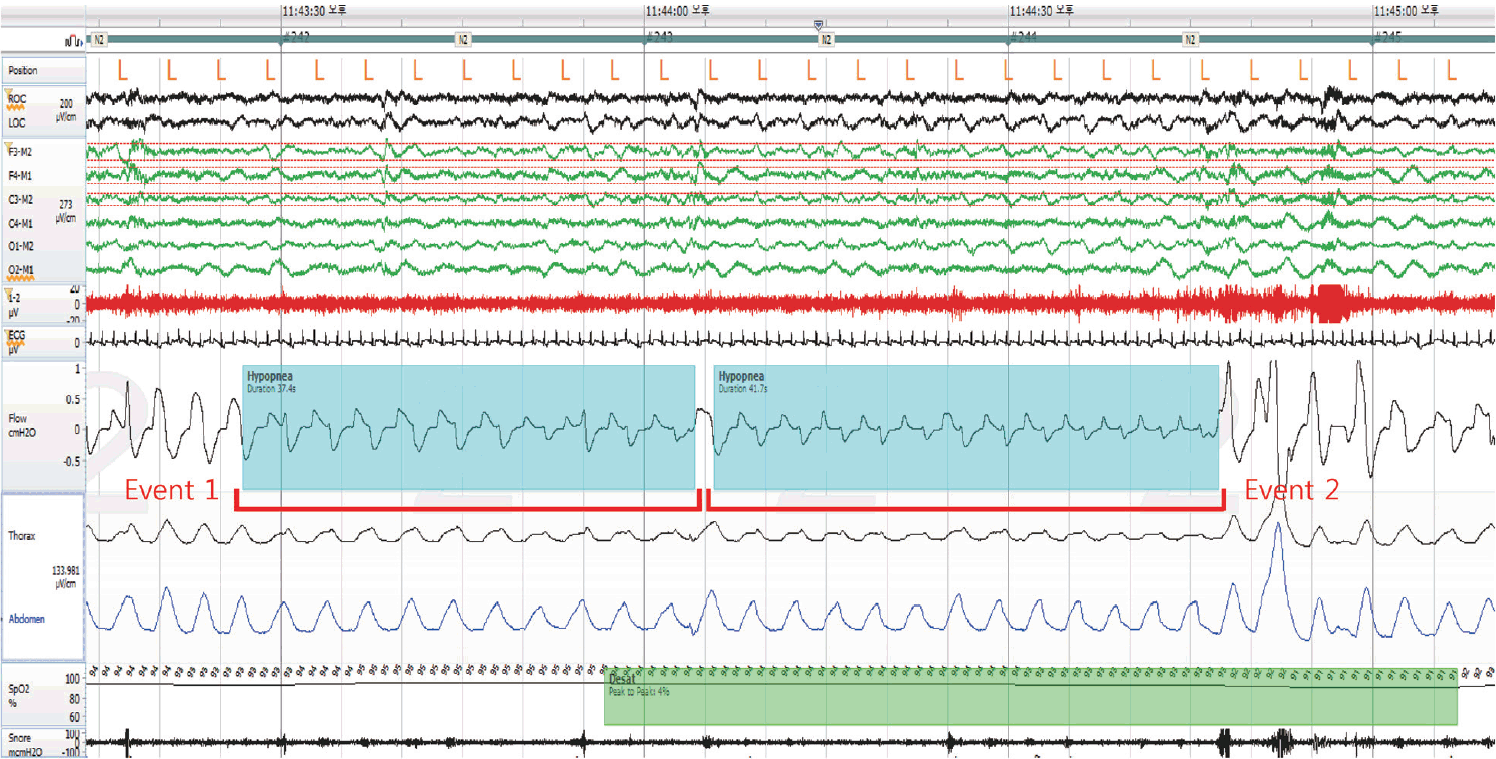
Table 1.
Table 2.
| Category | Auto scoring (n=20) | Manual scoring (n=20) | p-value* |
|---|---|---|---|
| TST (min) | 340.8 (298.0-393.9) | 299.3 (235.4-379.1) | 0.001 |
| Sleep latency (min) | 17.9 (5.3-33.9) | 18.0 (9.4-31.3) | 0.619 |
| REM latency (min) | 75.8 (5.4-109.3) | 139.0 (85.9-219.3) | 0.001 |
| WASO (min) | 67.3 (34.5-104.4) | 104.3 (35.8-151.2) | 0.001 |
| Sleep efficiency (%) | 79.4 (67.5-85.4) | 68.4 (54.1-84.4) | 0.001 |
| Sleep stage N1 | 3.2 (2.2-4.8) | 21.0 (11.0-37.0) | <0.001 |
| Sleep stage N2 | 54.8 (49.0-67.8) | 48.1 (41.5-53.2) | 0.015 |
| Sleep stage N3 | 19.0 (12.9-27.8) | 12.0 (6.1-21.3) | 0.000 |
| Sleep stage REM | 17.6 (11.5-23.5) | 17.2 (10.1-21.1) | 0.249 |
| AI (events/hours) | 3.3 (1.2-12.6) | 3.4 (1.1-8.1) | 0.164 |
| HI (events/hours) | 12.9 (5.5-21.2) | 8.9 (3.6-16.4) | 0.001 |
| AHI (events/hours) | 17.9 (7.9-34.1) | 13.6 (5.6-26.9) | <0.001 |
| RDI (events/hours) | 17.9 (7.9-34.1) | 14.0 (5.6-26.9) | <0.001 |
Table 3.
| Category | Manual scoring (n=20) | Corrected scoring (n=20) | p-value* |
|---|---|---|---|
| TST (min) | 299.3 (235.4-379.1) | 282.7 (222.8-368.5) | 0.024 |
| Sleep latency (min) | 18.0 (9.4-31.3) | 20.3 (11.6-31.1) | 0.807 |
| REM latency (min) | 139.0 (85.9-219.3) | 92.7 (57.0-146.8) | 0.009 |
| WASO (min) | 104.3 (35.8-151.2) | 116.0 (45.4-166.2) | 0.013 |
| Sleep efficiency (%) | 68.4 (54.1-84.4) | 68.1 (50.4-84.7) | 0.099 |
| Sleep stage N1 | 21.0 (11.0-37.0) | 2.3 (1.6-3.2) | <0.001 |
| Sleep stage N2 | 48.1 (41.5-53.2) | 56.4 (51.3-68.0) | 0.005 |
| Sleep stage N3 | 12.0 (6.1-21.3) | 20.2 (14.9-28.9) | <0.001 |
| Sleep stage REM | 17.2 (10.1-21.1) | 15.9 (12.5-22.3) | 0.749 |
| AI (events/hours) | 3.4 (1.1-8.1) | 3.2 (0.8-9.9) | 1.000 |
| HI (events/hours) | 8.9 (3.6-16.4) | 10.7 (4.4-19.3) | 0.026 |
| AHI (events/hours) | 13.6 (5.6-26.9) | 15.5 (5.8-29.0) | 0.170 |
| RDI (events/hours) | 14.0 (5.6-26.9) | 15.5 (5.8-29.0) | 0.140 |
Table 4.
P1: Patient #1, P2: Patient #2, Aauto: awakening analyzed by auto scoring, N1auto: sleep stage N1 analyzed by auto scoring, N2auto: sleep stage N2 analyzed by auto scoring, N3auto: sleep stage N3 analyzed by auto scoring, Rauto: sleep stage REM analyzed by auto scoring, AManual: awakening analyzed by manual scoring, N1Manual: sleep stage N1 analyzed by manual scoring, N2Manual: sleep stage N2 analyzed by manual scoring, N3Manual: sleep stage N3 analyzed by manual scoring, RManual: sleep stage REM analyzed by manual scoring. REM: rapid eye movement




 PDF
PDF Citation
Citation Print
Print



 XML Download
XML Download