Abstract
Congestive heart failure (CHF) is a growing epidemiologic and clinical problem, and is increasing in incidence, prevalence and mortality. Therefore, the optimal treatment of heart failure (HF) is important to reduce hospitalization and mortality. In the treatment of CHF, diuretics are the first-line drug treatment for patients with fluid retention and are necessary to relieve symptoms but cannot halt progression or improve the prognosis of CHF. Angiotensin-converting enzyme inhibitors, beta-adrenergic receptor antagonists and mineralocorticoid/aldosterone receptor antagonist therapy have been shown to decrease mortality and progression of CHF and should be used early in HF with reduced ejection fraction. Angiotensin receptor antagonists are recommended in patients with current or prior symptoms who are angiotensin-converting enzyme inhibitor intolerant, unless contraindicated, to reduce morbidity and mortality. However, no treatment has been shown convincingly to reduce morbidity and mortality in patients with HF with preserved ejection fraction. Adequate treatment of hypertension and myocardial ischemia is also considered to be important, as is control of the ventricular rate in HF with preserved ejection fraction. For chronic HF with reduced ejection fraction, ivabradine and angiotensin receptor-neprilysin inhibition have been tested and may be used in evidence-based medicine in the near future. This review presents the evidence base for current drug treatments and their practical implications in chronic HF.
심부전은 심장의 기능적 혹은 구조적 이상으로 심실의 혈액 충만 혹은 심실의 혈액의 구출에 이상이 발생하여 울혈 혹은 피로 등으로 발현하는 임상 증후군이다[1]. 특히, 만성심장질환자 증가, 고령인구의 급격한 증가와 치료기술의 발달로 심부전 발생이 증가 추세에 있으며 심부전 환자는 임상양상으로 반복적인 입원 및 응급실 방문, 장기적인 외래치료의 과정의 악순환을 반복하여 의학적인 측면뿐만 아니라 사회 경제적인 측면에서도 매우 중요한 질환으로 알려져 있다[23]. 그러므로 심부전의 올바른 약물치료를 통한 적절한 진료는 장기적인 측면 즉, 장기적인 예후와 삶의 질 측면에서 매우 중요하다. 본 논고에서는 만성심부전의 경구용 약제를 사용한 약물치료에 대해 기술하고자 한다.
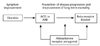
과거 심부전의 병태 생리적 기전을 심근 수축력의 저하와 이로 인한 수분 저류(울혈)로 생각하여 강심제나 이뇨제의 사용이 치료의 근간이었다. 그러나 이러한 치료는 환자의 임상증상은 호전시켰으나 장기적인 예후를 개선시키지는 못하였다. 레닌-안지오텐신-알도스테론 시스템 (renin-aniotensin-aldosterone system)이나 교감신경계 (sympathetic nervous system)의 활성화와 같은 신경-호르몬(neuro-hormone)의 활성이 중요한 기전으로 밝혀지면서 치료에서도 많은 변화와 발전이 있었다[456]. 또한, 심부전 상태는 만성 안정형 심부전에서 급성 악화로 인해 응급실을 경유하여 급성 비대상성 심부전으로 입원하고 퇴원 후 초기 시기를 거쳐서 안정화 후에 만성심부전 상태로 이행된다 (Figure 1) [17]. 이는 심부전의 원인 및 임상상태에 따라 약물치료의 우선 순위 및 원칙이 달라 각 시기에 맞는 적절한 치료가 필요하다[45].
심부전치료에서 약물치료는 크게 두 가지 임상양상으로 나누어 생각할 수 있는데, 첫째로는 불안정한 심부전의 경우에는 환자를 임상적으로 안정시키고 여러 신체기관의 관류를 개선하고 심실 충만압을 적정수준으로 유지시키는 것을 목표로 한다. 둘째로는 이렇게 안정화된 만성심부전의 치료는 생존을 증가시키고 증상의 개선을 목표로 한다[456]. 따라서 지금까지 알려진 대표적인 약물요법의 특성을 이해하는 것이 중요하다. 현재까지 좌심실 수축기능 보존 심부전 (heart failure with preserved ejection fraction) 환자를 대상으로 대규모 연구들은 아직까지 생존율 개선 효과가 확실히 증명된 약은 없다. 하지만 좌심실 수축기능 저하 심부전 감소 심부전(heart failure with reduced ejection fraction, 혹은 수축기 심부전)에서 사망의 위험을 줄일 수 있는 약물
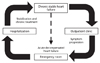
로는 안지오텐신 전환효소 저해제(angiotensin converting enzyme inhibitor, ACEI), 안지오텐신II 수용체 길항제 (angiotensin II receptor blocker, ARB), 베타수용체 차단제, spironolactone 등이 있으며, 이뇨제나 디곡신은 유병률의 개선 또는 증상의 호전을 기대할 수 있는 약물들이다(Figure 2) [4567]. 그러므로 심부전 약물치료를 적용할 때는 각 치료약물들이 생존율의 개선효과가 있는지, 그렇지 않다면 유병률을 낮출 수는 있는지, 증상의 호전만을 기대할 수 있는지를 잘 이해하고 이를 임상에 적용해야 한다.
이뇨제는 울혈상태가 있는 경우에만 사용하고, 체액저류로 인한 증상을 완화시켜 주는데 효과적이다. 이때 염분과 수분의 제한이 적절하게 이루어지지 않는다면 이뇨제의 사용으로 심한 전해질 불균형, 특히 저나트륨혈증이 유발될 수 있다[8]. 이뇨제를 처음 사용하는 경우에나 고령인 경우에는 thiazide계를 사용할 수 있으나 염분배설 효과가 이론적으로는 1주일 이내에 사라지게 되며 이후에는 혈관저항감소에 의한 혈압 조절 효과가 나타나게 된다. 따라서 체액량 조절 목적으로는 고리작용이뇨제(loop diuretics)를 사용하는 것이 적절하다[9]. 하지만 thiazide계열 이뇨제를 고리작용이뇨제와 병합하는 것이 원위 세뇨관에서 염분 재흡수를 억제함으로써 고리작용이뇨제 만으로는 이뇨효과가 불충분한 환자에서 보다 효과적인 이뇨효과를 얻을 수 있다[9]. 이뇨제의 사용 시에는 반드시 전해질을 주기적으로 확인을 해야 하며 특히 급속한 이뇨가 있는 경우에는 전해질을 함께 보충해 주면서 치료한다. 울혈성 증상이 해결된 경우에는 이뇨제의 사용을 줄이거나 중지하여야 한다. 이뇨제를 사용하는 경우 이미 언급한 전해질 장애뿐 아니라 고혈당증, 인슐린 저항성, 비케톤성 고삼투압 상태에 빠지기 쉽다. 또한 이뇨제는 LDL (low density lipoprotein) 콜레스테롤, VLDL (very low density lipoprotein) 콜레스테롤, 총콜레스테롤 중성지방을 포함한 지질대사의 이상을 초래 할 수 있으며, furosemide 등의 약들은 청각장애를 유발 시킬 수 있다[10]. 고리작용 이뇨제는 사구체에서 신세뇨관으로 배설이 되어 신세뇨관 내강 안에 존재하여야 효과를 나타낸다. 따라서 일정 수준의 역치를 넘어서야 비로서 이뇨작용을 나타내며 역치에 미치지 못하는 낮은 용량에서는 효과가 전혀 없다. 일정 수준까지는 용량을 증량하였을 때 이뇨 효과가 더 증가하는 용량 의존적 효과를 보이지만 최대 이뇨효과를 보이는 농도에 도달한 이후에는 이뇨 효과가 더 이상 증가하지 않는 'ceiling effect'를 보인다[8]. Furosemide의 경우 초기 용량은 20-40 mg을 하루 1-2회 투여하며(torsemide는 10-20 mg 하루 한번) 통상적인 용량은 240 mg을 넘지 않는다(Table 1) [45]. 신장기능 저하로 인해 소변이 배출되지 않는 경우 최대 400-600 mg까지도 사용할 수는 있지만 대개 thiazide 계열 이뇨제와 병합요법을 하거나 한외여과를 시행하는 것이 일반적이다.
디곡신은 심부전 환자에서 가장 오래 전부터 사용되어 온 치료약물로서 좌심실 수축기능 향상, 교감신경계의 활성도 저하 등의 효과를 통해 증상을 완화시키고 운동능력을 향상시킨다[11]. 특히 심방세동을 동반한 심부전 환자에서 심박동수의 조절 및 효과적인 좌심실의 혈류 충만을 위해 필수적인 약제로 사용되고 있다[12]. RADIANCE (Randomized Assessment of Digoxin on Inhibitors of the ANgiotensin Converting Enzyme) 연구나 PROVED (Prospective Randomized study Of Ventricular failure and the Efficacy of Digoxin) 연구에서는 디곡신을 투여 중이던 환자들에서 이의 투여를 중단했을 때 증상이 악화된다는 것이 확인되었고, DIG (Digitalis Investigators Group) 연구에서는 디곡신 투여가 이미 이뇨제와 ACEI를 사용 중이고 정상 동율동을 보이는 심부전 환자들에서도 증상을 호전시킨다고 보고하였다[456]. 그러나 좌심실 수축기능 저하가 있는 환자라도 증상이 없는 경우에는 디곡신의 효과가 명확히 밝혀져 있지 않고, 아직까지 디곡신이 심부전 환자들의 전체 생존율을 높인다는 보고는 없다. 따라서 현재 심부전 환자에서 디곡신 투여가 고려되는 경우는 심방세동을 동반한 울혈성 심부전 환자에서 맥박수 조절을 위해서 투여되는 경우, 그리고 정상 동률동이면서 다른 심부전 약제를 사용 중에도 심부전 증상이 지속되는 환자에서 가장 낮은 용량인 0.125 mg이 가장 합리적인 용량으로 사용되며[45], 디곡신 중독증이 의심되는 경우(환자가 구토, 식욕부진, 혼돈, 시각 이상을 보이거나, 또는 부정맥이 있을 때)에는 혈청 디곡신 농도를 측정한다. 적절한 치료 용량은 0.8-1.2 mg/dL로 알려져 있다.
ACEI는 좌심실 수축기능 감소 심부전 환자의 증상을 호전시키며, 사망률과 재입원율을 낮춘다[1314]. 이러한 효과는 이전에 심부전이 증상이 있었거나, 현재 증상이 있는 경우, 증상의 중증도 및 관상동맥질환 동반 유무와 상관없이 모두 확인되었다[1516]. 따라서 검사를 통해 좌심실 수축기능 감소가 확인된 심부전 환자에서 금기증이 없다면 ACEI를 사용해야 하고, 심혈관 사건을 줄인 것으로 보고되었던 목표용량까지 가능하면 올려야 한다(Table 2) [45]. 이전에 투약 중 심한 혈관부종이 발생한 적이 있었거나 임신을 하였을 경우에는 절대 투여하지 말아야 하며, 수축기 혈압이 80 mmHg 이하로 매우 낮거나 크레아티닌이 3 mg/dL 이상, 양측 신동맥 협착 혹은 혈청 칼륨이 5 mEq/L 이상인 경우에는 투약을 매우 조심스럽게 결정해야 한다. 초기에는 저 용량부터 시작하여 서서히 증량해야 하며, 투약 1-2주 이내에는 혈청 칼륨을 포함한 신기능검사를 해야 한다[45]. 약과 관련된 부작용은 대부분 안지오텐신 전환효소 억제에 따른 안지오텐신 억제와 키닌 분해 억제와 관련이 있다. 기침이 가장 흔하고, 일부에서는 심한 혈관부종이 발생할 수 있다.
ARB는 ACEI의 제한점, 즉 레닌-안지오텐신 계를 차단하더라도 다른 시스템(non-ACE)을 통해 안지오텐신 II가 지속적으로 생성되며, 키닌 분해를 억제하여 기침과 혈관부종의 부작용을 발생시키는 두 가지 제한 점을 이론적으로 극복할 수 있는 레닌-안지오텐신계 차단제이다[1617]. ARB를 이용한 임상 연구의 경험은 ACEI보다는 적지만, 최근에 시행되었던 여러 임상연구에서 ARB를 사용하였을 때 예상하였던 혈역학적, 신경호르몬과 임상학적 개선 효과는 일정하게 우수하였다. ACEI 사용 후 대체 사용된 valsartan (Valsartan Heart Failure Trial, Val-HeFT 연구)과 candesartan (Candesartan in Heart Failure Assessment of Reduction in Mortality and Morbidity, CHARM 연구)은 환자의 입원율과 사망률을 감소시켜 ARB가 ACEI를 대체 할 수 있는 임상적 효과를 증명하였다[18]. 초기에 사용하는 경우에는 적은 용량에 서 시작하여 목표 용량까지 증량을 해 나가야 하며 이때 생길 수있는 고칼륨혈증과 신기능 이상에 대한 대처는 ACEI와 유사하다(Table 2) [45].
심부전 병태생리에 있어서 알도스테론은 자율신경계의 균형을 저해시키며 콜라겐 합성을 증가시켜 심혈관계의 재형성에 관여하는 중요한 역할을 담당하는데, 이는 레닌-안지오텐신 계통의 차단만으로는 억제가 부족하다[19]. 따라서 염류코르티코이드(mineralocorticoid) 길항제는 심부전 치료에 있어서 기존의 ACEI, ARB와 베타 수용체 차단제를 사용하고 있는 환자에 부가적으로 사용해야 한다[45]. 약제로는 국내에서 사용하고 있지 않은 eplerenone (Inspra)과 spironolactone (Aldactone)이 있으며 심부전의 임상 연구는 New York Heart Association (NYHA) IIIIV 환자를 대상으로 한 RALES (Randomized Aldactone Evaluation Study) 연구와 NYHA II-II 환자를 대상으로 한 EMPHASIS-HF (Eplerenone in Mild patients Hospitalization and Survival Study in Heart Failure) 연구에서 대조군과 비교하여 심혈관 사망률과 입원율을 감소시키는 효과를 나타내어 수축기 수축기능 감소 심부전 환자에서 광범위한 사용이 권장된다[4520]. 이 약제는 초기 혈청 Cr <2.0 mg/dL이거나 최근에 악화된 소견이 없는 Cr <2.5 mg/dL이면서, 심한 칼륨혈증의 기왕력이 없는 혈청 K+ <5.0 mEq/dL인 경우에 사용한다. Spironolactone은 하루 12.5-25 mg의 용량으로 시작하고 50 mg까지 증량할 수 있다[45]. 남성들에게서는 spironolactone이 유방비대와 유방
의 통증을 유발시킬 수 있다.
베타수용체 차단제가 경증으로부터 중증의 심부전에 이르기까지 심부전에 의한 사망률을 감소시킬 수 있음은 US Carvedilol (Effect of Carvedilol on Morbidity and Mortality in Patients with Chronic Heart Failure), CIBISII (Randomized Cardiac Insufficiency Bisoprolol Study II), MERIT-HF (Metoprolol Extended-Release Randomized Intervention Trial in Heart Failure), COPERNICUS (Carvedilol Prospective Randomized Cumulative Survival), SENIOR (Study of the Effects of Nebivolol Intervention on Outcomes and Rehospitalisation in Seniors With Heart Failure) 연구 등의 20여 개의 대규모 임상연구를 통해 2만여 명의 환자에서 효과가 입증된 약제이다[45]. 베타수용체 차단제의 장기적 치료로 환자의 증상을 호전시킬 뿐 아니라, 사망률과 입원율을 감소시킬 수 있다[2122]. 이는 좌심실 수축 기능 감소 심부전 환자 중 안정 상태에 있으면서 금기증이 없고 약을 잘 견디면 되도록 이른 시기에 처방해야 하며 증상이 경미하고 다른 치료로 증상이 호전되더라도 베타 차단제는 질병 초기에 생명 연장을 위하여 반드시 처방해야 한다[45]. 베타수용체 차단제를 사용할 때에는 반드시 고용량의 ACEI 혹은 ARB를 사용할 필요가 없으며 저용량의 ACEI 를 사용하고 있다고 해도 가능한 빨리 베타수용체 차단제를 사용하는 것이 좋다. 하지만 현재 울혈증상이 있거나 그로 인하여 호흡곤란이 있는 환자에서는 베타수용체 차단제가 수분의 저류를 악화시킬 수 있으므로 증상이 호전된 안정된 상태에서 사용해야 한다. 현재까지 4가지 약제(bisoprolol, sustained-released metoprolol, carvediol, nebivolol)만이 효과가 입증되어 이들 약제 사용을 권고하고 있다(Table 3) [45]. 베타수용체 차단제는 처음에는 carvediol 3.125 mg, metoprolol 12.5 mg, bisoprolol 1.25 mg, nebivilol 1.25 mg의 낮은 용량에서 시작하여 1-4주 간격을 두고 두 배씩 증량하여 목표 용량에 도달하도록 사용한다. 낮은 베타수용체 차단제의 용량에서는 아직도 심부전에 대한 효과가 입증되지 않았기 때문에 가능한 목표용량에 도달하도록 한다. 베타수용체 차단제의 사용과 관련해서 생기는 피로감 및 무기력증은 시간이 지나면 자연히 호전되는 경향이 많으므로 특별한 치료가 필요 없는 경우가 많다. 서맥과 방실차단이 생기는 경우에는 임상적으로 큰 문제가 없다면 베타수용체 차단제의 사용을 지속하며 임상증상이 동반되는 경우에는 용량을 줄이거나 아니면 사용중인 다른 약제와의 상호작용을 고려하여 판단한다[22].
Ivabradine은 동결절(sinus node)에서 If channel을 억제하여 동율동에서 맥박수를 떨어뜨리는 작용의 약제로 동율동인 환자에서만 맥박수를 감소시키는 효과가 있다. Ivabradine은 심혈관계 다른 채널에는 작용하지 않기 때문에 베타차단제와는 다르게 좌심실 구혈률 감소 심부전 환자에서 심근 수축력이나 심장내 전도에 영향을 미치지 않고 If channel에만 작용하여 맥박수만을 감소시킨다. SHIFT 연구는 좌심실 구혈율 35% 이하, 맥박수가 70회 이상인 동율동의 NYHA II-IV인 심부전 환자 6,588명을 대상으로 표준 심부전 치료를 받는 환자들에게서 ivabradine(최대용량: 하루 7.5 mg 두 번 복용) 혹은 대조약을 사용하여 평균 23개월 추적 관찰한 결과 일차종결점(primary endpoint)인 심혈관계 사망률 혹은 심부전의 악화로 인한 입원율이 18%(P<0.0001) 감소하였고, 이차 종결점 중 심부전 악화로 인한 사망률과 심부전으로 인한 사망률이 각각 26%(P<0.0001)와 26%(P<0.014) 감소시켰다[23]. 그러므로 Ivabradine은 좌심실 구혈률 감소 심부전에서 맥박수 분당 70회 이상이면서 다른 심부전 약물치료에도 지속되는 NYHA II-IV인 사용할 수 있는 효과적인 약제로 판단된다[524].
Vasopressin antagonist (Tolvaptane)는 용적과부하가 동반된 저나트륨혈증에서 나트륨 농도를 상승시켜 유용하다[25]. 그러므로, 심부전 환자에서 동반된 저나트륨혈증의 치료제로서 유용할 것으로 생각되나 심부전 환자에서의 장기치료가 생존율을 개선하지는 못하였다. 기존의 이뇨제와는 작용기전이 다르기 때문에 다른 이뇨제에서 체액 저류가 개선되지 않는 이뇨제 저항성이 동반된 심부전 환자에서 vasopressin antagonist의 유용성이 기대된다[26].
Neprilysin이라 불리는 중성 엔도펩티다제는 나트륨 이뇨펩티드, 브라디키닌등 여러 내인성 혈관 활성 펩타이드를 저하시킨다. Neprilysin의 억제는 이들 물질의 농도를 증가시켜, 혈관 수축, 나트륨 저류, 비정상적인 적응을 일으키는 신경 호르몬의 과활성화를 막는다. LCZ696는 최초의 안지오텐신 II 수용체와 neprilysin의 이중 저해제이며, neprilysin 억제제 sacubitril (AHU377)와 ARB의 Valsartan의 작용기를 가지고 있는 angiotensin receptor neprilysin inhibition 계열 약제로 심각한 혈관부종의 위험을 최소화하도록 설계되었다[27]. PARADIGM-HF라는 대규모 임상 결과로, 심장 박출계수 40% 이하인 NYHA II, III, IV 등급의 심부전 환자 총 8,442명을 대상으로 ACEI인 enalapril 1일 2회 10 mg군과 LCZ696 1일 2회 200 mg을 비교한 결과 enalapril군 대비 LCZ696군이 심혈관원인 사망 위험도 20%, 심부전 입원율 21%, 모든 원인으로 인한 사망 위험도 16%를 감소시킨 것으로 나타났고 연구는 27개월 시점에 조기 종료됐다[28]. 본 임상시험의 중요한 점 중 하나는 기존의 심부전 치료의 표준치료를 하고 있는 환자에서 이미 사망률과 입원율 감소가 입증된 약제인 enalapril과 비교한 것으로 좌심실 수축기능 감소 심부전 환자 치료 파라다임의 변화가 예상된다.
좌심실 수축기능 감소 심부전 환자의 약물치료는 사망률과 이환율을 현저히 낮추므로 증거에 입각한 약제를 가능한 투여하는 것이 중요하다. 하지만 좌심실 수축기능 보존 심부전 환자에서 이루어진 대규모 임상연구 결과는 입원율과 이환율을 감소시키는 일부 연구는 있었으나 명확하게 사망률을 감소시킨 약제는 없었다. 그러므로, 이들 심부전의 치료 목적은 심박출량의 감소 없이 좌심실의 충만압을 감소시켜 심부전의 증상을 조절하는 것이다[29]. 그러므로 현재 이와 같은 심부전의 치료에서 가장 중요한 것은 적절한 고혈압 조절, 정상 동율동을 유지, 빈맥 예방, 심근허혈 예방 등 기저질환 및 상태를 회복 시키는 것이고 각기 환자에서 따른 약물 선택의 적용이 필요하다[45]. 폐울혈 및 심근 허혈이 동반되었을 경우에는 이뇨제나 nitrate 계통의 약물을 병용할 수 있다. 칼슘통로 차단제는 직접적으로 칼슘 항상성에 영향을 주어 이완기 기능을 호전시키거나, 간접적으로는 혈압감소, 심근허혈 방지, 좌심실 비대의 퇴행, 심박동수 감소 등을 유발시켜 이완 기능의 호전을 기대할 수 있다. ACEI, ARB는 간질성 콜라겐 침착 및 섬유화에 관여하는 안지오텐신 II의 생성을 억제하여 심근의 순응도를 호전시켜 이완기 기능을 향상시킬 수 있다[45].
심부전의 올바른 경구 약물치료는 환자의 증상 완화와 장기적인 예후를 고려한 선택이 필요하다. 특히 좌심실 수축 기능 감소 심부전 환자에서 장기간 임상연구로 입증된 약물로 치료하는 것은 증상의 개선뿐만 아니라 장기 예후를 개선시킨다.
이미 고령화 사회로 접어든 우리나라에서도 만성질환들이 점차적으로 증가하고 있는 상태이다. 본 논문은 의학적 측면뿐만 아니라 사회 경제적으로도 중요한 만성 심혈관 질환인 심부전에 대한 약물치료를 최신 임상연구 결과들을 반영하여 요약 기술한 논문이다. 최근에 대규모 임상에서 좌심실 구혈률 저하 심부전의 치료에 효과가 증명된 약제들이 많이 있어 심부전의 치료에 많은 발전이 있었고 따라서 치료약제 사용에 대한 정확한 이해가 매우 중요하다. 심부전의 약물치료에 대한 내용을 비교적 알기 쉽게 기술하고 있어, 전공의나, 심부전을 전공하지 않은 일반의들도 심부전의 치료를 보다 쉽게 이해하는데 참고할 수 있는 유익한 논문이라 판단된다.
[정리: 편집위원회]
Figures and Tables
Figure 2
Treatment overview of medical treatment in heart failure. ACEI, angiotensin converting enzyme inhibitor; ARB, angiotensinogen receptor blocker (From Yoo BS. Korean J Med 2011;81:716-719, according to the Creative Commons license) [7].
References
1. McKee PA, Castelli WP, McNamara PM, Kannel WB. The natural history of congestive heart failure: the Framingham study. N Engl J Med. 1971; 285:1441–1446.

2. Writing Group Members. Lloyd-Jones D, Adams RJ, Brown TM, Carnethon M, Dai S, De Simone G, Ferguson TB, Ford E, Furie K, Gillespie C, Go A, Greenlund K, Haase N, Hailpern S, Ho PM, Howard V, Kissela B, Kittner S, Lackland D, Lisabeth L, Marelli A, McDermott MM, Meigs J, Mozaffarian D, Mussolino M, Nichol G, Roger VL, Rosamond W, Sacco R, Sorlie P, Roger VL, Thom T, Wasserthiel-Smoller S, Wong ND, Wylie-Rosett J. American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Heart disease and stroke statistics: 2010 update: a report from the American Heart Association. Circulation. 2010; 121:e46–e215.
3. Krumholz HM, Chen YT, Wang Y, Vaccarino V, Radford MJ, Horwitz RI. Predictors of readmission among elderly survivors of admission with heart failure. Am Heart J. 2000; 139(1 Pt 1):72–77.

4. WRITING COMMITTEE MEMBERS. Yancy CW, Jessup M, Bozkurt B, Butler J, Casey DE Jr, Drazner MH, Fonarow GC, Geraci SA, Horwich T, Januzzi JL, Johnson MR, Kasper EK, Levy WC, Masoudi FA, McBride PE, McMurray JJ, Mitchell JE, Peterson PN, Riegel B, Sam F, Stevenson LW, Tang WH, Tsai EJ, Wilkoff BL. American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. 2013 ACCF/AHA guideline for the management of heart failure: a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. Circulation. 2013; 128:e240–e327.
5. McMurray JJ, Adamopoulos S, Anker SD, Auricchio A, Bohm M, Dickstein K, Falk V, Filippatos G, Fonseca C, Gomez-Sanchez MA, Jaarsma T, Kober L, Lip GY, Maggioni AP, Parkhomenko A, Pieske BM, Popescu BA, Ronnevik PK, Rutten FH, Schwitter J, Seferovic P, Stepinska J, Trindade PT, Voors AA, Zannad F, Zeiher A. ESC Committee for Practice Guidelines. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: the Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2012; 33:1787–1847.
6. Heart Failure Society of America. Lindenfeld J, Albert NM, Boehmer JP, Collins SP, Ezekowitz JA, Givertz MM, Katz SD, Klapholz M, Moser DK, Rogers JG, Starling RC, Stevenson WG, Tang WH, Teerlink JR, Walsh MN. HFSA 2010 Comprehensive Heart Failure Practice Guideline. J Card Fail. 2010; 16:e1–e194.
7. Yoo BS. Pharmacological treatment of heart failure. Korean J Med. 2011; 81:716–719.
9. Vargo DL, Kramer WG, Black PK, Smith WB, Serpas T, Brater DC. Bioavailability, pharmacokinetics, and pharmacodynamics of torsemide and furosemide in patients with congestive heart failure. Clin Pharmacol Ther. 1995; 57:601–609.

10. Roush GC, Kaur R, Ernst ME. Diuretics: a review and update. J Cardiovasc Pharmacol Ther. 2014; 19:5–13.
11. Ehle M, Patel C, Giugliano RP. Digoxin: clinical highlights: a review of digoxin and its use in contemporary medicine. Crit Pathw Cardiol. 2011; 10:93–98.
12. May CW, Diaz MN. The role of digoxin in the treatment of heart failure. Circ Heart Fail. 2008; 1:206–207.

13. Valluri A, Struthers AD, Lang CC. Novel blockers of the renin-angiotensin-aldosterone system in chronic heart failure. Curr Heart Fail Rep. 2014; 11:31–39.

14. Flather MD, Yusuf S, Kober L, Pfeffer M, Hall A, Murray G, Torp-Pedersen C, Ball S, Pogue J, Moye L, Braunwald E. Long-term ACE-inhibitor therapy in patients with heart failure or left-ventricular dysfunction: a systematic overview of data from individual patients: ACE-Inhibitor Myocardial Infarction Collaborative Group. Lancet. 2000; 355:1575–1581.

15. Basuray A, French B, Ky B, Vorovich E, Olt C, Sweitzer NK, Cappola TP, Fang JC. Heart failure with recovered ejection fraction: clinical description, biomarkers, and outcomes. Circulation. 2014; 129:2380–2387.
16. Dezsi CA. Differences in the clinical effects of angiotensin-converting enzyme inhibitors and Angiotensin receptor blockers: a critical review of the evidence. Am J Cardiovasc Drugs. 2014; 14:167–173.

17. Lang CC, Struthers AD. Targeting the renin-angiotensin-aldosterone system in heart failure. Nat Rev Cardiol. 2013; 10:125–134.

18. Von Lueder TG, Krum H. RAAS inhibitors and cardiovascular protection in large scale trials. Cardiovasc Drugs Ther. 2013; 27:171–179.

19. Van den Berg TN, Rongen GA, Frohlich GM, Deinum J, Hausenloy DJ, Riksen NP. The cardioprotective effects of mineralocorticoid receptor antagonists. Pharmacol Ther. 2014; 142:72–87.

20. Iqbal J, Parviz Y, Pitt B, Newell-Price J, Al-Mohammad A, Zannad F. Selection of a mineralocorticoid receptor antagonist for patients with hypertension or heart failure. Eur J Heart Fail. 2014; 16:143–150.

21. Lymperopoulos A, Rengo G, Koch WJ. Adrenergic nervous system in heart failure: pathophysiology and therapy. Circ Res. 2013; 113:739–753.
22. Klapholz M. Beta-blocker use for the stages of heart failure. Mayo Clin Proc. 2009; 84:718–729.
23. Swedberg K, Komajda M, Bohm M, Borer JS, Ford I, Dubost-Brama A, Lerebours G, Tavazzi L. SHIFT Investigators. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet. 2010; 376:875–885.

24. Ekman I, Chassany O, Komajda M, Bohm M, Borer JS, Ford I, Tavazzi L, Swedberg K. Heart rate reduction with ivabradine and health related quality of life in patients with chronic heart failure: results from the SHIFT study. Eur Heart J. 2011; 32:2395–2404.

25. Schrier RW, Gross P, Gheorghiade M, Berl T, Verbalis JG, Czerwiec FS, Orlandi C. SALT Investigators. Tolvaptan, a selective oral vasopressin V2-receptor antagonist, for hyponatremia. N Engl J Med. 2006; 355:2099–2112.

26. Gheorghiade M, Konstam MA, Burnett JC Jr, Grinfeld L, Maggioni AP, Swedberg K, Udelson JE, Zannad F, Cook T, Ouyang J, Zimmer C, Orlandi C. Efficacy of Vasopressin Antagonism in Heart Failure Outcome Study With Tolvaptan (EVEREST) Investigators. Short-term clinical effects of tolvaptan, an oral vasopressin antagonist, in patients hospitalized for heart failure: the EVEREST Clinical Status Trials. JAMA. 2007; 297:1332–1343.

27. Von Lueder TG, Sangaralingham SJ, Wang BH, Kompa AR, Atar D, Burnett JC Jr, Krum H. Renin-angiotensin blockade combined with natriuretic peptide system augmentation: novel therapeutic concepts to combat heart failure. Circ Heart Fail. 2013; 6:594–605.





 PDF
PDF ePub
ePub Citation
Citation Print
Print






 XML Download
XML Download