Abstract
Bedside ultrasonographic examination is known to be a quick, noninvasive, cost-effective, repeatable, and harmless diagnostic modality. It can be a powerful tool for clinicians, especially in time-dependent situations including trauma. Focused assessment with sonography in trauma (FAST) has been established as a protocol especially specifically for hemodynamically unstable patients with blunt abdominal trauma. The physiologic priority of airway, breathing, circulation, and disability (ABCD) of injured patients should be assessed using a multi-systemic, multi-focused, problem-based, and point-of-care ultrasound as an extension of physical examination. This ultrasound-enhanced trauma life support, so called FAST-ABCD, can provide a great deal of important information for helping the primary physician in critical decision-making by systemically combining the airway, lung, cardiovascular, abdominopelvic, orbital, and transcranial ultrasound. Additionally, it can provide information on airway patency, guidance of endotracheal intubation and cricothyroidotomy, lung contusion, limited hemodynamics, differential diagnosis of shock, intracranial hypertension, and even more extensively on a secondary survey from head to toe. The indications for the utility of ultrasound in trauma continue to evolve beyond FAST. FAST-ABCD could be incorporated into advanced trauma life support by obtaining more evidence through more studies worldwide.
다발성 외상환자의 초기평가와 안정화를 위해서는 복합적이고 시간의존적 의사결정 및 다양한 술기들이 필요하다. 그 중에 실시간의 침상 옆 초음파는 응급상황에서 수 많은 결정적인 정보들을 제공해주기 때문에 응급 및 외상의사들의 임상적 판단에 지대한 역할을 하는 부가적 검사이다. 물론 컴퓨터단층촬영이 최근의 비약적인 발전에 힘입어 외상처치에 대한 최종 결정을 위한 필수 진단도구로 자리잡고 있지만, 방사선피폭의 문제점 이외에도 혈류역학적으로 불안정한 외상환자들의 초기진단 검사로 컴퓨터단층촬영을 채택하는 것이 수술시기를 지연시키고 사망률을 높일 수 있다 는 것 또한 감안해야 할 것이다[1].
초음파를 이용한 다발성 외상환자의 초기평가를 기술함에 있어서 focused assessment with sonography for trauma (FAST)를 논하지 않을 수 없을 것이다. 외상환자를 대상으로 초음파를 이용하기 시작한 이들은 외과의사들이었다. 1980년대에 유럽과 일본에서 외상환자의 평가에 초음파가 이용되기 시작하면서 대륙간으로 퍼지기 시작했고 1995년에 Rozycki 등[2]은 대규모 전향적 연구에서 외상 초음파검사의 심장막삼출(pericardial effusion)과 복막삼출 (peritoneal effusion) 진단에 대한 민감도와 특이도가 각각 81.5%, 99.7%라고 발표하였고, 처음으로 focused abdominal sonography for trauma, 즉 FAST라는 용어를 사용하기 시작했다. 곧이어 외상 초음파검사를 전문외상소생술에 포함시키는 과정에서, 현재 우리에게 익숙한 FAST로 정착되었다. FAST는 1999년 국제합의회의를 통해 pericardial, perihepatic, perisplenic, pelvic의 4Ps 평가가 확립되고 권장되었다. 그 이후 FAST는 기흉이나 혈흉 평가가 포함된 extended FAST (EFAST) [3]와 사지골절까지 포함된 FAST including extremities and respiratory tract [4]를 거쳐서 최근에는 여러 장기들에 대하여 다양한 초점에 맞춘, 문제해결형 초음파검사인 외상소생술(multi-systemic, multi-focused, problem-based ultrasound-enhanced trauma life support)로 보다 정교한 프로토콜로 재조합되어 보급되고 있다. 즉 FAST including airway, breathing, circulation, and disability (FAST-ABCD)로서 세계응급 및 중환자초음파학회인 World Interactive Network Focused on Critical Ultrasound (WINFOCUS)에서 체계적인 교육모델을 연구 및 확립하여 교육을 진행하고 있다[5]. WINFOCUS는 현장 초음파(point-of care ultrasound)를 임상의료에 접목하여 일차의료 및 응급, 중환자의학의 질적 향상을 지향한다는 것을 목적과 비전으로 삼은 국제학술단체이다. 현재 한국에도 WINFOCUS-KOREA가 설립되어 지속적으로 국내외 전문 강사들과 함께 워크샵을 진행하고 있다.
근본적으로 FAST-ABCD의 개념은 외상환자에만 국한된 것은 아니다. 외상 및 비외상환자 모두에게 적용되며, 기본 개념은 통합적인 초음파를 지향한다. ABCD 우선순위에 따라 여러 장기 및 기능들을 통합하는 교육모델로 지식과 경험을 습득하고, 중증 환자의 침상 옆에서 응급 및 중환자 의사가(영상의학과나 심장내과의사가 환자 평가 및 처치에 현장에 참여하고 있기 힘들기 때문임) 여러 가지 목적에 맞추어 문제해결 방식으로 초음파를 활용하여 신속하고 적절한 의사결정을 할 수 있도록 도와주는 방법이라고 할 수 있다. 특히 시간 요인이 매우 중요한 외상환자에게는 더욱 효율적인 도구일 것이다. 중증 외상환자의 처치는 생리적 우선순위에 근거하여 ABCD 순서에 따라 접근하도록 되어 있다. 다발성 외상환자에서 초음파적 접근에서 복부는 반드시 검사해야 하는 주요 부위인 것은 맞지만, 기도, 폐 및 심장 검사가 더 우선이 되어야 한다. 복강 내의 유리삼출물(free fluid)이 확인해야 할 주요 소견인 것은 맞지만, 심장과 흉막의 기능 및 운동 또는 흉막간 공기(기흉) 등보다 우선해서 검사해야 하는 것이 아니다. 숙련된 응급 및 중환자 의사는 다발성 외상환자에 대한 일차평가에서 초음파를 이용함으로써, 이동형 방사선촬영이 이루어지기 전에, 기도, 호흡, 순환 및 중추신경계(경부, 흉부, 복부 및 안구 초음파) 등의 상태에 대한 체계적인 통찰력을 가질 수 있을 것이다(Figure 1).
외상환자를 치료함에 있어서 우선순위는 그 외 다른 치명적인 상황과 마찬가지로 기도확보, 적절한 환기유지, 출혈통제(bleeding control) 및 쇼크의 치료가 첫 번째 우선순위이다. 또 하나의 중요한 점은 가능한 최악의 손상을 고려하고 그 진단이 확진되거나 배제될 때까지는 그 가정에 따라 행동해야 한다는 것이다. 전문외상소생술에 근거한 외상환자의 응급처치 단계는 일차평가 및 처치(primary survey and intervention)와 이차평가(secondary survey)로 나눌 수 있다. 초음파를 이용한 다발성 외상환자의 평가는 일차 평가와 함께 시행하는 것이 권장된다. 물론 FAST-ABCD를 이용한 이차평가도 정립되어 있지만, 여기에서는 일차평가에 주안점을 두고 기술하고자 한다. 또한 상대적으로 잘 알려진 FAST 이외의 ABCD 평가방법(기도, 폐, 심장, 안구 초음파)에 조금 더 무게를 두고 기술하고자 한다. 아울러 지면 관계상 모든 일차평가 및 처치에 관련된 내용을 다루지 못하였음에 대한 양해를 바란다.
외상환자에서 기도, 산소화 및 환기에 대한 적절한 평가와 처치는 최고로 중요한 과정이지만, 때로 매우 어렵고 곤란할 수 있는 과정이기도 하다. 대형 외상센터에서 9년 동안 입원시킨 44,404명의 환자와 2,594명의 사망환자를 분석한 결과를 보면, 예방 가능한 사망의 16%가 기도확보 및 유지와 관련된 경우였다고 한다[6]. 경부초음파는 대개 고주파수의 선형탐촉자를 이용하여 관찰한다. 경부외상에 의해서 상기도외상이 의심되는 경우, 초음파를 이용하여 기도의 해부학적 이상, 상기도의 전위 유무 및 기도 주변의 압박성 혈종 유무 등을 판단할 수 있다. 또한 침습적 기도 확보를 결정한 다음에는 시술 직전, 시술 중 실시간으로, 그리고 시술 직후에 모두 초음파를 적용함으로써 신속하고 안전하게 임상적 판단을 할 수 있다(Table 1, Figures 2, 3, 4).
기관삽관 중에 선형 탐촉자를 흉골상절흔 바로 위에 위치시 켜 횡스캔을 하면, 성공적으로 기도삽관이 되는지 혹은 식도삽 관이 되고 있는지를 실시간으로 확인할 수 있다(Figure 5). 이 수기의 장점은 식도삽관을 실시간으로 확인할 수 있으므로, 기도삽관 확인을 위한 앰부주머니 환기 시도 없이 곧바로 기도삽관을 재시도하도록 하여, 긴박한 상황에서 시간을 절약할 뿐 아니라 불필요한 위 팽창을 예방할 수 있어 흡인 등의 합병증을 피할 수 있다.
식도 모양의 변화가 없었거나 기도로 들어가는 모습이 관찰되면, 다음 단계는 튜브 말단의 위치 확인을 위하여 폐 초음파를 시행하는 것이다. 사용하고 있는 선형 탐촉자를 양측 중간액와선에 적용하고 앰부주머니 환기를 하면서 폐 미끄럼 현상(lung sliding)의 유무를 확인한다. 반드시 중간액와선일 필요는 없지만, 폐첨부보다는 기저부 쪽이 흡기 시에 폐의 이동량이 많은 것을 감안하고, 혹시나 존재할 수 있는 기흉이 주로 전흉부 쪽에 모여 있을 것이므로, 양측 폐의 환기를 평가하기 위한 목적의 폐 미끄럼의 확인은 측흉부 및 폐 기저부 쪽이 이상적일 것으로 생각된다. 폐 미끄럼 현상이란 벽 쪽 흉막에 대한 내장 쪽 흉막의 움직임으로서, 초음파 화면에서 미끄러지는 듯한 움직임이 호흡에 따라 나타나는 것을 말한다. 양측에서 폐 미끄럼이 확인되었다면 튜브의 말단이 기관지 분기점(carina) 위쪽에 적절하게 위치하고 있다는 것을 의미한다. 만약 우 기관지로 너무 깊게 들어갔다면 좌측 흉부에서 폐 미끄럼 현상이 관찰되지 않을 것이므로 좌측에서 폐 미끄럼 현상이 관찰될 때까지 튜브를 빼내도록 한다. 우 기관지 삽관이 된 경우에는 또 하나의 흥미로운 폐 초음파 징후인 lung pulse 징후가 좌측 전흉부에서 관찰될 수 있다. 이는 폐 미끄럼 현상이 소실된 흉막에서 심장의 진동이 전해져서 흉막이 박동하는 모양으로 관찰되는 징후이다(Figure 6).
만약 삽관 후에 양측 흉부 모두에서 폐 미끄럼 현상이 없고 lung pulse만 관찰된다면, 식도삽관의 가능성을 다시 생각해봐야 한다. 만약 폐 미끄럼 현상과 lung pulse가 모두 관찰되지 않는다면 기흉의 가능성을 반드시 고려해야 한다. 기흉에 관해서는 후술하겠다.
경부 초음파를 이용하면 윤상갑상막절개를 위한 정확한 해부학적 위치를 확인할 수 있다(Figure 4). 윤상갑상막은 기도 처치에 있어서 매우 중요한 구조이다. 하지만 체표면 지표와 촉진으로 정확하게 윤상갑상막을 확인할 수 있는 경우는 건강한 성인들을 대상으로 해도 30% 밖에 되지 않는다고 한다[7]. 기도관리에 있어서 실패한 기도(failed airway) 알고리즘에서는 기관삽관과 환기가 모두 어려운 경우(can't intubate, can't oxygenate)의 대처방안으로 윤상갑상막절개를 권장하고 있다[8]. 응급 윤상갑상막절개나 바늘 윤상갑상막절개 전에 초음파를 이용하면 윤상갑상막의 정확한 위치 및 깊이 등의 정보를 쉽게 얻을 수 있을 뿐 아니라 윤상갑상막절개를 어렵게 만드는, 비정상적으로 왜곡된 기도나 기관 앞으로 지나가는 예상치 못한 혈관 등을 사전에 알아낼 수도 있다. 또한 심한 안면부 손상이나 혈종 등에 의한 상기도 폐쇄 환자들과 같이 매우 어려운 기도(difficult airway)가 예상되는 경우에도 예방적으로 바늘 윤상갑상막절개를 통한 고빈도제트환기를 이용함으로써 서둘지 않고 안전하게 기도확보를 할 수 있으며 일차 기관절개술의 빈도도 감소시켜준다는 보고도 있다[9].
일부 외상환자에서는 기흉이나 혈흉에 의해서 호흡부전을 일으키기도 하기 때문에, 기관삽관과 더불어 흉관삽관이 필요할 수 있다. 심한 경우에는 호흡부전뿐 아니라 긴장성 기흉에 의한 폐쇄성 쇼크나 대량 혈흉에 의한 저혈량성 쇼크를 일으키기도 한다. 폐 초음파는 침상 옆에서 기흉, 혈흉, 폐 좌상 등을 즉시 진단하고 이동형 흉부방사선촬영을 기다릴 필요 없이 바로 흉관삽관을 시행할 수 있게 해준다(Table 2). 응급상황에서 폐 초음파의 활용에 대해서는 익숙하지 않은 독자들을 위해서 우선 기본적인 초음파 소견부터 기술하고자 한다.
폐 초음파를 위해서는 5-MHz의 microconvex 탐촉자가 권장되나, 없는 경우에는 복부검사에서 주로 쓰는 곡선형 탐촉자를 쓰도록 권장하고 있다. 물론 흉막선 관찰이 주 목적인 경우에는 고주파의 선형 탐촉자를 사용해도 된다. 폐 초음파는 종스캔을 기본으로 한다. 종스캔으로 늑골과 그로 인한 음향그림자(acoustic shadow)를 먼저 인지해야 한다. 정상 성인에서 늑골은 대략 2 cm의 너비를 가진 아치형 고에코의 구조물이다. 늑골은 서로 2 cm 정도 떨어져 있다. 늑골선의 0.5 cm 아래에(성인에서) 고에코의 거친 가로선이 항상 보이는데, 이를 흉막선이라고 한다. 상하의 늑골(화면에서는 좌우)과 흉막선의 경계가 만들어내는 모양이 박쥐 모양과 비슷하여 박쥐 징후(bat sign)라고 한다. 박쥐 징후는 폐 초음파에서 기본적인 징후로, 이것을 이용하여 폐 표면(흉막선)을 정확히 찾을 수 있다(Figure 7). 흉막선은 벽쪽 흉막과 내장쪽 흉막으로 이루어져 있고 그 사이에 흉막강이 존재하지만, 정상적인 상태에서는 초음파 검사로 두 층을 구별하기는 어렵다. 모든 징후는 흉막선이 있는 층에서 발생한다. 기흉에 의해서 흉막층들이 분리되면 내장 쪽 흉막이 공기에 가려져서 보이지 않게 되지만, 흉막삼출인 경우에는 내장 쪽 흉막이 완벽하게 관찰된다.
흉막선에서 기인하는 다른 폐 초음파적 주요 관심 소견으로 기흉과 흉막삼출 이외에 간질증후군(interstitial syndrome) 과 폐포경화(alveolar consolidation) 가 있으며, 이들이 폐 초음파의 주요 4대 병적 소견이다. 외상과 관련하여 각 병적 소견을 설명하고자 한다.
정상 폐에서는 내장쪽 흉막이 호흡에 따라 화면에서 좌우로 움직이는 것이 관찰되는데, 이를 폐 미끄럼 현상이라 한다. 흡기 시에는 내장 쪽 흉막이 벽 쪽 흉막면에 접촉한 상태로 미끄러져 다리 방향으로 내려가고 호기 시에는 머리 방향으로 올라가는 운동이다. M모드를 사용하면 이런 동적 정보를 한 장의 정지영상으로 표현할 수 있다. 정상 폐의 M모드 영상에서 우리는 흉막선을 경계로 상부와 하부가 확연히 차이가 난다는 것을 알 수 있다. 흉막선의 상부는 파도가 밀려오는 수평선처럼 보인다. 흉막선 하부의 폐 움직임은 M모드에서 모래사장과 같은 형태로 기록되어 이 전체를 해안징후(sea shore sign)라고 부른다. 정상 폐에서 흉막선 아래로 흉막과 평행한 고에코의 수평선들이 관찰되는데, 이를 A선이라고 부른다(Figure 8). 공기는 초음파 빔을 차단하며 탐촉자로 되돌려 보내는데, 이들이 반복되면서 규칙적인 허상들이 만들어지는 것이다(반향허상, reverberation). 흉막과 A선과의 거리는 피부와 흉막선과의 거리와 동일하다. 이에 반해 수직 허상은 혜성꼬리허상으로 서, B선이라 하고, 3 개 이상의 수직허상이 한 늑골사이공간에서 관찰되는 것을 lung rockets 징후라고 한다(Figure 9). 이 징후의 병태생리학적 의미는 비후된 소엽사이막(thickened interlobular septum)으로, 간질증후군에서 관찰되는 초음파적 징후이다[10].
외상에 의한 기흉이나 혈흉은 혼란스럽고 긴박한 응급상황에서 전통적인 임상적 소견만으로는 인식하기 힘들 수 있다. 외상환자 검사를 위한 EFAST의 일부인 침상 옆 흉부 초음파검사는 앙와위 전후 흉부방사선촬영의 제한점을 극복할 수 있다. 둔상환자에서 폐 초음파검사의 기흉에 대한 민감도는 92-100% 정도로 매우 높은 반면에, 앙와위 흉부방사선촬영은 28-75% 밖에 되지 않는다[11].
흉부방사선촬영으로는 확인되지 않았으나 컴퓨터단층촬영으로 진단되는 잠재기흉의 빈도는 모든 외상환자의 약 5% 정도이고, 컴퓨터단층촬영이 시행된 외상환자군에서는 15% 정도가 잠재기흉이라고 한다[12]. 손상중증도(injury severity score)가 12 이상인 중증의 다발성 둔상환자들에 대한 한 전향적 연구에서는 전체의 26%가 잠재기흉이었는데, 놀랍게도 이들 중 76%가 외상센터에서 앙와위 전후 흉부방사선촬영의 실시간 판독 결과가 음성이었다고 한다[13]. 아직까지 잠재기흉에 대한 치료방침이 확정되지는 않았지만, 기흉의 중증도는 역동적이기 때문에, 특히 양압환기의 기계호흡을 적용하거나 항공이송을 하는 경우, 적은 양의 기흉이라도 치명적으로 변할 수 있으므로 세심한 추적관찰이 힘든 경우에는 흉관삽관을 하는 것이 유리하다 하겠다[14].
기흉은 비체위의존성 질환이다. 즉 앙와위에서 하늘 쪽에 모이게 되어 전흉부에 위치하게 된다. 266명의 외상성 기흉의 해부학적 위치 분포를 후향적으로 컴퓨터단층촬영을 통해 분석한 결과를 보면, 기흉의 빈도와 크기가 양측 흉강 모두에서, 하부로 갈수록 그리고 내측으로 갈수록 증가하는 것이 관찰되었다[15]. 즉 극도로 응급 상황에서 앙와위의 외상환자의 기흉 진단을 위해서는 전흉부의 내측 하부에서부터 시작하여 외측으로 이동하면서 관찰하는 것이 유리할 것이다. 반좌위 환자에게는 상대적으로 좀 더 상부에 초음파를 적용하는 것이 효과적일 것이다. 이때에 탐촉자는 지면-하늘 축(earth-sky axis)에서 지면 쪽을 향하고 있어야 한다. 기흉의 초음파적 징후에는 폐 미끄럼 현상의 소실, A선 징후, lung point 징후 등이 있다.
기흉에서는 벽 쪽 흉막 아래에 공기가 내장 쪽 흉막을 가리고 있으므로 내장 쪽 흉막의 움직임이 관찰되지 않게 된다. 부가적으로 M모드를 적용하면 해안징후 대신에 오로지 수평선들로만 기록되는 성층권 징후(stratosphere sign)가 나타난다. 이는 폐의 움직임이 없음을 보여주는 징후이다(Figure 10).
Lung pulse는 폐 미끄럼 현상의 소실과 함께 심장의 미세한 박동이 폐 초음파에서 관찰되는 것으로, 기흉을 배제할 수 있는 초음파 징후이다. 한쪽 폐 기관삽관에서 관찰되는 소견이다.
기흉 진단을 위한 폐 초음파 소견을 정리하면 다음과 같다. 폐 초음파에서 폐 미끄럼 현상, B선, lung pulse 중에 하나라도 관찰되면 기흉을 배제할 수 있다. 폐 미끄럼 현상과 B선이 모두 관찰되지 않으면서 lung point가 확인되면 기흉을 확진할 수 있다. Lung point를 찾을 수 없는 경우에는 lung pulse를 찾아서 이것마저 없다면 기흉이라고 진단한다.
급성호흡부전이나 긴장성기흉을 의심할 만한 초응급상황에서는, 흉막선에서 수평운동(폐 미끄럼 현상)과 수직운동 (lung pulse) 모두 관찰되지 않고 B선도 관찰되지 않으면 lung point를 찾을 필요 없이 기흉을 신속하게 진단하여 처치할 수 있다[18]. 후술하겠지만 이런 상황에서 심장과 하대정맥 초음파검사를 결합하면 임상적 판단에 더욱 도움이 될 수 있다(작고 과운동적인 심장이 기흉의 반대편으로 전위되어 있으며 하대정맥의 직경이 호흡에 따른 크기변화가 없는 소견).
초음파를 이용한 외상성 혈흉 진단은 높은 민감도와 특이도를 보인다. Sisley 등[19]의 보고에 의하면, 혈흉에 대한 초음파검사는, 민감도와 특이도가 각각 97.5%, 99.7%로, 흉부방사선촬영과 유사하였으나 진단의 속도를 의미 있게 향상시킬 수 있었다고 보고하였다.
혈흉은 기흉과 반대로 체위의존적이므로 전흉부가 아니라 측흉부나 후흉부에서 하늘 쪽을 향하여 스캔하여야 한다. 혈흉은 횡격막 위쪽에서 두 흉막 사이에서 무에코 또는 에코성 삼출로 관찰된다(Figure 12). 이 외의 진단기준으로 사각 징후와 사인곡선 징후가 있다. 흉막삼출 진단에 있어서 두 징후의 특이도는 97%였다20].
흉막삼출의 정적 징후로서, 흉막선, 위쪽과 아래쪽 늑골의 후방 그림자, 그리고 폐 선(흉막선과 평행한 심부의 매끈한 경계선)에 둘러싸여 사각형 모양을 형성하는 것이다.
흉막삼출의 동적 징후로서, 호기 시에 두 흉막 사이의 거리가 변하는 현상을 뜻한다. 폐가 몸의 중심에서 표면 쪽으로 움직이기 때문에 M모드에서는 사인곡선으로 나타난다(Figure 13).
Ball 등[12]이 제안한 흉부둔상 환자에 대한 알고리즘에 의하면, 초기평가에서 EFAST를 첫 번째 진단도구로 시행하고 기흉이나 혈흉이면서 환자상태가 불안정하면, 흉부방사선촬영을 기다리지 말고 즉시 흉관삽관을 시행하도록 권장하고 있다. EFAST가 흉부방사선촬영을 지연시키면 안되지만, 준비된 외상센터에서는 두 가지를 동시에 시행할 수 있을 것이다. EFAST 이후에 흉부방사선촬영을 시행하고 여기에서 확장된 종격동 소견이 보이거나 잠재기흉의 가능성이 있는 경우에는 컴퓨터단층촬영을 시행하도록 한다. 지속적이고 세밀한 임상적 관찰이 어려운 경우라면 모든 잠재기흉에 대해 반드시 흉관삽관을 하도록 권장하고 있다.
EFAST의 검사항목에는 포함되어 있지 않지만, 폐 초음파가 정착되면서 외상성 호흡부전의 원인 중의 하나인 폐 좌상에 대한 폐 초음파적 관심도 늘어났다. 폐 좌상은 acute respiratory distress syndrom (ARDS) 발생에 대한 독립적인 위험인자이며 10-25%의 사망률을 초래한다고 알려져 있다. 폐 좌상의 해부생리적 진화는 다음과 같이 세 단계를 거친다. 1) 외상 자체: 폐 실질에 전달된 직접적인 에너지에 의한 폐 출혈이나 열상, 2) 부종기: 일차 손상 이후 1-2시간 이내에 점차적으로 간질 침윤 발생, 3) 경화기: 공기로 차있던 공간에 혈액, 염증세포 및 조직 찌꺼기들의 충만이 이루어지는 시기로, 손상 후 24-48시간에 최고조를 이룬다. 흉부방사선촬영으로는 세 번째의 경화기에서만 폐 좌상을 감지할 수 있지만, 초음파는 간질증후군을 매우 정확하게 전달할 수 있기에 보다 조기에 폐 좌상을 진단할 수 있을 것이다. Soldati 등[21]은 다발성 B선들(병소적 간질증후군)의 폐 좌상에 대한 민감도, 특이도는 각각 94.6%, 96.1%였고, 초기 흉부방사선촬영의 민감도는 27%밖에 되지 않는다고 발표하였다. Rocco 등[22]은, 폐 초음파 소견이 간 조직과 유사한 형태의 저에코를 띄고(hepatization) 가장자리가 불분명한 모양이며, 흡기에도 그 크기가 변하지 않는 특징을 보이는 폐포경화 패턴(경화의 병소는 1 cm 정도로 매우 작을 수도 있으며, 폐엽 전체만큼 클 수도 있다)(Figure 14) 또는 다발성 B 선들의 패턴을(Figure 15) 폐 좌상으로 정의했을 때, 폐 초음파 검사의 폐 좌상에 대한 민감도는 86%였고 특이도는 97%라고 보고하였다. 인공호흡기로 치료를 시작한 후에도 폐 좌상의 정도를 초음파로 모니터링 한다면, 폐 기능의 회 복을 위해서 양압환기의 유지 결정에도 도움이 될 수 있으므로 외상에 의한 조기 발생 폐렴(early onset pneumonia)의 예방 및 사망률의 감소에 도움이 될 수 있을 것으로 생각된다.
결론적으로, 폐 초음파의 주요 4대 병변인 기흉, 흉막삼출(혈흉), 폐포경화(alveolar consolidation) 및 간질증후군이 흉부외상에서도 모두 관찰될 수 있다. 폐 좌상의 초음파적 소견은 폐포경화와 병소적 간질증후군(focal interstitial syndrome)으로 관찰된다. 내과적 문제로 발생한 폐렴(폐포경화)이나 심인성 폐부종 또는 ARDS(간질증후군)과의 구분을 위해서는, 외상에 의한 경우에 한해서 임상적 판단을 해야 할 것이다.
외상성 심장막삼출은 FAST의 검사 항목 중의 하나이며, 초음파를 이용한 진단의 정확도는 매우 높다고 알려져 있다[19]. 외상환자에서의 심장 초음파를 이용하면 심장막삼출의 진단 이외에도, 외상에 의한 쇼크의 대부분을 차지하는 저혈량성 쇼크와 심장눌림증이나 긴장성기흉에 의한 폐쇄성 쇼크를 감별진단하는데 도움이 된다(Table 3). 이때 폐 초음파와 함께 통합적인 초음파검사를 하면 더욱 효과적이다. 쇼크의 감별진단 이외에도 적절한 외상환자 처치에 있어서도 중요한 혈류역학 정보를 제공한다. Gunst 등[23]은 bedside echocardiographic assessment in trauma (BEAT)를 FAST와 병용하여 사용하자고 주장하였는데, 심장 및 하대 정맥 초음파를 시행하여 beat (cardiac function), effusion (pericardial effusion), area (right and left ventricular size), tank (volume status)를 평가하였을 때, 심기능과 용적상태가 폐동맥 카테터로 측정한 값과 의미 있는 연관성을 보였다고 보고하였다. Ferrada 등[24]은 외상 중환자실에서 수액 또는 심장 수축촉진제(inotropics) 사용에 대한 결정을 위하여 focused rapid echocardiographic examination (FREE)를 시행한 후 그 정보가 임상적 의문점에 적절한 답변을 준 경우가 87%였고 54%에서 초음파 소견에 기초하여 치료계획을 변경할 수 있었다고 보고하였다. 하대정맥의 직경은 외상환자에서 혈관 내 용적 결핍과 반비례한다고 알려져 있다. Carr 등[25]의 보고에 의하면, 전부하 평가에 있어서 간정맥 합류부에서 2 cm 아래 정도에서 측정한 하대정맥의 크기가 작고 (1 cm 미만 또는 전후 직경이 좌우직경의 1/3 미만) 하대정맥 collapse index가 50%보다 큰 경우에서 전문가의 임상적 판단과 각각 67%, 65% 일치를 보였다.
BEAT 방법을 단순화하여 소개하면, 흉골연장축단면스캔 및 M모드를 이용해서 심박출량과 심장의 수축기능(beat)을 측정하고 심장막삼출(effusion)을 평가한 다음, 흉골연단축단면과 심첨 4방 단면스캔을 이용해서 각각 좌심실과 우심실의 크기(area)를 평가하고, 마지막으로 늑골하에서 하대정맥을 장축 스캔하여 전부하 (tank)를 평가한다. 이 방법의 제한점은 저자들의 권장 체위인 좌 측와위가 다발성 외상환자에서 항상 가능하지 않다는 것과 응급상황에서 M모드까지 사용할 여유가 없을 수 있다는 것이다. 저자의 생각으로는, 앙와위에서도 위와 같은 순서로 시행하면서 오직 이면성(2-dimensional) 영상만으로 평가하도록 노력하고, 불량한 스캔으로 평가가 불가능한 경우에는 늑골하 4방 단면(beat, effusion, area 평가), 늑골하단축단면(좌심실의 area 평가) 및 하대정맥 장축 스캔(tank 평가)을 통해 BEAT를 평가할 수 있다.
폐 초음파 소견은 임상적 소견, 즉 호흡곤란이나 쇼크 상황과 연계하여 시행하고 의사결정에 이용해야 한다. 전술하였듯이 lung point를 찾기 위해 시간을 허비할 필요가 없이 바늘 응급감압술을 바로 시행한다. 과운동성의 작은 심장을 초음파에서 확인할 수 있고, 기흉의 반대쪽으로 심장이 전위된 것을 늑골하스캔에서 확인할 수 있다. 하대정맥은 확장되어 있고 호흡주기에 따른 변화가 없거나 미약하게 관찰된다.
폐 좌상이나 기흉이 동반되지 않았다면, 전흉부 폐 초음파에서 정상소견(폐 미끄럼 현상 및 A선)이 관찰될 것이다. 좌우 심실의 크기가 작고 과운동성의 심장을 관찰할 수 있으며, 하대정맥 종축스캔에서는 긴장성 기흉과는 달리 직경이 작고 흡기 시에 50% 이상 감소되는 소견이 관찰된다(Figure 16).
Neal 등[1]은 National Trauma Data Bank 자료를 이용하여, 응급센터 도착 후 90분 안에 수술이 시행되었던 혈류 역학적으로 불안정한 복부외상환자들의 초기진단검사로 컴퓨터단층촬영이 시행된 군의 사망률이 아닌 군에 비해 70% 높았으며, 30분 안에 수술했던 환자들에서는 무려 일곱 배로 사망률이 높았다고 보고하였다. FAST는 복부 또는 심장손상이 의심되는 둔상환자가 혈류역학적으로 불안정한 상황에서 일차선택 진단방법이다. FAST의 단점은 일부 환자에서 상대적으로 낮은 민감도를 보인다는 것이다. 특히 골반골절이나 신장손상과 같은 후복막 손상의 진단에서 가음성이 많다. 즉, 혈류역학적으로 불안정한 환자에서 FAST 결과가 음성이라도 복부출혈을 완전히 배제시킬 수 없다는 것이다. 즉 이런 경우에는 부가적으로 다른 출혈 원인을 수색함과 동시에 복부평가를 지속적으로 해야 한다. 진단적 복막 흡입/세척(DPA/DPL)을 시행하거나 일단 환자의 상태를 안정화시킨 후에 컴퓨터단층촬영을 시행하도록 한다.
혈류역학적으로 안정된 환자에서 FAST는 특이도는 여전히 높았지만 민감도가 매우 낮고 장기-특이(organ-specific) 정보를 제공하지 못하므로 컴퓨터단층촬영의 도움이 필요하다고 보고되어 있다[27].
혈류역학적으로 불안정한 복부 관통상 환자는 개복술이 필요한 상황이다. 그러면 혈류역학적으로 안정된 환자에서의 FAST의 역할은 무엇일까? Udobi 등[28]은 명백하게 응급개복술이 필요한 경우를 배제하고 전향적 연구를 한 결과, 양성 FAST는 의미 있는 복강 내 손상을 강력하게 시사하지만, FAST가 음성인 경우에는 그 민감도가 46%로 매우 낮아서, 부가적인 검사가 필요하다고 결론지었다. 가음성 FAST에는 수술이 필요한 장관손상이나 횡격막손상 등이 포함된다. 반면에 관통 심장손상이 의심되는 환자를 대상으로 한 전향적 다기관 연구에서 FAST의 민감도, 특이도, 정확도가 각각 100%, 96.9%, 97.3%였고 초음파에서 수술까지의 평균 시간은 12.1±5으로 FAST의 유용성이 입증되었다[29].
두부외상에 대한 검사에서 뇌 컴퓨터촬영이 결정적이지만, 상황이 여의치 않은 경우에 초음파 검사로 도움을 받을 수 있다. 즉, 안구 초음파로 시각신경집(optic nerve sheath) 직경을 측정함으로써 상승된 두개내압을 예측할 수 있으며, 측두골을 통한 경두개골 스캔을 통해 대뇌의 중심선이동(midline shift)을 확인할 수 있다. 또한 심한 안검 부종 등의 의해 동공의 크기나 대광반사를 검사하기 힘든 경우에도 초음파를 이용하면 정확한 동공의 크기 및 대광 반사를 확인할 수 있다(Table 6). 여기서는 시각신경집 직경 측정에 대해서만 언급하겠다.
시각신경의 말초 쪽 일부는 안와 내에 위치하고 있어서 초음파검사로 정확하게 관찰가능하다. 그리고 각 시각신경은 중추신경계의 일부이므로 경막집(dural sheath)에 둘러 싸여 있고, 뇌를 감싸고 있는 지주막하공간과 직접적으로 통해있다. 그러므로 두개내압이 증가하면 시각신경집도 확장하게 된다. 시각신경유두의 부종은 몇 시간에서 며칠이 걸리지만, 시각신경집의 확장은 몇 초 만에 발생한다. 시각신경집 초음파검사가 침습적인 두내내압 측정을 대체할 수는 없겠지만, 정상과 증가된(> 20 mmHg) 두개내압을 구분하는 것은 가능하다. Rajajee 등[30]은 시각신경집 직경의 차단 값(cutoff value)을 4.8 mm로 하였을 때, 증가된 두개내압에 대한 민감도와 특이도가 각각 96%, 94%라고 발표하였다. 따라서 침습적인 두개내압 측정이 불가능한 상황에서, 초음파를 이용한 시각신경집 직경의 측정은 증가된 두개내압을 감지할 수 있는 선별검사로서 사용 가능할 것으로 생각된다.
시각신경집 직경 측정 방법은 다음과 같다. 고주파 (6-13 MHz) 선형 탐촉자를 감은 눈꺼풀 위로 안구의 외측 상부에 적용하고 내측 및 아래쪽으로 약간 각도를 주어서 횡스캔하면, 시각신경이 확연한 경계로 구분되는 안쪽 선형 저에코 구조로 관찰되도록 한다. 저에코 구조(시각신경)의 직경을 측정하는 위치는 망막에서 3 mm 후방에서 측정하도록 한다(Figure 19).
외상환자의 초기 평가 및 처치에서 초음파의 사용은 기도 확보, 호흡 및 환기, 쇼크 관리 및 두개내압 평가까지 여러 단계에서 비침습적으로 신속하게 결정적인 정보들을 제공해 준다. 또한 치료 과정 중에서도 반복적으로 재평가 및 감시가 가능하므로 응급의학 뿐 아니라 외상의학이나 중환자 의학 의사들에게도 유용한 도구라고 할 수 있다. 외상환자 진료에서 진단 및 치료의 결과를 향상시키기 위해서는 초음파 검사의 유용성 및 한계점을 숙지하고 체계적으로 적절하게 적용분야를 확대시켜 나가는 노력이 필요하다 하겠다. 앞으로 관련 임상전문과 간의 초음파적 의사소통이 보다 원활하게 이루어져 효율적인 외상처치 환경 및 치료결과의 향상으로 이어지기를 기대해 본다.
Figures and Tables
Figure 1
Focused assessment with sonography in trauma including airway, breathing, circulation, and disablity (FAST-ABCD). Numbers on a figure indicate positions where probe would be applied to get images about airway, breathing, circulation, and disability. 1. Airway (neck) ultrasound (A). 2. Lung ultrasound (B). 3. Cardiovascular ultrasound (C). 4. Focused assessment with sonography in trauma (C). 5. Orbital and transcranial ultrasound (D).
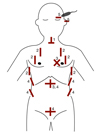
Figure 3
Cricoid cartilage, transverse scan. Cricoid cartilage (arrows). Transverse scan. The tissue-air border is shown as white line (arrow head).
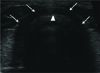
Figure 4
Cricothyroid membrane. (A) Upper airway scanned in the midsagittal plane. (B) From the right side, thyroid cartilage (T), cricoid cartilage (C), and tracheal rings (TR). Cricothyroid membrane (arrow). The tissue-air border (arrow head).
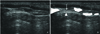
Figure 5
Esophageal intubation. Transverse scan just cranial to the suprasternal notch. Enlarged esophagus by tube is shown on the deep left side of trachea (arrow head) in real time (arrow).
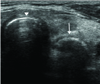
Figure 6
Lung pulse. (A) Left lung sliding is abolished in this selectively intubated patient and vertical movement of pleural line is identified along to the cardiac pulsation on a real-time 2D image, but it cannot be objectified on this static image. (B) M-mode can record vibrations in rhythm with the cardiac activity (arrows).
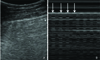
Figure 7
Longitudinal scan on thorax of a normal subject. (A) Upper and lower ribs and their acoustic shadows (vertical arrows). Pleural line and it's reverberation artifacts, Alines (horizontal arrows). (B) The upper rib-pleural line-lower rib profile shapes a sort of bat flying toward you, bat sign which is the basic landmark in lung ultrasound.
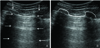
Figure 8
Seashore sign on M-mode. (A) This static image can not show lung sliding, which can be identified in real time. A-lines (horizontal arrows) (B) This M-mode image shows a double component pattern separated by the pleural line (vertical arrows). The top looks waves, and the bottom looks sand. It recalls the beach, hence the seashore sign.
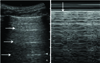
Figure 9
Multiple B-lines (lung rockets). Vertical lines arising from pleural line are shown. They are comet tails with well-defined, laser-like lines spreading up to the edge of the screen without fading. These artifacts are caused by thickened interlobular septum.
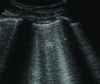
Figure 10
Pneumothorax: A-line sign and stratosphere sign. (A) The absence of lung sliding cannot be visualized in this static image, but horizontal artifacts arising from the pleural line can be seen, and no B line is visible. This pattern called the A-line sign. (B) M-mode can show a pattern of completely horizontal lines, which means no motion of the structures above and below the pleural line (vertical arrow). This M-mode pattern called the stratosphere sign.
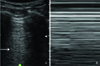
Figure 11
Pneumothorax: lung point. In real time, a transient inspiratory movement is visible at the pleural line. Arrows indicate the border between lung and air (pneumothorax), which is moving. This is the lung point sign. + LS, presence of lung sliding; - LS, absence of lung sliding.
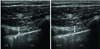
Figure 12
Hemothorax. Hemothorax (H) can have internal echo. Consolidated lung (C) caused by compressive atelectasis is visualized. Bright echogenic spots in the consolidated lung are the airbrochogram (arrows).
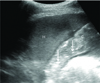
Figure 13
Pleural effusion: sinusoid sign. (A) Small pleural effusion is visible at a middle axillary line (arrow). (B) The thickness of effusion varies in rhythm with the respiratory cycle. Deep border, a visceral pleura (arrow) moves toward the chest wall, thus shaping sinusoid.
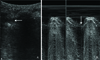
Figure 14
Lung contusion (LC): consolidation. Image scanned sagittally on the left side (probe was positioned on a little bit higher than usual region of focused assessment with sonography in trauma in left upper quadrant). Hypoechoic lesion for alveolar consolidation (socalled hepatization) whose dimensions remained unchanged during the inspiration phase (LC). Blood within the thorax (horizontal arrows). Diaphragm (vertical arrow). H, hematoma; S, spleen; St, stomach gas. Courtesy of Dr. Gordon Lee.
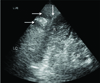
Figure 15
Lung contusion: B-lines. Lung contusion can be visualized as B-lines. Within 1 to 2 hours after primary injury, A progressive infiltrate into interstitial space cause thickened interlobular septum. Focal B-lines are shown in the upper intercostal space (arrows), but no B-line is visible in the lower intercostal space.
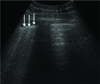
Figure 16
Flattened inferior vena cava (IVC). Subcostal longitudinal view in hemorrhagic shock. Flattened IVC is demonstrated (arrows). Additionally small and hyperkinetic ventricles can be identified on cardiac ultrasound.
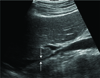
Figure 17
Cardiac tamponade. Subcostal 4 chamber view in the hypotensive patient. Echogenic pericardial effusion (E) compressing the right ventricle is visible (arrow).
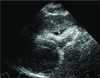
Figure 18
Focused assessment with sonography for trauma: hemoperitoneum. (A) Peritoneal effusion in Morison's pouch. (B) Peritoneal effusion in Douglas pouch. (C) Peritoneal effusion in subdiaphragmatic and splenorenal recess.
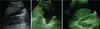
Figure 19
Measurement of optic nerve sheath diameter (ONSD). The optic nerve sheath is a linear hypoechoic structure posterior to the globe. Caliper 1 identifies the site of ONSD measurement 0.3 cm behind the retina. Caliper 2 measures the ONSD (0.3 cm in this case).
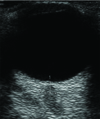
Table 1
Ultrasound-enhanced airway assessment and resuscitation of the trauma patient: airway ultrasound
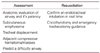
Table 2
Ultrasound-enhanced breathing assessment and resuscitation of the trauma patient: lung ultrasound

Table 3
Ultrasound-enhanced circulation assessment and resuscitation of the trauma patient: cardiovascular ultrasound

Acknowledgement
I would like to express my gratitude to all those who gave me the opportunity to complete this review. I want to thank Luca Neri, the former president of World Interactive Network of Focused Critical Ultrasound (WINFOCUS), Gordon Lee, and Hanho Doh for providing me valuable clinical data.
References
1. Neal MD, Peitzman AB, Forsythe RM, Marshall GT, Rosengart MR, Alarcon LH, Billiar TR, Sperry JL. Over reliance on computed tomography imaging in patients with severe abdominal injury: is the delay worth the risk? J Trauma. 2011. 70:278–284.

2. Rozycki GS, Ochsner MG, Schmidt JA, Frankel HL, Davis TP, Wang D, Champion HR. A prospective study of surgeon-performed ultrasound as the primary adjuvant modality for injured patient assessment. J Trauma. 1995. 39:492–498.

3. Kirkpatrick AW, Sirois M, Laupland KB, Liu D, Rowan K, Ball CG, Hameed SM, Brown R, Simons R, Dulchavsky SA, Hamiilton DR, Nicolaou S. Hand-held thoracic sonography for detecting post-traumatic pneumothoraces: the Extended Focused Assessment with Sonography for Trauma (EFAST). J Trauma. 2004. 57:288–295.

4. Dulchavsky SA, Henry SE, Moed BR, Diebel LN, Marshburn T, Hamilton DR, Logan J, Kirkpatrick AW, Williams DR. Advanced ultrasonic diagnosis of extremity trauma: the FASTER examination. J Trauma. 2002. 53:28–32.

5. Neri L, Storti E, Lichtenstein D. Toward an ultrasound curriculum for critical care medicine. Crit Care Med. 2007. 35:5 Suppl. S290–S304.

6. Gruen RL, Jurkovich GJ, McIntyre LK, Foy HM, Maier RV. Patterns of errors contributing to trauma mortality: lessons learned from 2,594 deaths. Ann Surg. 2006. 244:371–380.

7. Elliott DS, Baker PA, Scott MR, Birch CW, Thompson JM. Accuracy of surface landmark identification for cannula cricothyroidotomy. Anaesthesia. 2010. 65:889–894.

8. Walls RM, Murphy MF. Manual of emergency airway management. 2008. 3rd ed. Philadelphia: Lippincott Williams & Wilkins.

9. Gerig HJ, Schnider T, Heidegger T. Prophylactic percutaneous transtracheal catheterisation in the management of patients with anticipated difficult airways: a case series. Anaesthesia. 2005. 60:801–805.

10. Lichtenstein D, Meziere G, Biderman P, Gepner A, Barre O. The comet-tail artifact: an ultrasound sign of alveolar-interstitial syndrome. Am J Respir Crit Care Med. 1997. 156:1640–1646.

11. Wilkerson RG, Stone MB. Sensitivity of bedside ultrasound and supine anteroposterior chest radiographs for the identification of pneumothorax after blunt trauma. Acad Emerg Med. 2010. 17:11–17.

12. Ball CG, Kirkpatrick AW, Feliciano DV. The occult pneumothorax: what have we learned? Can J Surg. 2009. 52:E173–E179.

13. Ball CG, Ranson K, Dente CJ, Feliciano DV, Laupland KB, Dyer D, Inaba K, Trottier V, Datta I, Kirkpatrick AW. Clinical predictors of occult pneumothoraces in severely injured blunt polytrauma patients: a prospective observational study. Injury. 2009. 40:44–47.

14. Enderson BL, Abdalla R, Frame SB, Casey MT, Gould H, Maull KI. Tube thoracostomy for occult pneumothorax: a prospective randomized study of its use. J Trauma. 1993. 35:726–729.

15. Mennicke M, Gulati K, Oliva I, Goldflam K, Skali H, Ledbetter S, Platz E. Anatomical distribution of traumatic pneumothoraces on chest computed tomography: implications for ultrasound screening in the ED. Am J Emerg Med. 2012. 30:1025–1031.

16. Lichtenstein D, Meziere G, Biderman P, Gepner A. The comettail artifact: an ultrasound sign ruling out pneumothorax. Intensive Care Med. 1999. 25:383–388.

17. Lichtenstein D, Meziere G, Biderman P, Gepner A. The "lung point": an ultrasound sign specific to pneumothorax. Intensive Care Med. 2000. 26:1434–1440.

18. Volpicelli G, Elbarbary M, Blaivas M, Lichtenstein DA, Mathis G, Kirkpatrick AW, Melniker L, Gargani L, Noble VE, Via G, Dean A, Tsung JW, Soldati G, Copetti R, Bouhemad B, Reissig A, Agricola E, Rouby JJ, Arbelot C, Liteplo A, Sargsyan A, Silva F, Hoppmann R, Breitkreutz R, Seibel A, Neri L, Storti E, Petrovic T. International Liaison Committee on Lung Ultrasound (ILC-LUS) for International Consensus Conference on Lung Ultrasound (ICC-LUS). International evidence-based recommendations for point-of-care lung ultrasound. Intensive Care Med. 2012. 38:577–591.

19. Sisley AC, Rozycki GS, Ballard RB, Namias N, Salomone JP, Feliciano DV. Rapid detection of traumatic effusion using surgeon-performed ultrasonography. J Trauma. 1998. 44:291–296.

20. Lichtenstein D, Hulot JS, Rabiller A, Tostivint I, Meziere G. Feasibility and safety of ultrasound-aided thoracentesis in mechanically ventilated patients. Intensive Care Med. 1999. 25:955–958.

21. Soldati G, Testa A, Silva FR, Carbone L, Portale G, Silveri NG. Chest ultrasonography in lung contusion. Chest. 2006. 130:533–538.

22. Rocco M, Carbone I, Morelli A, Bertoletti L, Rossi S, Vitale M, Montini L, Passariello R, Pietropaoli P. Diagnostic accuracy of bedside ultrasonography in the ICU: feasibility of detecting pulmonary effusion and lung contusion in patients on respiratory support after severe blunt thoracic trauma. Acta Anaesthesiol Scand. 2008. 52:776–784.

23. Gunst M, Ghaemmaghami V, Sperry J, Robinson M, O'Keeffe T, Friese R, Frankel H. Accuracy of cardiac function and volume status estimates using the bedside echocardiographic assessment in trauma/critical care. J Trauma. 2008. 65:509–516.

24. Ferrada P, Murthi S, Anand RJ, Bochicchio GV, Scalea T. Transthoracic focused rapid echocardiographic examination: real-time evaluation of fluid status in critically ill trauma patients. J Trauma. 2011. 70:56–62.

25. Carr BG, Dean AJ, Everett WW, Ku BS, Mark DG, Okusanya O, Horan AD, Gracias VH. Intensivist bedside ultrasound (INBU) for volume assessment in the intensive care unit: a pilot study. J Trauma. 2007. 63:495–500.

26. Ma OJ, Mateer JR, Ogata M, Kefer MP, Wittmann D, Aprahamian C. Prospective analysis of a rapid trauma ultrasound examination performed by emergency physicians. J Trauma. 1995. 38:879–885.

27. Natarajan B, Gupta PK, Cemaj S, Sorensen M, Hatzoudis GI, Forse RA. FAST scan: is it worth doing in hemodynamically stable blunt trauma patients? Surgery. 2010. 148:695–700.
28. Udobi KF, Rodriguez A, Chiu WC, Scalea TM. Role of ultrasonography in penetrating abdominal trauma: a prospective clinical study. J Trauma. 2001. 50:475–479.




 PDF
PDF ePub
ePub Citation
Citation Print
Print





 XML Download
XML Download